文档内容
高频考点 17 硫及其氧化物
题点(一)硫和二氧化硫的性质
1.(2021·河北卷)硫和氮及其化合物对人类生存和社会发展意义重大,但硫氧化物和氮氧化物造成的环
境问题也日益受到关注,下列说法正确的是( )
A.NO 和SO 均为红棕色且有刺激性气味的气体,是酸雨的主要成因
2 2
B.汽车尾气中的主要大气污染物为NO、SO 和PM2.5
2
C.植物直接吸收利用空气中的NO和NO 作为肥料,实现氮的固定
2
D.工业废气中的SO 可采用石灰法进行脱除
2
1.D A. 是红棕色且有刺激性气味的气体,而 是无色有刺激性气味的气体,A错误;B.汽车尾
气的主要大气污染物为C与N的氧化物,如NO 和CO等,B错误;
x
C.氮的固定是指将游离态的氮元素转化为化合态,且植物可吸收土壤中的铵根离子或硝酸根离子作为肥
料,不能直接吸收空气中的氮氧化物,C错误;D.工业废气中的 可采用石灰法进行脱除,如加入石灰
石或石灰乳均可进行脱硫处理,D正确;故选D。
2.(2021·北京卷)室温下,1体积的水能溶解约40体积的SO 。用试管收集SO 后进行如下实验。对实验
2 2
现象的分析正确的是( )
A.试管内液面上升,证明SO 与水发生了反应
2
B.试管中剩余少量气体,是因为SO 的溶解已达饱和
2
C.取出试管中的溶液,立即滴入紫色石蕊试液,溶液显红色,原因是:SO +H O H SO 、H SO H++
2 2 2 3 2 3
⇌ ⇌
、 H++
⇌
D.取出试管中溶液,在空气中放置一段时间后pH下降,是由于SO 挥发
2
2.C A.由信息可知,SO 易溶于水,也能使液面上升,故A错误;B.二氧化硫与水的反应为可逆反应,
2
当反应达到限度后,二氧化硫的量不再减少,液面高度也无明显变化,故B错误;C.滴入石蕊试液,溶
液变为红色,说明溶液显酸性,SO 与水反应生成亚硫酸,亚硫酸为弱酸,分步电离出氢离子,故C正确;
2D.亚硫酸具有较强的还原性,易被氧化为硫酸,弱酸变强酸,也能使pH下降,故D错误;故选C。
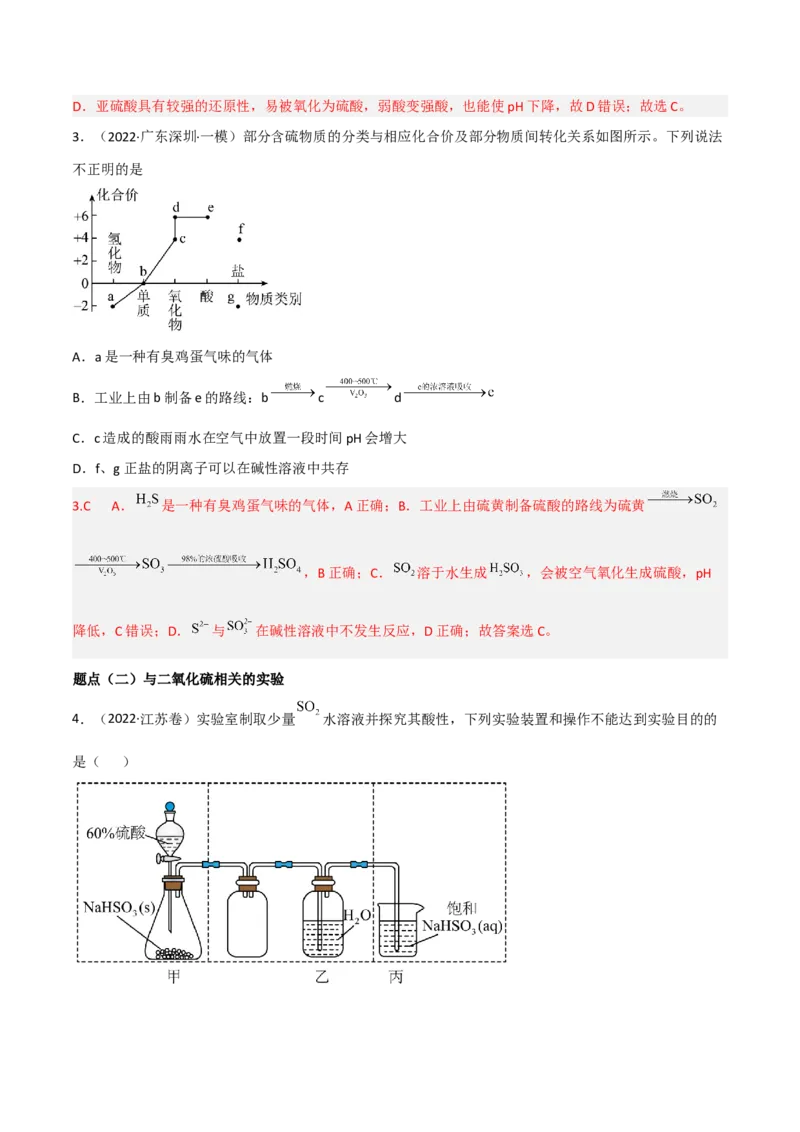
3.(2022·广东深圳·一模)部分含硫物质的分类与相应化合价及部分物质间转化关系如图所示。下列说法
不正明的是
A.a是一种有臭鸡蛋气味的气体
B.工业上由b制备e的路线:b c d
C.c造成的酸雨雨水在空气中放置一段时间pH会增大
D.f、g正盐的阴离子可以在碱性溶液中共存
3.C A. 是一种有臭鸡蛋气味的气体,A正确;B.工业上由硫黄制备硫酸的路线为硫黄
,B正确;C. 溶于水生成 ,会被空气氧化生成硫酸,pH
降低,C错误;D. 与 在碱性溶液中不发生反应,D正确;故答案选C。
题点(二)与二氧化硫相关的实验
4.(2022·江苏卷)实验室制取少量 水溶液并探究其酸性,下列实验装置和操作不能达到实验目的的
是( )A.用装置甲制取 气体 B.用装置乙制取 水溶液
C.用装置丙吸收尾气中的 D.用干燥pH试纸检验 水溶液的酸性
4.C A.60%硫酸和NaHSO3(s)可发生反应:H SO +2NaHSO =Na SO +2SO ↑+2H O,因此装置甲可以制取
2 4 3 2 4 2 2
气体,A正确;B.气体通入液体时“长进短处”,装置乙可以制取 水溶液,B正确;C.SO 不会
2
与饱和NaHSO 溶液发生反应,因此装置丙不能吸收尾气中的 ,C错误;D. 水溶液显酸性,可用
3
干燥的pH试纸检验其酸性,D正确;答案选C。
5.(2021·山东卷)工业上以SO 和纯碱为原料制备无水NaHSO 的主要流程如图,下列说法错误的是(
2 3
)
A.吸收过程中有气体生成 B.结晶后母液中含有NaHCO
3
C.气流干燥湿料时温度不宜过高 D.中和后溶液中含Na SO 和NaHCO
2 3 3
5.B A.根据上述分析可知,吸收过程中有二氧化碳生成,A正确;B.结晶后母液中含饱和NaHSO 和过
3
量的二氧化硫形成的亚硫酸,没有NaHCO ,假设产物中存在NaHCO ,则其会与生成的NaHSO 发生反应,
3 3 3
且NaHCO 溶解度较低,若其残留于母液中,会使晶体不纯,假设不成立,B错误;C.NaHSO 高温时易分
3 3
解变质,所以气流干燥过程中温度不宜过高,C正确;D.结合上述分析可知,中和后溶液中含Na SO 和
2 3
NaHCO ,D正确;故选B。
3
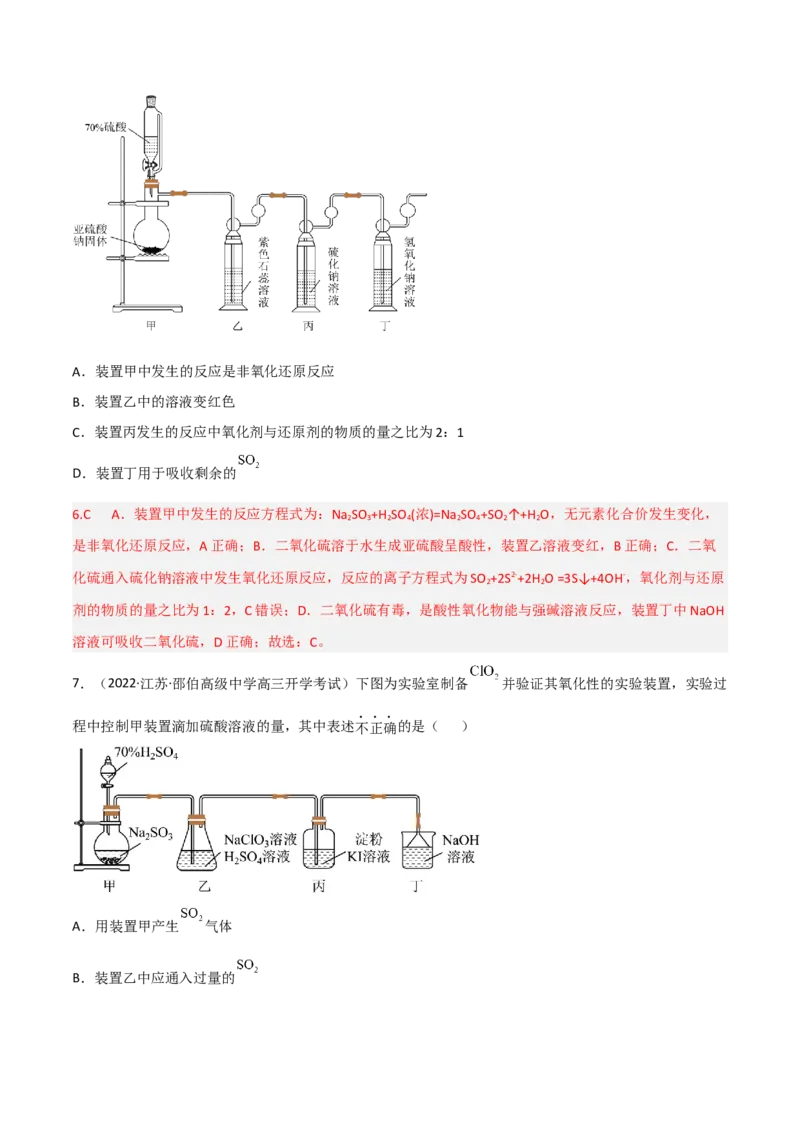
6.(2022·黑龙江·牡丹江市第二高级中学高三阶段练习)二氧化硫是一种在空间地理、环境科学等领域受
到广泛研究的气体。某研究小组设计了一套制备及检验 部分性质的装置,如图所示。下列分析不正确
的是( )A.装置甲中发生的反应是非氧化还原反应
B.装置乙中的溶液变红色
C.装置丙发生的反应中氧化剂与还原剂的物质的量之比为2:1
D.装置丁用于吸收剩余的
6.C A.装置甲中发生的反应方程式为:Na SO +H SO (浓)=Na SO +SO ↑+H O,无元素化合价发生变化,
2 3 2 4 2 4 2 2
是非氧化还原反应,A正确;B.二氧化硫溶于水生成亚硫酸呈酸性,装置乙溶液变红,B正确;C.二氧
化硫通入硫化钠溶液中发生氧化还原反应,反应的离子方程式为SO +2S2-+2H O =3S↓+4OH-,氧化剂与还原
2 2
剂的物质的量之比为1:2,C错误;D.二氧化硫有毒,是酸性氧化物能与强碱溶液反应,装置丁中NaOH
溶液可吸收二氧化硫,D正确;故选:C。
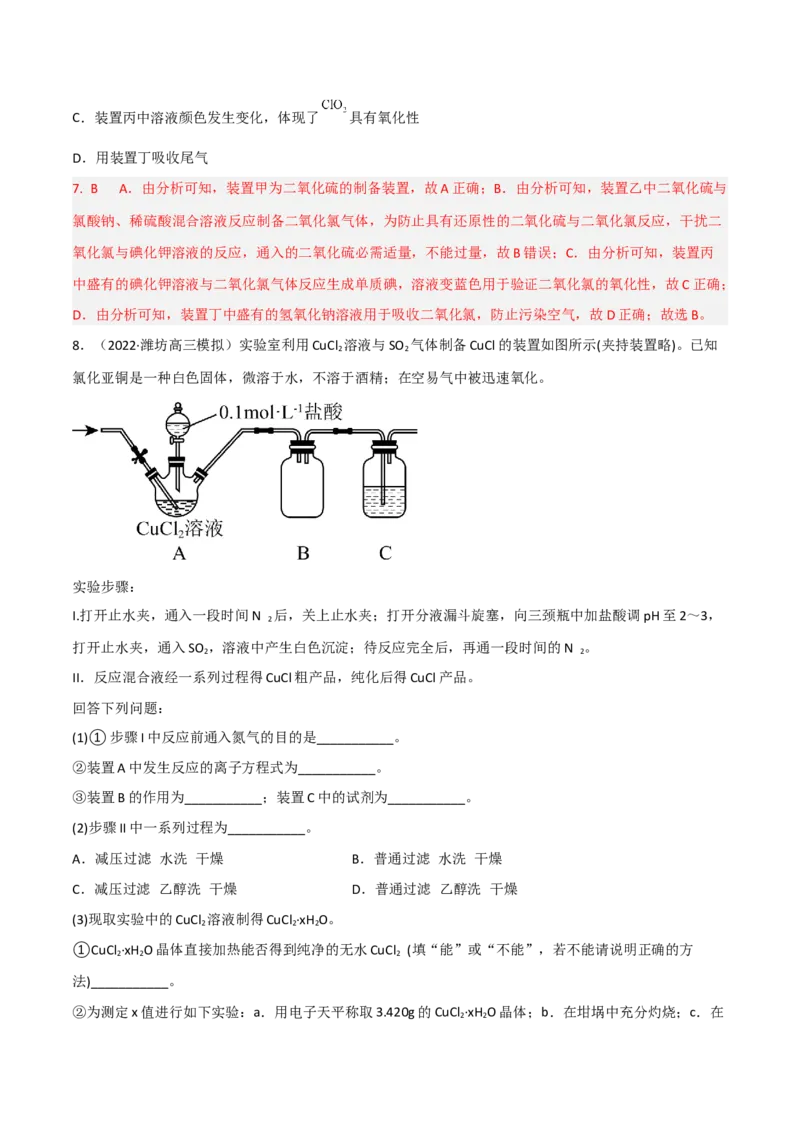
7.(2022·江苏·邵伯高级中学高三开学考试)下图为实验室制备 并验证其氧化性的实验装置,实验过
程中控制甲装置滴加硫酸溶液的量,其中表述不正确的是( )
A.用装置甲产生 气体
B.装置乙中应通入过量的C.装置丙中溶液颜色发生变化,体现了 具有氧化性
D.用装置丁吸收尾气
7. B A.由分析可知,装置甲为二氧化硫的制备装置,故A正确;B.由分析可知,装置乙中二氧化硫与
氯酸钠、稀硫酸混合溶液反应制备二氧化氯气体,为防止具有还原性的二氧化硫与二氧化氯反应,干扰二
氧化氯与碘化钾溶液的反应,通入的二氧化硫必需适量,不能过量,故B错误;C.由分析可知,装置丙
中盛有的碘化钾溶液与二氧化氯气体反应生成单质碘,溶液变蓝色用于验证二氧化氯的氧化性,故C正确;
D.由分析可知,装置丁中盛有的氢氧化钠溶液用于吸收二氧化氯,防止污染空气,故D正确;故选B。
8.(2022·潍坊高三模拟)实验室利用CuCl 溶液与SO 气体制备CuCl的装置如图所示(夹持装置略)。已知
2 2
氯化亚铜是一种白色固体,微溶于水,不溶于酒精;在空易气中被迅速氧化。
实验步骤:
I.打开止水夹,通入一段时间N 后,关上止水夹;打开分液漏斗旋塞,向三颈瓶中加盐酸调pH至2~3,
2
打开止水夹,通入SO ,溶液中产生白色沉淀;待反应完全后,再通一段时间的N 。
2 2
II.反应混合液经一系列过程得CuCl粗产品,纯化后得CuCl产品。
回答下列问题:
(1)①步骤I中反应前通入氮气的目的是___________。
②装置A中发生反应的离子方程式为___________。
③装置B的作用为___________;装置C中的试剂为___________。
(2)步骤II中一系列过程为___________。
A.减压过滤 水洗 干燥 B.普通过滤 水洗 干燥
C.减压过滤 乙醇洗 干燥 D.普通过滤 乙醇洗 干燥
(3)现取实验中的CuCl 溶液制得CuCl ·xH O。
2 2 2
①CuCl ·xH O晶体直接加热能否得到纯净的无水CuCl (填“能”或“不能”,若不能请说明正确的方
2 2 2
法)___________。
②为测定x值进行如下实验:a.用电子天平称取3.420g的CuCl ·xH O晶体;b.在坩埚中充分灼烧;c.在
2 2干燥器中冷却;d.称量所得黑色固体质量;e.重复b~d操作直至连续两次称量差值不超过0.001g。若最
终得到黑色固体质量为1.600g,则 ___________。
8.(1) 排尽装置中的空气,防止氯化亚铜被空气中氧气氧化 SO +2Cu2++2Cl—+2H O=2CuCl↓+SO
2 2
+4H+ 安全瓶,防倒吸 NaOH溶液
(2)C(3) 不能,在干燥的氯化氢气流中加热 2
解析:由实验装置图可知,装置A中二氧化硫与盐酸、氯化铜混合溶液反应制备氯化亚铜,装置B为空载
仪器,起到安全瓶,防倒吸的作用,装置C中盛有的氢氧化钠溶液用于吸收二氧化硫,防止污染空气。
(1)①由题给信息可知,氯化亚铜在空易气中被迅速氧化,反应前应通入氮气排尽装置中的空气,防止
氯化亚铜被空气中氧气氧化,故答案为:排尽装置中的空气,防止氯化亚铜被空气中氧气氧化;
②由分析可知,装置A中发生的反应为二氧化硫与氯化铜溶液反应生成氯化亚铜沉淀、硫酸和盐酸,反应
的离子方程式为SO +2Cu2++2Cl—+2H O=2CuCl↓+SO +4H+,故答案为:SO +2Cu2++2Cl—+2H O=2CuCl↓+SO
2 2 2 2
+4H+;
③由分析可知,装置B为空载仪器,起到安全瓶,防倒吸的作用,装置C中盛有的氢氧化钠溶液用于吸收
二氧化硫,防止污染空气,故答案为:安全瓶,防倒吸;NaOH溶液;
(2)为防止微溶于水的氯化亚铜被氧化,步骤II中一系列过程为减压过滤、乙醇洗、干燥,故选C;
(3)①氯化铜是强酸弱碱盐,在溶液中易发生水解,为防止CuCl ·xH O晶体直接加热时发生水解反应,应
2 2
在干燥的氯化氢气流中加热使CuCl ·xH O晶体失去结晶水得到无水氯化铜,故答案为:不能,在干燥的氯
2 2
化氢气流中加热;
②由题意可得如下转化关系:CuCl ·xH O—CuO,由CuCl ·xH O和氧化铜的质量可得: =
2 2 2 2
,解得x=2,故答案为:2。