文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(广东专用)
黄金卷01
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 F 19 Al 27 Bi 209
第Ⅰ卷
一、选择题:本题共16个小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在
每小题给出的四个选项中,只有一项是符合题目要求的。
1.中华优秀传统文化,是中华民族的根与魂,是我们坚定文化自信的力量源泉。下列载体主要由合金材
料制成的是
载体
选项 A.玛瑙围棋子 B.竹笛 C.青铜器 D.中国山水画
2.绢本宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀石[主要
成分为Cu(OH) ·CuCO],红色来自赭石(赤铁矿),黑色来自炭黑。下列说法错误的是
2 3
A.蚕丝制品绢的主要成分是蛋白质 B.孔雀石受热易分解
C.赭石的主要成分是Fe O D.炭黑由松枝烧制,该过程是化学变化
3 4
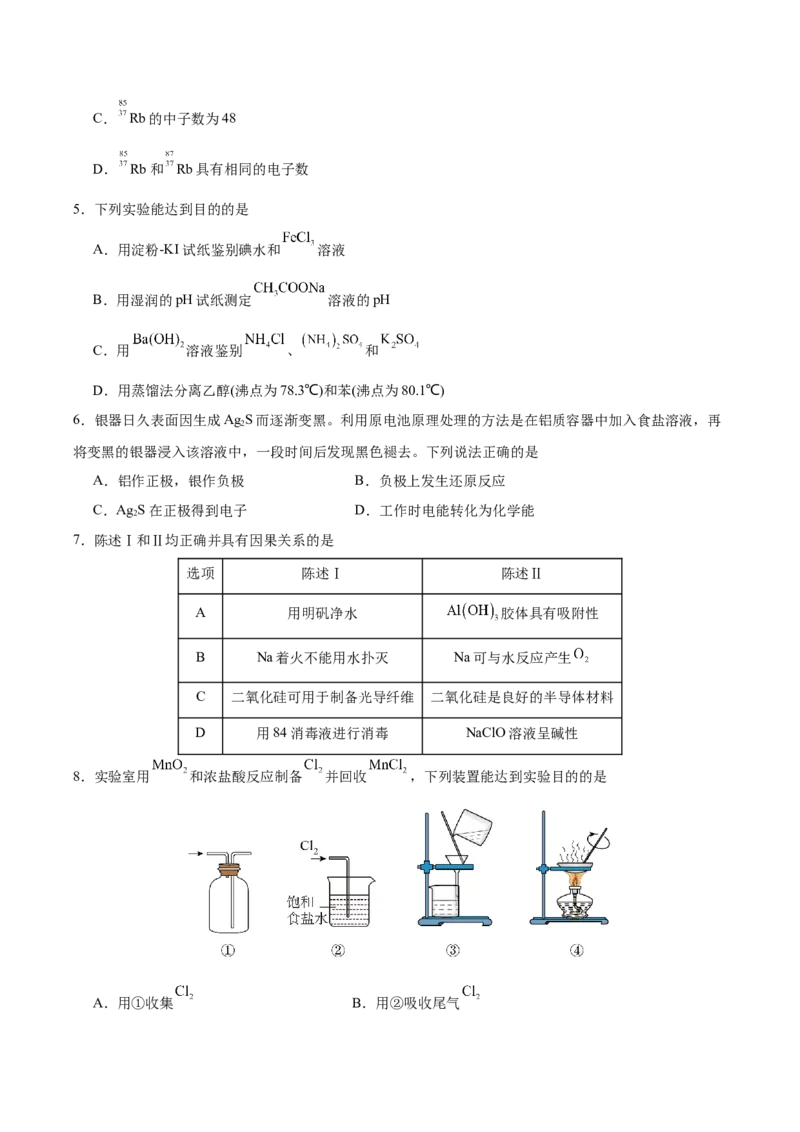
3.甘氨酸是人体必须氨基酸,其结构如图,下列有关说法不正确的是
A.分子中碳原子有两种杂化形式
B.能与氢氧化钠、盐酸反应生成相应的盐
C.各元素的电负性大小顺序为:N>O>C>H
D.由结构推测,固态的甘氨酸易溶于水
4.我国北斗三号全球卫星导航系统中的“铷(Rb)原子钟”被誉为卫星的“心脏”,下列有关说法错误的是
A.铷元素位于IA族
B.铷的金属性比钠弱C. Rb的中子数为48
D. Rb和 Rb具有相同的电子数
5.下列实验能达到目的的是
A.用淀粉-KI试纸鉴别碘水和 溶液
B.用湿润的pH试纸测定 溶液的pH
C.用 溶液鉴别 、 和
D.用蒸馏法分离乙醇(沸点为78.3℃)和苯(沸点为80.1℃)
6.银器日久表面因生成Ag S而逐渐变黑。利用原电池原理处理的方法是在铝质容器中加入食盐溶液,再
2
将变黑的银器浸入该溶液中,一段时间后发现黑色褪去。下列说法正确的是
A.铝作正极,银作负极 B.负极上发生还原反应
C.Ag S在正极得到电子 D.工作时电能转化为化学能
2
7.陈述Ⅰ和Ⅱ均正确并具有因果关系的是
选项 陈述Ⅰ 陈述Ⅱ
A 用明矾净水 胶体具有吸附性
B Na着火不能用水扑灭 Na可与水反应产生
C 二氧化硅可用于制备光导纤维 二氧化硅是良好的半导体材料
D 用84消毒液进行消毒 NaClO溶液呈碱性
8.实验室用 和浓盐酸反应制备 并回收 ,下列装置能达到实验目的的是
A.用①收集 B.用②吸收尾气C.用③分离 和 溶液 D.用④蒸干 溶液制
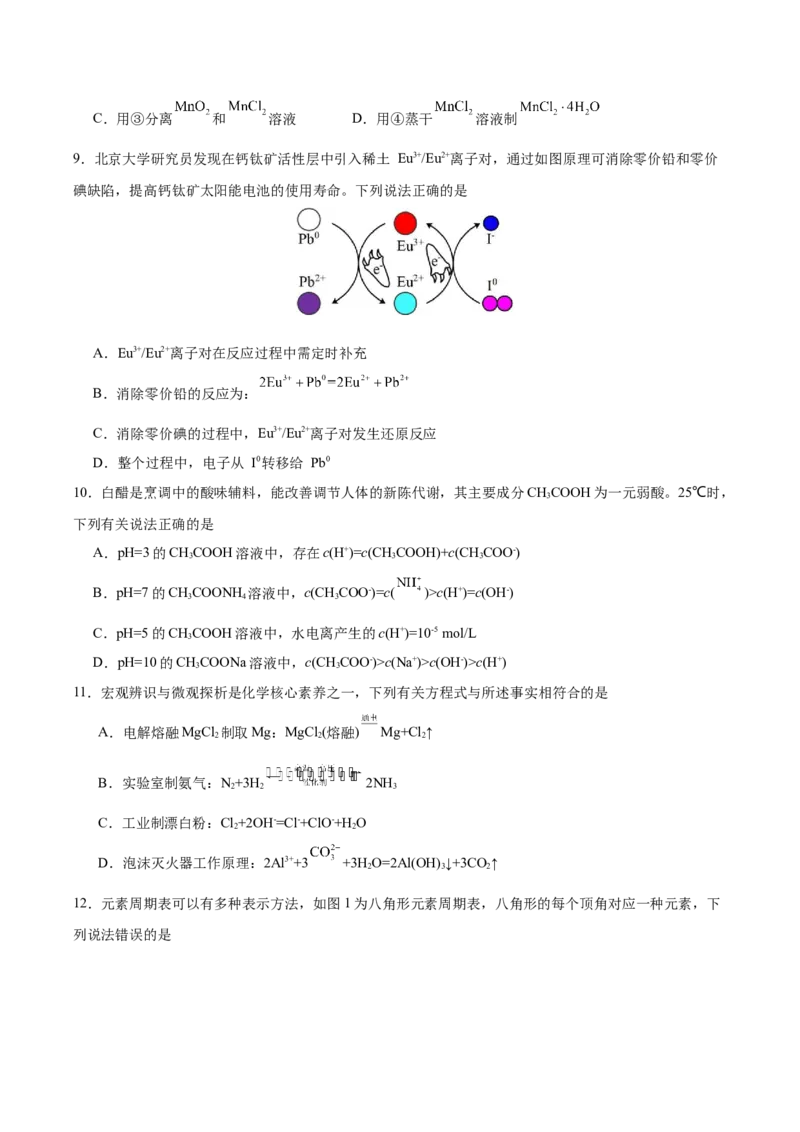
9.北京大学研究员发现在钙钛矿活性层中引入稀土 Eu3+/Eu2+离子对,通过如图原理可消除零价铅和零价
碘缺陷,提高钙钛矿太阳能电池的使用寿命。下列说法正确的是
A.Eu3+/Eu2+离子对在反应过程中需定时补充
B.消除零价铅的反应为:
C.消除零价碘的过程中,Eu3+/Eu2+离子对发生还原反应
D.整个过程中,电子从 I0转移给 Pb0
10.白醋是烹调中的酸味辅料,能改善调节人体的新陈代谢,其主要成分CHCOOH为一元弱酸。25℃时,
3
下列有关说法正确的是
A.pH=3的CHCOOH溶液中,存在c(H+)=c(CHCOOH)+c(CHCOO-)
3 3 3
B.pH=7的CHCOONH 溶液中,c(CHCOO-)=c( )>c(H+)=c(OH-)
3 4 3
C.pH=5的CHCOOH溶液中,水电离产生的c(H+)=10-5 mol/L
3
D.pH=10的CHCOONa溶液中,c(CHCOO-)>c(Na+)>c(OH-)>c(H+)
3 3
11.宏观辨识与微观探析是化学核心素养之一,下列有关方程式与所述事实相符合的是
A.电解熔融MgCl 制取Mg:MgCl (熔融) Mg+Cl ↑
2 2 2
B.实验室制氨气:N+3H 2NH
2 2 3
C.工业制漂白粉:Cl+2OH-=Cl-+ClO-+H O
2 2
D.泡沫灭火器工作原理:2Al3++3 +3H O=2Al(OH) ↓+3CO ↑
2 3 2
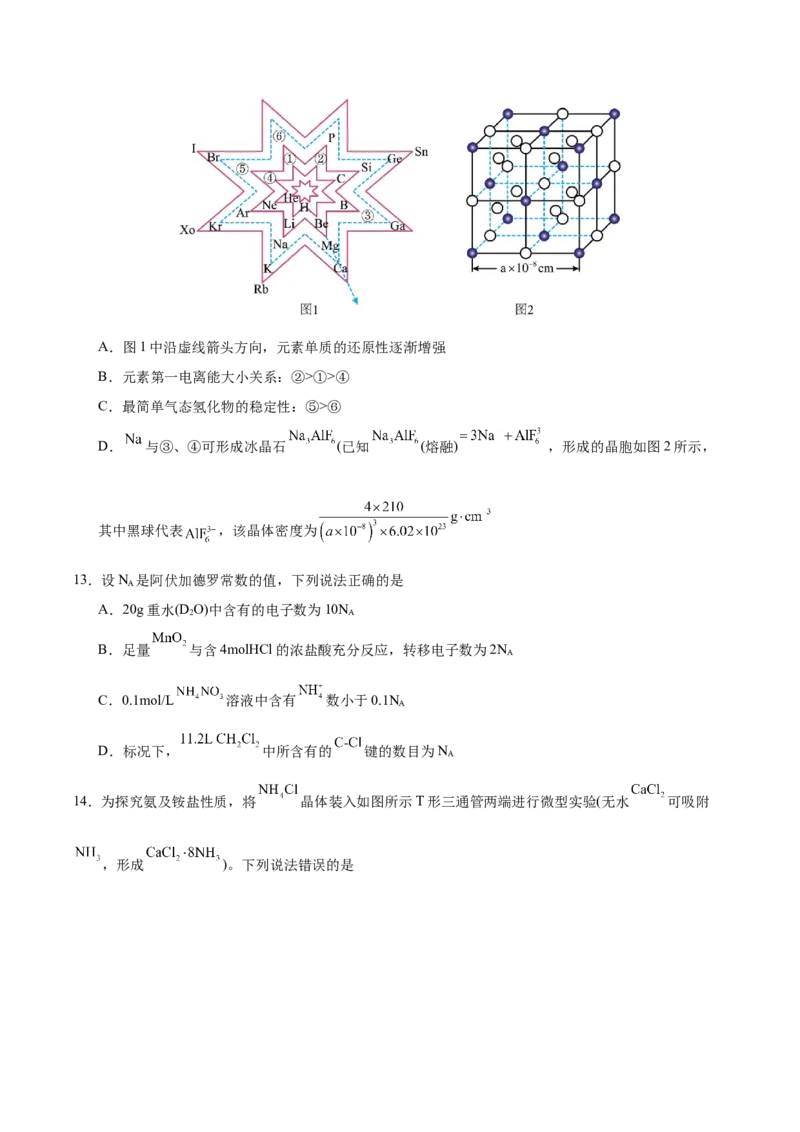
12.元素周期表可以有多种表示方法,如图1为八角形元素周期表,八角形的每个顶角对应一种元素,下
列说法错误的是A.图1中沿虚线箭头方向,元素单质的还原性逐渐增强
B.元素第一电离能大小关系:②>①>④
C.最简单气态氢化物的稳定性:⑤>⑥
D. 与③、④可形成冰晶石 (已知 (熔融) ,形成的晶胞如图2所示,
其中黑球代表 ,该晶体密度为
13.设N 是阿伏加德罗常数的值,下列说法正确的是
A
A.20g重水(D O)中含有的电子数为10N
2 A
B.足量 与含4molHCl的浓盐酸充分反应,转移电子数为2N
A
C.0.1mol/L 溶液中含有 数小于0.1N
A
D.标况下, 中所含有的 键的数目为N
A
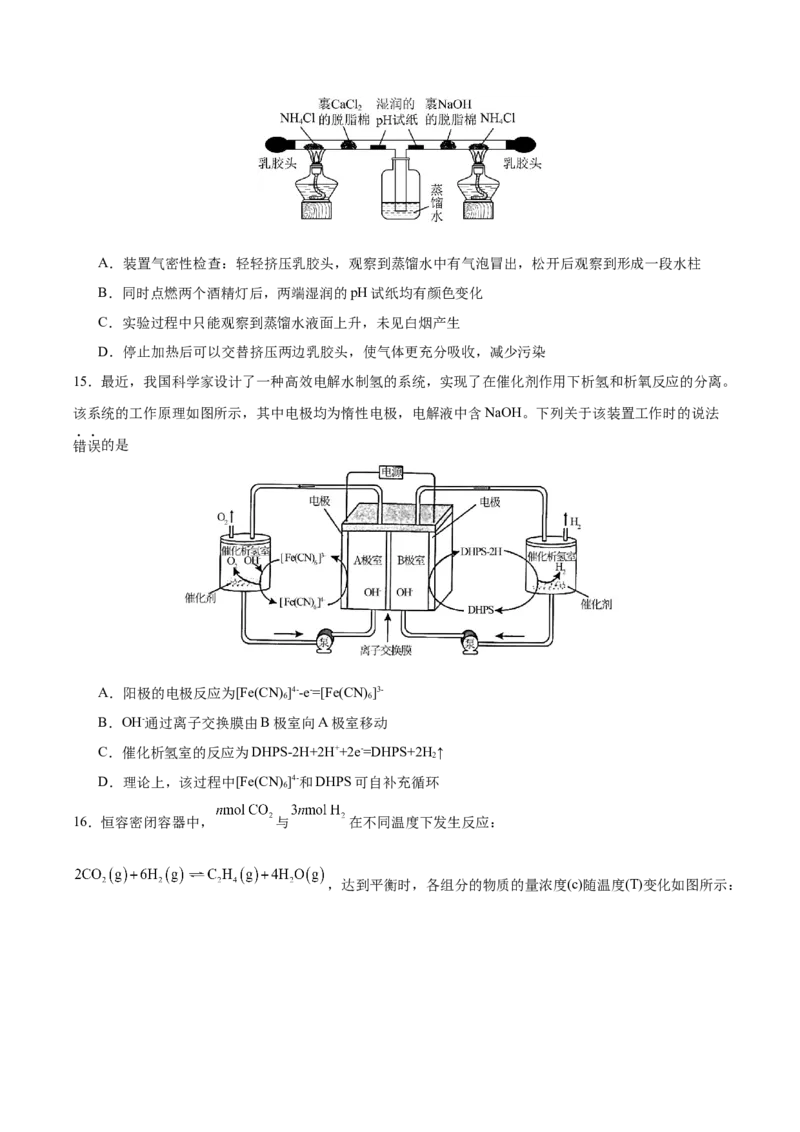
14.为探究氨及铵盐性质,将 晶体装入如图所示T形三通管两端进行微型实验(无水 可吸附
,形成 )。下列说法错误的是A.装置气密性检查:轻轻挤压乳胶头,观察到蒸馏水中有气泡冒出,松开后观察到形成一段水柱
B.同时点燃两个酒精灯后,两端湿润的pH试纸均有颜色变化
C.实验过程中只能观察到蒸馏水液面上升,未见白烟产生
D.停止加热后可以交替挤压两边乳胶头,使气体更充分吸收,减少污染
15.最近,我国科学家设计了一种高效电解水制氢的系统,实现了在催化剂作用下析氢和析氧反应的分离。
该系统的工作原理如图所示,其中电极均为惰性电极,电解液中含NaOH。下列关于该装置工作时的说法
错误的是
A.阳极的电极反应为[Fe(CN) ]4--e-=[Fe(CN)]3-
6 6
B.OH-通过离子交换膜由B极室向A极室移动
C.催化析氢室的反应为DHPS-2H+2H++2e-=DHPS+2H ↑
2
D.理论上,该过程中[Fe(CN) ]4-和DHPS可自补充循环
6
16.恒容密闭容器中, 与 在不同温度下发生反应:
,达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示:下列说法正确的是
A.该反应的平衡常数随温度升高而增大
B.曲线Y表示 随温度的变化关系
C.提高投料比 ,可提高 的平衡转化率
D.其他条件不变, 与 在 ℃下反应,达到平衡时
第Ⅱ卷
二、非选择题:本题共4个小题,共56分。
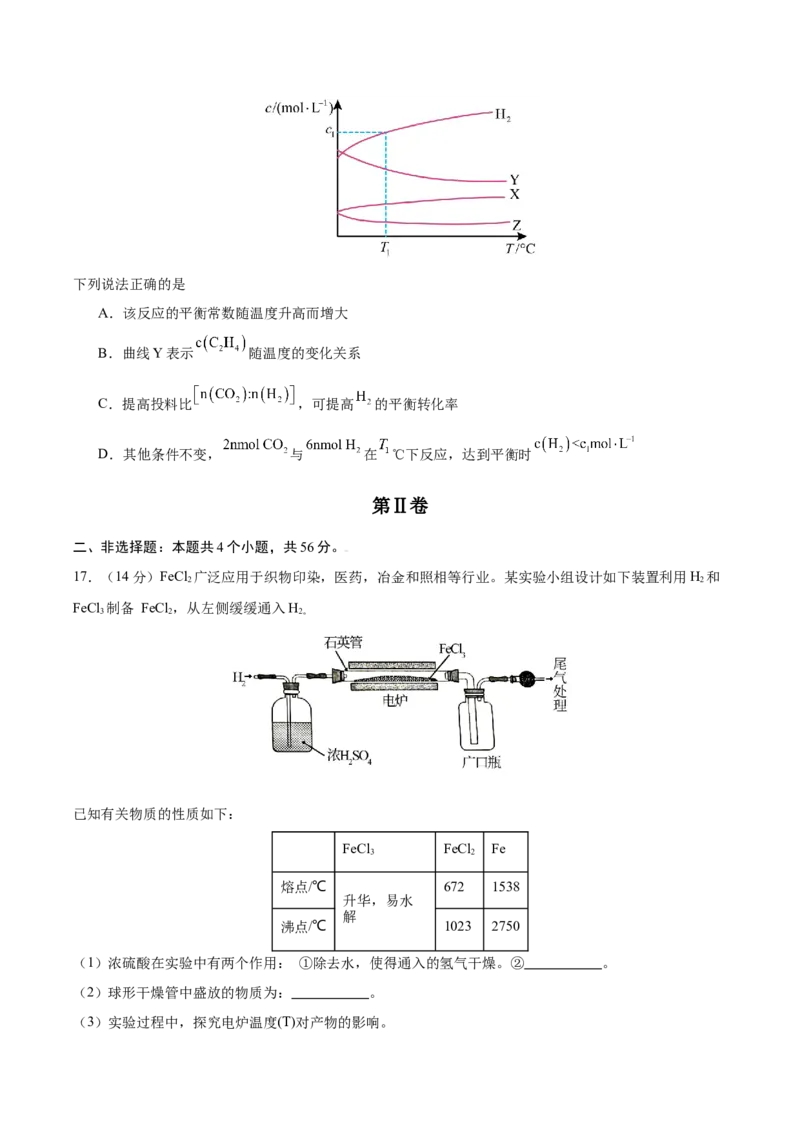
17.(14分)FeCl 广泛应用于织物印染,医药,冶金和照相等行业。某实验小组设计如下装置利用H 和
2 2
FeCl 制备 FeCl ,从左侧缓缓通入H
3 2 2。
已知有关物质的性质如下:
FeCl FeCl Fe
3 2
熔点/℃ 672 1538
升华,易水
解
沸点/℃ 1023 2750
(1)浓硫酸在实验中有两个作用: ①除去水,使得通入的氢气干燥。② 。
(2)球形干燥管中盛放的物质为: 。
(3)实验过程中,探究电炉温度(T)对产物的影响。①当温度T为300℃时,加热一段时间后发现石英管内几乎没有固体剩余,请指出出现该现象可能的原因:
。
②当温度T为 330℃时,加热后石英管内有固体剩余,取少量固体于试管中并加入稀盐酸,全部溶解且无
气泡,对固体成分进行猜测并设计实验验证。
猜测1:只有 FeCl ;猜测2: 含有FeCl 和 FeCl ;猜测3: 只有FeCl
2 2 3 3
实验方案:
实验步
操作 现象
骤
第一步 取溶液2mL于试管中,加入KSCN 现象一
第二步 另取溶液2mL于试管中,加入 现象二
第二步加入的物质为: 。
实验结论:现象一为 ,现象二为 。则猜测1 成立。
③当温度T为350℃时,加热后石英管内有固体剩余,取少量固体于试管中并加入稀盐酸,固体溶解的同
时有少量气泡产生,写出加热过程中发生的副反应的化学方程式: 。
(4)三次实验中,广口瓶中都可以收集到大量固体,则其成分主要为 。
18.(14分)铋及其化合物广泛应用于电子材料、医药等领域。一种以含铋烧渣(主要成分为 、
,还含有少量MnS、 、CuO及 等)制取 并回收锰的工艺流程如下:
已知:①氧化性: ;
② 易水解成BiOCl沉淀;常温下,BiOCl存在的pH范围约为2.0~11.0;
③常温下, ; 。
回答下列问题:
(1)基态锰原子的价电子排布式为 。
(2)“水浸提锰”时,另加入少量稀硫酸可促进 (填化学式)溶解,进一步提高锰的浸取率。(3)“滤渣2”的主要成分有 (填化学式)、Bi。
(4)常温下,“含 滤液”中 的浓度为 。为保证BiOCl产品的纯度,理论上,“沉
铋”时应控制溶液的pH< (保留一位小数)。
(5)“脱氯”过程中发生主要反应的离子方程式为 。
(6)BiOCl是一种性能优良的光催化剂,可催化降解有机污染物对硝基苯酚( )等。对
硝基苯酚的熔点高于邻硝基苯酚( )的熔点,其原因是 。
(7)我国科学家在新型二维半导体芯片材料——硒氧化铋的研究中取得突破性进展。硒氧化铋的晶胞结
构如图所示,晶胞棱边夹角均为90°,晶胞参数为a pm,a pm,b pm。
①该晶胞沿z轴方向的投影图为 (填标号)。
A. B. C. D.
②该晶体中,每个 周围紧邻的 共有 个。
③该晶体的密度为 (列出计算式, 为阿伏加德罗常数的值)。
19.(14分)HS是石油化工行业广泛存在的污染性气体,但同时也是重要的氢源和硫源,工业上可以采
2
取多种方式处理。
I.硫碘循环法脱硫(1)下面是热化学硫碘循环中硫化氢分解制备氢气、硫磺的反应过程。
H=-151 kJ·mol -1
1
△
2HI(aq)=H(g)+ I (s) H=110 kJ·mol -1
2 2 2
△
H=61 kJ·mol -1
3
△
则HS(g) H(g)+S(s) = 。
2 2
II.热分解法脱硫
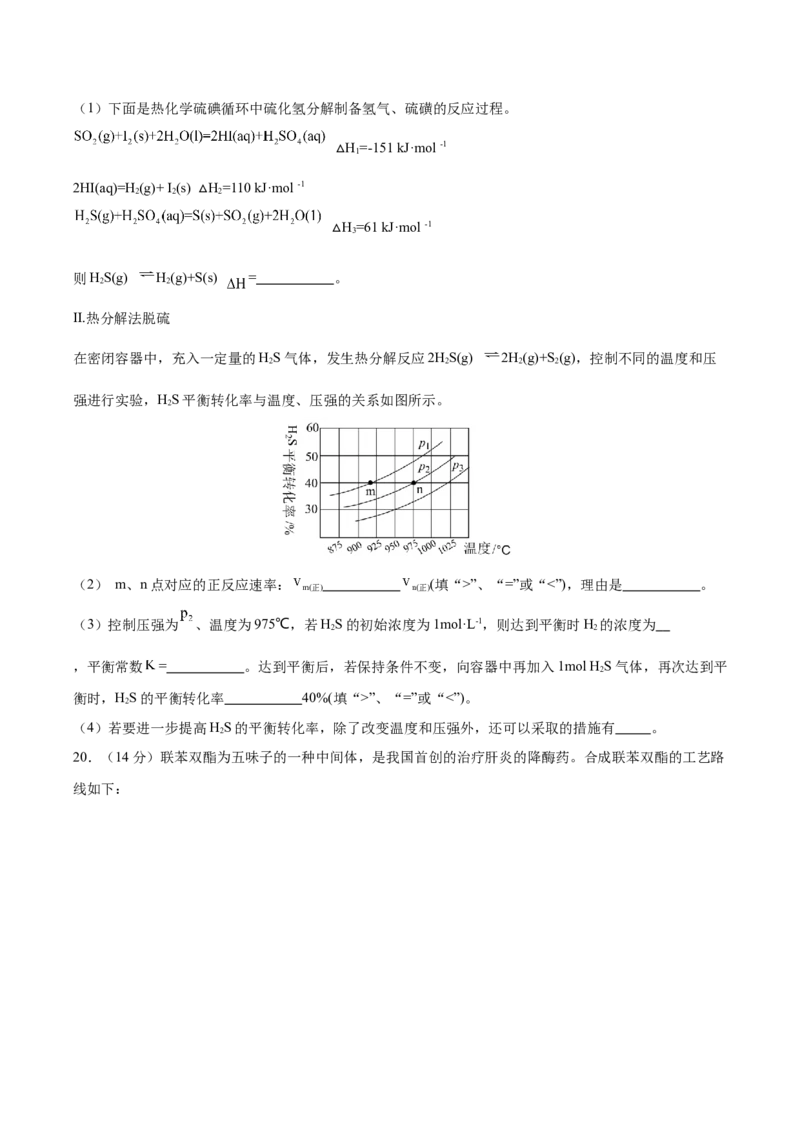
在密闭容器中,充入一定量的HS气体,发生热分解反应2HS(g) 2H(g)+S (g),控制不同的温度和压
2 2 2 2
强进行实验,HS平衡转化率与温度、压强的关系如图所示。
2
(2) m、n点对应的正反应速率: (填“>”、“=”或“<”),理由是 。
m(正) n(正)
(3)控制压强为 、温度为975℃,若HS的初始浓度为1mol·L-1,则达到平衡时H 的浓度为
2 2
,平衡常数 = 。达到平衡后,若保持条件不变,向容器中再加入1mol HS气体,再次达到平
2
衡时,HS的平衡转化率 40%(填“>”、“=”或“<”)。
2
(4)若要进一步提高HS的平衡转化率,除了改变温度和压强外,还可以采取的措施有 。
2
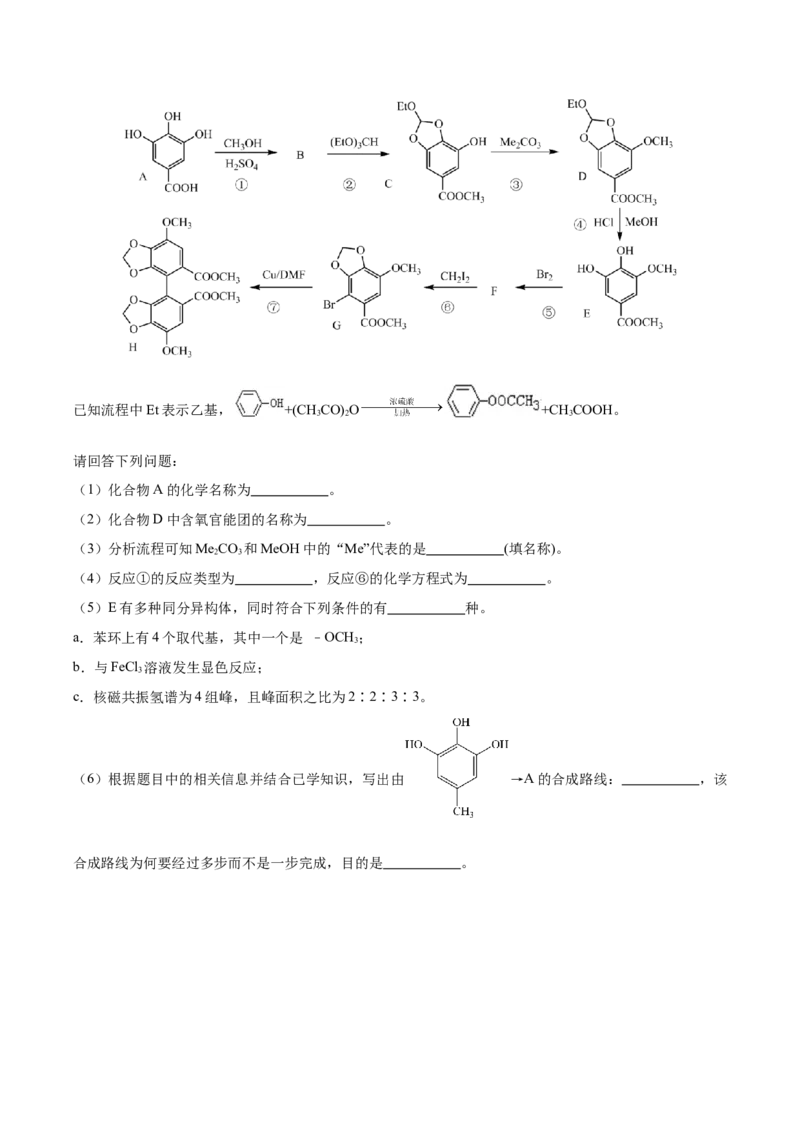
20.(14分)联苯双酯为五味子的一种中间体,是我国首创的治疗肝炎的降酶药。合成联苯双酯的工艺路
线如下:已知流程中Et表示乙基, +(CH CO) O +CH COOH。
3 2 3
请回答下列问题:
(1)化合物A的化学名称为 。
(2)化合物D中含氧官能团的名称为 。
(3)分析流程可知MeCO 和MeOH中的“Me”代表的是 (填名称)。
2 3
(4)反应①的反应类型为 ,反应⑥的化学方程式为 。
(5)E有多种同分异构体,同时符合下列条件的有 种。
a.苯环上有4个取代基,其中一个是 –OCH ;
3
b.与FeCl 溶液发生显色反应;
3
c.核磁共振氢谱为4组峰,且峰面积之比为2∶2∶3∶3。
(6)根据题目中的相关信息并结合已学知识,写出由 →A的合成路线: ,该
合成路线为何要经过多步而不是一步完成,目的是 。