文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(全国卷新教材)
黄金卷02
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 O 16 Si 28 Al 27 K 39 Fe 56 Cu 64
第Ⅰ卷
一、单项选择题:共14题,每题3分,共42分。每题只有一个选项最符合题意。
1.化学与社会发展和人类进步息息相关。下列说法错误的是
A.华为Mate60pro系列“争气机”的芯片材料主要为晶体硅
B.用机械剥离法从石墨中分离出的石墨烯能导电,石墨烯与金刚石互为同素异形体
C.国产飞机C919用到的氮化硅陶瓷是新型无机非金属材料
D.维生素C可用作水果罐头的抗氧化剂是由于其难以被氧化
【答案】D
【详解】A.单晶硅可用于制作计算机芯片,华为Mate60pro系列“争气机”的芯片材料主要为晶体硅,A
项正确;
B.石墨烯与金刚石均为碳的单质,它们互为同素异形体,B项正确:
C.氮化硅陶瓷是新型无机非金属材料,C项正确;
D.维生素C可用作水果罐头的抗氧化剂,是由于其具有强还原性,易于被氧化,D项错误;
故选D。
2.N 为阿伏伽德罗常数的值,下列说法正确的是
A
A.30gSiO 中含有硅氧键个数为N
2 A
B.将1molNH Cl与少量的稀氨水混合后,溶液呈中性,则溶液中NH 数目为N
4 A
C.标准状况下,44.8LNO和22.4LO 反应后的分子数是2N
2 A
D.常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3N
A
【答案】B
【详解】A.1molSiO 含4molSi-O键,30gSiO 中含有硅氧键个数为2N ,故A错误;
2 2 A
B.将1molNH Cl与少量的稀氨水混合后,溶液呈中性,根据电荷守恒有:n(NH )+n(H+)=n(OH-)+n(Cl-),
4
溶液呈中性n(H+)=n(OH-),则溶液中NH 数目为N ,故B正确;
AC.标况下44.8LNO和22.4LO 反应后生成NO ,有一部分NO 转化为NO,因此反应后的分子数小于
2 2 2 2 4
2N ,故C错误;
A
D.常温下,铝片投入足量的浓硫酸中发生钝化,故D错误;
答案选B。
3.下列过程的离子方程式书写正确的是
A.用FeS除去废水中的Hg2+:FeS(s)+Hg2+(aq)=HgS(s)+Fe2+(aq)
B.向NaHSO 溶液中滴加Ba(OH) 溶液至中性:H++ +Ba2++OH﹣=BaSO ↓+H O
4 2 4 2
C.将Fe O 溶于过量HI溶液:Fe O+6H+=2Fe3++3H O
2 3 2 3 2
D.用醋酸处理水垢中的氢氧化镁:Mg(OH) +2H+=Mg2++2H O
2 2
【答案】A
【详解】A.用FeS除去废水中的Hg2+的离子方程式为:FeS(s)+Hg2+(aq)=HgS(s)+Fe2+(aq),故A正确;
B.向NaHSO 溶液中滴加Ba(OH) 溶液至中性:2H++ +Ba2++2OH﹣=BaSO ↓+2H O,故B错误;
4 2 4 2
C.将Fe O 溶于过量HI溶液时,Fe O 在酸性环境下与碘离子发生氧化还原反应生成Fe2+、碘单质和
2 3 2 3
HO,离子方程式为Fe O+2I﹣+6H+=2Fe2++I +3H O,故C错误;
2 2 3 2 2
D.醋酸是弱酸,不能拆开,应为Mg(OH) +2CH COOH=Mg2++2CH COO﹣+2H O,故D错误;
2 3 3 2
故选:A。
【点评】本题考查离子方程式的书写判断,明确物质性质、反应实质为解答关键,注意掌握离子方程式的
书写原则,试题侧重考查学生的分析能力及规范答题能力。
4.下列化学用语表达正确的是
A.碳的基态原子的轨道表示式:
B.甲烷分子和四氯化碳分子的空间填充模型均为:
C.CHCH(CH )CHCOOH 的名称:2-甲基丁酸
3 3 2
D.CHOH分子中,碳原子与氧原子之间的共价键: sp3 p 键
3
【答案】A
【详解】A.碳的基态原子电子排布式为1s22s22p2,轨道表示式: ,故A正确;B.甲烷分子和四氯化碳分子都是正四面体形,但原子半径:Cl>C>H,该模型不能表示四氯化碳分子的空
间填充模型,故B错误;
C.CHCH(CH )CHCOOH中羧基碳为1号碳,甲基在3号碳原子上,命名为:3-甲基丁酸,故C错误;
3 3 2
D.CHOH分子中C原子杂化方式为sp3杂化,O原子杂化方式也是sp3杂化,碳原子与氧原子之间的共价
3
键:sp3-sp3σ键,故D错误;
故选A。
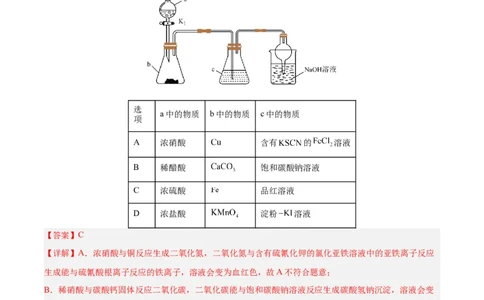
5.常温下,实验室利用如图装置进行实验,仪器 中无明显现象的是
选
a中的物质 b中的物质 c中的物质
项
A 浓硝酸 含有 的 溶液
B 稀醋酸 饱和碳酸钠溶液
C 浓硫酸 品红溶液
D 浓盐酸 淀粉 溶液
【答案】C
【详解】A.浓硝酸与铜反应生成二氧化氮,二氧化氮与含有硫氰化钾的氯化亚铁溶液中的亚铁离子反应
生成能与硫氰酸根离子反应的铁离子,溶液会变为血红色,故A不符合题意;
B.稀硝酸与碳酸钙固体反应二氧化碳,二氧化碳能与饱和碳酸钠溶液反应生成碳酸氢钠沉淀,溶液会变
混浊,故B不符合题意;
C.常温下,铁在浓硫酸中会发生钝化,致密的钝化膜阻碍反应的继续进行,不可能生成能使品红溶液褪
色的二氧化硫,所以品红溶液中无明显现象,故C符合题意;
D.浓盐酸与高锰酸钾固体反应生成氯气,氯气能与淀粉碘化钾溶液中的碘化钾反应生成单质碘,溶液会
变为蓝色,故D不符合题意;
故选C。6.化石燃料燃烧会产生大气污染物 、 等,科学家实验探究用硫酸铈循环法吸收 ,其转化原理
如图所示,下列说法正确的是
A.检验 可以选用盐酸酸化的 溶液
B.反应①的离子方程式为
C.反应②中氧化剂与氧化产物的物质的量之比为1:2
D.理论上每吸收标准状况下 ,一定消耗
【答案】B
【详解】A.硫酸根的检验需要先加入盐酸排查银离子的干扰,再加氯化钡产生白色沉淀证明有硫酸根,
A错误;
B.从图中看,反应①中氧化剂是 ,还原剂是 ,两者发生氧化还原反应生成 、 ,方程式
为 , B正确;
C.反应②中氧气中氧元素化合价由0变为-2,为氧化剂, 化合价升高发生氧化反应得到氧化产物
,根据电子守恒可知 ,故氧化剂与氧化产物的物质的量之比为1:4,C错误;
D.根据电子守恒可知 ,理论上每吸收标准状况下 (为0.01mol),消耗
0.005mol氧气,为0.16g,D错误;
故选B。
7.迷迭香酸是从蜂花属植物中提取得到的酸性物质,其分子结构如图所示,下列叙述正确的是A.迷迭香酸的分子式为
B.迷迭香酸可以发生氧化、还原、取代、消去、缩聚等反应
C.1mol迷迭香酸与烧碱溶液共热反应时最多消耗6mol NaOH
D.迷迭香酸分子中碳原子的杂化方式只有 杂化
【答案】C
【详解】A.由键线式分析分子式为 ,A错误;
B.迷迭香酸不能发生消去反应,B错误;
C.酚羟基、酯基、羧基均能和氢氧化钠反应,则1mol迷迭香酸与烧碱溶液共热反应时最多消耗6mol
NaOH,C正确;
D.迷迭香酸分子中碳原子的杂化方式有 和 杂化,D错误;
故选C。
8.中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量含氧橄榄石矿物(Z W RX)。
x 2-x 4
已知前四周期元素X、Y、Z、R、W的原子序数依次增大,Y的氢化物常用于雕刻玻璃,R元素的一种氧
化物可制作光导纤维,W的合金材料是生活中用途最广泛的金属材料,基态Z原子核外s,p能级上电子
总数相等。下列叙述正确的是
A.原子半径:Z>R>Y>X
B.X的第一电离能比同周期相邻元素小
C.X的简单氢化物的热稳定性强于Y的简单氢化物
D.熔点:ZY>RX
2 2
【答案】B
【分析】Y的氢化物常用于雕刻玻璃,则Y为氟元素;R元素的一种氧化物可制作光导纤维,故R为硅元素;
W的合金材料是生活中用途最广泛的金属材料,故W为铁元素,前四周期中只有氧、镁原子的s,p能级
上电子总数相等,根据原子系数递增可得Z为镁元素,X为氧元素。
【详解】A.原子半径根据元素周期律从上往下逐渐增大,从左往右逐渐减小,可得Z>R>X>Y,A错误;
B.根据电离能从左到右逐渐增大可得氟大于氧,但特殊的是氮原子2p轨道处于较稳定的半充满状态而氧
原子的不是,故氮大于氧,B正确;
C.从左往右气态氢化物的稳定性逐渐增强,故O的简单氢化物的热稳定性弱于F的简单氢化物,C错误;
D.二氧化硅是原子晶体熔点高于二氟化镁离子晶体,D错误;
故选B。
9.下列方案设计、现象和结论正确的是
选项 实验目的 实验方案 现象或结论
判断KCl的化学 将KCl固体溶于水,进行导电
A 溶液可导电,说明KCl中含有离子键
键类型 性实验
向鸡蛋清溶液中滴加饱和 溶液变浑浊,再加水浑浊消失说明鸡蛋清
B 检验蛋白质性质
(NH )SO 溶液 溶液发生了盐析
4 2 4
检验溶液中是否 取少量该溶液于试管中,滴加 有白色沉淀生成,说明该溶液中一定含有
C
含有SO BaCl 溶液 SO
2
探究不同价态硫 向NaS与NaSO 的混合溶液中 溶液变浑浊,说明NaS与NaSO 之间发生
D 2 2 3 2 2 3
元素的转化 加入硝酸 了氧化还原反应
【答案】B
【详解】A.KCl为强电解质,不管K与Cl之间存在离子键还是共价键,在水中都可发生完全电离,生成
K+和Cl-,所以不能证明KCl中含有离子键,A错误;
B.蛋白质中加入盐,出现盐析现象,B正确;
C.若溶液中含有 或Ag+,可以生成BaCO 、AgCl均为白色沉淀,则可以先通入HCl,若无现象出现
3
再加入BaCl 溶液,出现沉淀说明溶液中含有 ,C错误;
2
D.硝酸具有强氧化性,也能与硫化钠溶液发生氧化还原反应生成硫沉淀,则溶液变混浊不能说明硫化钠
溶液和亚硫酸钠溶液酸性条件下发生了氧化还原反应,D错误;
故答案:B。
10.利用反应 可实现从燃煤烟气中回收硫。向三个体积相同
的恒容密闭容器中通入 和 发生反应,反应体系的总压强随时间的变化如图所示。
下列说法错误的是A.实验b中,40min内CO的平均反应速率
B.与实验a相比,实验b改变的条件是加入催化剂
C.实验b中 的平衡转化率是75%
D.实验abc相应条件下的平衡常数:
【答案】D
【分析】反应为放热反应,三个反应容器体积相同且恒容,反应物起始量相同,实验a、b起始压强相同,
说明反应温度相同,实验b达到平衡快,反应速率大,但两者平衡状态相同,说明实验b使用了催化剂;
与实验a相比,实验c达到平衡快,反应速率大,且平衡时体系压强大,说明实验c的反应温度更高。
【详解】A.对反应 ,反应时混合气体减小的物质的量相同于消耗SO
2
的物质的量,根据压强之比等于物质的量之比,实验b中, 40min内体系压强减小了 ,相当于二氧
化硫的分压强减小了40kPa,则CO的分压强减小了80kPa,故CO的平均反应速率为
,A正确;
B.根据分析知实验b改变的条件是加入催化剂,B正确;
C.设达到平衡状态时,SO 消耗了 ,列三段式得:
2
40min达到平衡,此时压强为120kPa,根据压强之比等于物质的量之比,得: ,解
得 ,故二氧化硫的转化率为 ,C正确;D.平衡常数只受温度影响,根据分析知实验a、b反应温度相同,则 。反应 ,说明该反应
是放热反应,升高温度,平衡逆向移动,平衡常数减小,实验c 温度比实验a、b高,则 ,D
错误;
故选D。
11.某溶液中可能含有 、 、 、 、 、 和 ,取该溶液 ,加入过量
溶液,加热,得到 气体,同时产生红褐色沉淀,过滤、洗涤、灼烧,得到 固体;向上述滤液
中加足量 溶液,得到 不溶于盐酸的沉淀,由此可知原溶液中
A.至少存在3种离子 B. 一定存在,且
C. 、 一定存在, 不能确定 D. 、 一定不存在, 可能存在
【答案】B
【分析】由溶液中加入过量氢氧化钠溶液,加热,得到气体和红褐色沉淀可知,溶液中一定含有铵根离子
和铁离子,则溶液中一定不含有碳酸根离子,由原子个数守恒可知,溶液中铵根离子的物质的量为
0.02mol,铁离子的物质的量为 ×2=0.02mol;向滤液中加入足量氯化钡溶液,产生不溶于盐酸的
沉淀说明溶液中含有硫酸根离子,由硫酸钡的质量可知,溶液中硫酸根离子的物质的量为
=0.02mol,阳离子电荷总数为0.02mol+3×0.02mol=0.08mol,阴离子电荷总数为2×0.02mol=0.04mol,阳离
子电荷总数大于阴离子电荷总数,则由电荷守恒可知,溶液中一定含有氯离子,无法确定是否含有铝离子
和钾离子。
【详解】A.由分析可知,溶液中一定含有铵根离子、铁离子、硫酸根离子和氯离子,一定不含有碳酸根
离子,无法确定是否含有铝离子和钾离子,故A错误;
B.由分析可知,溶液中一定含有铵根离子、铁离子、硫酸根离子和氯离子,一定不含有碳酸根离子,无
法确定是否含有铝离子和钾离子,则由电荷守恒可知,溶液中氯离子浓度不小于
=0.4mol/L,故B正确;C.由分析可知,溶液中一定含有铵根离子、铁离子、硫酸根离子和氯离子,故C错误;
D.由分析可知,溶液中一定不含有碳酸根离子,无法确定是否含有铝离子,故D错误;
故选B。
12.氮化钛为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品。 晶体的晶
胞结构如图所示(白球代表N,黑球代表Ti)。下列说法错误的是
A.基态 原子的价层电子排布式为
B. 均位于N构成的八面体空隙中
C.该晶胞中含有6个 原子和4个N原子
D. 元素位于元素周期表d区,是过渡元素
【答案】C
【详解】A.Mn是25号元素,处于第四周期第VIIB族,核外电子排布式为:1s22s22p63s23p63d54s2,价层
电子排布式为 ,A正确;
B.由晶胞结构可知,钛原子位于氮原子构成的八面体空隙中,B正确;
C.由晶胞结构可知,晶胞中位于棱上和体心的Ti原子个数为 ,位于顶点和面心的N原子个数
为 ,C错误;
D.钛元素的原子序数为22,价电子排布式为 ,是位于元素周期表d区的过渡元素,D正确;
答案选C。
13.新能源汽车在我国蓬勃发展,新能源汽车所用电池多采用三元锂电池,某三元锂电池放电时工作原理
如图所示。下列说法错误的是A.充电时,M极有电子流入,发生还原反应
B.锂电池的优点是质量小,电容量大,可重复使用
C.用该电池电解精炼铜,当电池中迁移 时,理论上可获得 纯铜
D.充电时,N极的电极反应式为
【答案】C
【分析】原电池中阳离子向正极移动,由图中锂离子运动方向可知,M为负极、N为正极;
【详解】A.充电时,M极连接外接电源的负极,M为阴极,阴极有电子流入,发生还原反应,A正确;
B.锂电池的能量比较高,优点是质量小,电容量大,可重复使用,B正确;
C.根据电子守恒可知, ,当电池中迁移 时,理论上可获得32g纯铜,C错误;
D.充电时,N极为阳极,发生氧化反应,电极反应式为 ,D
正确;
故选C。
14.已知 ,25℃时, 的 , 。常温下,用0.1mol·L NaOH溶液滴定
20mL0.1mol·L 溶液的滴定曲线如图所示。下列说法错误的是A.a点加入NaOH溶液的体积 mL
B.a、b、c、d四点所得溶液均满足:
C.当加入NaOH溶液的体积为80mL时,有
D.a、b、c、d四点对应的溶液中水的电离程度:a