文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(上海专
用)
黄金卷03
(考试时间:60分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64
一、文物保护中的化学知识(本题共18分)
铜锈为 Cu(OH)CO, 俗称铜绿,可溶于酸。出土铜器多带有铜锈。
2 2 3
1.《我在故宫修文物》这部纪录片里关于古代青铜器的修复引起了某研学小组的兴趣。
“修旧如旧”是文物保护的主旨。(18分)
(1)请写出铜绿与盐酸反应的化学方程式
(2)继续查阅中国知网,了解到铜锈的成分非常复杂,主要成分有Cu (OH) CO 和
2 2 3
Cu (OH) Cl。考古学家将铜锈分为无害锈和有密锈,结构如图所示:
2 2
① Cu (OH) CO 可否作无害锈,请解释原因。
2 2 3
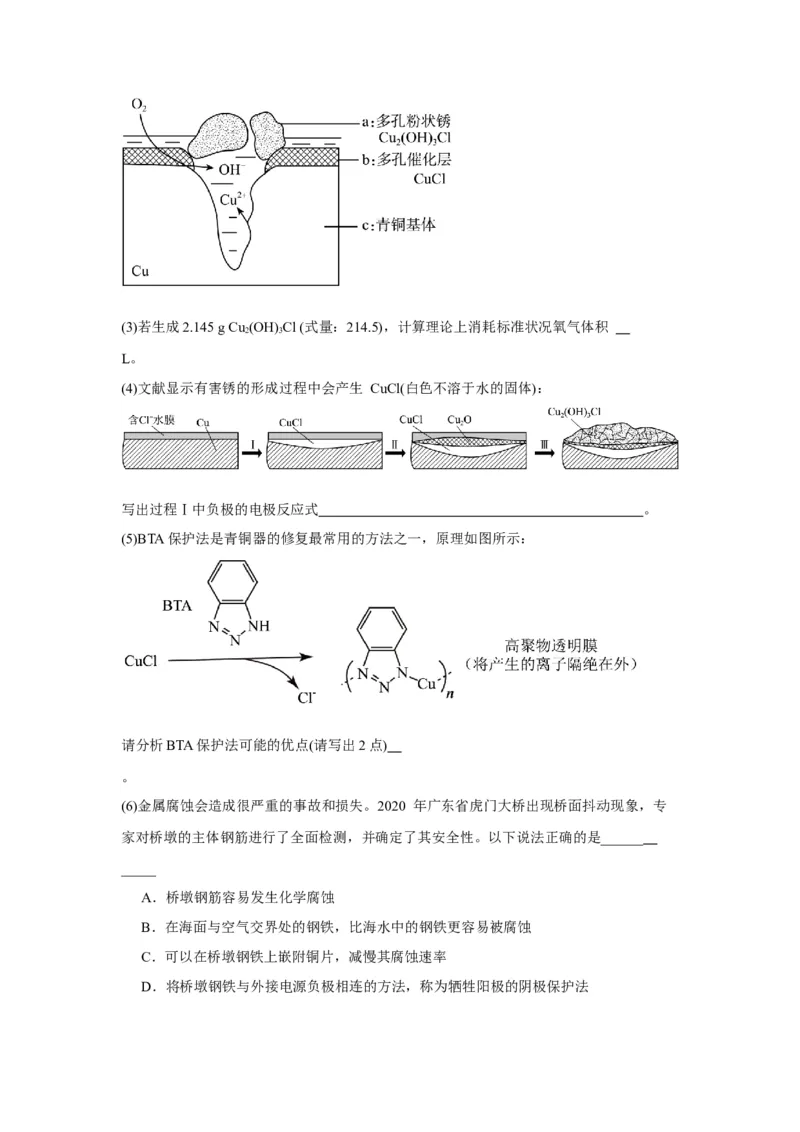
② 如图为青铜器在潮湿环境中发生电化学腐蚀生成有害锈Cu (OH) Cl的原理示
2
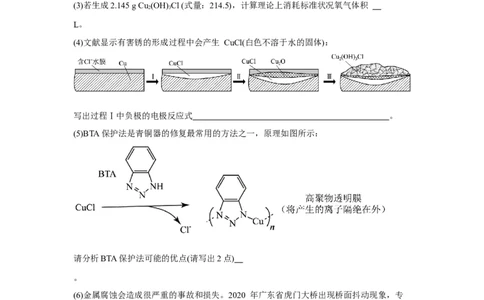
意图:(3)若生成2.145 g Cu (OH) Cl (式量:214.5),计算理论上消耗标准状况氧气体积
2 3
L。
(4)文献显示有害锈的形成过程中会产生 CuCl(白色不溶于水的固体):
写出过程Ⅰ中负极的电极反应式 。
(5)BTA保护法是青铜器的修复最常用的方法之一,原理如图所示:
请分析BTA保护法可能的优点(请写出2点)
。
(6)金属腐蚀会造成很严重的事故和损失。2020 年广东省虎门大桥出现桥面抖动现象,专
家对桥墩的主体钢筋进行了全面检测,并确定了其安全性。以下说法正确的是______
_____
A.桥墩钢筋容易发生化学腐蚀
B.在海面与空气交界处的钢铁,比海水中的钢铁更容易被腐蚀
C.可以在桥墩钢铁上嵌附铜片,减慢其腐蚀速率
D.将桥墩钢铁与外接电源负极相连的方法,称为牺牲阳极的阴极保护法二、次氯酸钠处理氮氧化物等有害尾气 (本题共22分)
含氯物质在生产、生活中有重要作用。工业上常用次氯酸钠处理含有NO等氮氧化物的尾气,
反应方程式如下:NaClO + NO + HO —— NaCl + HNO (未配平)。
2 3
2. 完成下列填空。(22分)
(1)氯在元素周期表中的位置是 ,其所在主族的元素中,
最高价氧化物对应的水化物酸性最强的是 (填化学式)。
(2)配平上述反应方程式 。
每有0.3mol电子发生转移,可消耗标准状况下NO气体的体积约为 L。
(3)NaClO溶液中存在如下关系:c(OH-) c(HClO)(填“>”、“=”、或
“<”)。
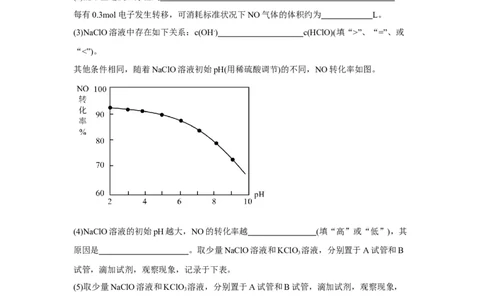
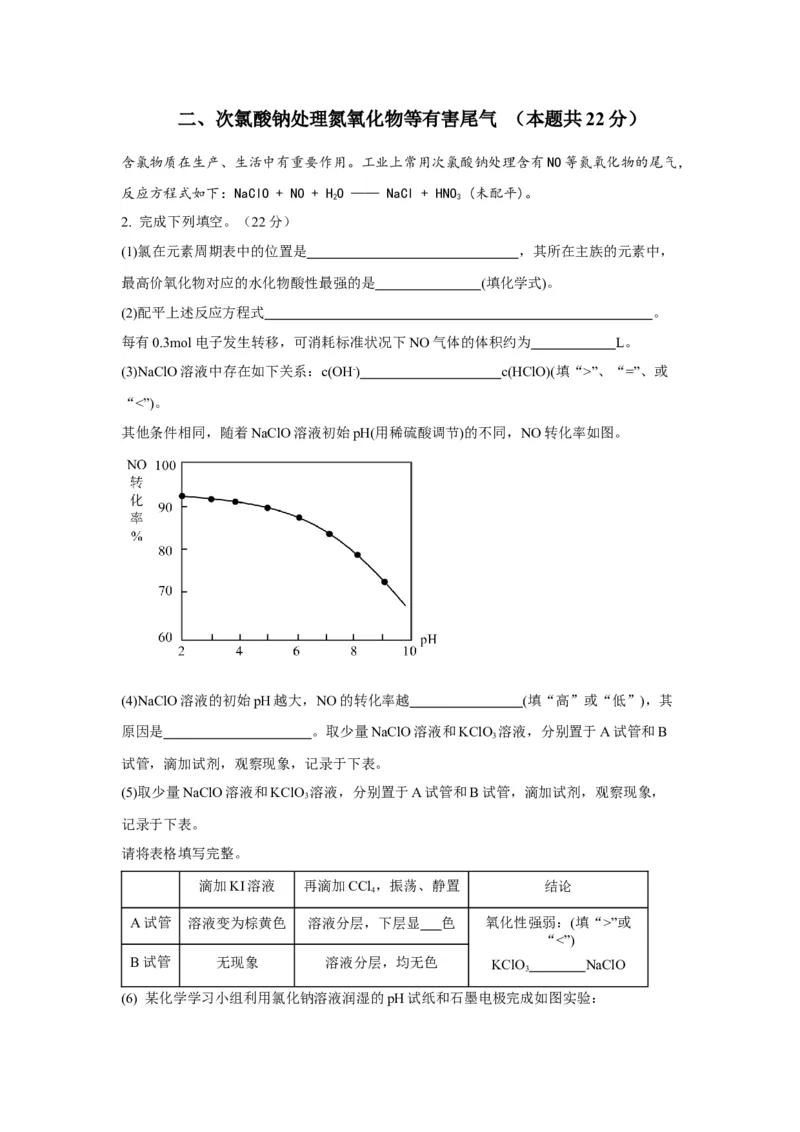
其他条件相同,随着NaClO溶液初始pH(用稀硫酸调节)的不同,NO转化率如图。
(4)NaClO溶液的初始pH越大,NO的转化率越 (填“高”或“低”),其
原因是 。取少量NaClO溶液和KClO 溶液,分别置于A试管和B
3
试管,滴加试剂,观察现象,记录于下表。
(5)取少量NaClO溶液和KClO 溶液,分别置于A试管和B试管,滴加试剂,观察现象,
3
记录于下表。
请将表格填写完整。
滴加KI溶液 再滴加CCl ,振荡、静置 结论
4
A试管 溶液变为棕黄色 溶液分层,下层显 色 氧化性强弱:(填“>”或
“<”)
B试管 无现象 溶液分层,均无色 KClO NaClO
3
(6) 某化学学习小组利用氯化钠溶液润湿的pH试纸和石墨电极完成如图实验:下列说法错误的是
A.a处试纸变蓝色
B.b处只发生反应2Cl--2e-=Cl↑
2
C.d处发生的反应为2HO+2e-=H ↑+2OH-
2 2
D.c极为阳极
三、重要的化工原料 —— 硫酸亚铁铵(本题共20分)
(NH)Fe(SO)·6HO(硫酸亚铁铵)是一种重要的化工原料,用途广泛。
4 2 4 2 2
3. 完成下列填空:(20分)
(1)Fe的电子排布式为1s22s22p63s23p63d64s2,铁原子核外有 种能量不同的电子,占有的
轨道总数是 个。铁在元素周期表的第ⅦB和第
ⅠB之间。铁位于第 周期 族。
(2)将(NH )Fe(SO ) 中非金属元素的简单负离子按半径由小到大的顺序排列:
4 2 4 2
。
(3) 1mol·L-1硫酸亚铁铵溶液中各微粒浓度的大小排序正确的是( )
A. c(SO )>c(NH )>2c(Fe2+)> c(H+)>c(OH—)
2− +
❑ ❑
4 4
B. c(SO )>c(NH )>2c(Fe2+)>c(OH—)> c(H+)
2− +
❑ ❑
4 4
C. c(NH )>c(SO )>>2c(Fe2+)>c(OH—)> c(H+)
+ 2−
❑ ❑
4 4
D. c(SO )=c(NH )>2c(Fe2+)>c(OH—)> c(H+)
2− +
❑ ❑
4 4
(4)设计实验,证明(NH )Fe(SO )·6H O晶体中含有Fe2+
4 2 4 2 2
。
(5)已知:(NH )Fe(SO )·6H O在200℃失去全部结晶水。将一定质量的粉末状该晶体置于
4 2 4 2 2
坩埚中,保持200℃受热,经冷却、恒重等正确操作,计算得到的1mol晶体中结晶水含量
总是偏低,偏低的可能原因是(写一条即可)。
四、 酸雨及其形成气体(本题共15分)
空气质量与我们的健康息息相关,目前我国通过监测6项污染物的百分比浓度来计算空气
质量指数(AQI),SO、NO 和CO是其中3项中的污染物。(15分)
2 2
4. 酸雨的形成可能由多种气体造成的,保护环境刻不容缓,工厂产生的有害气体必须经过
处理才可以排放至大气当中。
(1)上述3种气体直接排入空气后会引起酸雨的气体有 (填化学式)。
❑
(2)早期人们曾经使用铅室法生产硫酸,其主要反应为:SO (g)+NO (g) SO (g)+NO(g)
2 2 ⇌ 3
❑
❑ ❑
①若已知2SO (g)+O(g) 2SO (g) + Q 2NO(g)+O(g) 2NO (g) + Q
2 2 ⇌ 3 1 2 ⇌ 2 2
❑ ❑
❑
则SO (g)+NO (g) SO (g)+NO(g)+ Q , Q= kJ·mol-1。
2 2 ⇌ 3 3 3
❑
②一定温度下,向固定体积为2 L的密闭容器中充入SO 和NO 各1 mol,发生反应:
2 2
❑
SO (g)+NO (g) SO (g)+NO(g)。下列事实中不能说明该反应达到平衡状态的是 (选
2 2 ⇌ 3
❑
填序号)。
a.体系压强保持不变 b.混合气体的颜色保持不变
c.NO的物质的量保持不变 d.每生成1 mol SO 的同时消耗1 mol NO
3 2
(3)矿石燃料的燃烧是造成酸雨的主要因素之一 。而甲醇日趋成为重要的有机燃料,通常
❑
利用CO和H 合成甲醇,其反应的化学方程式为CO(g)+ 2H(g) CHOH(g)。今在一容
2 2 ⇌ 3
❑
积可变的密闭容器中,充有10 mol CO和20 mol H ,用于合成甲醇。CO的平衡转化率(α)
2
与温度(T)、压强(P)的关系如图所示:
①上述合成甲醇的反应为 反应(填“放热”或“吸热”)。
②A、B、C三点的平衡常数K 、K 、K 的大小关系为 。
A B C五、帕金森治疗药物盐酸罗替戈汀的合成(本题共25分)
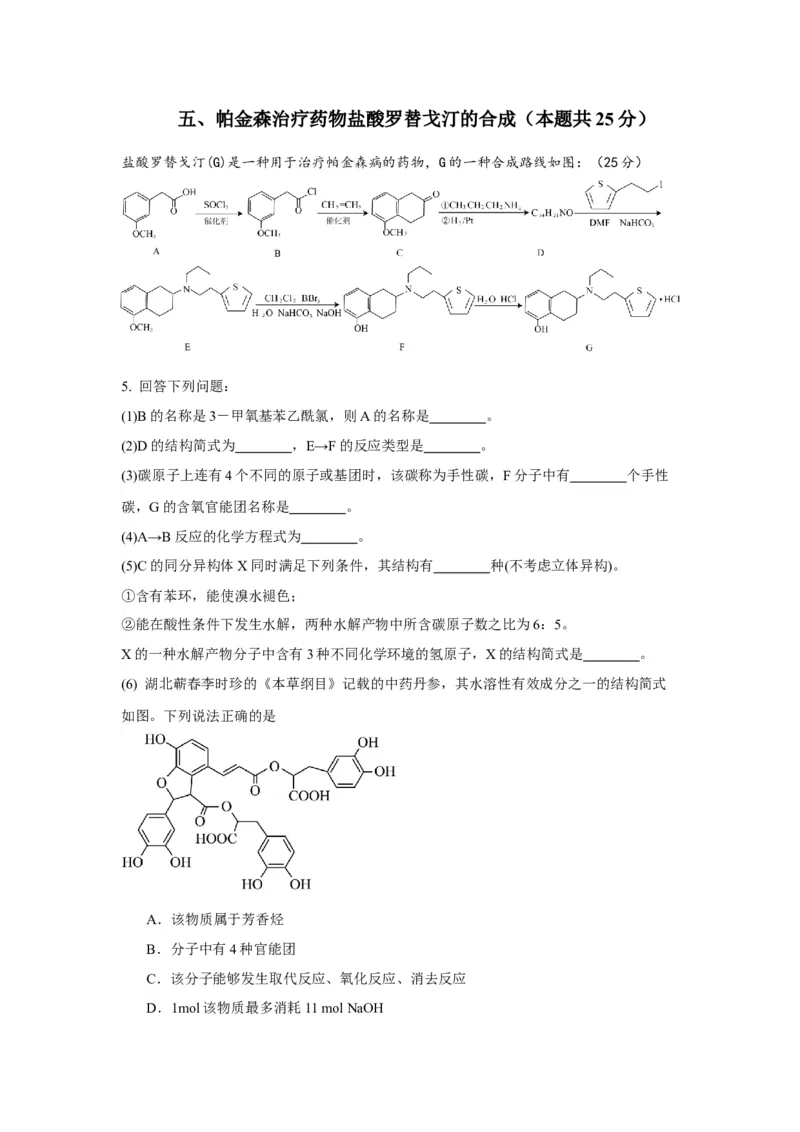
盐酸罗替戈汀(G)是一种用于治疗帕金森病的药物,G的一种合成路线如图:(25分)
5. 回答下列问题:
(1)B的名称是3-甲氧基苯乙酰氯,则A的名称是 。
(2)D的结构简式为 ,E→F的反应类型是 。
(3)碳原子上连有4个不同的原子或基团时,该碳称为手性碳,F分子中有 个手性
碳,G的含氧官能团名称是 。
(4)A→B反应的化学方程式为 。
(5)C的同分异构体X同时满足下列条件,其结构有 种(不考虑立体异构)。
①含有苯环,能使溴水褪色;
②能在酸性条件下发生水解,两种水解产物中所含碳原子数之比为6:5。
X的一种水解产物分子中含有3种不同化学环境的氢原子,X的结构简式是 。
(6) 湖北蕲春李时珍的《本草纲目》记载的中药丹参,其水溶性有效成分之一的结构简式
如图。下列说法正确的是
A.该物质属于芳香烃
B.分子中有4种官能团
C.该分子能够发生取代反应、氧化反应、消去反应
D.1mol该物质最多消耗11 mol NaOH