文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(广东专用)
黄金卷03
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H- 1 C -12 N-14 O -16 S-32 Cl 35.5 K 39 Pt 195
第Ⅰ卷
一、选择题:本题共16个小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在
每小题给出的四个选项中,只有一项是符合题目要求的。
1.2023中国景德镇国际陶瓷博览会在江西景德镇举办。以下关于陶瓷说法正确的是
A.CaCO 是陶瓷的主要成分
3
B.烧结黏土制陶瓷属于物理变化
C.“雨过天晴云破处”所描述瓷器的青色与氧化铁有关
D.某种硅酸盐的主要成分为KAlSi O,用氧化物形式表示为
3 8
【答案】D
【解析】A.陶瓷属于传统硅酸盐产品,主要成分为硅酸盐,A错误;
B.从黏土到陶瓷需要经过高温煅烧,黏土中易分解的物质,如碳酸盐等,在煅烧过程中,均会发生分解,
故属于化学变化,B错误;
C.氧化铁的颜色为红棕色,故瓷器的青色不可能是Fe O 造成,C错误;
2 3
D.硅酸盐改写后不能改变原子比例和元素化合价,故KAlSi O 改写成氧化物形式为:KO·Al O·6SiO,
3 8 2 2 3 2
D正确;
故答案选D。
2.我国科研人员创造出了迄今世界上最轻的镁原子 ,下列说法正确的是
A.镁离子结构示意图: B. 与18O具有相同的中子数
C.Mg的相对原子质量为18g/mol D.18Mg与24Mg互为同位素
【答案】D
【解析】A.镁原子失去最外层的2个电子变成镁离子,镁离子结构示意图为: ,A错误;
B.18Mg中子数为6, 18O中子数为10,中子数不相同,B错误;
C.Mg的相对原子质量为18,C错误;
D.18Mg与24Mg质子数相同中子数不同,互为同位素,D正确;
故选D。
3.化学改善人类的生活,创造美好的世界。下列生产生活情境中涉及的化学原理不正确的是选项 生产生活情境 化学原理
A 国庆节天安门广场燃放烟花,色彩绚丽 利用了某些金属的焰色反应
用氯化铁溶液刻蚀覆铜板制作印刷电路
B 铜与FeCl 发生置换反应
3
板
C 汽车尾气催化转化器处理NO和CO NO和CO发生反应生成无毒气体
秸秆、餐厨垃圾等进行密闭发酵提供燃
D 发酵过程中产生CH
4
料
【答案】B
【解析】A.金属元素发生焰色反应会出现不同的色彩,燃放的烟花即是某些金属元素发生焰色反应所呈
现出来的色彩,A正确;
B.用氯化铁溶液刻蚀覆铜板制作印刷电路板发生的反应为2Fe3++Cu=Cu2++2Fe2+,该反应不属于置换反应,
B错误;
C.汽车尾气催化转化器处理NO和CO,可以将二者转化为无毒的N、CO,C正确;
2 2
D.秸秆、餐厨垃圾中含有大量的有机物,发酵过程中产生CH,CH 是一种燃料,D正确;
4 4
综上所述答案为B。
4.丁烯基苯酞存在于当归等中药里,该物质具有抗凝血、抗氧化等功能,其结构简式如图所示。下列有
关丁烯基苯酞的说法错误的是
A.分子式为C H O B.官能团有碳碳双键
12 12 2
C.能使酸性高锰酸钾溶液褪色 D.不能与NaOH溶液反应
【答案】D
【解析】A. 由该有机物的结构简式可知其分子式为C H O,A正确;
12 12 2
B. 由该有机物的结构简式可知,其官能团中含有碳碳双键,B正确;
C. 因为含有碳碳双键,则能被酸性高锰酸钾溶液氧化,从而能使酸性高锰酸钾溶液褪色,C正确;
D. 该有机物含有酯基 -COO-,能与NaOH溶液发生水解反应,D错误;
故选D。
5.化学实验是化学探究的一种重要途径。下列有关实验的描述正确的是
A.用湿润的蓝色石蕊试纸检验
B.中学实验室中,可将未用完的钠放回原试剂瓶
C.进行焰色试验时,可用玻璃棒替代铂丝
D.酸碱中和滴定实验中,应先用待测液润洗锥形瓶
【答案】B【解析】A. 溶于水呈碱性,可以用湿润的红色石蕊试纸检验 ,故A错误;
B.易燃物如钠、钾等不能随便丢弃,中学实验室可以将未用完的钠、钾等放回原试剂瓶,故B正确;
C.玻璃的成分里边有硅酸钠,钠盐的焰色试验为黄色,对其他元素的试验存在干扰,进行焰色试验时,
不可用玻璃棒替代铂丝,故C错误;
D.酸碱中和滴定实验中,洗锥形不能用待测液润洗,否则会导致测量结果偏大,故D错误;
故选B。
6.离子鉴别能让我们感受微观世界的神奇。下列在透明溶液中能大量共存的离子组是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
【答案】A
【解析】A.该组离子彼此不 发生反应可以大量共存,故A正确;
B. 与 能发生氧化还原反应,不能大量共存,故B错误;
C. 与 和 均能发生完全双水解,不能大量共存,故C错误;
D. 与 能反应,不能大量共存,故D错误;
故选:A。
7.以熔融盐( 、 )为电解液,以石墨为阳极,电解 和 获取电池材料 ,下列说法正
确的是
A.阳极上 被还原 B.阴极发生的反应为
C.电解时,阳离子向阳极移动 D.理论上每生成 电路中转移 电子
【答案】D
【解析】A.石墨为阳极,电解池阳极发生氧化反应,A错误;
B. 和 为电池阴极,发生还原反应,反应方程式为 + +8e-=TiSi+4O2-,B错误;
C.电解时阳离子向阴极移动,阴离子向阳极移动,C错误;
D.由阴极电极反应式可知,每生成 ,电路中转移8mol电子,D正确;
故选D。
8.某金属有机多孔材料(MOFA)对 具有超高吸附能力,并能催化 与环氧丙烷反应,其工作原理如
图所示。下列说法错误的是
A.b分子中碳原子采用 和 杂化B.物质a为醚类有机物,与环氧乙烷互为同系物
C.1molb最多可与2molNaOH反应
D.a转化为b发生取代反应,并有非极性共价键的形成
【答案】D
【解析】A.b分子中存在单键碳,采用 杂化,羰基中的C原子采用 杂化,故A正确;
B.物质a为醚类有机物,与环氧乙烷结构相似,且组成上相差1个CH,两者互为同系物,故B正确;
2
C.由b的结构简式可知1molb中等同于含有2mol酯基,最多可消耗2molNaOH,故C正确;
D.a转化为b发生加成反应,由断键过程可知该转化过程中只形成了极性键,故D错误;
故选:D。
9.二乙胺[ ]是一种有机弱碱,可与盐酸反应生成盐酸盐 。下列叙述正确的是
A.0.01 水溶液的
B. 水溶液的pH随温度升高而减小
C. 水溶液加水稀释,pH降低
D. 水溶液中:
【答案】B
【解析】A.二乙胺是弱碱,其对应的盐酸盐溶液显酸性,水解是微弱的,所以0.01
水溶液的 ,故A错误;
B.由于 水解, 水溶液显酸性,加热能促进水解的进行,所以
水溶液的pH随温度升高而减小,故B正确;
C. 水溶液显酸性,加水稀释,溶液酸性减弱,pH增大,故C错误;
D. 水溶液中存在电荷守恒: ,
水解的方程式为: +H O +H O+,还存在着水的电离:HO H++OH-,所以
2 3 2
,故D错误;
故选B。
10.部分含氯物质的分类与相应化合价关系如图所示,下列说法不正确的是
A.a的浓溶液与KMnO 反应制得b B.b溶于水制得液氯
4C.c可用于自来水消毒 D.存在a→b→d→a的转化关系
【答案】B
【解析】A.a的浓溶液为-1价的氯的酸,为盐酸;盐酸与KMnO 反应发生氧化还原反应生成单质氯气
4
b,A正确;
B.氯气溶于水得到氯水,是混合物不是液态氯,B错误;
C.c为+4价氯形成的氧化物ClO ,具有氧化性,可用于自来水消毒,C正确;
2
D.abd为盐酸、氯气、次氯酸;浓盐酸和二氧化锰加热生成氯气、氯气和水生成次氯酸、次氯酸分解能生
成盐酸,存在a→b→d→a的转化关系,D正确;
故选B。
11.某化合物结构式为 ,W、X、Y、Z为原子序数依次增大的短周期元素,其中Y
与Z的原子序数差8,X元素在空气中的含量最大。下列说法正确的是
A.第一电离能:XY D.该化合物中Z的化合价均为 价
【答案】B
【解析】由化合物的结构式可知,Z形成6条共价键,Y形成2条共价键,Y与Z的原子序数差8,则Y、
Z分别为短周期第VIA族的O和S元素;W、X、Y、Z为原子序数依次增大,X元素在空气中的含量最大,
则X为N元素,W能形成1条共价键,且原子序数比N小,则W为H元素,综上,W、X、Y、Z分别为
H、N、O、S四种元素,据此分析解答。
A.第一电离能:氮>氧,A项错误;
B.XW 为NH ,氨气的空间结构为三角锥形,B项正确;
3 3
C.同一主族从上到下元素的非金属性逐渐减弱,元素的非金属性:氧>硫,C项错误;
D.根据化合物中元素化合价代数和为0,设硫元素化合价为x,则2x+(+1) 2+(-2) 6=0,解得x=5,即该
化合物中硫元素显 价,D项错误;
答案选B。
12.白磷易自燃,国际上明令禁止使用白磷弹,工业上可用来生产磷酸。白磷制备反应为:
2Ca (PO )+6SiO +10C 6CaSiO +P +10CO↑。设N 为阿伏加德罗常数。下列有关说法正确
3 4 2 2 3 4 A
的是
A.62 gP ( )中含P-P键数目为2N
4 A
B.30 gSiO 中分子数目为0.5N
2 A
C.1 mol/L Ca (PO ) 溶液中含有 数目为2N
3 4 2 AD.上述反应每生成1 mol CO时转移电子数目为2N
A
【答案】D
【解析】A.62gP 物质的量为 ,含P-P键数目为:0.5mol×6×N mol-1=3N ,故A
4 A A
错误;
B.二氧化硅为共价晶体,不含分子,故B错误;
C.溶液体积未知,无法计算磷酸根离子数目,故C错误;
D.依据2Ca (PO )+6SiO +10C 6CaSiO +P +10CO↑,可得10CO~20e-,每生成1molCO时转移
3 4 2 2 3 4
电子数目为2N ,故D正确;
A
故选:D。
13.乙酸甲酯催化醇解反应方程式为:
,已知 , ,
其中 、 为速率常数, 为物质的量分数。己醇和乙酸甲酯按物质的量之比1∶1投料,测得
348K、338K两个温度下乙酸甲酯转化率 随时间 的变化关系如图所示,下列说法中错误的是
A.曲线①②中,曲线①对应的 更大
B.升高温度,该醇解平衡向正反应方向移动
C.a、b、c、d四点中, 与 差值最大的是b点
D.338K时,该反应的化学平衡常数为1
【答案】C
【解析】根据图像可知,①曲线的反应速率最快,说明温度高,即曲线①对应温度为348K,曲线②对应温
度为338K;
A.温度越高,反应速率越快, 值越大,根据分析以及图像可知,曲线①对应的 更大,故A说法正
确;
B.由图可知,温度越高,乙酸甲酯转化率越高,反应正向进行程度变大,说明反应为吸热反应,故升高
温度,该醇解平衡向正反应方向移动,故B说法正确;
C. 、 是温度的函数,该反应为吸热反应,升高温度,平衡向正反应方向进行, 受温度的影响较
大,因此升高温度, 增大程度大于 ,即 - 的值最大的是曲线①;据图像可知,a点是反应向正方向进行,c点为平衡点,随着反应进行,v 逐渐减小,v 逐渐增大,因此四点中, 与 差值最大的
正 逆
是a点,故C说法错误;
D.338K时,令乙酸甲酯的物质的量为1mol,C H OH的物质的量为1mol,则达到平衡时,消耗乙酸甲
6 13
酯、C H OH的物质的量均为1mol×50%=0.5mol,则生成CHCOOC H 和甲醇的物质的量为0.5mol,K=
6 13 3 6 13
,故D说法正确;故选C。
14.下列实验操作、现象与结论都正确的是
选项 操作 现象 结论
溴水与植物油发生取
A 往溴水中滴加植物油,振荡 溶液褪色
代反应
浓硫酸有吸水性和强
B 将浓硫酸滴到蔗糖表面 固体变黑膨胀
氧化性
在葡萄糖溶液中加入适量新制氢氧化
C 产生砖红色沉淀 葡萄糖具有还原性
铜悬浊液,加热
加热浸透石蜡油的矿物棉,将产生的 产生的气体一定含有
D 紫色溶液逐渐变浅
气体通入酸性高锰酸钾溶液 乙烯
【答案】C
【解析】A.植物油烃基部分含有不饱和的碳碳双键,可以与Br 发生加成反应,从而使溴水褪色,A结论
2
错误;
B.蔗糖遇浓硫酸变黑,是因为蔗糖被浓硫酸脱水炭化,体现浓硫酸脱水性,B结论错误;
C.葡萄糖与新制氢氧化铜反应产生砖红色沉淀,体现其还原性,C符合题意;
D.KMnO 溶液褪色,说明石蜡油分解产物中含有不饱和烃,但不一定是乙烯,D结论错误;
4
故答案选C。
15.将氯化氢转化为氯气是科学研究的热点。科学家设计了一种电解氯化氢回收氯气的方案,原理如图所
示。下列叙述错误的是
A.阴极的电极反应式为
B.工作时,溶液中 向b极移动
C.若消耗8g氧气,电路中转移1mol电子D.总反应为
【答案】B
【解析】根据电极反应左边化合价降低,得到电子,为电解池的阴极,右边化合价升高,失去电子,为电
解池的阳极。
根据电解池a、b电极表面的反应得a为阴极、b为阳极;
A.a极的电极方程式为 ,A正确;
B. 为阳离子,在电解池工作时应向阴极a极移动,B错误;
C.消耗1mol氧气转移4mol电子,8g氧气为 ,故转移0.25mol×4=1mol电子,C
正确;
D.根据电解池的工作图知反应物为 和HCl,生成物为 和 ,总反应为 ,
D正确;
故选B。
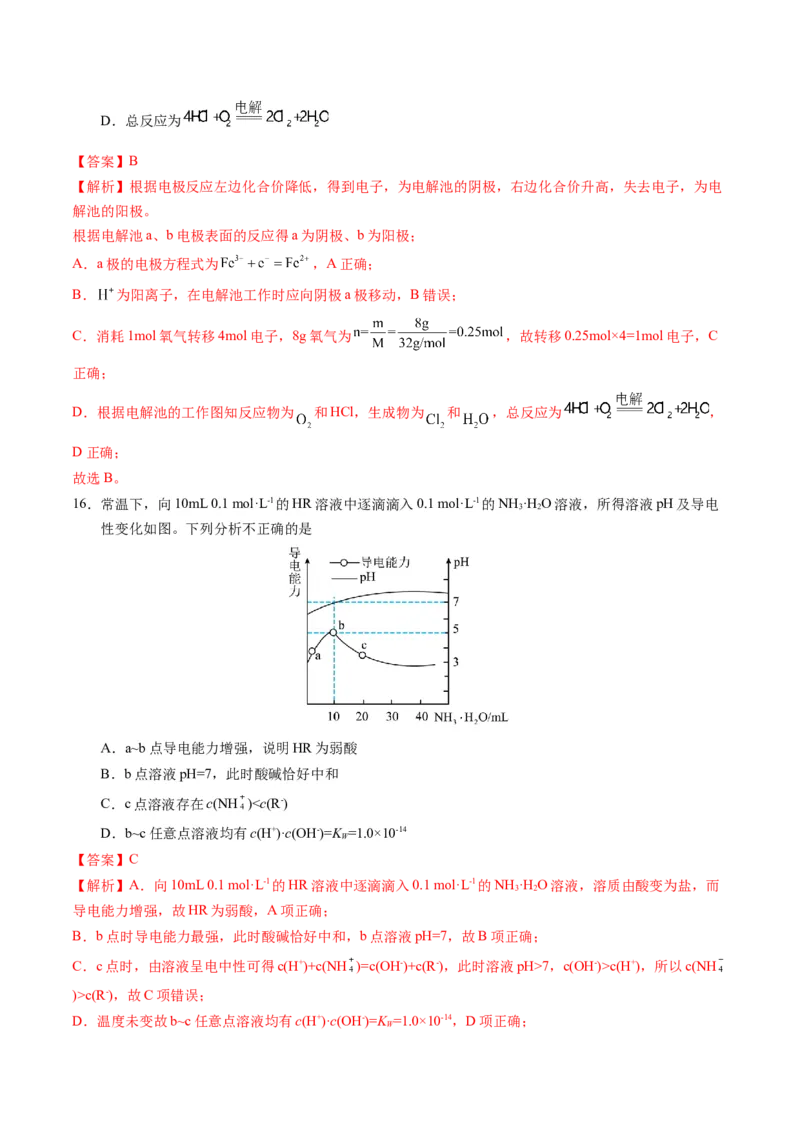
16.常温下,向10mL 0.1 mol·L-1的HR溶液中逐滴滴入0.1 mol·L-1的NH ·H O溶液,所得溶液pH及导电
3 2
性变化如图。下列分析不正确的是
A.a~b点导电能力增强,说明HR为弱酸
B.b点溶液pH=7,此时酸碱恰好中和
C.c点溶液存在c(NH )7,c(OH-)>c(H+),所以c(NH
)>c(R-),故C项错误;
D.温度未变故b~c任意点溶液均有c(H+)·c(OH-)=K =1.0×10-14,D项正确;
W答案选C。
第Ⅱ卷
二、非选择题:本题共4个小题,共56分。
17.(14分)络氨铜 受热易分解产生氨气,络氨铜在乙醇—水混合溶剂中溶解度变化曲线
如图所示,溶于水产生的 存在平衡:
I.制备少量 晶体,设计实验方案如下:
(1)仪器A的名称为 ,对比铜和浓硫酸加热制备硫酸铜,该方案的优点
是
(答一条即可)。
(2)悬浊液B为 ,补全下列离子方程式:
(3)某同学认为上述方案中的溶液C中一定含 ,设计如下方案证明其存在:加热深蓝
色溶液并检验逸出气体为氨气。你认为此方案 (填“可行”或“不可行”),理由是
。
(4)取溶液C于试管中,加入 (填试剂),并用玻璃棒摩擦试管壁,即可得到产物晶体。
Ⅱ.探究浓氨水和 溶液反应
(5)某同学阅读教材中浓氨水和 溶液反应实验步骤:“取 的 溶液于试管
中,滴加几滴 的氨水,立即产生浅蓝色沉淀,继续滴加氨水并振荡试管,沉淀溶解,得到
深蓝色透明溶液”,设计如下方案探究浓氨水和 溶液反应产物的影响因素。①利用平衡移动原理对实验b的现象进行解释 。
②某同学测得 溶液的 ,于是设计实验c的试剂为 ,
硫酸和硫酸钠混合液,其目的是 。
【答案】(1)坩埚(1分) 没有SO 生成,更环保(2分)
2
(2) (2分)
(3)不可行(1分) 溶液C中含有氨水,氨水不稳定,加热也能生成氨气(2分)
(4)无水乙醇(2分)
(5)OH-与Cu2+生成浅蓝色沉淀,使得Cu2+浓度降低,平衡向右移动, 浓度降低,溶液变为无
色(2分) 研究硫酸根的对浓氨水和 溶液反应产物的影响(2分)
【解析】(1)Cu在仪器A中和O 加热生成CuO,所以仪器A为坩埚;然后CuO与硫酸反应生成硫酸铜,
2
对比铜和浓硫酸加热制备硫酸铜,该方案的优点是没有SO 生成,更环保。
2
(2)硫酸铜溶液中通入氨水得到悬浊液B为 ,
。
(3)溶液C为悬浊液B加入过量氨水得到,所以溶液C中含有氨水,氨水不稳定,加热也能生成氨气;
所以该同学设计方案不合理;故答案为不可行;溶液C中含有氨水,氨水不稳定,加热也能生成氨气。
(4)有题可知,络氨铜在乙醇—水混合溶剂中溶解度随着乙醇体积分数增大,溶解度减小,所以取溶液C
于试管中,加入无水乙醇,并用玻璃棒摩擦试管壁,即可得到产物晶体。
(5)①已知 溶于水产生的 存在平衡 ,加入NaOH溶
液,OH-与Cu2+生成浅蓝色沉淀,使得Cu2+浓度降低,平衡向右移动, 浓度降低,溶液变为无
色。
②实验a和b分别研究了铜离子浓度和溶液酸碱性对浓氨水和 溶液反应产物的影响,某同学测得
溶液的 ,于是设计实验c的试剂为 , 硫酸和硫酸钠混合液,对比实验a和b,设计此实验的目的是研究硫酸根的对浓氨水和 溶液反应产物的影响。
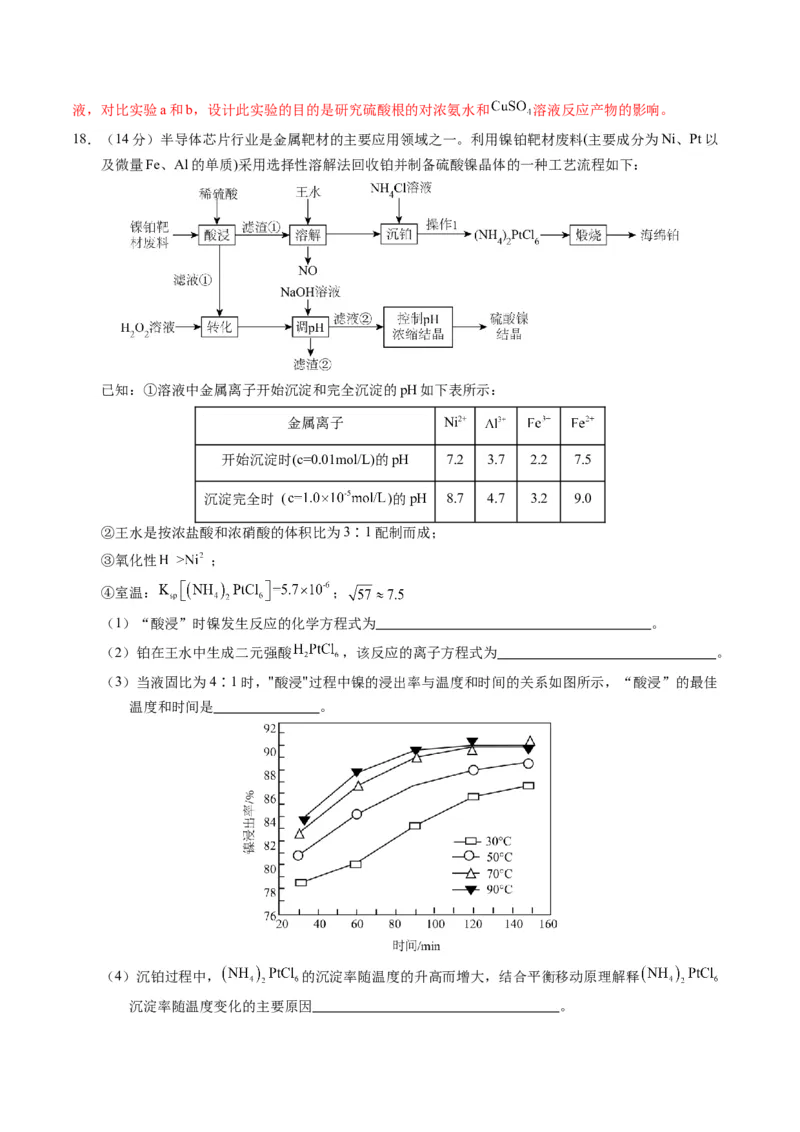
18.(14分)半导体芯片行业是金属靶材的主要应用领域之一。利用镍铂靶材废料(主要成分为Ni、Pt以
及微量Fe、Al的单质)采用选择性溶解法回收铂并制备硫酸镍晶体的一种工艺流程如下:
已知:①溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Ni2+
开始沉淀时(c=0.01mol/L)的pH 7.2 3.7 2.2 7.5
沉淀完全时 ( )的pH 8.7 4.7 3.2 9.0
②王水是按浓盐酸和浓硝酸的体积比为3∶1配制而成;
③氧化性 ;
④室温: ;
(1)“酸浸”时镍发生反应的化学方程式为 。
(2)铂在王水中生成二元强酸 ,该反应的离子方程式为 。
(3)当液固比为4∶1时,"酸浸"过程中镍的浸出率与温度和时间的关系如图所示,“酸浸”的最佳
温度和时间是 。
(4)沉铂过程中, 的沉淀率随温度的升高而增大,结合平衡移动原理解释
沉淀率随温度变化的主要原因 。(5)在“沉铂”过程中,若向 的溶液里加入等体积的 溶液,使 沉
淀完全,则加入 溶液的浓度最小值为 mol/L(结果保留两位小数,忽略
溶液混合后体积的变化)。
(6)PtCl 2-可被还原为PtCl ,PtCl 的价层电子对互斥模型如图所示,已知该离子是平面形结构,
6
则该离子中的键角是 ,中心原子采用的杂化类型可能是
(填 “dsp2”“sp3”“sp2”或“sp3d2”)。
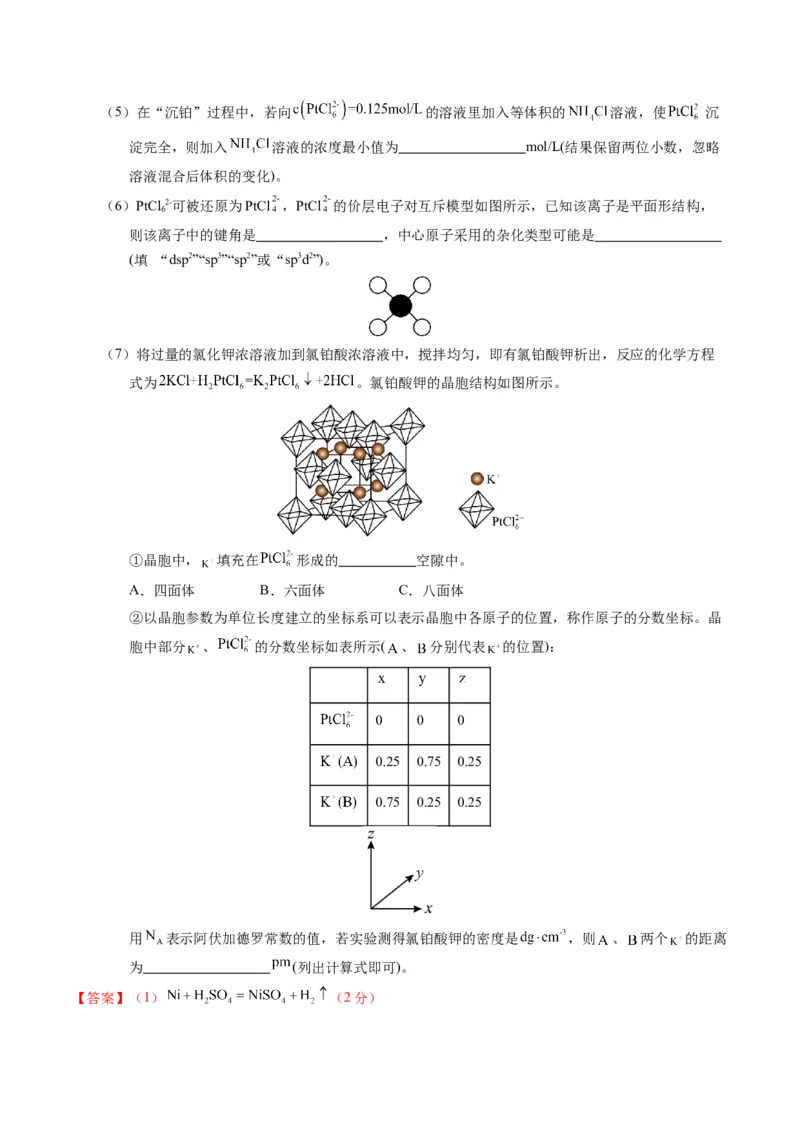
(7)将过量的氯化钾浓溶液加到氯铂酸浓溶液中,搅拌均匀,即有氯铂酸钾析出,反应的化学方程
式为 。氯铂酸钾的晶胞结构如图所示。
①晶胞中, 填充在 形成的 空隙中。
A.四面体 B.六面体 C.八面体
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。晶
胞中部分 、 的分数坐标如表所示( 、 分别代表 的位置):
0 0 0
0.25 0.75 0.25
0.75 0.25 0.25
用 表示阿伏加德罗常数的值,若实验测得氯铂酸钾的密度是 ,则 、 两个 的距离
为 (列出计算式即可)。
【答案】(1) (2分)(2) (2分)
(3)70℃、120min(1分)
(4)存在可逆反应 ,升高温度有利于HCl挥发,促使平衡正
向移动,使 沉淀率升高(2分)
(5)1.75(2分)
(6)90°(1分) dsp2(1分)
(7)A(1分) (2分)
【解析】酸浸时生成的离子为 、 、 ,用过氧化氢溶液氧化亚铁离子变为铁离子,则溶液变为
、 、 用NaOH溶液调节pH变为沉淀,需要调节pH为4.7时 和 完全沉淀,
pH为7.2时开始沉淀, 为二元强酸可以计算化合价和书写离子方程式,由图可
知最佳温度和时间为70℃和120min,根据平衡移动原理,温度升高NH Cl水解正向移动,温度越高
4
沉淀率越大,完全沉淀时离子浓度为 ,据此答题。
(1)已知氧化性 ,化学方程式为:
(2)浓硝酸和浓盐酸可拆开,Pt由0价变为+4价,硝酸中的N原子由+5价生成NO变为+2价,铂在王水
中生成二元强酸 ,反应的离子方程式为: ;
(3)由图可知,温度升高,酸浸浸出率在变大,70℃和90℃时酸浸率相接近,考虑成本原因,最佳温度
为70℃,由图可知,酸浸率与酸浸时间成正比,时间为120min后,镍浸出率随时间变化不显著,则最佳
时间为120min;
(4)存在可逆反应 ,升高温度有利于HCl挥发,促使平衡正
向移动,使 沉淀率升高;
(5) , , 沉淀完全时浓度小于
,代入数据可得 ,设原溶液体积为VL,则沉
淀 需要 溶液的物质的量为2 ,溶液等体积混合后, ,则
加入 溶液的浓度最小为 ;
(6)由四氯合铂离子的价层电子对互斥模型和离子的空间构型为平面形结构可知,离子中的键角为90°,
铂原子的杂化类型为dsp2杂化,故答案为:90°;dsp2;
(7)①由图可知,晶胞中 填充在 形成的四面体空隙中。②1个晶胞含有 的数是 ,含有K+的数是8,设晶胞的边长为apm,则
,a= ;由表可知A、B两个 的
距离为晶胞面对角线的一半,为 ;
19.(14分)CO 作为未来的重要碳源,其选择性加氢合成CHOH一直是研究热点。在CO 加氢合成
2 3 2
CHOH的体系中,同时发生以下反应:
3
反应ⅰ:CO(g)+3H(g) CHOH(g)+H O(g) ΔH<0
2 2 3 2 1
反应ⅱ:CO(g)+H(g) CO(g)+HO(g) ΔH>0
2 2 2 2
(1)原料CO 可通过捕获技术从空气或工业尾气中获取,下列物质能作为CO 捕获剂的是
2 2
(填标号)。
A.NaCO 溶液 B.NaOH溶液 C. CHCHOH D.NH Cl溶液
2 3 3 2 4
(2)在特定温度下,由稳定态单质生成1mol化合物的焓变叫该物质在此温度下的标准生成焓( fH
)。下表为几种物质在298K的标准生成焓,则反应ⅱ的ΔH 2 = kJ•mol-1。 △
物质 H(g) CO(g) CO(g) HO(g)
2 2 2
ΔfH (kJ•mol-1) 0 -394 -111 -242
(3)在CO 加氢合成CHOH的体系中,下列说法错误的是 (填标号)。
2 3
A.增大H 浓度有利于提高CO 的转化率
2 2
B.若气体的平均相对分子质量保持不变,说明反应体系已达平衡
C.体系达平衡后,若压缩体积,则反应ⅰ平衡正向移动,反应ⅱ平衡不移动
D.选用合适的催化剂可以提高CHOH在单位时间内的产量
3
(4)某温度下,向容积为1L的密闭容器中通入1molCO (g)和5molH (g),10min后体系达到平衡,此
2 2
时CO 的转化率为20%,CHOH的选择性为50%。
2 3
已知:CHOH的选择性χ= ×100%
3
①用CO 表示0~10min内平均反应速率v(CO)= 。
2 2
②反应ⅰ的平衡常数K= (写出计算式即可)。
(5)维持压强和投料不变,将CO 和H 按一定流速通过反应器,二氧化碳的转化率α(CO)和甲醇的
2 2 2
选择性χ(CHOH)随温度变化的关系如图所示:
3已知催化剂活性受温度影响变化不大。结合反应ⅰ和反应ⅱ,分析235℃后曲线变化的原因。
①甲醇的选择性随温度升高而下降的原因是 ;
②二氧化碳的转化率随温度升高也在下降的可能原因是 。
【答案】(1)AB(2分)
(2)+41(2分)
(3)C(2分)
(4)① (2分) ② (2分)
(5)①ⅰ为放热反应,反应达平衡后,升高温度,平衡逆向移动 (2分)
②反应达平衡后,升高温度,反应 ⅰ 使二氧化碳的转化率减小的程度大于反应 ⅱ 使二氧化碳的转化率
增大的程度(2分)
【解析】(1)能与CO 反应的,均可以作为CO 捕获剂,故选AB;
2 2
(2)根据已知信息可得热化学方程式:①H(g)+ O(g)= H O(g) ΔH=-242kJ•mol-1;②C(s)+ O(g)=
2 2 2 2
CO(g) ΔH=-111kJ•mol-1;③C(s)+ O (g)= CO (g) ΔH=-394kJ•mol-1;根据盖斯定律可得,由①+②-③可
2 2
得反应ⅱ:CO(g)+H(g) CO(g)+HO(g) ΔH=+41kJ•mol-1;
2 2 2 2
(3) A. 增大H 浓度,平衡正向移动,CO 的转化率增大,正确;B. 混合气体的总质量不变,但是总物
2 2
质的量随反应进行发生变化,则气体的平均相对分子质量会随反应的进行发生变化,则若气体的平均相对
分子质量保持不变,说明反应体系已达平衡,B正确;C. 体系达平衡后,若压缩体积,增大压强,则反应
ⅰ正向移动,CO、H 的浓度减小,则反应ⅱ逆向移动,错误;D. 催化剂虽然不能使平衡发生移动,但是
2 2
可以加快反应速率,故选用合适的催化剂可以提高CHOH在单位时间内的产量,正确;故选C;
3
(4)①用CO 表示0~10min内平均反应速率;
2
②反应达到平衡时,CO 的转化量为0.2mol,CHOH的选择性为50%,则
2 3
,则 ,则
可得: ,,则平衡时,c(CO)=1mol/L-0.1 mol/L -0.1 mol/L =0.8
2
mol/L,c(H )=5mol/L-0.3mol/L -0.1 mol/L =4.6 mol/L,c(CHOH)=0.1 mol/L ,c(H O)=0.1 mol/L+0.1 mol/L
2 3 2
=0.2mol/L,反应ⅰ的平衡常数 ;
(5)①甲醇的选择性随温度升高而下降的原因是反应ⅰ为放热反应,反应达平衡后,升高温度,平衡逆
向移动;
②反应ⅰ为放热反应,反应达平衡后,升高温度,平衡逆向移动,会使二氧化碳的转化率有减小的趋势;
反应ⅱ为吸热反应,反应达平衡后,升高温度,平衡正向移动,会使二氧化碳的转化率有增大的趋势,反
应 ⅰ 使二氧化碳的转化率减小的程度大于反应 ⅱ 使二氧化碳的转化率增大的程度,故二氧化碳的转化
率随温度升高在下降。
20.(14分)血脂过高能引起动脉粥样硬化、冠心病、胰腺炎等疾病,已成为现代人的健康杀手之一、下
图是一种治疗高血脂新药I的合成路线:
已知:R CHO+R CHCHO (R可以是氢或烃基)
1 2 2
回答下列问题:
(1)A→B反应的试剂及条件为 ,F的官能团名称是 。
(2)下列说法正确的是 (填标号)。
A.常温下,化合物B易溶于水
B.化合物F的水溶液具有杀菌、防腐性能
C.化合物D所有原子可能在同一平面
D.1mol化合物I最多能与3molNaOH发生反应
(3)写出F→G反应的化学方程式: 。
(4)符合下列条件的E的同分异构体有 种(不含立体异构)。
①属于芳香族化合物;②能发生银镜反应。
其中核磁共振氢谱有4组吸收峰,且峰面积比为2∶2∶1∶1的结构简式为
。(任写一种)
(5)聚戊二酸丙二醇酯(PPG)是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的
应用前景,请以戊二酸,甲醛和乙醛为原料(其它无机试剂任选),写出PPG的合成路线。
【答案】(1)氯气、光(2分) 醛基(1分)(2)BCD(2分)
(3)2CHO+ (2分)
2
(4)4(2分) 或 (2分)
(5) (3分)
【解析】根据A的分子式和B的结构简式可知,A发生取代反应生成B,A为 ,根据C的分子式推
断B中氯原子被羟基取代生成C,C为 ;C发生氧化反应生成D,D为 ;D
经氧化反应生成E,E为 ;F为甲醛,与根据已知,推断G的结构简式
,G与氢气发生加成反应生成H为 ,H中含有羟基与E发生
酯化反应生成I为 ;
(1)根据A的分子式和B的结构简式可知,A发生取代反应生成B,A→B反应的试剂及条件为氯气、光,
F为甲醛,F的官能团名称是醛基。
(2)A.常温下,B为 ,化合物B难溶于水,故A错误;B.F为甲醛,化合物F的水溶液具有杀菌、
防腐性能,故B正确;C.D为 ,苯平面和碳氧双键平面通过碳碳单键旋转,化合物D所有原子可能在同一平面,故C正确;D.1mol化合物 有3mol酯基,最多能与
3molNaOH发生反应,故D正确;故答案为:BCD;
(3)根据题目提供的信息R CHO+R CHCHO ,F→G反应的化学方程式:2CHO+
1 2 2 2
。
(4)E为 ,符合下列条件的E的同分异构体①属于芳香族化合物,含有苯环;②能发生
银镜反应含有醛基,含有2个侧链为-OH、-CHO,有邻间对三种,只有一个侧链,-OOCH,有1种,共有
4种同分异构,其中核磁共振氢谱有4组吸收峰,且峰面积比为2∶2∶1∶1的结构简式为
或 。
(5)甲醛和乙醛在稀碱性条件下生成 用氢气还原得到丙二醇,与戊二酸发生缩聚反应生成聚戊
二酸丙二醇酯(PPG),PPG的合成路线
。