文档内容
【赢在高考·黄金8卷】
2024年普通高中学业水平等级性考试模拟║天津专用
黄金卷04
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.作答时,务必将答案写在答题卡上。写在本试卷及草稿纸上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量: H-1 C-12 N-14 O-16 Mg -24 Fe-56
一、选择题:本题共12小题,每小题3分,共36分。每小题给出的四个选项中,只有一项符合题目要
求.
1.“化学——人类进步的关键”,前提是必须根据化学物质的特性合理使用,下列关于化学物质使用的
说法正确的是
A.同时施用草木灰(有效成分为KCO)和氮肥可促进植物的生长、增强抗倒伏能力
2 3
B.农药施用后一定不会通过农作物、农产品等发生转移
C.随意丢弃聚乙烯制品(如食品包装袋)会产生“白色污染”
D.由于钢铁在空气中会发生锈蚀而损耗,故废旧钢铁制品不需回收利用
【答案】C
【解析】A.草木灰(有效成分为KCO)溶液呈碱性,铵态氮肥溶液呈酸性,两者会反应产生氨气,同时施
2 3
用会降低肥效,故A错误;
B.农药可以通过生物转移,故B错误;
C.塑料垃圾可以造成白色污染,随意丢弃聚乙烯制品(如食品包装袋)会产生“白色污染”,故C正确;
D.回收利用废旧金属是保护金属资源的有效途径,故D错误;
故选:C。
2.高分子材料是当代生产生活的重要物质基础。下列高分子材料通过加聚反应得到的是
A.顺丁橡胶 B.聚酯纤维 C.酚醛树脂 D.聚酰胺纤维
【答案】A
【解析】A.顺丁橡胶单体为1,3-丁二烯,是通过加聚反应得到 ,A正确;
B.聚酯纤维是有机二元酸和二元醇缩聚而成,B错误;
C.酚醛树脂单体为苯酚和甲醛通过缩聚反应得到,C错误;
D.聚酰胺纤维通过缩聚反应得到,D错误;
故选A。3.下列各组物质的鉴别方法错误的是
选项 物质 鉴别方法
A CO(g)和 分别通入澄清石灰水
B 和 分别取少许试剂加入金属钠
和
C 分别取少许试剂加入 溶液
D 和 分别取少许固体加入盐酸中
A.A B.B C.C D.D
【答案】D
【解析】A.将CO(g)和 分别通入澄清石灰水,使其变浑浊的为 ,可以鉴别,故A正确;
B.分别取少许 和 加入金属钠,反应剧烈的为 ,可以鉴别,故B正确;
C.分别取少许 和 加入 溶液,形成沉淀的是 ,可以鉴别,
故C正确;
D.分别取少许 和 加入盐酸中,均可产生气体,现象相同,无法鉴别,故D错误;
答案选D。
4.物质的性质决定用途,下列两者对应关系正确的是
A.液氨汽化时吸收大量热,可用作制冷剂
B. 具有氧化性,葡萄酒中添加 起到漂白作用
C.钾钠合金具有还原性,用于快中子反应堆的热交换剂
D. 具有氧化性,可用作净水剂
【答案】A
【解析】A.氨气中的氮元素化合价是-3价,具有还原性,做制冷剂,是因为液氨汽化时吸收大量热,A
正确;
B.二氧化硫可用于漂白纸浆是因为其具有漂白性,与二氧化硫的氧化性无关,B错误;
C.在快中子反应堆中,不能使用水来传递堆芯中的热量,因为它会减缓快中子的速度,钠和钾的合金可用于快中子反应堆作热交换剂,C错误;
D.FeCl 溶液水解生成Fe(OH) 胶体具有吸附性,用作净水剂,与氧化性无关,D错误;
3 3
故答案为:A。
5.下列各组物质性质的比较,结论正确的是
A.酸性:
B.还原性:
C.酸性:
D.沸点: <
【答案】C
【解析】A. 是强酸, 是中强酸, 是弱酸, 是弱酸,酸性顺序是错误的,A错
误;
B. 与 同一主族元素,非金属性 > ,还原性 ,B错误;
C.由于氟的电负性大于氯的电负性, 的极性大于 ,使 的极性大于 的极性,导致三氟
乙酸的羧基更易电离出氢离子,酸性强于三氯乙酸,C正确;
D. 易形成分子间氢键沸点高, 更容易形成分子内氢键沸点低,二者
沸点为 > ,D错误;
答案选C。
6.元素As、Se、Br位于元素周期表中第四周期。下列说法正确的是
A.原子半径大小: B.电离能大小:
C.氢化物稳定性: D.电负性大小:
【答案】A【解析】A.同周期元素自左向右半径依次减小,所以 ,A正确;
B.同周期元素自左向右电离能依次增大,当最外层出现半满和全满时第一电离能比相邻元素都要大,所
以 ,B错误;
C.非金属性越强氢化物越稳定,非金属性溴最强砷最弱,所以稳定性 ,C错误;
D.同周期元素自左向右电负性依次增大,所以 ,D错误;
故选A。
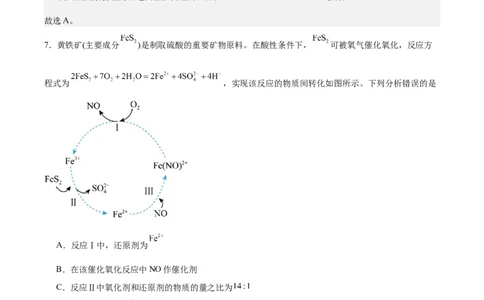
7.黄铁矿(主要成分 )是制取硫酸的重要矿物原料。在酸性条件下, 可被氧气催化氧化,反应方
程式为 ,实现该反应的物质间转化如图所示。下列分析错误的是
A.反应Ⅰ中,还原剂为
B.在该催化氧化反应中NO作催化剂
C.反应Ⅱ中氧化剂和还原剂的物质的量之比为
D.反应Ⅲ中 可吸收标准状况下
【答案】A
【分析】由图可知:反应Ⅰ中Fe(NO)2+中铁由+2价变+3价,氧气中氧由0价变成-2价,反应Ⅱ的Fe3+由+3
价变成+2价,FeS 中硫元素化合价升高,反应Ⅲ的离子方程式为Fe2+ +NO=Fe(NO)2+,无元素化合价变化,
2
总反应2FeS+7O +2H O=2Fe2+ +4 +4H+可知,NO参加反应但反应前后性质和质量不变,据此分析。
2 2 2【解析】A.由分析可知,反应Ⅰ中Fe(NO)2+中铁由+2价变+3价,Fe(NO)2+做还原剂,故A错误;
B.由分析可知,NO参加反应但反应前后性质和质量不变,属于NO催化剂,故B正确;
C.反应Ⅱ的Fe3+由+3价变成+2价,FeS 中硫元素化合价由-1价升高到+6价,由电子守恒可知Fe3+和FeS
2 2
的物质的量之比为14∶1,即氧化剂和还原剂的物质的量之比为14∶1,故C正确;
D.反应Ⅲ的离子方程式为Fe2+ +NO=Fe(NO)2+,则1mol Fe2+可吸收1mol NO,即标准状况下22.4L,故D
正确;
答案选A。
8.乙酰水杨酸(阿司匹林)的结构如图,下列说法中错误的
A.阿司匹林有镇痛、解热的功效
B.乙酰水杨酸分子中含有羧基、碳碳双键官能团
C.乙酰水杨酸可发生酯化反应和水解反应
D.乙酰水杨酸是一种不饱和烃的衍生物
【答案】B
【解析】A.阿司匹林是人们熟知的感冒药,是第一个重要的人工合成药物,具有解热镇痛作用,故A正
确;
B.阿司匹林分子中含有2种官能团,分别为酯基和羧基,故B错误;
C.该有机物分子中含有羧基、酯基,能够发生酯化反应和水解反应,故C正确;
D.该有机物除含C、H两种元素外,还含有氧元素,不属于烃,属于烃的含氧衍生物,故D正确;
故选:B。
9.利用图中装置进行实验,能达到实验目的的是。
装置测定醋酸浓 模拟侯氏制碱法制
合成氨并检验氨的生成 制备
度 备
A B C D
A.A B.B C.C D.D【答案】B
【解析】A.测定醋酸浓度,应用酚酞作指示剂, 溶液应该用碱式滴定管盛装,A项不符合题意;
B.氢气和氮气在催化剂(铁丝)、加热条件下反应生成氨气,氨气与HCl反应生成氯化铵固体,若观察
到导管口产生白烟,即可验证有氨气生成,B项符合题意;
C. 易溶于水,不能用排水法收集 ,C项不符合题意;
D.模拟侯氏制碱法制备 时应先向饱和食盐水中通入过量氨气,再通入二氧化碳反应生成
,D项不符合题意。
故选B。
10.室温下,通过下列实验探究 、 溶液的性质。
实验1:用 试纸测量 溶液的 ,测得 约为8
实验2:将 溶液与 溶液等体积混合,产生白色沉淀
实验3:饱和 溶液中通入 产生白色沉淀,溶液 从12下降到约为9
实验4:向 溶液中滴加几滴酚酞,加水稀释,溶液红色变浅
下列说法正确的是
A.由实验1可得出:
B.由实验2可推测:
C.实验3中发生反应的离子方程式为
D.实验4中加水稀释后,溶液中 的值增大
【答案】D
【解析】A.由实验1可得出碳酸氢钠溶液中碳酸氢根水解程度大于电离程度即,则 ,故A错误;
B.实验2是等体积混合, ,由于混合后碳酸氢钠中碳酸根浓度小于0.05 mol∙L−1,氢
氧化钙是微溶物,钙离子浓度小于0.05 mol∙L−1,因此不能推测: ,故B错误;
C.实验3中发生反应的离子方程式为 ,故C错误;
D.实验4中加水稀释后,水解程度增大,由于溶液体积增大,溶液碱性减弱,氢离子浓度增大,因此溶
液中 的值增大,故D正确。
综上所述,答案为D。
11.研究表明,臭氧层的破坏与“氟利昂”的排放密切相关,其化学反应机理如图[以二氯二氟甲烷
(CFCl)为例],下列说法不正确的是
2 2
A.紫外线使CFCl 分解产生的Cl·是臭氧生成氧气的催化剂
2 2
B.ClOOCl(过氧化氯)中含有非极性共价键
C.CFCl 分解为CFCl·和Cl·反应中有化学键的断裂和形成
2 2 2
D.臭氧层破坏的关键因素是氟利昂和紫外线
【答案】C
【分析】由图可知,CFCl→CFCl·+Cl·,生成的Cl促进臭氧分解生成氧气,同时最后又生成Cl;ClOOCl
2 2 2
相当HO2中的H原子被Cl取代形成,根据ClOOCl的结构式判断作答;CFCl 分解为CFC1和Cl,反应
2 2 2 2
中有化学键的断裂,没有形成新的化学键;
【解析】A.根据过程分析可知,生成的Cl·促进臭氧分解生成氧气,同时最后又生成Cl·,所以Cl·是促进
臭氧分解生成氧气的催化剂,A正确;
B.ClOOCl的结构式为Cl—O—O—Cl,含有氧氧非极性共价键,B正确;
C.CFCl 分解为CFCl·和Cl·反应中有化学键的断裂,没有形成新的化学键,C错误;
2 2 2
D.氟利昂在紫外线条件下产生的Cl·促进臭氧分解生成氧气,臭氧层破坏的关键因素是氟利昂和紫外线,
D正确;故选C。
12.以炼铁厂锌灰(主要成分为 ,含少量的 、 、 )为原料制备 的工艺流程如下。
下列说法正确的是
已知:浸取工序中 、 分别转化为 和 。
A.“浸取”采用较高温度更有利于提高浸取率
B.“滤渣①”经稀盐酸溶浸、过滤可获得
C.“除杂”的主要目的是将铁元素从溶液中分离
D.“煅烧”时加入焦炭可提高 的产率
【答案】B
【分析】浸取时,ZnO、CuO转化为[Zn(NH )]2+、[Cu(NH )]2+,MnO 、Fe O 不反应,滤液1中含有
3 4 3 4 2 2 3
[Zn(NH )]2+、[Cu(NH )]2+、NH HCO 、NH •H O,加入Zn粉时,发生反应Zn+[Cu(NH)]2+=Cu+
3 4 3 4 4 3 3 2 3 4
[Zn(NH )]2+,从而实现去除杂质[Cu(NH )]2+,滤液2中主要含[Zn(NH )]2+、NH HCO 、NH •H O,经
3 4 3 4 3 4 4 3 3 2
过蒸氨沉锌操作获得沉淀ZnCO ,最后煅烧获得ZnO。
3
【解析】A.浸取时温度过高会导致碳酸氢铵和氨水分解,故A错误;
B.由分析可知,滤渣1的主要成分为 和 ,用稀盐酸溶浸时 溶解,得到 ,故B正确;
C.加入过量锌粉发生的反应为Zn+[Cu(NH)]2+=Cu+[Zn(NH)]2+ ,“除杂”的主要目的是将铜元素元
3 4 3 4
素从溶液中分离;故C错误;
D.煅烧时加入焦炭, 会变为单质Zn,会降低 的产率,故D错误。
答案选B。
二、非选择题:本题共4小题,共64分。
13.(16分)Li、B、C、Ga等元素的单质或化合物在很多领域有广泛的应用。请回答:
(1)基态 原子的价电子排布式为 。(2)一种含B化合物可用作吸附材料,其化学式为 ,部分晶体结构如图1所示,
其中 为平面结构。
下列说法不正确的是___________。
A.基态原子的第一电离能:
B.基态原子未成对电子数:
C.该晶体中存在的化学键有离子键、共价键、配位键、氢键
D.晶体中B、C、N和O原子轨道的杂化类型分别为
(3)比较 键角大小: (填“>”“=”或“<”),并说明理由
。
(4)一种锂离子电池负极材料为两层石墨层中嵌入 ,形成如图2所示的晶胞结构。该物质的化学式可以
表示为 , 的配位数为 。
【答案】(1)
(2)BCD
(3) > 中B为 杂化, 中B为 杂化(4) 12
【解析】(1)基态 原子的电子排布式为1s22s22p63s23p63d104s24p1,价电子排布式为4s24p1。
(2)A.同一周期元素原子的第一电离能呈递增趋势,但是第IIA、VA 元素的原子结构比较稳定,其第
一电离能高于同周期的相邻元素的原子,因此,基态原子的第一电离能从小到大的顺序为 C