文档内容
【赢在高考·黄金8卷】
2024年普通高中学业水平等级性考试模拟║天津专用
黄金卷04
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.作答时,务必将答案写在答题卡上。写在本试卷及草稿纸上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量: H-1 C-12 N-14 O-16 Mg -24 Fe-56
一、选择题:本题共12小题,每小题3分,共36分。每小题给出的四个选项中,只有一项符合题目要
求.
1.“化学——人类进步的关键”,前提是必须根据化学物质的特性合理使用,下列关于化学物质使用的
说法正确的是
A.同时施用草木灰(有效成分为KCO)和氮肥可促进植物的生长、增强抗倒伏能力
2 3
B.农药施用后一定不会通过农作物、农产品等发生转移
C.随意丢弃聚乙烯制品(如食品包装袋)会产生“白色污染”
D.由于钢铁在空气中会发生锈蚀而损耗,故废旧钢铁制品不需回收利用
2.高分子材料是当代生产生活的重要物质基础。下列高分子材料通过加聚反应得到的是
A.顺丁橡胶 B.聚酯纤维 C.酚醛树脂 D.聚酰胺纤维
3.下列各组物质的鉴别方法错误的是
选项 物质 鉴别方法
A CO(g)和 分别通入澄清石灰水
B 和 分别取少许试剂加入金属钠
和
C 分别取少许试剂加入 溶液
D 和 分别取少许固体加入盐酸中
4.物质的性质决定用途,下列两者对应关系正确的是
A.液氨汽化时吸收大量热,可用作制冷剂
B. 具有氧化性,葡萄酒中添加 起到漂白作用C.钾钠合金具有还原性,用于快中子反应堆的热交换剂
D. 具有氧化性,可用作净水剂
5.下列各组物质性质的比较,结论正确的是
A.酸性:
B.还原性:
C.酸性:
D.沸点: <
6.元素As、Se、Br位于元素周期表中第四周期。下列说法正确的是
A.原子半径大小: B.电离能大小:
C.氢化物稳定性: D.电负性大小:
7.黄铁矿(主要成分 )是制取硫酸的重要矿物原料。在酸性条件下, 可被氧气催化氧化,反应方
程式为 ,实现该反应的物质间转化如图所示。下列分析错误的是
A.反应Ⅰ中,还原剂为
B.在该催化氧化反应中NO作催化剂
C.反应Ⅱ中氧化剂和还原剂的物质的量之比为D.反应Ⅲ中 可吸收标准状况下
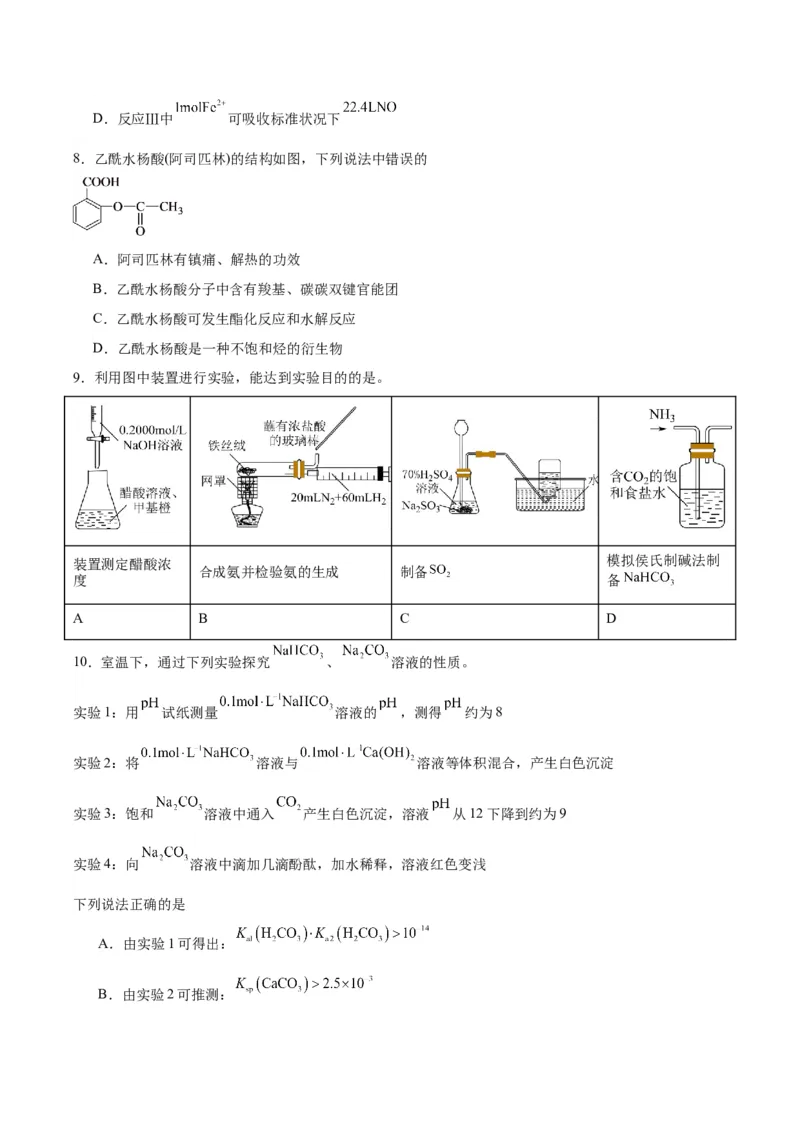
8.乙酰水杨酸(阿司匹林)的结构如图,下列说法中错误的
A.阿司匹林有镇痛、解热的功效
B.乙酰水杨酸分子中含有羧基、碳碳双键官能团
C.乙酰水杨酸可发生酯化反应和水解反应
D.乙酰水杨酸是一种不饱和烃的衍生物
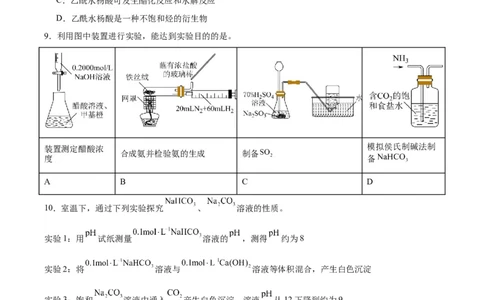
9.利用图中装置进行实验,能达到实验目的的是。
装置测定醋酸浓 模拟侯氏制碱法制
合成氨并检验氨的生成 制备
度 备
A B C D
10.室温下,通过下列实验探究 、 溶液的性质。
实验1:用 试纸测量 溶液的 ,测得 约为8
实验2:将 溶液与 溶液等体积混合,产生白色沉淀
实验3:饱和 溶液中通入 产生白色沉淀,溶液 从12下降到约为9
实验4:向 溶液中滴加几滴酚酞,加水稀释,溶液红色变浅
下列说法正确的是
A.由实验1可得出:
B.由实验2可推测:C.实验3中发生反应的离子方程式为
D.实验4中加水稀释后,溶液中 的值增大
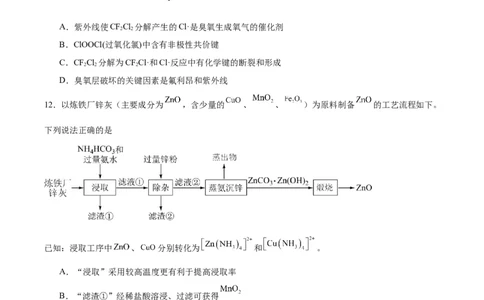
11.研究表明,臭氧层的破坏与“氟利昂”的排放密切相关,其化学反应机理如图[以二氯二氟甲烷
(CFCl)为例],下列说法不正确的是
2 2
A.紫外线使CFCl 分解产生的Cl·是臭氧生成氧气的催化剂
2 2
B.ClOOCl(过氧化氯)中含有非极性共价键
C.CFCl 分解为CFCl·和Cl·反应中有化学键的断裂和形成
2 2 2
D.臭氧层破坏的关键因素是氟利昂和紫外线
12.以炼铁厂锌灰(主要成分为 ,含少量的 、 、 )为原料制备 的工艺流程如下。
下列说法正确的是
已知:浸取工序中 、 分别转化为 和 。
A.“浸取”采用较高温度更有利于提高浸取率
B.“滤渣①”经稀盐酸溶浸、过滤可获得
C.“除杂”的主要目的是将铁元素从溶液中分离
D.“煅烧”时加入焦炭可提高 的产率
二、非选择题:本题共4小题,共64分。
13.(16分)Li、B、C、Ga等元素的单质或化合物在很多领域有广泛的应用。请回答:
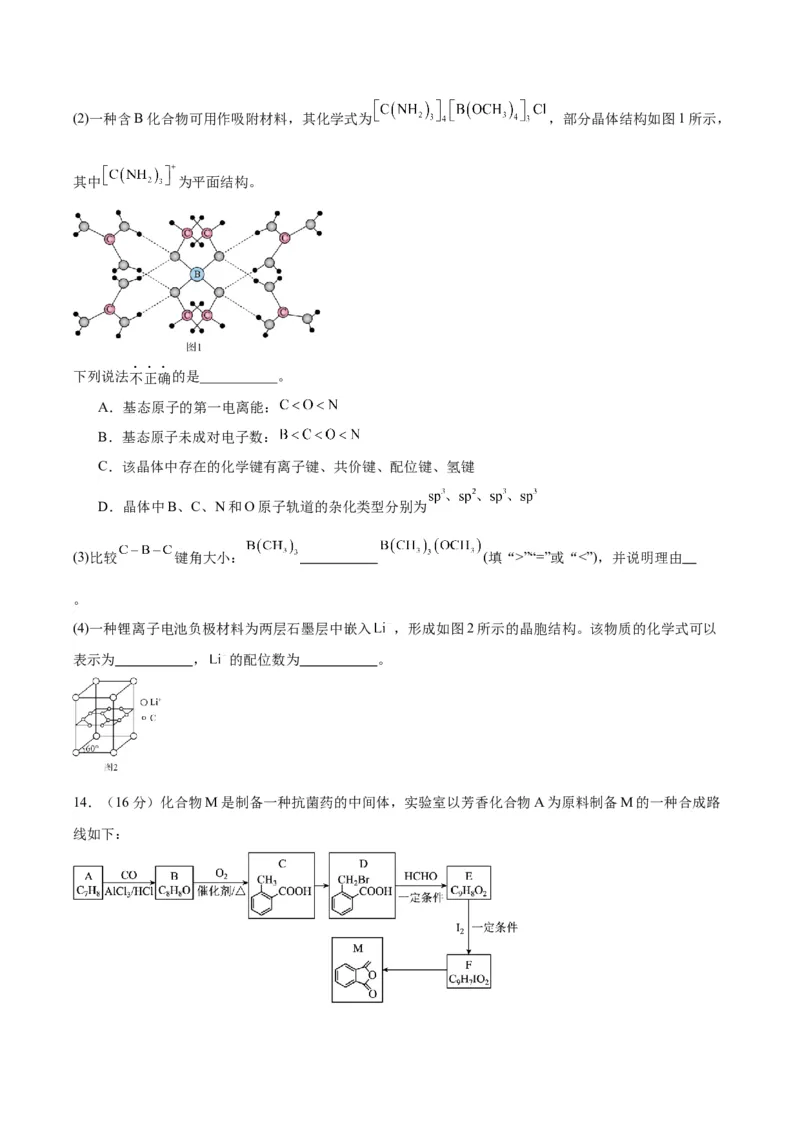
(1)基态 原子的价电子排布式为 。(2)一种含B化合物可用作吸附材料,其化学式为 ,部分晶体结构如图1所示,
其中 为平面结构。
下列说法不正确的是___________。
A.基态原子的第一电离能:
B.基态原子未成对电子数:
C.该晶体中存在的化学键有离子键、共价键、配位键、氢键
D.晶体中B、C、N和O原子轨道的杂化类型分别为
(3)比较 键角大小: (填“>”“=”或“<”),并说明理由
。
(4)一种锂离子电池负极材料为两层石墨层中嵌入 ,形成如图2所示的晶胞结构。该物质的化学式可以
表示为 , 的配位数为 。
14.(16分)化合物M是制备一种抗菌药的中间体,实验室以芳香化合物A为原料制备M的一种合成路
线如下:已知:R CHBr R CH=CHR
1 2 1 2
回答下列问题:
(1)B的化学名称为 ;E中官能团的名称为 。
(2)写出D与氢氧化钠水溶液共热的化学方程式 。
(3)由F生成M所需的试剂和条件为 。
(4)X是D的同分异构体,同时符合下列条件的X可能的结构有 种(不含立体异构)。
①苯环上有两个取代基,含两个官能团;②能发生银镜反应。
其中核磁共振氢谱显示4组峰的结构简式是 (任写一种)。
(5)碳原子上连有4个不同的原子或原子团时,该碳称为手性碳。写出F的结构简式并用星号(*)标出F中的
手性碳: 。
15.(16分)I.NaCO 和NaHCO 是厨房中常见的两种盐。回答下列问题:
2 3 3
(1)与酸反应的差异进行鉴别。甲组进行了如图4组实验。
其中实验 和 (填实验序号)可以鉴别NaCO 和NaHCO 。
2 3 3
(2)利用如图实验比较碳酸钠和碳酸氢钠的热稳定性,则物质甲的化学式为 。
取某碳酸钠和碳酸氢钠混合物2.74g,加热到质量不再变化时,剩余固体的质量为2.12g,则混合物中碳酸
钠的质量为 克。
Ⅱ.如图所示,此装置可用来制备Fe(OH) 并验证其还原性,填写下列空白:
2(3)制备Fe(OH) :
2
仪器X的名称为 ,实验开始时先将止水夹“a”打开,滴入HSO 和铁粉反应。一段时间后关闭
2 4
止水夹a,使A中溶液流入B中进行反应。
(4)验证Fe(OH) 还原性:
2
实验完毕,打开b处止水夹,充入一部分空气,此时B瓶中发生的反应为(写化学方程式) ,现象:
。
(5)某同学欲用36.5%浓盐酸(密度1.2g/mL)配制480mL上述实验所需盐酸。
配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果 (填写“偏大”、“偏小”、“不
变”)。
16.(16分)明矾[KAl(SO)•12H O]是一种常用的净水剂,以废易拉罐(主要成分为铝和少量不溶于碱性
4 2 2
溶液的物质)为原料制取明矾晶体的实验流程如图:
回答下列问题:
(1)“碱溶”步骤中发生反应的化学方程式为 。
(2)“沉铝”步骤在煮沸条件下进行,生成Al(OH) 、NH 和NaHCO 检验“沉铝”所得滤液中主要阳离子的
3 3 3.
定性分析操作为 (填操作名称)。
(3)由浓硫酸配制250mL“酸溶”所需的9mol•L-1HSO 溶液需要用到的玻璃仪器有烧杯、玻璃棒、量筒、
2 4
、 。
(4)“酸溶”步骤在如图所示的装置中进行,导管的作用是 。圆底烧瓶中发生反应的离子方程式
为 。