文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(河北专用)
黄金卷08
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64 Ce 140
第Ⅰ卷
一、单项选择题:共14题,每题3分,共42分。每题只有一个选项最符合题意。
1.化学与生活、科技密切相关。下列说法正确的是
A.加入浓盐酸可增强“84”消毒液的消毒效果
B.华为手机mate60使用的麒麟9000s芯片,其主要成分是二氧化硅
C.《神农本草经》中记载的“石胆能化铁为铜”的变化属于化学变化
D.速滑竞赛服使用的聚氨酯材料属于天然有机高分子材料
2.下列有关化学用语表示正确的是
A.HClO的电子式:
B.O 的分子结构空间模型:
3
C.基态As原子的电子排布式:[Ar]3d104s24p3
D.反式聚异戊二烯的结构简式:
3.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.常温常压下,23g钠在足量的氧气中燃烧,转移的电子数为2N
A
B.1molH O中,中心原子的孤电子对数为2N
2 A
C.标准状况下,0.1molHF的体积约为2.24L
D.1L0.1mol•L-1的(NH )SO 溶液中,含有NH 的数目为0.2N
4 2 3 A
4.能正确表示下列反应的离子方程式为
A.臭碱(硫化钠)溶液中滴加足量的稀硝酸:S2-+2H+=H S↑
2
B.氯化铝溶液中通入过量的氨气:Al3++4NH+4H O= +4NH
3 2C.石钟乳(CaCO)溶于醋酸:CaCO +2H+=Ca2++H O+CO↑
3 3 2 2
D.1.5molCl 通入到含1molFeI 的溶液中:2Fe2++4I-+3Cl=2Fe3++6Cl-+2I
2 2 2 2
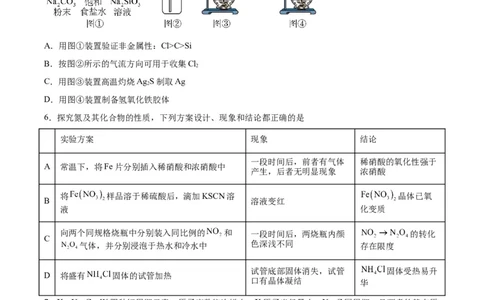
5.用下列实验装置进行相应的实验,能达到实验目的的是
A.用图①装置验证非金属性:Cl>C>Si
B.按图②所示的气流方向可用于收集Cl
2
C.用图③装置高温灼烧Ag S制取Ag
2
D.用图④装置制备氢氧化铁胶体
6.探究氮及其化合物的性质,下列方案设计、现象和结论都正确的是
实验方案 现象 结论
一段时间后,前者有气体 稀硝酸的氧化性强于
A 常温下,将Fe片分别插入稀硝酸和浓硝酸中
产生,后者无明显现象 浓硝酸
将 样品溶于稀硫酸后,滴加KSCN溶 晶体已氧
B 溶液变红
液 化变质
向两个同规格烧瓶中分别装入同比例的 和 一段时间后,两烧瓶内颜 的转化
C
气体,并分别浸泡于热水和冷水中 色深浅不同 存在限度
试管底部固体消失,试管 固体受热易升
D 将盛有 固体的试管加热
口有晶体凝结 华
7.X、Y、Z、W四种短周期元素,原子序数依次增大。X原子半径最小。Y、Z同周期,且两者的基态原
子核外均有2个未成对电子。W元素与X的同族元素相邻。下列说法不正确的是
A.W的第一电离能大于同周期相邻元素
B. 的水溶液呈酸性
C.W单质与 晶体可发生置换反应
D.简单氧化物熔点:8.一种超导材料(仅由 三种元素组成)的长方体晶胞结构如图所示(已知 ,用 表示
阿伏加德罗常数的值):
下列说法正确的是
A.基态 失去 能级上的一个电子转化为
B.若 点原子分数坐标为 ,则 点原子分数坐标为
C. 之间的距离为
D.晶体的密度为
9.布洛芬(Ibuprofen)为解热镇痛类,非甾体抗炎药。但口服该药对胃、肠道有刺激性,可以对该分子进行
修饰,其修饰后的产物如图所示。下列说法错误的是
A.该有机物的分子式为C H ON B.该有机物能发生取代、加成、氧化反应
19 23 2
C.该有机物的部分官能团可用红外光谱仪检测 D.该有机物苯环上的一氯代物有3种
10.我国科学家研发的水系可逆Zn﹣CO 电池可吸收利用CO,将两组阴离子、阳离子复合膜反向放置分
2. 2
隔两室电解液充、放电时,复合膜间的HO解离成H+和OH﹣,工作原理如图所示。下列说法正确的是
2A.放电时负极反应式是Zn﹣2e﹣=Zn2+ B.充电时在电解质溶液中电子向阳极移动
C.充电时复合膜中向Zn极移动的离子是H+ D.放电时多孔Pd纳米片上有少量的氯气产生
11.X、Y、Z、W、Q为原子序数依次增大的短周期主族元素,已知X、Q为同主族元素且这两种元素能
组成离子化合物;Y元素的气态氢化物水溶液显碱性。下列说法正确的是
A.简单离子半径:
B. 分子的空间结构为平面三角形
C.X分别与Y、Z、W组成的常见化合物均为极性分子
D.由Y、Z、Q组成的化合物的水溶液一定显中性
12.活性ZnO是一种面向新世纪的新型高功能精细无机产品,某锌泥[主要含Zn、ZnO和 ]回
收活性ZnO的工业流程如下:
下列说法错误的是
A.“化浆”的目的是增大固液接触面积
B.温度越高,“氧化”步骤速率越快
C.增大压强可增大“碳化”过程中 的吸收量
D.可通过所得活性ZnO质量和煅烧后产生 的质量计算x
13.某反应可有效降低汽车尾气污染物的排放,其反应热 。一定条件下该反应经历三
个基元反应阶段,反应历程如图所示(TS表示过渡态),下列说法正确的是( )A.三个基元反应中只有③是放热反应
B.该化学反应的速率主要由反应②决定
C.该过程的总反应为
D.
14.已知 属于难溶于水、可溶于酸的盐。常温下,用 调节 浊液的 ,测得在不同 条件
下,体系中 或 与 的关系如图所示(不考虑
的挥发等)。下列说法不正确的是
A.曲线Ⅰ代表 与 的变化曲线B.常温下,
C.c点的溶液中存在关系:
D.d点的溶液中存在关系:
第Ⅱ卷
二、非选择题:共4题,共58分。
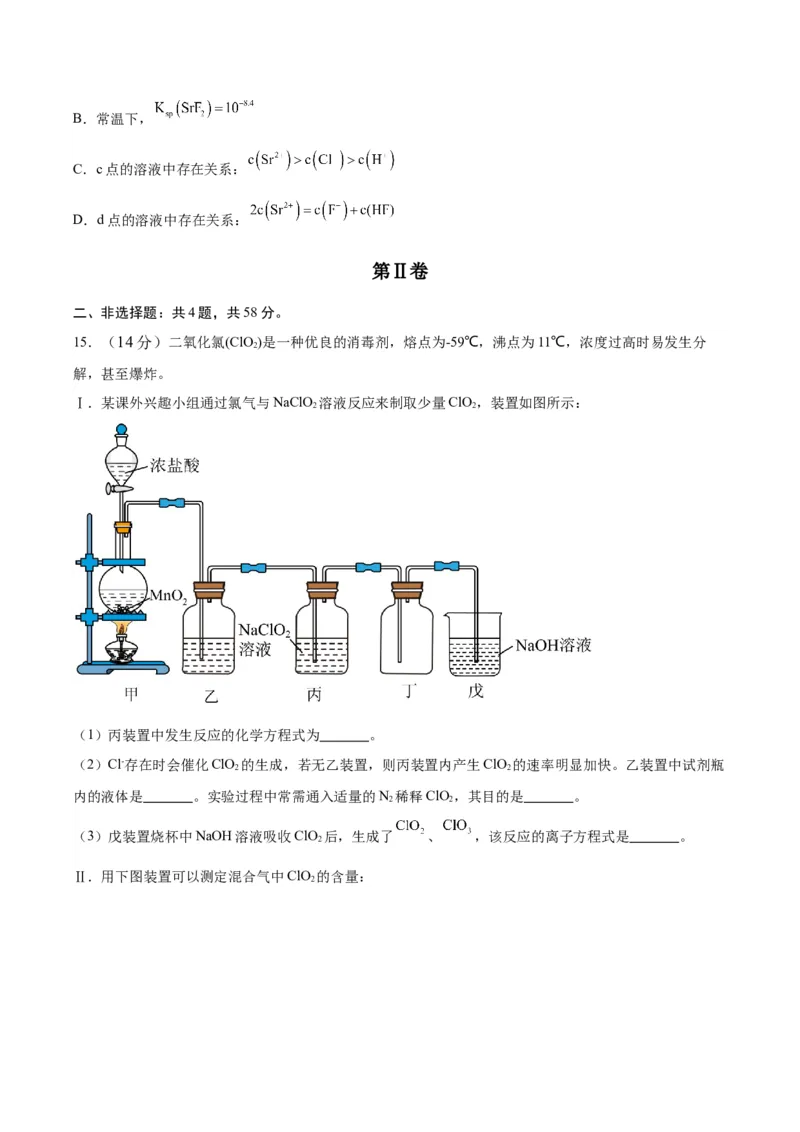
15.(14分)二氧化氯(ClO )是一种优良的消毒剂,熔点为-59℃,沸点为11℃,浓度过高时易发生分
2
解,甚至爆炸。
Ⅰ.某课外兴趣小组通过氯气与NaClO 溶液反应来制取少量ClO ,装置如图所示:
2 2
(1)丙装置中发生反应的化学方程式为 。
(2)Cl-存在时会催化ClO 的生成,若无乙装置,则丙装置内产生ClO 的速率明显加快。乙装置中试剂瓶
2 2
内的液体是 。实验过程中常需通入适量的N 稀释ClO ,其目的是 。
2 2
(3)戊装置烧杯中NaOH溶液吸收ClO 后,生成了 、 ,该反应的离子方程式是 。
2
Ⅱ.用下图装置可以测定混合气中ClO 的含量:
2①在锥形瓶中加入足量的碘化钾-淀粉溶液,用50 水溶解后,再加入3 稀硫酸:
②在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;
③将一定量的混合气体通入锥形瓶中吸收;
④将玻璃液封装置中的水倒入锥形瓶中:
⑤用0.1000 硫代硫酸钠标准溶液滴定锥形瓶中的溶液( ),指示剂显示终点
时共用去20.00 硫代硫酸钠溶液。在此过程中:
(4)玻璃液封装置的作用是 , 。
(5)滴定至终点的现象是 。
(6)测得混合气中ClO 的质量为 g。
2
16.(14分)某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶
性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO ·7H O):
4 2
某温度下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Ni2+ Al3+ Fe3+ Fe2+
开始沉淀时(c=0.01mol·L-1)的pH 7.2 3.7 2.2 7.5
沉淀完全时(c=1.0×10-5mol·L-1)的pH 8.7 4.7 3.2 9.0
回答下列问题:
(1)“碱浸”中NaOH的作用除了去除催化剂表面的油脂外,还具有作用是 (用化学方程式表
示)。为回收金属,通常用稀硫酸将“滤液①”调为中性,生成沉淀,该沉淀的化学式为 。(2)“滤液②”中含有的金属离子除了“Ni2+”,还有 。
(3)“转化”中加入HO 的主要作用是 (用离子方程式表示)。
2 2
(4)利用上述表格数据,计算Fe(OH) 的K = (列出计算式即可,不用化简)。如果“转化”后的溶
2 sp
液中Ni2+浓度为1.0mol·L-1,则“调pH”应控制pH不超过 (填数值)。
(5)分离出硫酸镍晶体后的母液中含有的溶质是 。
(6)将400kg废弃镍催化剂进行上述流程,充分回收利用,最后制得硫酸镍晶体质量为281kg,则该废弃
镍催化剂中Ni元素的质量分数为 。
17.(15分)乙酸是基本的有机化工原料。
I.工业上合成乙酸有多种方法。
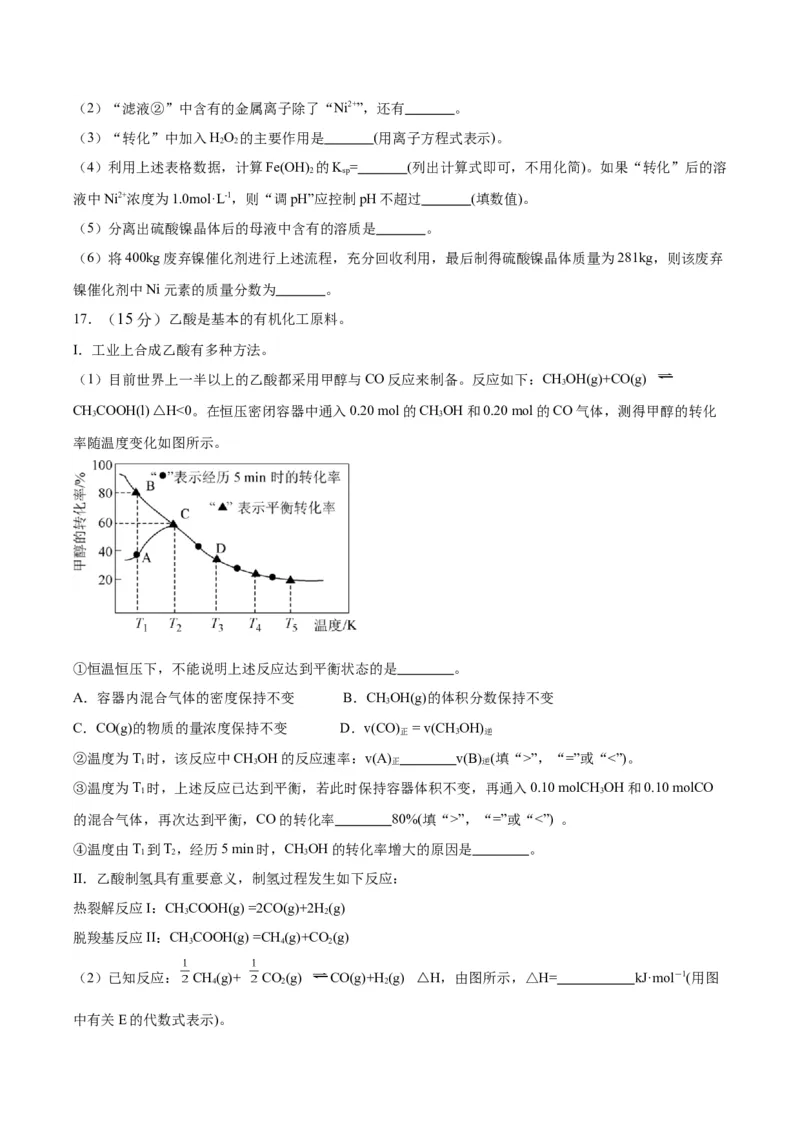
(1)目前世界上一半以上的乙酸都采用甲醇与CO反应来制备。反应如下:CHOH(g)+CO(g)
3
CHCOOH(l) △H<0。在恒压密闭容器中通入0.20 mol的CHOH和0.20 mol的CO气体,测得甲醇的转化
3 3
率随温度变化如图所示。
①恒温恒压下,不能说明上述反应达到平衡状态的是 。
A.容器内混合气体的密度保持不变 B.CHOH(g)的体积分数保持不变
3
C.CO(g)的物质的量浓度保持不变 D.v(CO) = v(CH OH)
正 3 逆
②温度为T 时,该反应中CHOH的反应速率:v(A) v(B) (填“>”,“=”或“<”)。
1 3 正 逆
③温度为T 时,上述反应已达到平衡,若此时保持容器体积不变,再通入0.10 molCH OH和0.10 molCO
1 3
的混合气体,再次达到平衡,CO的转化率 80%(填“>”,“=”或“<”) 。
④温度由T 到T,经历5 min时,CHOH的转化率增大的原因是 。
1 2 3
II.乙酸制氢具有重要意义,制氢过程发生如下反应:
热裂解反应I:CHCOOH(g) =2CO(g)+2H (g)
3 2
脱羧基反应II:CHCOOH(g) =CH (g)+CO (g)
3 4 2
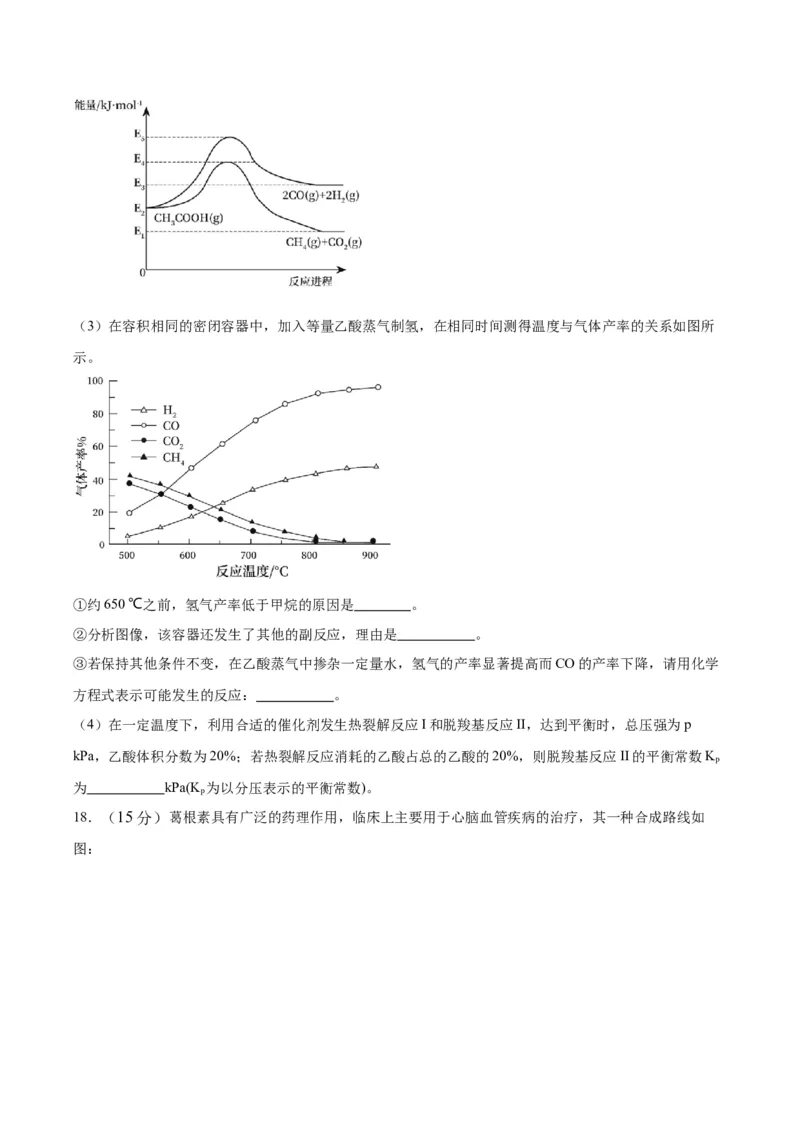
(2)已知反应: CH(g)+ CO(g) CO(g)+H(g) △H,由图所示,△H= kJ·mol-1(用图
4 2 2
中有关E的代数式表示)。(3)在容积相同的密闭容器中,加入等量乙酸蒸气制氢,在相同时间测得温度与气体产率的关系如图所
示。
①约650 ℃之前,氢气产率低于甲烷的原因是 。
②分析图像,该容器还发生了其他的副反应,理由是 。
③若保持其他条件不变,在乙酸蒸气中掺杂一定量水,氢气的产率显著提高而CO的产率下降,请用化学
方程式表示可能发生的反应: 。
(4)在一定温度下,利用合适的催化剂发生热裂解反应I和脱羧基反应II,达到平衡时,总压强为p
kPa,乙酸体积分数为20%;若热裂解反应消耗的乙酸占总的乙酸的20%,则脱羧基反应II的平衡常数K
p
为 kPa(K 为以分压表示的平衡常数)。
p
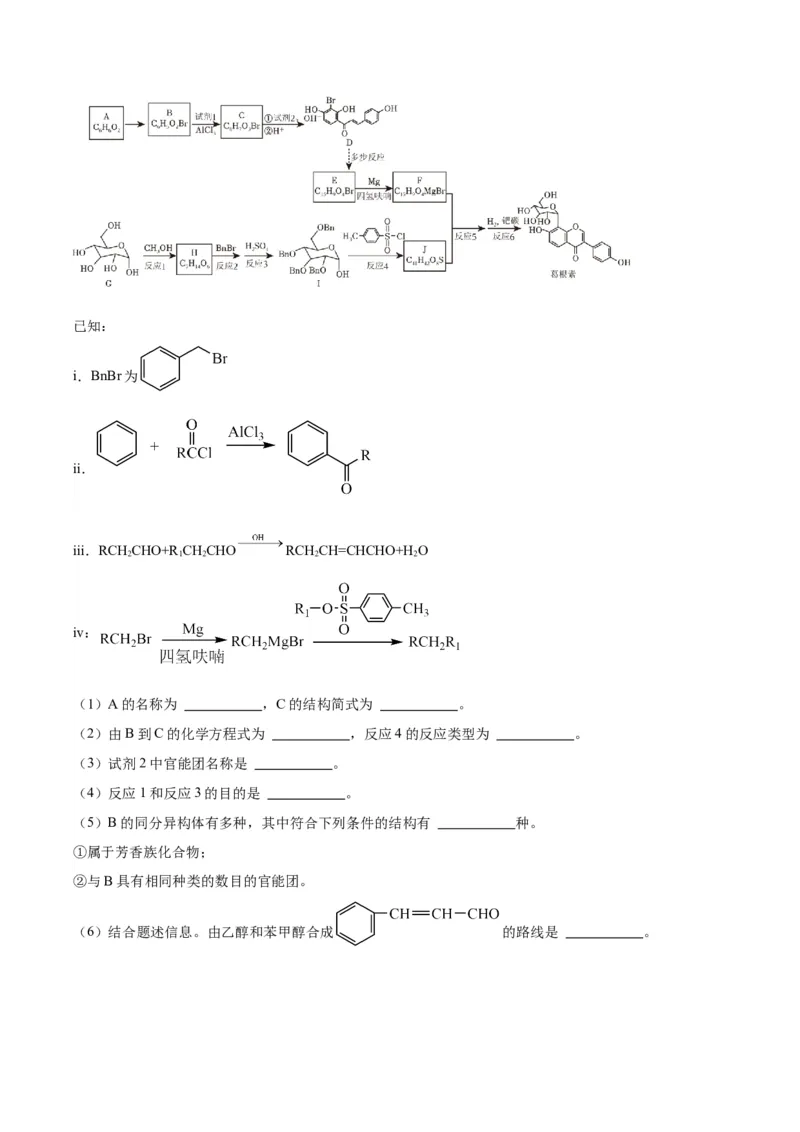
18.(15分)葛根素具有广泛的药理作用,临床上主要用于心脑血管疾病的治疗,其一种合成路线如
图:已知:
i.BnBr为
ii.
iii.RCHCHO+R CHCHO RCHCH=CHCHO+H O
2 1 2 2 2
iv:
(1)A的名称为 ,C的结构简式为 。
(2)由B到C的化学方程式为 ,反应4的反应类型为 。
(3)试剂2中官能团名称是 。
(4)反应1和反应3的目的是 。
(5)B的同分异构体有多种,其中符合下列条件的结构有 种。
①属于芳香族化合物;
②与B具有相同种类的数目的官能团。
(6)结合题述信息。由乙醇和苯甲醇合成 的路线是 。