文档内容
显了中华民族的文化自信。下列关于古诗词的说法中不正确的是
哈尔滨市第六中学 2020 级高三上学期 8 月月考
A.“愈风传乌鸡,秋卵方漫吃”中的“卵”主要指蛋白质
B.“壮志饥餐胡虏肉,笑谈渴饮匈奴血”中的“肉”和“血”都是脂肪
化学试题 C.“故人具鸡黍,邀我至田家”中的“黍”的主要成分是淀粉
D.“无边落木萧萧下”中的“落木”的主要成分是纤维素
可能用到的相对原子质量Cu:64Mn:55Al:27Cl:35.5 7.25℃时,有关弱酸的电离平衡常数如下,下列有关说法正确的是
一、选择题(每题2分,共50分) 弱酸化学式 CH
3
COOH HCN H
2
CO
3
1.室温下,有下列四种溶液:①0.1mol.L-1氨水②0.1mol·L-1NH
4
Cl溶液③0.2mol·L-1盐酸与0.2mol·L 电离平衡常数(25℃) 1.8×10-5 4.9×10-10 K
1
=4.3×10-7 K
2
=5.6×10-11
-1NH 4 Cl 溶液等体积混合④0.2mol·L-1NaOH 溶液与 0.2mol·L-1氨水等体积混合,四种溶液中 c A.等物质的量浓度的各溶液pH关系为pH(CH 3 COONa)>pH(Na 2 CO 3 )>pH(NaCN)
(NH + )由大到小排列正确的是 B.amol·L-1HCN溶液与bmol·L-1NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),
4
A.②③④① B.④①②③ C.①④②③ D.③②①④ 则a一定小于b
2.在25℃时,将amol/L的氨水与0.01mol/L的HCl溶液等体积混合,反应后溶液呈中性,下列说 C.0.1mol·L-1CH
3
COOH溶液中逐滴加入水,则溶液的导电性、醋酸的电离程度、pH均先增大
法不正确的是(忽略溶液混合后体积的变化) 后减小
A.溶液中c(NH
4
+)=c(Cl-) D.NaHCO
3
和Na
2
CO
3
混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HCO
3
-)+2c
B.此时水的电离程度最大 (CO
3
2-)
C.此时溶液中NH 3 ·H 2 O的物质的量浓度为1/2[(a-0.01)]mol/L 8.如图所示,向A中充入1molX和1molY,向B中充入2molX和2molY,起始V A =V B =aL,
在相同温度和有催化剂的条件下,两容器中各自发生下列反应:X(g)+Y(g) 2N(g)+W(g) ΔH>
109
D.用含a 的代数式 NH ·H O的电离平衡常数K = (mol/L) 0,达到平衡时,v(A)=1.2aL,则下列说法错误的是( )
3 2 b a0.01 K
A.反应开始时,B容器中化学反应速率快
3.常温下,下列四种溶液中由水电离生成的c(H+)之比(①∶②∶③∶④)为 B.A容器中X的转化率为40%,且比B中X的转化率小
①1mol/L的盐酸;②0.1mol/L盐酸;③0.01mol/L的NaOH溶液;④1mol/L的NaOH溶液. C.打开K达新平衡后,升高B容器温度,A容器体积会增大 A B
A.1:10:100:1 B.1:10-1:10-12:10-14 D.打开K一段时间,达到新平衡时,A的体积为2.6aL(两边通管中气体体积不计)
C.14:13:12:14 D.1:2:12:14 9.某化学科研小组研宄在其他条件不变时,改变某一条件对A
2
(g) +3B
2
(g) AB
3
(g)
4.不同温度下,水溶液中c(H+)与 c(OH+)的关系如图所示, 化学平衡状态的影响,得到如右图所示的变化规律(图中T表示温度, n表示物质的景),根据如
下列说法正确的是 图可得出的判断结论正确的是( )
A.若从a点到c点,可采用在水中加入酸的方法 A.反应速率a>b>c
B.b点对应的醋酸中由水电离的c(H+)=10-6mol·L-1 B.若T
2
>T
1
,则正反应一定是吸热反应
C.T℃时,0.05mol·L-1的Ba(OH)
2
溶液的pH=11 C.达到平衡时,AB
3
的物质的量大小为:b>c>a
D.c点对应溶液的K
w
大于d点对应溶液的K
w
D.达到平衡时A
2
的转化率大小为:b>a>c
5.如图是常见四种有机物的比例模型示意图。下列说法正确的是
10.中草药黄芩对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是
A.含有4种含氧官能团
B.遇FeCl 溶液能显色
3
A.甲能使酸性高锰酸钾溶液褪色 C.分子中碳原子均采用sp2杂化
B.乙可与溴水发生取代反应使溴水褪色 D.与足量H
2
发生完全加成反应,1mol该物质最多消耗7molH
2
C.丙中的碳碳键长是介于碳碳单键和碳碳双键之间
D.丁在稀硫酸作用下可与乙酸发生取代反应
6.中国古诗词中,不少名言佳句描写了劳动人民的生产与生活,其知识性与文艺性珠璧交辉,彰
高三化学试题 第1页 共5页13.已知Ag SO 的K 为2.0×10-5,将适量Ag SO 固体溶于100mL水中至刚好饱和, 该过程中
2 4 sp 2 4
Ag+和SO 2-浓度随时间变化关系如右图(饱和Ag SO 溶液中c(Ag+)=0.034mol/L)。若t 时刻在上
11.左旋多巴( )用于改善肌强直和运动迟缓效果明显,下列有关该物质的 4 2 4 1
述体系中加入100mL0.020mol/LNa SO 溶液,下列示意图中,能正确表示t 时刻后Ag+和SO 2-
2 4 1 4
浓度随时间变化关系的是
说法错误的是
A.其分子式为C H NO B.能与酸或碱反应生成盐
9 11 4
C.核磁共振氢谱上共有9个峰 D.分子中最多有6个碳原子共平面
12.下列图示与对应的叙述相符的是( )
A.向CH COOH溶液中逐步加入CH COONa固体后,溶液pH的变化
3 3
14.一定温度下,三种碳酸盐MCO (M:Mg2+、Ca2+、Mn2+)的沉淀溶
3
解平衡曲线如下图所示。已知:pM=-lgc(M),pc(CO 2-)=-lgc(CO 2-)。下
3 3
列说法正确的是
B.向CH COOH溶液中加水时溶液的导电性变化,则CH COOH溶液的pH:a>b A.MgCO 、CaCO 、MnCO 的K 依次增大
3 3 3 3 3 sp
B.a 点可表示MnCO 的饱和溶液,且c(Mn2+)=c(CO 2-)
3 3
C.b 点可表示CaCO 的饱和溶液,且c(Ca2+)c(CO 2-)
3 3
15.一定温度下,难溶电解质A B 在水中溶解平衡的溶度积为K =cm(An+)×cn(Bm-)。25℃,向
m n sp
AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na S溶液,先出现黄色沉淀,最终生成黑色
2
沉淀。已知有关物质的颜色和溶度积如下:
C.催化剂能改变化学反应的焓变 物质 AgCl AgI Ag S
2
颜色 白 黄 黑
K (25℃) 1.8×10-10 1.5×10-16 1.8×10-50
sp
下列叙述不正确的是( )
A.溶度积小的沉淀可以转化为溶度积更小的沉淀
B.若先加入Na S溶液,再加入KI溶液,则无黄色沉淀产生
2
C.25℃时,饱和AgCl、AgI、Ag S溶液中所含Ag+的浓度相同
2
D.25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl 溶液中的溶度积相同
2
D.等量NO 在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO(g)⇌ N O(g),
2 2 2 4
16.工业上以乙苯催化脱氢制取苯乙烯的反应如下: CH CH (g)== CH CH (g)
相同时间后测得NO 含量的曲线,则该反应的△H<0 2 3 2
2
+H (g)现将xmol乙苯蒸气通入体积可变的密闭容器中反应,维持体系总压强p 恒定。在某催
2 总
化剂作用下,乙苯的平衡转化率随温度变化如图所示。
高三化学试题 第2页 共5页20.为除去MgCl 酸性溶液中的Fe3+,可在加热搅拌的条件下加入的一种试剂是
2
A.NH ·H O B.NaOH C.Na CO D.MgCO
3 2 2 3 3
21.已知在25℃时,FeS、CuS的溶度积常数(K )分别为6.3×10-18、1.3×10-36。常温时下列有
sp
关说法正确的是
A.除去工业废水中的Cu2+可以选用FeS作沉淀剂
B.向H S的饱和溶液中通入少量SO 气体溶液的酸性增强
2 2
C.因为H SO 是强酸,所以反应:CuSO +H S=CuS↓+H SO 不能发生
2 4 4 2 2 4
D.将足量的CuSO 溶解在0.1mol/L的H S溶液中,溶液中Cu2+的最大浓度为1.3×10-35mol
4 2
/L
22.宏观辨识与微观探析是化学学科核心素养之一,下列用于解释事实的方程式书写不正确的是
已知:气体分压(p
分
)= 气体总压(p
总
)×体积分数。不考虑副反应,下列说法正确的是 A.用TiCl
4
制备TiO
2
:TiCl
4
+(x+2)H
2
O=TiO
2
·xH
2
O↓+4HCl
A.400℃时,向体系中通入水蒸气,v(正)、v(逆) 均减小,且乙苯转化率降低
B.向硫代硫酸钠溶液中加入稀硫酸:SO2+2H+=S↓+SO ↑+H O
B.500℃时,向体系中通入乙苯、苯乙烯、氢气各0.1xmol,平衡不移动 2 3 2 2
C.550℃时,用平衡分压代替平衡浓度表示的化学平衡常数K =9/16×p
p 总 C.用明矾[KAl(SO ) ·12H O]作净水剂:Al3++3H O AlOH (胶体)+3H+
D.550℃时平衡体系中苯乙烯的体积分数是450℃时的3倍 4 2 2 2 3
17.将固体NH I置于密闭容器中,在一定温度下发生下列反应:
4 D.泡沫灭火器喷出白色泡沫用于灭火:2Al3++3CO2+3H O=2Al(OH) ↓+3CO ↑
①NH I(s) NH (g)+HI(g);②2HI(g) H (g)+I (g),c(HI)=4 3 2 3 2
4 3 2 2
mol·L-1,c(H )=0.5mol·L-1,则此温度下反应①的平衡常数为( ) 23.下图表示的是难溶氢氧化物在不同pH下的溶解度(S/mol·L-1),下列说法中正确的是
2
A.9 B.16 C.20 D.25 A.pH=3时溶液中铁元素的主要存在形式是Fe3+
18.反应C(s)+H 2 O(g) CO(g)+H 2 (g)在一可变容积的密闭容 B.若Ni(NO 3 ) 2 溶液中含有少量的Co2+杂质,可通过调节溶液pH的方法来除去
器中进行,下列条件的改变对其反应速率几乎无影响的是( ) C.若分离溶液中的Fe3+和Cu2+,可调节溶液的pH在4左右
①增加C的量 ②将容器的体积缩小一半 ③保持体积不变,充
D.若在含有Cu2+和Ni2+的溶液中加入烧碱,Ni(OH) 优先沉淀
2
入N 使体系压强增大 ④保持压强不变,充入N 使容器体积变
2 2 24.定量分析中可用AgNO 溶液滴定Cl-溶液,加入K CrO 为指示剂,达到滴定终点时溶液体积
大 3 2 4
A.①④ B.②③ 为50mL,c(Cl-) =10-5mol·L-1,AgNO 3 与CrO 4 2- 生成砖红色的Ag 2 CrO 4 沉淀。已知K sp (AgCl)
C.①③ D.②④ =1.77×10-10, K sp (AgI)=8.51×10-17,K sp (Ag 2 CrO 4 )=1.12×10-12,根据以上实验操作和有关数据,
19.下列有关电解质溶液的说法正确的是 下列说法正确的是
A.常温下,向含AgCl固体的AgCl溶液中加入NaCl固体,AgCl沉淀的量不变
c(H)
B.滴定终点时,溶液中CrO 2-的浓度约为3.6×10-3mol·L-1
4
A.向0.1mol
L1
CH 3 COOH溶液中加入少量水,溶液中
c(CH
3
COOH)
减小 C.向 10mL0.1moL/LAgNO 3 溶液中滴加 3—5 滴 0.1moL/LNaCl 溶液生成 AgCl 沉淀,再滴加
KI溶液,生成AgI沉淀,能够说明K (AgI)< K (AgCl)
c(CH COO) sp sp
3 D.可用0.1mol·L-1的KI溶液代替K CrO 做指示剂
c(CH COOH)c(OH) 2 4
B.将CH 3 COONa溶液从20℃升温至60℃,溶液中 3 增大 25.某有机物的结构简式如右图,该物质不应有的化学性质是( )
①可燃烧;
c(NH)
4 1 ②可跟溴加成;
C.向盐酸中加入氨水至中性,溶液中
c(Cl)
③可使酸性KMnO 溶液褪色;
4
④可跟NaHCO 溶液反应;
c(Cl) 3
⑤可跟NaOH溶液反应;
D.向AgCl、AgBr的饱和溶液中加入少量AgNO
3
,溶液中c(Br)不变
⑥可在碱性条件下水解
A.①③ B.③⑥ C.④⑤ D.⑥
高三化学试题 第3页 共5页二、非选择题(共50分) 27(12分).铜及其化合物有许多特殊用途,最近科研人员用CuP
2
作电极电催化CO
2
,CO
2
经甲酸
26(13分).某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选 盐、乙醛最终转化为1-丁醇,铜则转化为Cu (PO ) 和Cu O。回答下列问题:。
3 4 2 2
择甲基橙作指示剂。请填写下列空白: (1)基态磷原子的价电子排布图为___________,基态Cu原子电子占据最高能级的电子云轮廓图为
(1)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,标准液应该装在_______(填仪器名称)中;滴定 ___________形。
达到终点的现象为: 。 (2)Cu、O、P三种元素中,电负性由大到小的顺序为___________。
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是_______。
(3)PO3-的空间构型为___________,其中P采取___________杂化方式。
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液 4
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥 (4)1-丁醇、1-氯丁烷的沸点依次为118°C、78.2°C,前者沸点较高的原因是___________。
C.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 (5)Cu、Mn、Al形成的一种金属间化合物的晶体结构如图所示。已知晶胞参数为apm,内部正方形
(3)若滴定开始和结束时,滴定管中的液面如图所示,所用盐酸溶液的体积为_______mL。 的边长为bpm,N 表示阿伏加德罗常数。
A
(4)某学生根据三次实验分别记录有关数据如表:
0.1000mol/L盐酸的体积/mL
待测NaOH溶
滴定次数
液的体积/mL
滴定前刻度 滴定后刻度
溶液体积 该晶体的密度为___________(用含a、N
A
的代数式表示,不用化简);P、Q间的距离为___________pm
/mL (要求同上)。
第一次 25.00 0.00 26.11 26.11
第二次 25.00 1.56 30.30 28.74
第三次 25.00 0.22 26.31 26.09
28(12分).某种具有菠萝气味的香料M是有机化合物A与苯氧乙酸发生酯化反应的产物。M的
合成路线如下:
请选用数据计算该氢氧化钠溶液的物质的量浓度:c(NaOH)=_______mol/L(保留小数点后4位)。
(5)某学习小组用“间接碘量法”测定含有CuCl ·2H O晶体的试样(不含能与I-发生反应的氧化性杂质)
2 2
的纯度,过程如下:取0.36g试样溶于水,加过量KI固体,充分反应,生成白色沉淀。用0.1000mol/L
Na S O 标准溶液滴定,到达滴定终点时,消耗Na S O 标准溶液20.00mL。
2 2 3 2 2 3
已知:I 2 +2S 2 O 3 2-=S 4 O 6 2-+2I-
选用_______作滴定指示剂,试样中CuCl ·2H O的质量分数为_______。(保留小数点后一位)
2 2 已知:①A的化学式为C H O,能使溴水褪色。
3 6
②CH CH COOH Cl 2
3 2 催化剂
③R-ONaR-ClR-O-R′
Δ
高三化学试题 第4页 共5页回答下列问题:
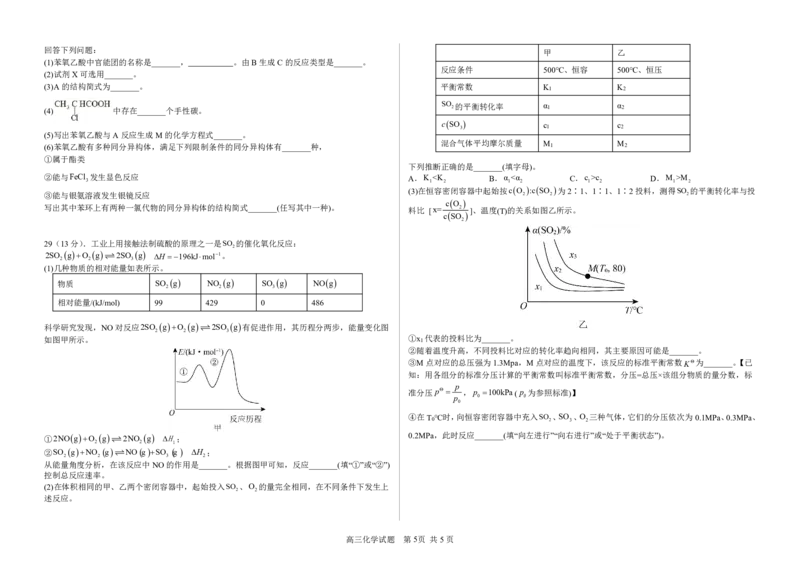
甲 乙
(1)苯氧乙酸中官能团的名称是_______, 。由B生成C的反应类型是_______。
反应条件 500℃、恒容 500℃、恒压
(2)试剂X可选用_______。
(3)A的结构简式为_______。 平衡常数 K K
1 2
SO 的平衡转化率 α α
(4) 中存在_______个手性碳。 2 1 2
cSO
c c
3 1 2
(5)写出苯氧乙酸与A反应生成M的化学方程式_______。
混合气体平均摩尔质量 M M
(6)苯氧乙酸有多种同分异构体,满足下列限制条件的同分异构体有_______种, 1 2
①属于酯类
下列推断正确的是_______(填字母)。
②能与FeCl 发生显色反应 A.K c D.M >M
3 1 2 1 2 1 2 1 2
(3)在恒容密闭容器中起始按cO :cSO 为2∶1、1∶1、1∶2投料,测得SO 的平衡转化率与投
③能与银氨溶液发生银镜反应 2 2 2
cO
写出其中苯环上有两种一氯代物的同分异构体的结构简式_______(任写其中一种)。 料比 [x= 2 ]、温度(T)的关系如图乙所示。
cSO
2
29(13分).工业上用接触法制硫酸的原理之一是SO 的催化氧化反应:
2
2SO gO g 2SO g H 196kJmol1。
2 2 3
(1)几种物质的相对能量如表所示。
物质 SO g NO g SO g NOg
2 2 3
相对能量/(kJ/mol) 99 429 0 486
科学研究发现,NO对反应2SO gO g 2SO g有促进作用,其历程分两步,能量变化图
2 2 3
如图甲所示。 ①x 代表的投料比为_______。
1
②随着温度升高,不同投料比对应的转化率趋向相同,其主要原因可能是_______。
③M点对应的总压强为1.3Mpa,M点对应的温度下,该反应的标准平衡常数 K为_______。【已
知:用各组分的标准分压计算的平衡常数叫标准平衡常数,分压=总压×该组分物质的量分数,标
p
准分压p ,p 100kPa(p 为参照标准)】
p 0 0
0
④在T ℃时,向恒容密闭容器中充入SO 、SO 、O 三种气体,它们的分压依次为0.1MPa、0.3MPa、
0 2 3 2
①2NOgO g 2NO g H ; 0.2MPa,此时反应_______(填“向左进行”“向右进行”或“处于平衡状态”)。
2 2 1
②SO gNO g NO g SO g H ;
2 2 3 2
从能量角度分析,在该反应中NO的作用是_______。根据图甲可知,反应_______(填“①”或“②”)
控制总反应速率。
(2)在体积相同的甲、乙两个密闭容器中,起始投入SO 、O 的量完全相同,在不同条件下发生上
2 2
述反应。
高三化学试题 第5页 共5页