文档内容
专题(4)铁三角的转化同步练习
(答题时间:25分钟)
一、选择题
1. 下列除杂的操作不正确的是
A. MgCl 溶液中混有少量FeCl :加入足量镁充分反应后过滤
2 3
B. FeCl 溶液中混有少量FeCl :加入过量铁粉充分反应后过滤
2 3
C. CuCl 溶液中混有少量FeCl :加入足量锌粉充分反应后过滤
2 3
D. CaCl 溶液中混有少量FeCl :先加入HO 将Fe2+氧化成Fe3+,再加入CaCO 充分
2 2 2 2 3
反应后过滤
2. 硫酸亚铁易被氧化而变质。为检验某补血剂中硫酸亚铁是否变质,可向该补血剂配成
的溶液中加入
A. 硝酸和硝酸银溶液 B. 盐酸酸化的BaCl 溶液
2
C. KSCN溶液 D. 硝酸酸化的Ba(NO )
3 2
3. 铁屑溶于过量稀硫酸,过滤后向滤液中加入过量氨水,有白色沉淀生成,过滤,在空
气中加热沉淀至质量不再发生变化为止,得到红棕色残渣,上述沉淀和残渣分别是
A. Fe(OH) Fe O B. Fe(OH) Fe O
3 2 3 2 2 3
C. Fe(OH) Fe(OH) D. Fe(OH) Fe O
2 3 2 3 4
4. 将1.12 g铁粉加入25 mL 2 mol·L-1的氯化铁溶液中,充分反应后,其结果是
A. 铁粉有剩余,溶液呈浅绿色,Cl-基本保持不变
B. Fe2+和Fe3+物质的量之比为5∶1
C. 往溶液中滴入无色KSCN溶液,显红色
D. 氧化产物和还原产物的物质的量之比为2∶5
5. A、B、C三种物质中均含有同一种元素M,它们之间有如图所示的转化关系。A为一
种金属单质,其产量直接关系国民经济命脉。反应①②③均为化合反应,反应④为置换反
应。下列有关说法不正确的是
A. ①中所加试剂可能是氯气
B. ③中需要加具有氧化性的试剂
C. A与稀硝酸反应一定能实现元素M在①中发生的价态变化
D. 元素M在②中发生的价态变化也能通过加碘化钾溶液实现
第1页二、填空题
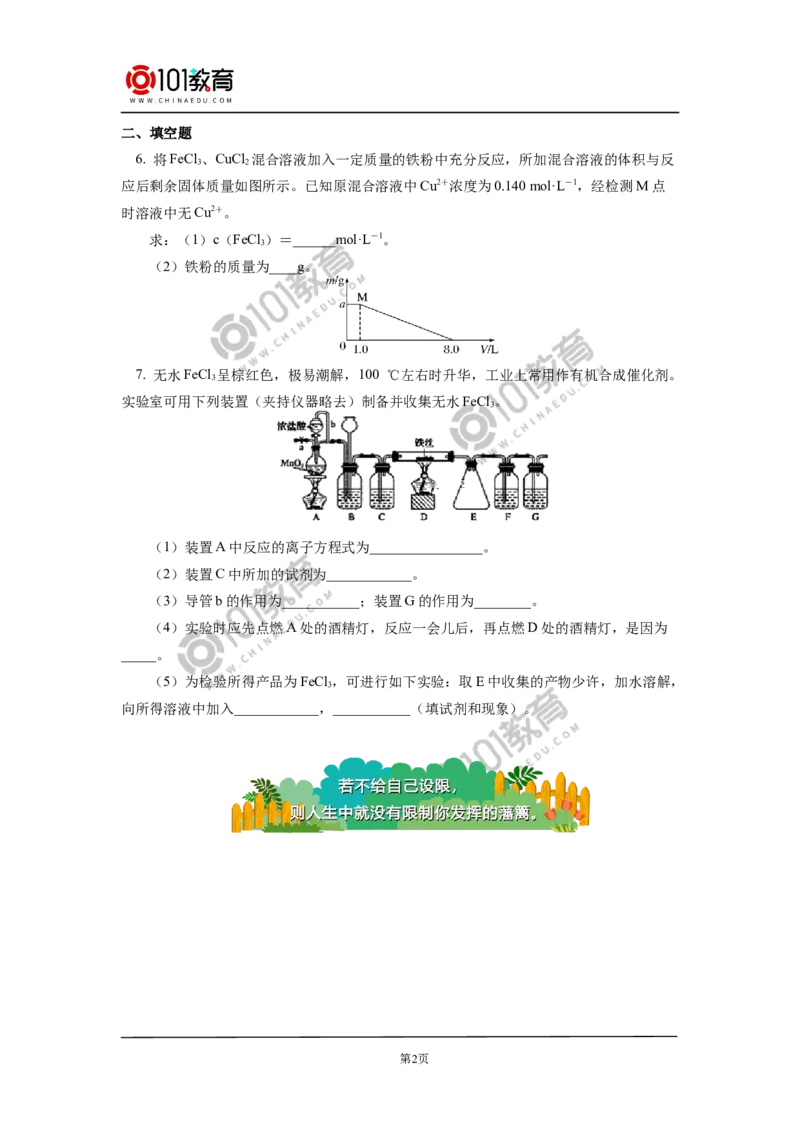
6. 将FeCl 、CuCl 混合溶液加入一定质量的铁粉中充分反应,所加混合溶液的体积与反
3 2
应后剩余固体质量如图所示。已知原混合溶液中Cu2+浓度为0.140 mol·L-1,经检测M点
时溶液中无Cu2+。
求:(1)c(FeCl )=______mol·L-1。
3
(2)铁粉的质量为____g。
7. 无水FeCl 呈棕红色,极易潮解,100 ℃左右时升华,工业上常用作有机合成催化剂。
3
实验室可用下列装置(夹持仪器略去)制备并收集无水FeCl 。
3
(1)装置A中反应的离子方程式为________________。
(2)装置C中所加的试剂为____________。
(3)导管b的作用为___________;装置G的作用为________。
(4)实验时应先点燃A处的酒精灯,反应一会儿后,再点燃D处的酒精灯,是因为
_____。
(5)为检验所得产品为FeCl ,可进行如下实验:取E中收集的产物少许,加水溶解,
3
向所得溶液中加入____________,___________(填试剂和现象)。
第2页专题(4)铁三角的转化同步练习参考答案
1. 【答案】C
【解析】FeCl 溶液中存在水解平衡:FeCl +3HO Fe(OH)+3HCl,加入Mg
3 3 2 3
与H+反应,平衡右移,使Fe3+转化成Fe(OH) 而除去,A正确;加入过量铁粉,FeCl
3 3
与Fe反应生成FeCl 而达到除杂的目的,B正确;C项中加入足量锌粉,Cu2+、Fe3+均与
2
Zn反应,不符合除杂要求,错误;先用HO 将Fe2+氧化成Fe3+,再利用FeCl 的水解,加
2 2 3
入CaCO 与H+反应将Fe3+转化成Fe(OH) 而除去,D正确。
3 3
2. 【答案】C
【解析】A选项 硝酸和硝酸银溶液,通常用于检验Cl-的存在;B. 盐酸酸化的BaCl
2
溶液,通常用于检验SO 2-的存在;C. KSCN溶液,通常用于检验Fe3+的存在,符合题意;
4
D. 硝酸酸化的Ba(NO ) 可用于检验不含SO 2-的溶液中SO 2-的存在。
3 2 3 4
3. 【答案】B
【解析】铁与稀硫酸反应生成FeSO ,再与过量氨水反应生成白色沉淀Fe(OH),
4 2
在空气中加热Fe(OH),铁元素被氧化为+3价,最后所得红棕色残渣为Fe O。
2 2 3
4. 【答案】C
将1.12g铁粉加入到25mL2mol·L-1的氯化铁溶液中,铁粉的物质的量n=
,氯化铁的物质的量n=c×V=2mol·L-1×0.025L=0.05mol,铁粉与氯
化铁的离子反应方程式为:Fe+2Fe3+=3Fe2+,根据反应的物质的量之比等于计量数之比知,
0.02mol铁粉完全反应需要0.04mol氯化铁,所以氯化铁剩余0.01mol,生成的Fe2+的物质的
量为0.06mol。
A. 氯化铁剩余了0.01mol,铁完全反应,故A错误;
B. Fe2+的物质的量为0.06mol,氯化铁的物质的量为0.01mol,所以Fe2+和Fe3+的物质的
量之比为6:1,故B错误;
C. 由于氯化铁剩余,向溶液中滴入无色KSCN溶液,显血红色,故C正确;
D. 氧化产物与还原产物的物质的量之比是1:2,故D错误;答案选C。
5. 【答案】C
【解析】根据转化关系可确定A为变价金属,应为Fe,反应①加入氯气能实现,B为
FeCl ,C为FeCl ,A项正确;反应③中铁元素由+2价升高到+3价,需要加具有氧化性的
3 2
试剂,B项正确;过量的铁与稀硝酸反应时,生成硝酸亚铁,C项错误;Fe3+能将I−氧化成
I,自身被还原成Fe2+,D项正确。
2
考点:铁及其化合物的转化
6. 【答案】0.04 8.96
第3页【解析】根据上述分析可知:
(1)1L溶液内氯化铜的物质的量为0.140 mol,设铁离子的物质的量为x mol,则
(0.140+0.5x)mol 56g/mol=0.140 64g/mol,解得x=0.04,则c(FeCl )=
3
=0.04 mol·L-1,故答案为:0.04;
(2)加入8.0 L溶液时固体全部溶解,说明铁只与铁离子反应,则铁离子的物质的量
为0.04 mol·L-1 8.0 L=0.32 mol,则根据2Fe3++Fe=3Fe2+可知,铁的物质的量为
56g/mol=8.96 g,故答案为:8.96。
7. 【答案】MnO +4H++2Cl- Mn2++Cl↑+2HO 浓硫酸(或浓HSO )
2 2 2 2 4
平衡压强(或使浓盐酸顺利流下) 吸收多余的Cl 排尽实验装置中的空气
2
KSCN溶液 溶液变红
【解析】(1)加热条件下,浓盐酸和二氧化锰反应生成氯化锰、氯气和水,反应的化
学方程式为:MnO +4H++2Cl- Mn2++Cl↑+2HO;
2 2 2
(2)氯气中有氯化氢和水杂质,为制备并收集无水FeCl ,B装置中装饱和食盐水,
3
除去氯气中的氯化氢, C装置中装浓硫酸干燥氯气,
(3)导管b的作用为平衡装置压强,是盐酸能顺利流下;装置G为尾气处理装置,未
反应的氯气有毒,不能排放到空气中,作用为吸收多余的Cl。
2
(4)实验时由于装置中有空气中的水蒸气,会与铁反应,也会使产物氯化铁潮解,导
致制备产品不纯,所以要先排除装置中的空气,因此实验时应先点燃A处的酒精灯,反应
一会儿后,排尽装置中的空气,再点燃D处的酒精灯。
(5)为检验所得产品为FeCl ,可进行如下实验:取E中收集的产物少许,加水溶解,
3
向所得溶液中加入KSCN溶液,溶液变红说明含有三价铁离子。
第4页