文档内容
氯及其化合物(1)
重难点 题型 分值
1. 氯气的物理性质
重点 2. 氯气与单质反应
3. 氯气与化合物反应 选择、
12-15分
填空
1. 氯气与单质的反应
难点
2. 氯气与化合物的反应
核心知识点一:
一、氯气的性质
1. 氯元素的概述
(1)氯元素的存在
在自然界中只以化合物的形式存在;以NaCl、MgCl 、CaCl 等形式大量存在与海水中,
2 2
还存在与陆地的盐湖和盐矿中。
第1页(2)氯的原子结构
氯原子最外层有7个电子,在化学反应中容易得到一个电子,使最外层达到8个电子
的稳定结构。因此,氯气是很活泼的非金属单质,具有强氧化性。
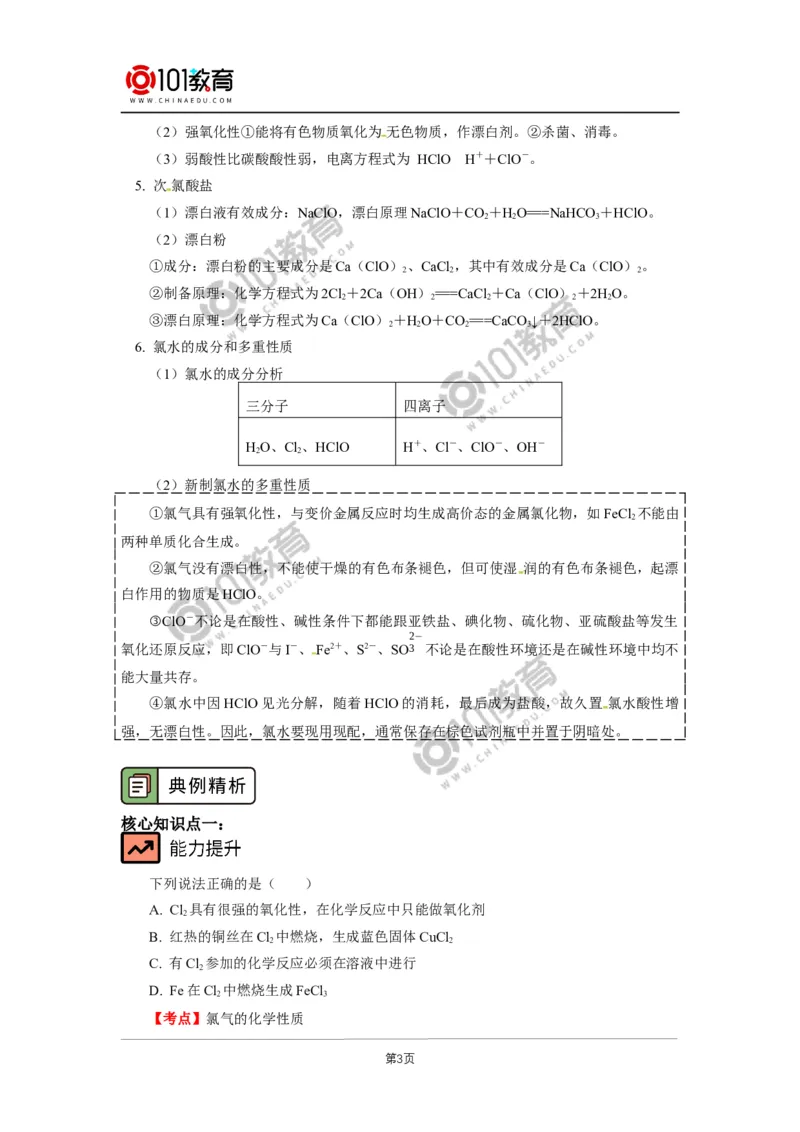
2. 氯气的物理性质
颜色 状态 气味 密度 毒性 溶解性
黄绿色 气体 刺激性气味 比空气大 有毒 1体积水溶解约2体积Cl
2
[注意]实验室里闻有毒气体及未知气体气味的方法是用手在瓶口轻轻扇动,仅使极少
量气体飘进鼻孔即可。
3. 氯气与单质反应
(1)与金属反应
①与钠反应:2Na+Cl=====2NaCl。钠在氯气中剧烈燃烧,火焰呈黄色,生成白烟
2
②与铁反应:2Fe+3Cl=====2FeCl 。剧烈燃烧,产生棕褐色的烟
2 3
③与铜反应:Cu+Cl=====CuCl 。剧烈燃烧,产生棕黄色的烟,加少量的水,溶液
2 2
呈绿色,加较多的水,溶液呈黄色
(2)与非金属反应与H 反应:H+Cl=====2HCl。
2 2 2
核心知识点二
二、氯气与化合物反应
1. 与水反应:溶于水的氯气部分与水反应,离子方程式为Cl+HO=H++Cl-+HClO。
2 2
2. 与碱反应 Cl+2NaOH===NaCl+NaClO+HO。
2 2
3. 与还原性无机化合物反应(书写离子方程式)
①与碘化钾溶液反应:2I-+Cl===I +2Cl-。
2 2
②与SO 水溶液反应:Cl+SO+2H O===4H++2Cl-+SO2-。
2 2 2 2 4
③与FeCl 溶液反应:2Fe2++Cl===2Fe3++2Cl-。
2 2
4. 次氯酸
(1)不稳定性见光易分解,化学方程式为2HClO=====2HCl+O↑。
2
第2页(2)强氧化性①能将有色物质氧化为无色物质,作漂白剂。②杀菌、消毒。
(3)弱酸性比碳酸酸性弱,电离方程式为 HClO H++ClO-。
5. 次氯酸盐
(1)漂白液有效成分:NaClO,漂白原理NaClO+CO+HO===NaHCO+HClO。
2 2 3
(2)漂白粉
①成分:漂白粉的主要成分是Ca(ClO)、CaCl ,其中有效成分是Ca(ClO)。
2 2 2
②制备原理:化学方程式为2Cl+2Ca(OH)===CaCl +Ca(ClO)+2HO。
2 2 2 2 2
③漂白原理:化学方程式为Ca(ClO)+HO+CO===CaCO ↓+2HClO。
2 2 2 3
6. 氯水的成分和多重性质
(1)氯水的成分分析
三分子 四离子
HO、Cl、HClO H+、Cl-、ClO-、OH-
2 2
(2)新制氯水的多重性质
①氯气具有强氧化性,与变价金属反应时均生成高价态的金属氯化物,如FeCl 不能由
2
两种单质化合生成。
②氯气没有漂白性,不能使干燥的有色布条褪色,但可使湿 润的有色布条褪色,起漂
白作用的物质是HClO。
③ClO-不论是在酸性、碱性条件下都能跟亚铁盐、碘化物、硫化物、亚硫酸盐等发生
2−
氧化还原反应,即ClO-与I-、Fe2+、S2-、SO3 不论是在酸性环境还是在碱性环境中均不
能大量共存。
④氯水中因HClO见光分解,随着HClO的消耗,最后成为盐酸,故久置 氯水酸性增
强,无漂白性。因此,氯水要现用现配,通常保存在棕色试剂瓶中并置于阴暗处。
核心知识点一:
下列说法正确的是( )
A. Cl 具有很强的氧化性,在化学反应中只能做氧化剂
2
B. 红热的铜丝在Cl 中燃烧,生成蓝色固体CuCl
2 2
C. 有Cl 参加的化学反应必须在溶液中进行
2
D. Fe在Cl 中燃烧生成FeCl
2 3
【考点】氯气的化学性质
第3页【答案】D
【解析】A. Cl 的化合价为0价,处于中间价态,在化学反应中既能做氧化剂也能做
2
还原剂。
B. 红热的铜丝在Cl 中剧烈燃烧,产生棕黄色的烟
2
C. 不一定,比如氯气与金属钠反应
下列化合物能用金属与氯气反应制备,又能用金属与盐酸反应制备的是( )
A. MgCl
2
B. CuCl
2
C. FeCl
2
D. FeCl
3
【考点】氯气与金属反应
【答案】A
【解析】A. Mg与Cl 反应可以生成MgCl ;Mg与盐酸反应可以生成MgCl
2 2 2
B. Cu与盐酸不反应
C. Fe与Cl 反应生成FeCl ;与盐酸反应生成FeCl ;
2 3 2
D. Fe与Cl 反应生成FeCl ;与盐酸反应生成FeCl ;
2 3 2
核心知识点二:
下列说法中不正确的( )
A. 氯水的pH小于7
B. 燃烧一定有氧气参加
C. 紫色的石蕊试液中滴加氯水,先变红后褪色
D. 用氯气消毒自来水的原因是:氯气与水反应生成的HCl有强氧化性,可杀灭水中的
细菌
【考点】氯水的性质
【答案】BD
【解析】A. 氯与水反应生成盐酸和次氯酸,显酸性,固pH小于7
B. 不一定吗,比如金属钠与氯气反应,属于燃烧,但是没有氧气参与反应
C. 紫色的石蕊试液中滴加氯水,溶液显酸性,所以紫色石蕊变红。因为有次氯酸,有
强氧化性,故褪色
第4页D. 氯气与水反应生成的HClO有强氧化性,可杀灭水中的细菌
新制的氯水与久置的氯水相比较,下列说法不正确的是( )
A. 都呈酸性
B. 前者能使有色布条褪色
C. 光照新制氯水有气体逸出,该气体是Cl
2
D. 加AgNO 溶液都能生成白色沉淀
3
【考点】考查氯水的性质
【答案】B
【解析】新制的氯水中含有分子Cl 、HClO、HO,离子H+、Cl-、ClO-、OH-,次
2 2
氯酸光照时发生反应生成盐酸与氧气。所以久置的氯水实际上已经是盐酸。
(答题时间:25分钟)
一、选择题:本题包括12小题,每小题4分,共48分。
1. 下列关于氯及其化合物说法正确的是( )
A. 漂白粉是混合物,有效成分是Ca(ClO)
2
B. 光照氯水有气泡逸出,该气体是Cl
2
C. Cl 能使湿润的有色布条褪色,说明Cl 具有漂白性
2 2
D. 实验室用二氧化锰与稀盐酸反应制取Cl
2
2. 关于氯水中存在的各种成分,下列说法中可能错误的是( )
A. 加入含有NaOH的酚酞试液,红色褪去,说明有H+存在
B. 加入有色布条后,有色布条褪色,说明有HClO分子存在
C. 氯水呈浅黄色,且有刺激性气味,说明有Cl 分子存在
2
D. 加入硝酸酸化的AgNO 溶液产生白色沉淀,说明有Cl-存在
3
3. 在自来水的生产中,常通入适量氯气进行杀菌消毒,氯气与水反应的产物之一是盐酸。
市场上有些不法商贩为牟取暴利,利用自来水冒充纯净水桶装出售。为辨别真伪,可用以
鉴别的一种试剂是( )
A. 氢氧化钠溶液 B. 酚酞试液 C. 硝酸银溶液 D. 氯化钡溶液
4. 下列关于漂粉精在空气中容易失效原因的准确表述是( )
①次氯酸不稳定,易分解 ②CaCl 易潮解
2
③Ca(ClO) 易和盐酸反应 ④Ca(ClO) 易和空气中的CO 和HO反应
2 2 2 2
第5页A. 只有① B. 只有② C. ①和② D. ①④
5. 下列物质中含有Cl-的是( )
A. 液氯 B. KClO C. HCl气体 D. 氯水
3
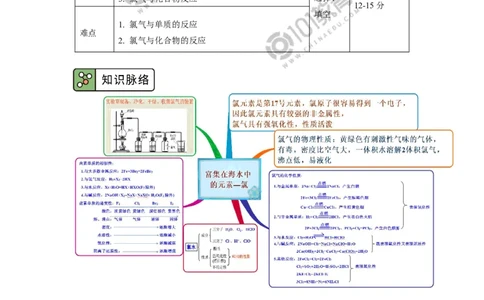
6. (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的
广口瓶,可观察到的现象是_______________。
(2)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用_______________溶液
吸收多余的氯气,原理是(用化学方程式表示)_________________________________。根
据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分
是__________(化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是
__________(字母代号填)。
A. O B. Cl C. CO D. HClO
2 2 2
(3)据报道,某化工总厂最近相继发生氯气泄漏和爆炸事故,当人们逃离爆炸现场时,
可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是
___________。
A. NaOH B. NaCl C. KBr D. Na CO
2 3
7. 有X、Y、Z三种元素:
(1)X、Y、Z的单质在常温下均为气体;
(2)X单质可以在Z的单质中燃烧,生成物为XZ,火焰呈苍白色;
(3)XZ极易溶于水,在水溶液中电离出X+和Z-,其水溶液能使蓝色石蕊试纸变红;
(4)每2个X 分子能与1个Y 分子化合成2个XY分子,XY常温下为液体;
2 2 2 2
(5)Z单质溶于XY中,所得溶液具有漂白性。
2
试写出其元素符号:
(1)X_______,Y_______, Z_______,以及化合物的分子式:XZ_______,
XY_________。
2
(2)写出Z单质与XY反应的化学反应方程式:____________________________。
2
第6页1. 答案:A
【解析】B、气体是O ,故错;C、应是HClO具有漂白性,故错;D、应是浓盐酸,
2
故错。故选A。
2. 答案:A
【解析】碱遇酚酞变红,氢离子与碱反应使颜色消失,但次氯酸具有漂白性,也能使
颜色褪去,则不能说明氢离子存在,A错误;次氯酸具有强氧化性,能够漂白有色物质,
则加入有色布条后,有色布条褪色,则说明氯水中有HClO分子存在,B正确;氯气为黄
绿色气体,具有刺激性气味,说明氯气分子存在 C正确;加入硝酸酸化的硝酸银溶液产生
白色沉淀,该沉淀为AgCl,说明氯水中有氯离子存在D正确
3. 答案:C
【解析】硝酸银与氯离子反应能生成氯化银白色沉淀。
4. 答案:D
【解析】漂粉精在空气中容易失效原因是Ca(ClO) 易和空气中的CO 和HO反应生
2 2 2
成次氯酸,次氯酸不稳定,易分解
5. 答案:B
【解析】A. 液氯中只含有氯分子
B. KClO 存在的是氯酸根,没有氯离子
3
C. HCl气体含有氯化氢分子
D. 氯水中氯气与水反应生成氯化氢,氯化氢在水中能电离生成氯离子
6. 答案:(1)潮湿有色布条褪色而干燥有色布条不褪色(2)氢氧化钠(NaOH)
2NaOH+Cl =NaClO+NaCl+H O
2 2
Ca(ClO); C
2
(3)D
7. 答案:(1)H O Cl HCl H O
2
(2)Cl+ H O==HCl+HClO
2 2
【解析】X、Y、Z的单质在常温下均为气体;
X单质可以在Z的单质中燃烧,生成物为XZ,火焰呈苍白色;且XZ极易溶于水,在
水溶液中电离出X+和Z-,其水溶液能使蓝色石蕊试纸变红;证明XZ是HCl,其中X是氢
气,Z是氯气
每2个X 分子能与1个Y 分子化合成2个XY分子,XY常温下为液体;且Z单质溶
2 2 2 2
于XY中,所得溶液具有漂白性。所以XY为HO。
2 2 2
第7页