文档内容
氮及其氧化物(1)
重难点 题型 分值
1. 氮气的性质
重点
2. 一氧化氮和二氧化氮的性质
选择和填空 4-6分
难点 一氧化氮和二氧化氮的性质
核心知识点一:
一、氮气
1. 氮的固定
将游离态的氮转化为化合态的氮的过程
(1)雷电固氮:
在放电条件下,氮气与氧气可直接化合成无色的一氧化氮气体。生成的一氧化氮常温
下与氧气化合成红棕色的二氧化氮气体,二氧化氮溶于水生成硝酸。硝酸随雨水降落,与
土壤里的碳酸盐等作用转变为易被作物吸收的硝酸盐。故农谚有“雷雨发庄稼”一说。过
程中反应的化学方程式为:___________________________________________。
(2)生物固氮:豆科植物根部的根瘤菌将N 转化为含氮化合物。
2
第1页(3)工业固氮:
N+3H 2NH ;
2 2 3
生成的氨气用以制取氨态氮肥或硝酸
2. 氮气
(1)物理性质:无色无味气体,密度比空气略小,难溶于水。
(2)化学性质
写出有关化学方程式:
①3Mg+N MgN;
2 3 2
②N+3H 2NH ;
2 2 3
③N+O 2NO。
2 2
核心知识点二:
二、一氧化氮和二氧化氮
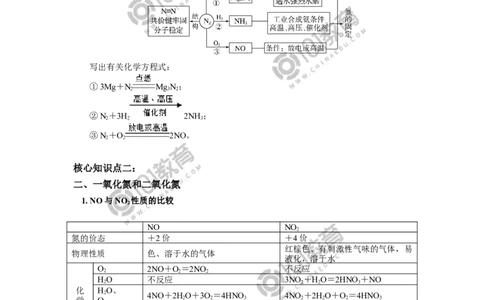
1. NO与NO 性质的比较
2
NO NO
2
氮的价态 +2价 +4价
红棕色、有刺激性气味的气体,易
物理性质 色、溶于水的气体
液化,溶于水
O 2NO+O=2NO 不反应
2 2 2
HO 不反应 3NO +HO=2HNO+NO
2 2 2 3
化 HO、
2 4NO+2HO+3O=4HNO 4NO +2HO+O=4HNO
学 O 2 2 3 2 2 2 3
2
性 有氧化性,但通常情况下表现出还 强氧化性,在溶液中能氧化S2-、
氧化性
质 原性 I-、Fe2+等离子
对环境
有毒,大气污染物之一 有毒,大气污染物之一
的影响
试剂 Cu和稀HNO Cu和浓HNO
3 3
制法
收集 通常用排水法收集 通常用向上排空气法收集
【注意】①验证某无色气体为NO的方法是向无色气体中通入O (或空气),无色气
2
体变为红棕色。
第2页2. 氮氧化物与O、HO的反应
2 2
①NO和O 通入水中
2
由 2NO+O =2NO 和 3NO +HO=2HNO +NO 得总反应为 4NO+3O +2HO=
2 2 2 2 3 2 2
4HNO
3
②NO 和O 混合气体通入水中
2 2
由 3NO +HO=2HNO +NO 和 2NO+O =2NO 得总反应为 4NO +O +2HO=
2 2 3 2 2 2 2 2
4HNO
3
核心知识点一:
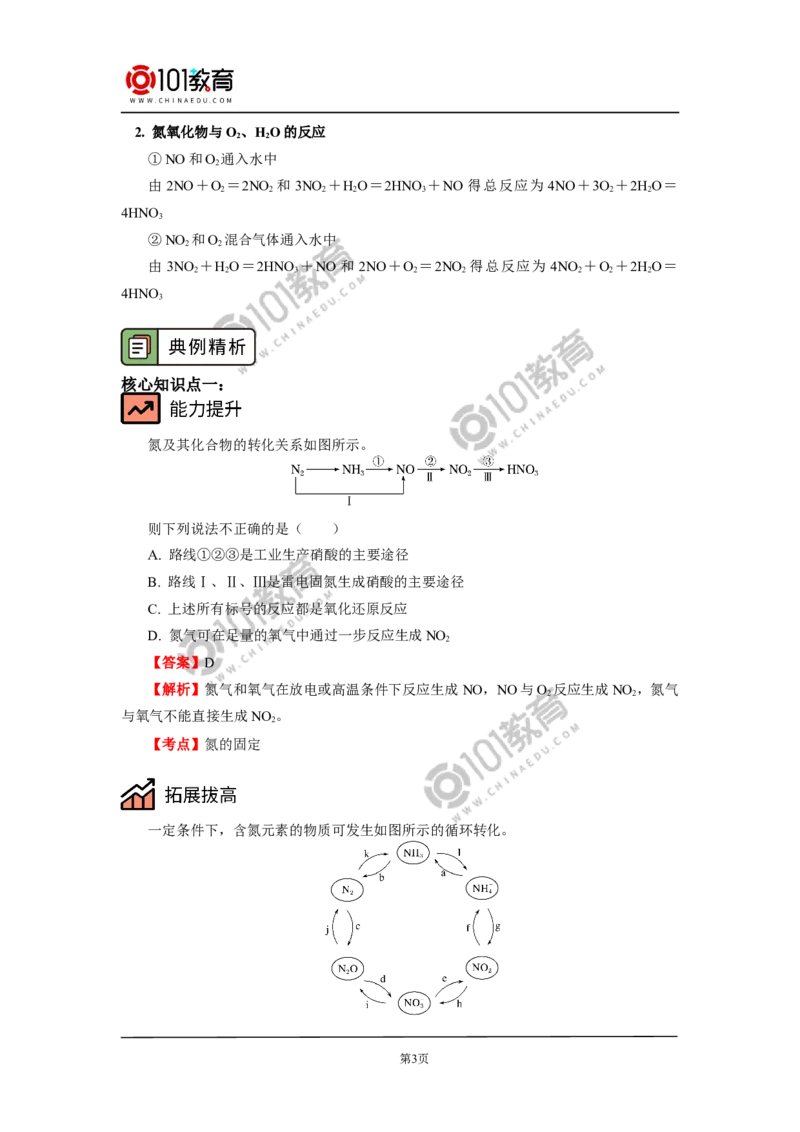
氮及其化合物的转化关系如图所示。
则下列说法不正确的是( )
A. 路线①②③是工业生产硝酸的主要途径
B. 路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径
C. 上述所有标号的反应都是氧化还原反应
D. 氮气可在足量的氧气中通过一步反应生成NO
2
【答案】D
【解析】氮气和氧气在放电或高温条件下反应生成NO,NO与O 反应生成NO ,氮气
2 2
与氧气不能直接生成NO 。
2
【考点】氮的固定
一定条件下,含氮元素的物质可发生如图所示的循环转化。
第3页回答下列问题:
(1)氮的原子结构示意图为______________。
(2)图中属于“氮的固定”的是__________(填字母,下同);转化过程中发生非氧
化还原反应的是________。
(3)若“反应h”是在NO 和HO的作用下实现,则该反应中氧化产物与还原产物的
2 2
物质的量之比为__________。
−
(4)若“反应i”是在酸性条件下由NO3 与Zn的作用实现,则该反应的离子方程式为
_________________。
【答案】(1) (2)k和c a和l (3)2∶1
−
(4)4Zn+2NO +10H+=4Zn2++NO↑+5HO
3 2 2
【解析】(1)N位于第二周期ⅤA族,其原子结构示意图为 。
(2)氮的固定是游离态的氮转化为化合态的氮,根据循环图可知,属于氮的固定的是
k和c;发生非氧化还原反应,说明反应前后各元素化合价没有发生变化,则属于非氧化还
原反应的是a和l。
(3)反应h的化学方程式为3NO +HO=2HNO +NO,HNO 是氧化产物,NO是还
2 2 3 3
原产物,因此氧化产物和还原产物的物质的量之比为2∶1。
−
(4)根据信息,Zn+H++NO3 ―→Zn2++NO↑+HO,根据电荷守恒、得失电子守
2 2
−
恒以及原子守恒得离子方程式为4Zn+2NO3 +10H+=4Zn2++NO↑+5HO。
2 2
【考点】氮气的固定
核心知识点二:
将盛有12 mL NO 和O 的混合气体的量筒倒立于水槽中,充分反应后,还剩余 2 mL
2 2
无色气体,则原混合气体中O 的体积和剩余的2 mL气体分别是( )
2
A. 1. 2 mL,NO B. 2. 4 mL,O
2
C. 3. 5 mL,O D. 4 mL,NO
2
【答案】A
【解析】解题依据的化学反应原理为
4NO +O+2HO=4HNO
2 2 2 3
3NO +HO=2HNO+NO
2 2 3
设O 的体积为x。剩余的气体有两种可能:
2
第4页1
4
①若剩O,则V =x- (12 mL-x)=2 mL,
2 剩
解得x=4 mL,选项B、C不正确。
1
3
②若剩NO,则V = [(12 mL-x)-4x]=2 mL,
剩
解得x=1. 2 mL,选项D不正确。
【考点】氮氧化合物与氧气反应计算
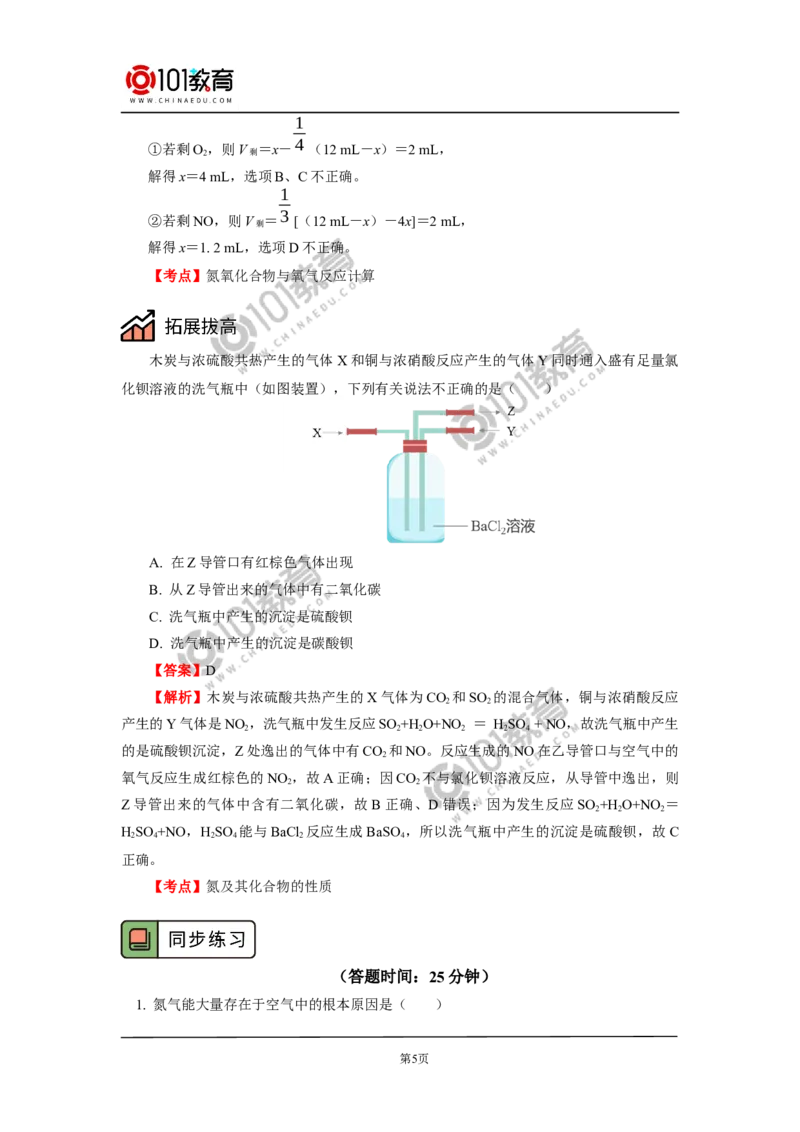
木炭与浓硫酸共热产生的气体X和铜与浓硝酸反应产生的气体Y同时通入盛有足量氯
化钡溶液的洗气瓶中(如图装置),下列有关说法不正确的是( )
A. 在Z导管口有红棕色气体出现
B. 从Z导管出来的气体中有二氧化碳
C. 洗气瓶中产生的沉淀是硫酸钡
D. 洗气瓶中产生的沉淀是碳酸钡
【答案】D
【解析】木炭与浓硫酸共热产生的X气体为CO 和SO 的混合气体,铜与浓硝酸反应
2 2
产生的Y气体是NO ,洗气瓶中发生反应SO +H O+NO = HSO + NO,故洗气瓶中产生
2 2 2 2 2 4
的是硫酸钡沉淀,Z处逸出的气体中有CO 和NO。反应生成的NO在乙导管口与空气中的
2
氧气反应生成红棕色的NO ,故A正确;因CO 不与氯化钡溶液反应,从导管中逸出,则
2 2
Z导管出来的气体中含有二氧化碳,故B正确、D错误;因为发生反应SO +H O+NO =
2 2 2
HSO +NO,HSO 能与BaCl 反应生成BaSO ,所以洗气瓶中产生的沉淀是硫酸钡,故C
2 4 2 4 2 4
正确。
【考点】氮及其化合物的性质
(答题时间:25分钟)
1. 氮气能大量存在于空气中的根本原因是( )
第5页A. 氮气性质稳定,即使在高温下也不与其他物质发生反应
B. 氮气比空气轻且不溶于水
C. 氮气分子中两个氮原子结合很牢固,分子结构稳定
D. 氮气既无氧化性,也无还原性,不与其他物质反应
2. 如图所示,集气瓶内充满某混合气体,将集气瓶置于光亮处,然后挤压胶头滴管使胶
头滴管内的水进入集气瓶,发现烧杯中的水会倒吸进入集气瓶,则集气瓶内的混合气体可
能是( )
①CO、O ②NO、O ③NO 、O ④N、H
2 2 2 2 2 2
A. ①② B. ②④
C. ③④ D. ②③
3. 下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
① ② ③
A. 由①中的红棕色气体,推断产生的气体一定是混合气体
B. 红棕色气体不能表明②中木炭与浓硝酸发生了反应
C. 由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D. ③的气体产物中检测出CO,由此说明木炭一定与浓硝酸发生了反应
2
4. 氮的某种氧化物和一氧化碳在催化剂的作用下充分反应,生成氮气和二氧化碳。若测
得氮气和二氧化碳的物质的量之比为1∶2,则这种氮的氧化物是( )
A. N O B. NO
2 2
C. NO D. N O
2 5
5. 如图所示,当向试管内通入21 mL O 时,最后试管中的液面仍在原来的位置,则原试
2
管中NO体积为( )
A. 6 mL B. 12 mL
C. 16 mL D. 18 mL
第6页6. 一定条件下,将等体积的NO和O 的混合气体置于试管中,并将试管倒立于水槽中,
2
充分反应后剩余气体的体积为原总体积的( )
1 3 1 3
4 4 8 8
A. B. C. D.
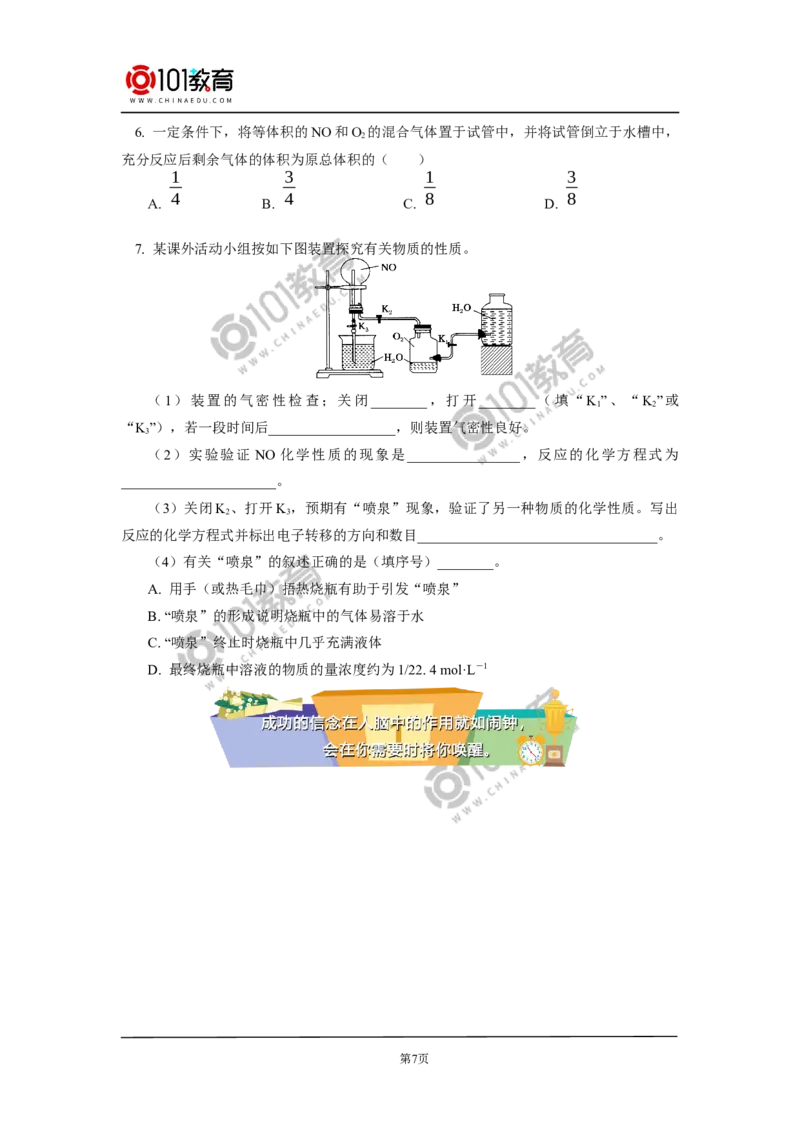
7. 某课外活动小组按如下图装置探究有关物质的性质。
(1)装置的气密性检查;关闭________,打开________(填“K”、“K”或
1 2
“K”),若一段时间后__________________,则装置气密性良好。
3
(2)实验验证 NO 化学性质的现象是________________,反应的化学方程式为
______________________。
(3)关闭K 、打开K ,预期有“喷泉”现象,验证了另一种物质的化学性质。写出
2 3
反应的化学方程式并标出电子转移的方向和数目__________________________________。
(4)有关“喷泉”的叙述正确的是(填序号)________。
A. 用手(或热毛巾)捂热烧瓶有助于引发“喷泉”
B. “喷泉”的形成说明烧瓶中的气体易溶于水
C. “喷泉”终止时烧瓶中几乎充满液体
D. 最终烧瓶中溶液的物质的量浓度约为1/22. 4 mol·L-1
第7页1.【答案】C
【解析】N 性质稳定,但高温下可与O 等物质发生反应,在反应中表现出氧化性或还
2 2
原性;氮气比空气轻且不溶于水并不是N 能大量存在于空气中的根本原因;N 能大量存在
2 2
于空气中的根本原因是氮气分子中两个氮原子结合很牢固,分子结构稳定。
2.【答案】D
【解析】①CO和O 在光照条件下不反应,且均难溶于水,不符合题意;②NO与O
2 2
可发生反应2NO+O =2NO 、3NO +HO=2HNO +NO,生成物易溶于水且气体分子数
2 2 2 2 3
减少,符合题意;③在O 存在的条件下,NO 可与水发生反应:4NO +O +2HO=
2 2 2 2 2
4HNO ,生成物溶于水且气体分子数减少,符合题意;④N 和H 在光照条件下不反应,
3 2 2
且均难溶于水,不符合题意。
3.【答案】D
【解析】①中灼热碎玻璃起加热作用,浓硝酸受热分解生成红棕色NO ,硝酸中氮元
2
素化合价降低,必有元素化合价升高,只能为氧元素,因此,还有O 生成,产生的气体为
2
混合气体,A项正确;由①可知,浓硝酸受热分解可生成红棕色气体,所以②中产生的
“红棕色气体”不一定是木炭与浓硝酸发生反应产生的,B项正确;③中浓硝酸挥发才能
与红热木炭接触,产生的NO 是还原产物,C项正确;红热的木炭还可与空气中的O 反应
2 2
生成CO,不一定是木炭与浓硝酸发生反应生成了CO,D项错误。
2 2
4.【答案】C
【解析】设这种氮的氧化物的化学式为NO,反应的化学方程式为2NO+2yCO=xN
x y x y 2
+2yCO,根据题意得x∶2y=1∶2,x∶y=1∶1。
2
5.【答案】B
【解析】此类题可用NO和O 溶于水的关系式:4NO+3O +2HO=4HNO 解题。当
2 2 2 3
V(NO)∶V(O )=4∶3时,混合气体完全与水反应,无气体剩余;当V(NO)∶V
2
(O)≠4∶3时,可能O 剩余或NO剩余。据题意可推知O 剩余,且剩余量与原NO体积
2 2 2
相同。设原试管中NO为x mL,则有4∶3=x∶(21-x),解得x=12。
6.【答案】C
【解析】NO、O 、HO之间的反应,先判断是否过量,若过量,找出剩余的气体,计
2 2
算其体积是多少,最后算出剩余气体的体积占原总体积的分数。由方程式 4NO+3O +
2
1 1
4 8
2HO=4HNO 计算,NO和O 等体积混合,剩余O 体积的 ,是原混合气体的 。
2 3 2 2
7.【答案】(1)K K、K 储气瓶中水面不再上升
3 1 2
(2)烧瓶中出现红棕色气体 2NO+O=2NO
2 2
第8页(3)
(4)A
【解析】(1)关闭K ,打开K 、K ,若装置气密性良好,则一段时间后储气瓶中水
3 1 2
面不再上升。
(2)本实验验证了2NO+O=2NO ,故烧瓶中应出现红棕色气体。
2 2
(3)“喷泉”现象表明烧瓶中形成负压,因而验证了NO 与水的反应:
2
(4)用手(或热毛巾等)捂热烧瓶,排出导管中的空气,使NO 与水接触起反应,烧
2
瓶中形成负压从而引发“喷泉”,A正确;B不正确,这里验证的是NO 与水的反应。C
2
不正确,由于K 关闭,由上述反应可知烧瓶中液体约为烧瓶容积的 2/3。D不正确,若实
2
验在标准状况下进行,且不考虑溶质的扩散,最终烧瓶中溶液的物质的量浓度约为1/22. 4
mol·L-1。
第9页