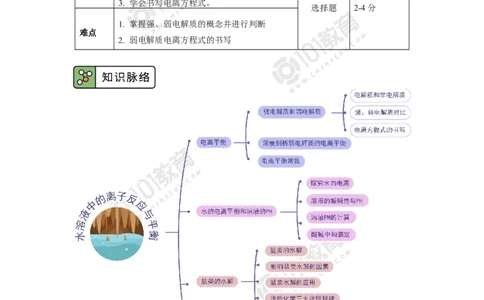
文档内容
强电解质和弱电解质
重难点 题型 分值
1. 掌握电解质和非电解质的概念
重点 2. 掌握强、弱电解质的概念
3. 学会书写电离方程式。
选择题 2-4分
1. 掌握强、弱电解质的概念并进行判断
难点
2. 弱电解质电离方程式的书写
一、强、弱电解质
1. 电解质和非电解质
第1页定义 物质类别 共同点
在水溶液中或熔融状态 酸、碱、盐、活泼金属的
电解质
下能够导电的化合物 氧化物、少数有机物、水
在水溶液中和熔融状态 均为化合物
大部分非金属氧化物、多
非电解质 下都不能够导电的化合
数有机物和氨气等
物
【求甚解】理解电解质的注意点
电解质在水溶液中或熔融状态下能导电的本质是化合物自身能够电离出自由移动的离
子。SO 、NH 等溶于水形成的溶液能导电,是因为它们与水反应生成的 HSO 、NH ·H O
3 3 2 4 3 2
等发生了电离,产生了能够自由移动的离子,而它们本身没有发生电离,故属于非电解质
NaO、CaO溶于水形成的溶液能导电,是因为它们与水反应生成的 NaOH、Ca(OH) 发
2 2
生了电离,产生了能够自由移动的离子,而它们本身也没有发生电离,不能就此说明NaO、
2
CaO是电解质,但二者在熔融状态下能发生电离产生自由移动的离子而导电,则可说明二
者是电解质。
【注意】理解电解质的注意点
(1)电解质与非电解质均属于化合物,单质和混合物既不是电解质也不是非电解质,
如铁和铜等单质、盐酸和NaCl溶液等混合物既不是电解质也不是非电解质。
(2)电解质电离而导电的条件是在水溶液中或熔融状态下,二者具备其一即可,如
HCl、HSO 等共价化合物只有在水溶液中电离而导电,NaO、CaO等活泼金属的氧化物只
2 4 2
有在熔融状态下电离而导电,NaCl、KSO 等可溶性的离子化合物在水溶液中和熔融状态
2 4
下均电离而导电,它们都是电解质。
2. 强电解质和弱电解质
(1)强、弱电解质的概念
定义 对应化合物类型 共同点
强电解质 在水溶液中能够全部电离的电解质 离子化合物、共价化合物 均属于化合
物
弱电解质 在水溶液中只有部分电离的电解质 共价化合物
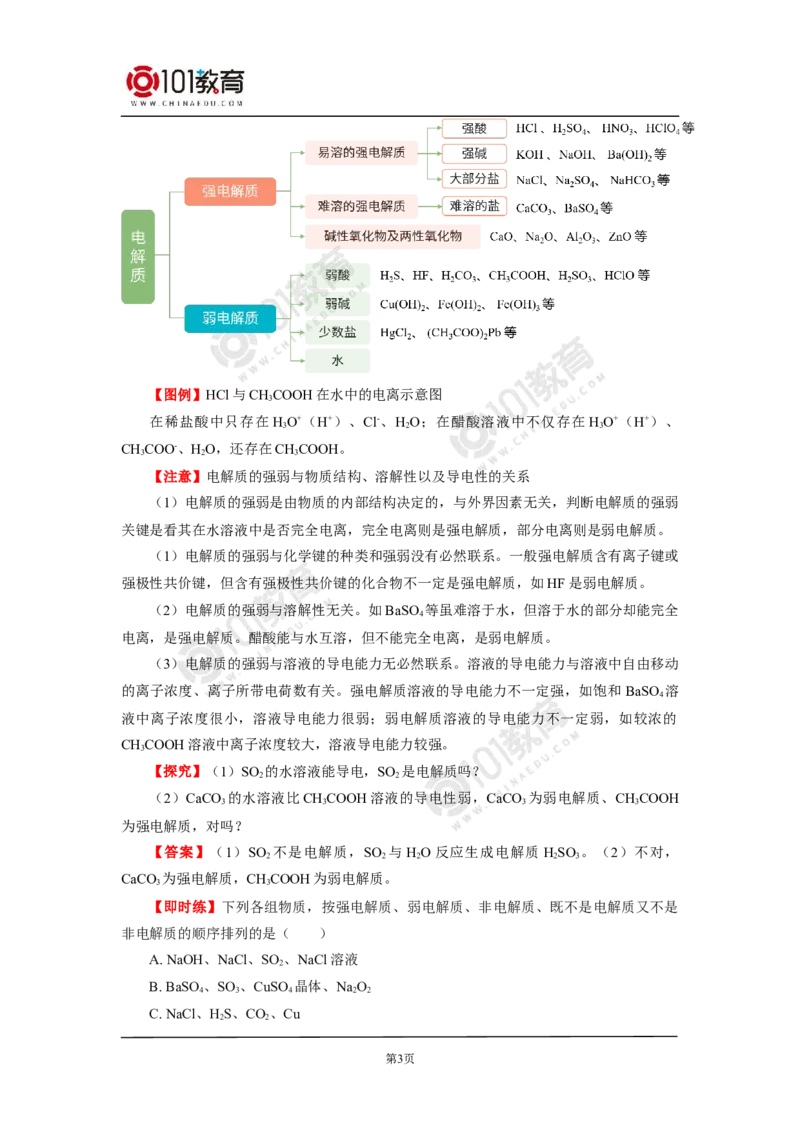
【举例】常见的强、弱电解质
第2页【图例】HCl与CHCOOH在水中的电离示意图
3
在稀盐酸中只存在HO+(H+)、Cl-、HO;在醋酸溶液中不仅存在 HO+(H+)、
3 2 3
CHCOO-、HO,还存在CHCOOH。
3 2 3
【注意】电解质的强弱与物质结构、溶解性以及导电性的关系
(1)电解质的强弱是由物质的内部结构决定的,与外界因素无关,判断电解质的强弱
关键是看其在水溶液中是否完全电离,完全电离则是强电解质,部分电离则是弱电解质。
(1)电解质的强弱与化学键的种类和强弱没有必然联系。一般强电解质含有离子键或
强极性共价键,但含有强极性共价键的化合物不一定是强电解质,如HF是弱电解质。
(2)电解质的强弱与溶解性无关。如BaSO 等虽难溶于水,但溶于水的部分却能完全
4
电离,是强电解质。醋酸能与水互溶,但不能完全电离,是弱电解质。
(3)电解质的强弱与溶液的导电能力无必然联系。溶液的导电能力与溶液中自由移动
的离子浓度、离子所带电荷数有关。强电解质溶液的导电能力不一定强,如饱和 BaSO 溶
4
液中离子浓度很小,溶液导电能力很弱;弱电解质溶液的导电能力不一定弱,如较浓的
CHCOOH溶液中离子浓度较大,溶液导电能力较强。
3
【探究】(1)SO 的水溶液能导电,SO 是电解质吗?
2 2
(2)CaCO 的水溶液比CHCOOH溶液的导电性弱,CaCO 为弱电解质、CHCOOH
3 3 3 3
为强电解质,对吗?
【答案】(1)SO 不是电解质,SO 与HO反应生成电解质 HSO 。(2)不对,
2 2 2 2 3
CaCO 为强电解质,CHCOOH为弱电解质。
3 3
【即时练】下列各组物质,按强电解质、弱电解质、非电解质、既不是电解质又不是
非电解质的顺序排列的是( )
A. NaOH、NaCl、SO 、NaCl溶液
2
B. BaSO 、SO 、CuSO 晶体、NaO
4 3 4 2 2
C. NaCl、HS、CO、Cu
2 2
第3页D. SO 、AgCl、NH ·H O、Ag
3 3 2
【答案】C
【解析】A中NaCl溶液是混合物,既不是电解质,又不是非电解质,NaCl是纯净物,
是强电解质;B中SO 为非电解质,CuSO 晶体、NaO 均为强电解质;D中SO 为非电解
3 4 2 2 3
质,AgCl为强电解质,NH ·H O为弱电解质。
3 2
(2)强、弱电解质比较
强电解质 弱电解质
化合物 离子化合物及具有强极性键的共
某些具有弱极性键的共价化合物
类型 价化合物(除HF)
电离程度 全部电离 部分电离
电离过程 不可逆过程 可逆过程,存在电离平衡
溶液中存在微
只有电离出的阴、阳离子,不存 既有电离出的阴、阳离子,又有
粒(水分子不
在电解质分子 电解质分子
计)
(3)强弱电解质的判断方法
①在相同浓度、相同温度下,比较导电能力的强弱。如同体积等浓度的盐酸和醋酸,
前者的导电能力强于后者。
②在相同浓度、相同温度下,比较反应速率的大小,如将足量的锌粒投入同体积等浓
度的盐酸和醋酸中,反应开始时前者产生气体的速率比后者的大。
③浓度与pH的关系。如0.1mol/LCH COOH,其pH>1,则证明CHCOOH是弱电解质。
3 3
④测定对应盐的酸碱性。如CHCOONa溶液呈碱性,则证明醋酸是弱酸。
3
⑤稀释前后pH的变化与稀释倍数的关系。如将pH=2的酸溶液稀释1000倍,若pH<
5,则证明该酸为弱酸;若pH=5,则证明该酸为强酸。
⑥采用实验证明溶液中存在电离平衡。如向醋酸中滴入紫色石蕊溶液,溶液变红,再
加CHCOONa,颜色变浅。
3
⑦利用较强酸(碱)制备较弱酸(碱)判断电解质强弱。如将CO 通入苯酚钠溶液中,
2
出现浑浊,说明酸性:HCO>苯酚
2 3
二、电离方程式的书写
1. 电离及电离方程式
电解质在水溶液中或熔融状态下产生自由移动的离子的过程叫做电离。电解质的电离
过程通常用电离方程式表示。
2. 电离方程式的书写
(1)强电解质完全电离,书写电离方程式时用“=”。
第4页如Ba(NO ) 的电离:Ba(NO ) = Ba2++2 NO -
3 2 3 2 3
(2)弱电解质部分电离,书写电离方程式时用“ ”。
①一元弱酸、弱碱一步电离。如CHCOOH CHCOO-+H+;NH ·HO NH + +
3 3 3 2 4
OH-。
②多元弱酸分步电离,且第一步电离程度远远大于第二步,必须分步写出电离方程式,
不可合并(其中以第一步电离为主)。
如HCO H++ HCO -(主),HCO - H++ CO2-(次)。
2 3 3 3 3
③多元弱碱分步电离(较复杂),在中学阶段要求一步写出电离方程式。
如Fe(OH) Fe3++3 OH-。
3
(3)酸式盐的电离方程式书写
①在水溶液中,强酸的酸式盐完全电离。如NaHSO=Na++ H++SO2-。
4 4
②在水溶液中,弱酸的酸式盐“强中有弱”。即酸式酸根离子不能完全电离,如
NaHCO =Na++ HCO -,HCO - H++ CO2-
3 3 3 3
【注意】(1)无论是强酸的酸式盐还是弱酸的酸式盐,在熔融状态下均完全电离出金
属阳离子与酸式酸根离子,如
NaHSO=Na+ + HSO -
4 4
NaHCO =Na++HCO-
3 3
(2)Al(OH) 是中学涉及的一种重要的两性氢氧化物,存在酸式电离和碱式电离。
3
酸式电离:Al(OH) H+ + AlO + H O;碱式电离:Al(OH) Al3+ + 3OH-。
3 2 2 3
例题1 下列说法正确的是( )
A. 强电解质溶液的导电能力一定比弱电解质溶液的导电能力强
B. 电解质一定属于纯净物
C. 强电解质都是离子化合物,弱电解质都是共价化合物
D. SO 、SO 的水溶液能导电,是电解质
3 2
【答案】B
【解析】溶液的导电能力与溶液中离子浓度的大小有关,与电解质强弱无关,故 A错
误;电解质强弱与化合物类型无关,共价化合物也可能是强电解质,如HCl等,故C错误;
SO 、SO 为非电解质,故D错误。
3 2
例题2 下列物质在水溶液中的电离方程式错误的是( )
第5页A. CaCO =Ca2+ + CO2-
3 3
B. NaHSO = Na+ + HSO -
4 4
C. HCO H+ + HCO -
2 3 3
D. NH ·H O NH ++ 3OH-
3 2 4
【答案】B
【解析】CaCO 是强电解质,溶于水的部分完全电离为Ca2+和CO2-,A项电离方程式
3 3
书写正确;NaHSO 是强酸的酸式盐,在水中完全电离为Na+、H+与SO 2-,B项电离方程式
4 4
书写错误;碳酸是二元弱酸,在水中分两步电离,且以第一步电离为主,C项电离方程式
书写正确;NH ·H O是一元弱成,在水溶液中存在电离平衡,D项电离方程式书写正确。
3 2
【方法总结】判断电离方程式书写是否正确需四看:一看“=”或“ ”使用是否正
确;二看电解质的电离是否正确,如多元弱酸、多元强酸以及弱酸的酸式盐在水溶液中的
电离;三看电解质电离生成的离子是否符合化学式的组成;四看离子符号与化学计量数是
否正确。
例题3 为证明醋酸是弱电解质,下列方法不正确的是( )
A. 比较相同物质的量浓度的NaOH溶液和醋酸溶液恰好反应完全时消耗两溶液的体积
B. 将1 mL pH=3 的醋酸溶液稀释到100mL,测其pH小于5
C. 比较浓度均为0.1mol·L的盐酸和醋酸溶液的导电能力
D. 测定0.1mol·L醋酸溶液的pH
【解析】恰好反应完全时,消耗醋酸溶液和NaOH溶液的体积相等,只能说明醋酸是
一元酸,不能说明醋酸是弱电解质,A错误;若醋酸为强电解质。稀释到100mL后溶液
pH应等于5,pH小于5则说明醋酸是弱电解质,B正确;若醋酸为强电解质,相同浓度的
盐酸和醋酸溶液导电能力相同,若醋酸的导电能力弱于盐酸,则说明醋酸是弱电解质,C
正确;若醋酸为强电解质,0.1mol·L醋酸溶液的pH=1,若pH>1,则说明醋酸是弱电解质,
D正确。
【答案】A
【点拨】判断弱电解质的关键点是证明该物质在水溶液中部分电离,可以从溶液的 pH、
导电能力、稀释后的pH变化情况等角度加以验证。
(答题时间:40分钟)
一、选择题
第6页1. 下列事实中能证明氯化氢是共价化合物的是( )
A. 氯化氢极易溶于水 B. 液态氯化氢不导电
C. 氯化氢不易分解 D. 氯化氢溶液可以电离
2. 下列电离方程式正确的是( )
3−
A. H PO 3H++PO4
3 4
2−
B. CaCO Ca2++CO3
3
C. NaHS Na++H++S2-
D. Fe(OH) Fe3++3OH-
3
*3. 下列叙述中正确的是( )
A. 氯化钠溶液中,氯化钠在电流的作用下电离成钠离子或氯离子
B. 溶于水后能电离出氢离子的化合物都是酸
C. 硫酸钡难溶于水,但硫酸钡是强电解质
D. SO 溶于水后部分电离,故二氧化硫属于弱电解质
2
4. 下列说法正确的是( )
2−
A. NaHSO 在熔融状态下的电离方程式为NaHSO=Na++H++SO4
4 4
B. HCO 是弱酸,故NaCO 是弱电解质
2 3 2 3
C. KClO 和SO 溶于水后能导电,故KClO 和SO 为电解质
3 3 3 3
− − 2−
D. NaHCO 在水溶液中的电离:NaHCO =Na++HCO3 、HCO3 H++CO3
3 3
5. 下列事实一定能说明HNO 为弱电解质的是( )
2
①常温下,NaNO 溶液的pH>7
2
②用HNO 溶液做导电实验灯泡很暗
2
③HNO 不能与NaCl反应
2
④常温下0.1mol-1L-1的HNO 溶液pH=2
2
⑤1LpH=1的HNO 溶液加水稀释至100L后溶液的pH=2.2
2
⑥1LpH=1的HNO 和1LpH=1的盐酸与足量的NaOH溶液完全反应,最终HNO 消耗
2 2
的NaOH溶液多
⑦HNO 溶液中加入一定量NaNO 晶体,溶液中c(OH-)增大
2 2
③HNO 溶液中加水稀释,溶液中c(OH-)增大
2
A. ①②③⑦ B. ①③④⑤
C. ①④⑤⑥⑦ D. ②④⑥⑧
二、非选择题
*6. 如图所示,烧杯中的溶液为2 mol·L-1CHCOOH溶液,接通直流电源,分别向烧杯
3
中加入下列物质(保持溶液温度不变),灯泡变暗的是( )
第7页A. 加入固体NaOH B. 加水稀释
C. 加入金属Na D. 通入HCl气体
7. 写出下列物质的电离方程式和反应的离子方程式。
(1)氢硫酸 。
(2)醋酸铵 。
(3)NaH PO 。
2 4
(4)明矾 。
(5)氯气溶于冷水 。
(6)氧化钠溶于稀硫酸 。
8. 有下列物质的溶液①CHCOOH ②HCl ③HSO ④NaHSO。
3 2 4 4
(1)若四种溶液的物质的量浓度相同,其c(H+)的大小比较为 (用序号表
示,下同)。
(2)若四种溶液的c(H+)相同,其物质的量浓度的大小比较为 。
*9. 下列物质中,A. KI(s) B. C HOH(l) C. Cl (g) D. CH COOH(l) E.
2 5 2 3
BaSO (s) F. NaHSO (s) G. 石墨(s) H. 蔗糖(s) I. NaOH(l)
4 4
(1)属于非电解质的是 ,属于强电解质的是 ,属于弱电解质的是
。
(2)能直接导电的是 ,能溶于水且水溶液能导电的是 。
第8页1.【答案】B
【解析】共价化合物液态时以分子形式存在,不能导电。
2.【答案】D
3.【答案】C
【解析】电解质电离不需电流作用,故A错;酸式盐如:NaHSO 也可电离出H+,故
4
−
B错;SO 溶于水并和水反应生成HSO ,HSO H++HSO3 可导电,故D错。
2 2 3 2 3
4.【答案】D
【解析】NaHSO 在熔融状态下电离出钠离子和硫酸氢根离子,正确的电离方程式为
4
−
NaHSO =Na++HSO4 ,故A错误;HCO 是弱酸,但是NaCO 在溶液中完全电离出钠离
4 2 3 2 3
子和碳酸根离子,NaCO 为强电解质,故B错误;SO 溶于水能够导电的离子是硫酸电离
2 3 3
的,不是SO 电离的,SO 为非电解质,故C错误;NaHCO 在水溶液中的电离方程式为
3 3 3
− − 2−
NaHCO =Na++HCO3 ,碳酸氢根离子在溶液中存在电离平衡:HCO3 H++CO3 ,
3
故D正确。
5.【答案】C
【解析】②如果盐酸(强酸)的浓度很小灯泡也很暗;④如果是强酸,pH=1;⑤如果
是强酸,加水稀释至100L后溶液的pH=3,实际pH=2.2,这说明HNO 溶液中存在HNO
2 2
H++NO-,是弱酸;⑥依据HNO+NaOH=NaNO +H O、HC1+NaOH=NaCl+H O可知,
2 2 2 2 2
c(HNO )大于c(HCl),而溶液中c (H+)相同,所以HNO 没有全部电离;⑦加入
2 2
NaNO ,溶液中c(OH一)增大,说明电离平衡移动;③不论是强酸还是弱酸,加水稀释,
2
溶液中c(H+)均减小,而c(OH-)增大。
6.【答案】B
【解析】A 项,加入固体 NaOH,会发生反应 CHCOOH+NaOH=CHCOONa+
3 3
HO,生成强电解质CHCOONa,导电能力增强,灯泡变亮;B项,加水稀释,溶液中的c
2 3
(H+)、c(CHCOO-)均减小,所以导电能力减弱,灯泡变暗;C项,加入金属Na,Na
3
与CHCOOH发生反应生成强电解质CHCOONa,导电能力增强,灯泡变亮;D项,HCl
3 3
是强电解质,通入HCl气体,导电能力增强,灯泡变亮。
7.【答案】(1)HS H++HS-
2
+
(2)CHCOONH=CHCOO-+NH4
3 4 3
− − 2− 2−
(3)NaH PO =Na++HPO4 、HPO4 H++HPO4 、HPO4 H++PO
2 4 2 2
3−
4
2−
(4)KAl(SO )=K++Al3++2SO4
4 2
(5)Cl+HO H++Cl-+HClO
2 2
第9页(6)NaO+2H+=2Na++HO
2 2
8.【答案】(1)③>②=④>① (2)①>②=④>③
【解析】②③④均为强电解质,能完全电离出H+,而①为弱电解质,部分电离出H
+。
9.【答案】(1)BH;AEFI;D;
(2)GI;ACDFI。
【解析】A. KI(s)是盐属于电解质,在水溶液中完全电离属于强电解质,但固体不
能电离出自由移动的离子不能导电,水溶液中能导电;
B. C HOH(l)属于有机物,是非电解质,不能导电;
2 5
C. Cl (g)是单质不是电解质,不能导电,水溶液中发生反应生成盐酸和次氯酸能导
2
电;
D. CH COOH(l)是弱酸属于电解质,溶液中操作电离平衡,属于弱电解质,纯净的
3
醋酸不能导电;水溶液中能导电;
E. BaSO (s)属于盐熔融状态完全电离属于强电解质,本身不导电,水溶液中不导电;
4
F. NaHSO (s)属于盐,是电解质,水溶液中完全电离属于强电解质,本身不导电,
4
水溶液中导电;
G. 石墨(s)属于非金属单质,不是电解质,固体能导电;
H. 蔗糖(s)属于有机物,是非电解质,不能导电;
I. NaOH(l)是强碱,是电解质,水溶液中完全电离. 属于强电解质,固体不导电,水
溶液中导电;
第10页深度剖析弱电解质的电离平衡
重难点 题型 分值
1. 理解弱电解质电离平衡
2. 掌握温度、浓度等条件对电离平衡的影
重点
响。
选择题 3-5分
3. 能应用电离平衡有关知识解决实际问题。
难点 掌握温度、浓度等条件对电离平衡的影响。
一、弱电解质的电离平衡
1. 电离平衡的建立
在一定条件下,电解质电离成离子的速率和离子结合成分子的速率相等时,电离过程
达到电离平衡状态。
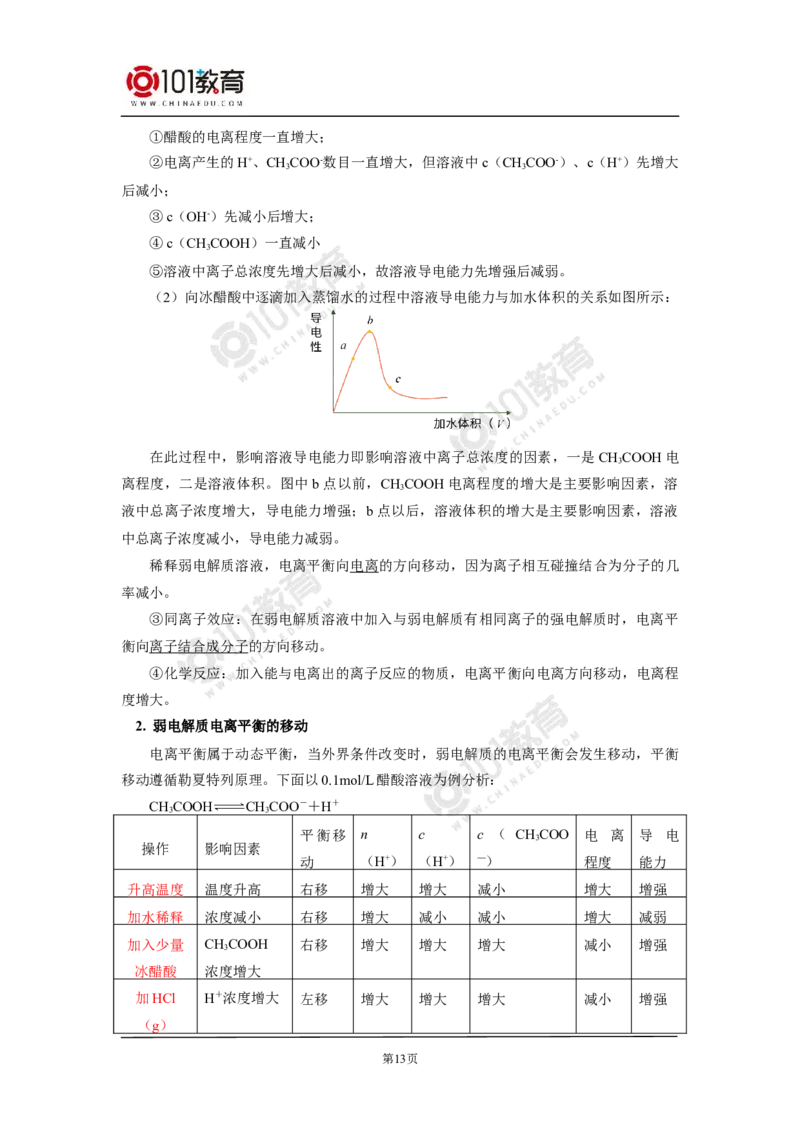
第11页如图所示:
2. 电离平衡的特征
弱电解质的电离平衡概括为六个字——弱、逆、等、动、定、变。具体为:
二、电离平衡的移动
1. 影响弱电解质电离平衡的因素
(1)内因:弱电解质本身的性质决定了其电离程度的大小,电解质越弱,电离程度越
小。
(2)外因
①温度:弱电解质的电离是吸热过程,所以升高温度,使电离平衡向电离的方向移动,
电离程度增大。
②浓度:用同一弱电解质配制溶液,增大溶液的浓度,电离平衡向电离方向移动,溶
液中离子的浓度增大,但电离程度减小;稀释溶液时,电离平衡向电离方向移动,电离程
度增大,但溶液中离子的浓度减小。
【易错】电离平衡向电离方向移动时,电解质分子的浓度不一定减小,电离程度也不
一定增大,比如稀醋酸中加入冰醋酸,c(CHCOOH)增大,电离程度减小。
3
【求甚解】在一定温度下,对于同一弱电解质来说,溶液越稀,离子相互碰撞结合成
分子的机会越小,弱电解质的电离程度越大,因此稀释溶液会使弱电解质向电离平衡方向
移动,电离程度增大。
【拓展】弱电解质溶液与稀释过程分析
(1)向冰醋酸中逐滴加入蒸馏水的过程中,各种变化如下:
第12页①醋酸的电离程度一直增大;
②电离产生的H+、CHCOO-数目一直增大,但溶液中c(CHCOO-)、c(H+)先增大
3 3
后减小;
③c(OH-)先减小后增大;
④c(CHCOOH)一直减小
3
⑤溶液中离子总浓度先增大后减小,故溶液导电能力先增强后减弱。
(2)向冰醋酸中逐滴加入蒸馏水的过程中溶液导电能力与加水体积的关系如图所示:
在此过程中,影响溶液导电能力即影响溶液中离子总浓度的因素,一是CHCOOH电
3
离程度,二是溶液体积。图中 b点以前,CHCOOH电离程度的增大是主要影响因素,溶
3
液中总离子浓度增大,导电能力增强;b点以后,溶液体积的增大是主要影响因素,溶液
中总离子浓度减小,导电能力减弱。
稀释弱电解质溶液,电离平衡向电离的方向移动,因为离子相互碰撞结合为分子的几
率减小。
③同离子效应:在弱电解质溶液中加入与弱电解质有相同离子的强电解质时,电离平
衡向离子结合成分子的方向移动。
④化学反应:加入能与电离出的离子反应的物质,电离平衡向电离方向移动,电离程
度增大。
2. 弱电解质电离平衡的移动
电离平衡属于动态平衡,当外界条件改变时,弱电解质的电离平衡会发生移动,平衡
移动遵循勒夏特列原理。下面以0.1mol/L醋酸溶液为例分析:
CHCOOH CHCOO-+H+
3 3
平衡移 n c c ( CHCOO 电 离 导 电
3
操作 影响因素
动 (H+) (H+) —) 程度 能力
升高温度 温度升高 右移 增大 增大 减小 增大 增强
加水稀释 浓度减小 右移 增大 减小 减小 增大 减弱
加入少量 CHCOOH 右移 增大 增大 增大 减小 增强
3
冰醋酸 浓度增大
加HCl H+浓度增大 左移 增大 增大 增大 减小 增强
(g)
第13页加NaOH H+浓度减小 右移 减小 减小 减小 增大 增强
(s)
加入镁粉 H+浓度减小 右移 减小 减小 增大 增大 增强
+
例题1 稀氨水中存在着平衡:NH ·H O NH4+OH-,若要使平衡向逆反应方向
3 2
移动,同时使c(OH-)增大,应加入的物质或采取的措施是( )
①NH Cl固体 ②硫酸 ③NaOH固体 ④水 ⑤加热 ⑥加入少量MgSO 固体
4 4
A. ①②③⑤ B. ③
C. ③④⑥ D. ③⑤
【答案】B
+
【解析】①若在氨水中加入NH Cl固体,c(NH4)增大,平衡向逆反应方向移动,c
4
(OH-)减小,错误;②硫酸中的H+与OH-反应,使c(OH-)减小,平衡向正反应方向
移动,错误;③当在氨水中加入NaOH固体后,c(OH-)增大,平衡向逆反应方向移动,
符合题意;④若在氨水中加入水,稀释溶液,平衡向正反应方向移动,但 c(OH-)减小,
错误;⑤电离属于吸热过程,加热平衡向正反应方向移动,c(OH-)增大,错误;⑥加入
MgSO 固体,MgSO 电离出的Mg2+与氨水中的OH-反应生成Mg(OH) 沉淀,使平衡向
4 4 2
正反应方向移动,且溶液中c(OH-)减小,错误。
例题2 将0.1 mol·L-1 HF溶液加水不断稀释,下列各量始终保持增大的是( )
A. c(H+) B. K(HF)
a
c(H+) c(F−)
c(HF) c(H+)
C. D.
【答案】C
【解析】因HF为弱酸,则浓度为0.1 mol·L-1 HF溶液加水不断稀释会促进HF的电离,
电离平衡正向移动,电离程度增大,n(H+)增大,但溶液体积也增大,且增大的程度大
于n(H+)增大的程度,所以c(H+)不断减小,A项错误;因电离常数只与温度有关,
c(F−)⋅c(H+)
c(HF)
则K(HF)在稀释过程中不变,B项错误;因K(HF)= ,当HF溶液加
a a
c(H+)
c(HF)
水不断稀释,c(F-)不断减小,K(HF)不变,则 增大,C项正确;刚开始稀释
a
时,电离产生等量的H+和F-,则两种离子的浓度比值可视为不变,但随着稀释的不断进
第14页行,由于水电离产生H+,则c(H+)不会低于10-7 mol·L-1,c(F-)不断减小,比值变
小,D项错误。
例题3 在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力 I随加入水的体积V
变化的曲线如图所示。请回答:
(1)“O”点导电能力为0的理由是_______________________________________。
(2)a、b、c三点处,溶液的c(H+)由小到大的顺序为___________________。
(3)a、b、c三点处,电离程度最大的是________。
(4)若将c点溶液中c(CHCOO-)增大,c(H+)减小,可采取的措施是
3
①_____________________________________________________________;
②_____________________________________________________________;
③_____________________________________________________________。
【答案】(1)在“O”点处醋酸未电离,无离子存在
(2)cH CO>HSO3 >HCO3 ,结合复分解反
a 2 3 2 3
2− 2−
应中强酸制弱酸的原理,HSO 与CO3 反应不可能生成HCO 和SO3 ,故B不合理。
2 3 2 3
3.【答案】D
【解析】二元酸(HA)在水中第一步电离为完全电离,则HA酸性较强,不是弱酸,
2 2
故A错误;加水稀释电离平衡正移,但氢离子浓度减小,所以稀释 0.1 mol·L-1HA溶液,
2
电离平衡向右移动,但是c(H+)减小,故B错误;二元酸(HA)在水中的电离方程式
2
为:HA=H++HA-,HA- H++A2-(K =1.0×10-2),第一步完全电离,第二步部
2 a2
(0.1+x)x
分电离,设电离的HA-为x,则有:K=
0.1−x
,解之得x=0.008 4。所以在0.1 mol·L
a
-1的HA溶液中,c(H+)=0.1 mol·L-1+0.008 4 mol/L=0.108 4 mol·L-1,故C错误;若
2
0.1 mol·L-1的NaHA溶液中c(H+)=0.02 mol·L-1,0.1 mol·L-1的HA溶液中存在HA=
2 2
H++HA-,HA-H++A2-,第一步电离出的氢离子,抑制了第二步电离,所以c(H+)
<0.12 mol·L-1,故D正确。
4.【答案】D
【解析】题中K为醋酸电离常数的表达式,由于电离常数不随浓度变化而变化,只随
温度变化而变化,所以排除A、B项;且醋酸的电离是吸热的,所以升高温度,K增大,
降低温度,K减小。标准状况下(0 ℃),温度低于25 ℃,则K小于1.75×10-5,所以C
项错误;正确答案为D项。
5.【答案】A
【解析】强酸能和弱酸盐反应生成弱酸,根据:NaCN+HNO =HCN+NaNO 、
2 2
NaCN+HF=HCN+NaF、NaNO +HF=HNO +NaF可知,亚硝酸的酸性大于氢氰酸,氢
2 2
氟酸的酸性大于亚硝酸,所以这三种酸的强弱顺序是:氢氟酸>亚硝酸>氢氰酸,因此HF
的电离常数是①,HNO 的电离常数是②,HCN的电离常数是③。
2
6.【答案】B
【解析】相同温度下,酸的电离常数越大,则酸的电离程度越大,酸的酸性越强,则
酸根离子水解程度越小,根据电离平衡常数知,这三种酸的强弱顺序是 HZ>HY>HX,故
A错误;由A知,HZ的酸性大于HY,根据强酸制取弱酸知,HZ+Y-=HY+Z-能发生,
故B正确;根据电离平衡常数知,这三种酸的强弱顺序是HZ>HY>HX,均属于弱酸,故
第18页C错误;相同温度下,同一物质的电离平衡常数不变,故D错误。
7.【答案】D
−
【解析】依据电离常数分析可知酸性由强至弱为HCO>HClO>HCO3 ,根据强酸可以
2 3
−
制取弱酸分析,A项与HClO>HCO3 矛盾,错误;B项与HCO>HClO矛盾,错误;C项
2 3
− −
与HClO>HCO3 矛盾,反应应该生成碳酸氢钠,错误;D项与HCO>HClO>HCO3 吻合,
2 3
正确。
8.【答案】0.1 mol·L-1 1.96×10-5 变大 变小 不变
【解析】开始时c(CHCOOH)=0.1 mol·L-1,由于CHCOOH电离的很少,平衡后
3 3
可认为c(CHCOOH)仍为0.1 mol·L-1。由CHCOOH CHCOO-+H+
3 3 3
c(CH
3
COO−)⋅c(H+) 1.4×10−3 ×1.4×10−3
c(CH COOH) 0.1
K= 3 ≈ =1.96×10-5。
a
第19页电离平衡常数
重难点 题型 分值
1. 电离平衡常数的概念、表达式
重点 2. 电离平衡常数的特点
3. 电离平衡常数的应用
选择题 3-5分
1. 电离平衡常数的应用
难点
2. 电离平衡常数的特点
一、电离平衡常数的概念
在一定条件下,当弱电解质的电离达到电离平衡时,该弱电解质在溶液中电离生成的
各种离子浓度的乘积与未电离的该弱电解质分子的浓度的比值是个常数,这个常数叫做电
离平衡常数,简称电离常数,用K来表示(一般弱酸的电离常数用K 表示,弱碱的电离常
a
数用K 表示)。
b
第20页如:CHCOOH H++CH COO-
3 3
c(H+)⋅c(CH COO−)
3
c(CH COOH)
K= 3
a
二、电离平衡常数的表示方法
1. 一元弱酸 HA 的电离常数:根据电离方程式 HA H++A-,可表示为 K =
a
c(A−)⋅c(H+)
c(HA)
。
2. 多元弱酸的电离常数
多元弱酸的电离是分步进行的,每步均有电离常数,通常用K 、 K 、K 等表示。
a1 a2 a3
如HSO 是二元弱酸,发生分步电离:HSO H++ HSO -、HSO - H++ SO 2-,则
2 3 2 3 3 3 3
第一步和第二步电离常数分别为K 。
a1=
【注意】(1)两步电离常数表达式不能合并书写,将HSO 的电离常数表达式写成
2 3
是不正确的。
(2)在运用电离常数表达式进行计算时,表达式中各粒子浓度必须是平衡时的浓度。
3. 一元弱碱BOH的电离常数:根据电离方程式BOH B++OH-,可表示为K =。
b
c(B+)⋅c(OH−)
c(BOH)
。
三、电离平衡常数的特点
(1)电离平衡常数与温度有关,与浓度无关,升高温度,K值增大。电离平衡常数同
化学平衡常数一样,只与温度有关,而不受溶液中粒子浓度的影响,由于电离过程是吸热
的,因此电离常数随着温度的升高而增大。
利用这一性质可以利用K判断微粒浓度比值的变化。加水稀释弱电解质溶液时,能促
进其电离,溶液中离子和分子的浓度会发生相应的变化,但电离平衡常数不变,题目中经
常利用电离常数不变这一特点来判断溶液中某些微粒浓度比值的变化情况。
如 将 0.1mol/LCH COOH 溶 液 加 水 稀 释 时 , 溶 液 中
3
,稀释过程中,c(H+)减小,K 值不变,
a
则 的值变大
(2)K可以用于衡量弱电解质电离的难易程度。在相同条件下,K值越大,表示该弱
第21页电解质越易电离,所对应的酸性或碱性相对越强。
例如,在25 ℃时,K(HNO )=4.6×10-4,K(CHCOOH)=1.8×10-5,因而HNO
2 3 2
的酸性比CHCOOH强。
3
(3)多元弱酸的各级电离常数的大小关系为K K K ……,因此多元弱酸的酸性主
1 2 3
要由第一步电离决定。
≫ ≫
【想一想】
HS的电离平衡常数K =1.3×10-7,K =7.1×10-15,它的K 、K 差别很大的原因
2 a1 a2 a1 a2
____________(从电离平衡的角度解释)。
【答案】第一步电离产生的H+对第二步的电离起抑制作用
四、多元弱酸溶液中的离子浓度关系
25 ℃时,HPO 分三步电离,第一步最强(K =7.1×10-3),第二步较弱(K =6.3×10-
3 4 1 2
8),第三步最弱(K =4.2×10-13),可知HPO 溶液中c(H+)>c(HPO -)>c(HPO 2-)>c
3 3 4 2 4 4
(P O 3-)>c(OH-)。
4
HS分两步电离,第一步强(K =1.3×10-7),第二步弱(K =7.1×10-15),可知HS溶
2 1 2 2
液中c(H+)>c(HS-)>c(S2-)>c(OH-)。
1. K只与温度有关,与浓度无关,升高温度,K值增大。利用这一性质可以利用K判断
微粒浓度比值的变化。
2. K可以用于衡量弱电解质电离的难易程度。在相同条件下,K值越大,表示该弱电解
质越易电离,所对应的酸性或碱性相对越强。
3. K可以用于判断弱酸酸性的相对强弱,进而判断某些有酸参加的复分解反应能否发生,
一般符合“强酸制弱酸”规律。
例题1 已知下面三个数据:7.2×10-4、4.6×10-4、4.9×10-10分别是三种酸的电离平衡
常数,已知这些酸可发生如下反应:①NaCN+HNO =HCN+NaNO ②NaCN+HF=
2 2
HCN+NaF ③NaNO +HF=HNO+NaF。由此可判断下列叙述中不正确的是( )
2 2
A. K(HF)=7.2×10-4
a
B. K(HNO)=4.9×10-10
a 2
C. 根据①③两个反应即可得出一元弱酸的强弱顺序:HF>HNO>HCN
2
第22页D. K(HCN)<K(HNO)<K(HF)
a a 2 a
【答案】B
【解析】相同温度下,酸的电离常数越大,该酸的酸性越强,较强酸和较弱酸反应能
生成较弱酸,根据:① NaCN+HNO =HCN+NaNO ② NaCN+HF=HCN+NaF
2 2
③NaNO +HF=HNO +NaF,可知HNO 的酸性强于HCN,HF的酸性强于HNO ,故这
2 2 2 2
三种酸的酸性强弱顺序是HF>HNO >HCN。通过以上分析知,HF的酸性最强,所以HF
2
的电离平衡常数最大,为 7.2×10-4,A正确;HNO 的酸性强于HCN而弱于HF,所以
2
HNO 的电离平衡常数为4.6×10-4,B错误;根据较强酸制较弱酸的原理,由反应①可知酸
2
性:HNO >HCN,由反应③可知酸性:HF>HNO ,故通过这两个反应就可以知道三种酸
2 2
的性对强弱,C正确;HNO 的酸性强于HCN但弱于HF,所以HNO 的电离平衡常数比
2 2
HCN大比HF小,D正确。
例题2 硼酸(HBO)溶液中存在:HBO(aq)+HO(l) [B(OH)]-(aq)
3 3 3 3 2 4
+H+(aq)。下列说法正确的是( )
化学式 电离常数(298 K)
硼酸 K=5.7×10-10
K =4.4×10-7
1
碳酸
K =4.7×10-11
2
醋酸 K=1.75×10-5
A. 等pH的碳酸溶液和醋酸溶液比较,物质的量浓度:前者>后者
B. 等物质的量浓度的碳酸溶液和硼酸溶液比较,pH:前者>后者
C. 将一滴碳酸钠溶液滴入硼酸溶液中一定能观察到有气泡产生
D. 将一滴醋酸溶液滴入碳酸钠溶液中一定能观察到有气泡产生
【答案】A
【解析】弱酸的电离常数越大,其酸性相对越强,根据电离常数可知,酸性强弱顺序:
CHCOOH>HCO >HBO >HCO -。醋酸的电离能力强于碳酸,等pH的碳酸溶液和
3 2 3 3 3 3
醋酸溶液,碳酸溶液的物质的量浓度大于醋酸溶液,A正确;碳酸的电离能力强于硼酸,
则等物质的量浓度的碳酸溶液和硼酸溶液,碳酸溶液的酸性更强,pH更小,B错误;根据
酸性强弱顺序和较强酸制较弱酸原理可知,硼酸与碳酸钠反应的产物是碳酸氢钠而不是碳
酸,所以观察不到气泡产生,C错误;醋酸溶液与碳酸钠溶液反应先生成碳酸氢钠,碳酸
钠完全转化为碳酸氢钠后,碳酸氢钠再与醋酸反应生成二氧化碳,醋酸少量,观察不到气
泡产生,D错误。
第23页例题3 电离平衡常数是衡量弱电解质电离程度的物理量。
Ⅰ. 已知:
化学式 电离常数(25℃)
HCN K=6.2×10-10
CHCOOH K=1.75×10--5
3
HCO K=4.5×10-7、K=4.7×10-11
2 3 1 2
(1)向NaCN溶液中通入少量的CO,发生反应的化学方程式为____________。
2
Ⅱ. 常温下有0.1mol·L-1的以下几种溶液,①HSO 溶液 ②NaHSO 溶液
2 4 4
③CHCOOH溶液 ④盐酸 ⑤HCN溶液 ⑥NH ·H O,其中如下几种溶液中溶质的电离
3 3 2
度如表(已知HSO 的第一步电离是完全的),回答下列问题:
2 4
③醋酸溶液
①HSO 溶液 ②NaHSO 溶液 ④盐酸
2 4 4
− 2− − 2− CH 3 COOH H++
HSO4 H++SO4 HSO4 H++SO4 HCl=H++Cl-
CHCOO-
3
10% 29% 1.33% 100%
(2)常温下,c(H+)相同的上述溶液,其物质的量浓度由大到小的顺序是
_________(填序号)
【答案】
Ⅰ.(1)NaCN+HO+CO=HCN+NaHCO
2 2 3
Ⅱ.(2)③>②>④>①
【解析】Ⅰ.(1)根据电离平衡常数大小可知酸性:HCO >HCN>HCO -,向NaCN
2 3 3
溶 液 中 通 入 少 量 CO , 反 应 生 成 HCN 和 NaHCO , 反 应 的 化 学 方 程 式 为
2 3
NaCN+HO+CO=HCN+NaHCO 。
2 2 3
Ⅱ.(2)等pH的酸溶液,酸的电离程度越大,则其物质的量浓度越小,根据表中数据
可知,电离程度大小为③>②>④,且由于HSO 的第一步电离是完全的,则四种溶液的
2 4
物质的量浓度由大到小的顺序为③>②>④>①。
(答题时间:40分钟)
1. 下列说法正确的是( )
A. 电离平衡常数受溶液浓度的影响
B. 电离平衡常数可以表示弱电解质的相对强弱
C. 电离常数大的酸溶液中c(H+)一定比电离常数小的酸中大
第24页c(H+)⋅c(CO2−)
3
c(H CO )
D. H CO 的电离常数表达式:K= 2 3
2 3
*2. 下表是常温下某些一元弱酸的电离常数:
弱酸 HCN HF CHCOOH HNO
3 2
电离常数 6.2×10-10 6.8×10-4 1.8×10-5 6.4×10-6
则0.1 mol·L-1的下列溶液中,c(H+)最大的是( )
A. HCN B. HF
C. CHCOOH D. HNO
3 2
3. 常温下,将0.1 mo1·L-1的醋酸溶液加水稀释至原来体积的10倍,下列有关叙述正确
的是( )
A. CH COOH的电离平衡常数增大为原来的10倍
3
B. CHCOO-与CHCOOH的浓度之比增大为原来的10倍
3 3
C. CHCOO-与H+的浓度之积减小为原来的0.1
3
D. CHCOOH与CHCOO-的浓度之和减小为原来的0.1
3 3
*4. 某温度下,等体积、c(H+)相同的盐酸和醋酸溶液分别加水稀释,溶液中的 c(H
+)随溶液体积变化的曲线如图所示。据图判断下列说法正确的是( )
A. 曲线Ⅱ表示的是盐酸的变化曲线
B. b点溶液的导电性比c点溶液的导电性强
C. 取等体积的a点、b点对应的溶液,消耗的NaOH的量相同
D. b点酸的总浓度大于a点酸的总浓度
5. 由表格中的电离常数判断可以发生的反应是( )
化学式 电离常数
HClO K=3×10-8
K =4.4×10-7
1
HCO
2 3
K =4.7×10-11
2
A.NaClO+NaHCO =HClO+NaCO
3 2 3
B. 2HClO+NaCO=2NaClO+CO↑+HO
2 3 2 2
C. 2NaClO+CO+HO=2HClO+NaCO
2 2 2 3
D. NaClO+CO+HO=HClO+NaHCO
2 2 3
第25页二、非选择题
*6. 将6 g CH COOH溶于水制成1 L溶液,此溶液的物质的量浓度为________,经测定
3
某温度时,溶液中c(CHCOO-)为1.4×10-3 mol·L-1,此温度下醋酸的电离常数 K =
3 a
________,温度升高,K 将________(填“变大”“不变”或“变小”,下同),加入少
a
量CHCOONa后c(H+)________________________,K________。
3 a
7. 根据题意完成下列问题。
(1)将等质量的锌粉分别投入10 mL 0.1 mol·L-1盐酸和10 mL 0.1 mol·L-1 CHCOOH
3
溶液中。
①若锌不足量,反应快的是________。
②若锌过量,产生氢气的量的关系为________。
(2)将等量的锌粉分别投入c(H+)均为1 mol·L-1、体积均为10 mL的盐酸和醋酸
溶液中。
①若锌不足量,反应快的是________。
②若锌过量,产生氢气的量的关系为________。
第26页1.【答案】B
2.【答案】B
【解析】一元弱酸的电离常数越大,电离程度越大,同浓度时,电离产生的 c(H+)
越大。
3.【答案】D
【解析】电离平衡常数只受温度的影响,温度不变,则平衡常数不变,故 A错误;加
1
c(H+)⋅c(CH COO−)
3
10 c(CH COOH)
水稀释促进电离,则溶液总H+的浓度大于原来的 ,由K= 3 不变
可知,CHCOO-与CHCOOH的浓度之比小于原来的10倍,故B错误;加水稀释时,醋
3 3
c(H+)⋅c(CH COO−)
3
c(CH COOH)
酸进一步电离,则CHCOOH浓度小于原来的0.1,由K= 3 不变可
3
知,CHCOO-与H+的浓度之积小于原来的0.1,故C错误;由物料守恒可知,CHCOOH
3 3
与CHCOO-的浓度之和减小为原来的0.1,故D正确。
3
4.【答案】B
【解析】醋酸属于弱电解质,在稀释时会电离出H+,故稀释相同倍数时醋酸溶液中c
(H+)的变化要比盐酸中c(H+)的变化小一些,即曲线Ⅰ表示盐酸,曲线Ⅱ表示醋酸,
A项错误;溶液的导电性与溶液中离子的浓度有关,离子浓度b>c,故导电性也是b>c,B
项正确;a点、b点表示溶液稀释相同倍数,溶质的量没有发生变化,都等于稀释前的物质
的量,稀释前两溶液中 c(H+)相同,但 CHCOOH 为弱酸,则 c(CHCOOH)>c
3 3
(HCl),故稀释前n(CHCOOH)>n(HCl),即CHCOOH消耗NaOH多,C项错误;
3 3
a点酸的总浓度大于b点酸的总浓度,D项错误。
5.【答案】D
−
【解析】依据电离常数分析可知酸性由强至弱为HCO>HClO>HCO3 ,根据强酸可以
2 3
−
制取弱酸分析,A项与HClO>HCO3 矛盾,错误;B项与HCO>HClO矛盾,错误;C项
2 3
− −
与HClO>HCO3 矛盾,反应应该生成碳酸氢钠,错误;D项与HCO>HClO>HCO3 吻合,
2 3
正确。
6.【答案】0.1 mol·L-1 1.96×10-5 变大 变小 不变
【解析】开始时c(CHCOOH)=0.1 mol·L-1,由于CHCOOH电离的很少,平衡后
3 3
可认为c(CHCOOH)仍为0.1 mol·L-1。由CHCOOH CHCOO-+H+
3 3 3
c(CH
3
COO−)⋅c(H+) 1.4×10−3 ×1.4×10−3
c(CH COOH) 0.1
K= 3 ≈ =1.96×10-5。
a
7.【答案】(1)①盐酸 ②相等
第27页(2)①CHCOOH ②CHCOOH与锌反应产生的氢气多
3 3
【解析】(1)两种一元酸溶质的物质的量相等,但盐酸中c(H+)大,故盐酸与锌反
应的速率大;由于金属均过量,酸全部消耗掉,故正确的答案是产生氢气的量相等。
(2)这两种酸的c(H+)相等,显然后者的物质的量浓度大,溶质的物质的量也大,
初始的速率相同,但随着反应的进行,H+不断被消耗,弱酸CHCOOH的电离平衡不断向
3
正向移动,又电离出H+,故在反应进行的同一时刻CHCOOH溶液中的c(H+)大于盐酸
3
溶液中的c(H+),所以醋酸与锌反应速率大。当锌过量时CHCOOH与锌反应产生的氢
3
气多。
第28页