文档内容
教材习题答案
专题 1 揭示物质结构的奥秘 接近但没有必然关系 错误 质子和电子带相反电荷 中子
ꎬB ꎻ ꎬ
不带电 正确 科学家已经研究发现更小的微粒 如夸克
ꎬC ꎻ ꎬ ꎬD
第一单元 物质结构研究的内容 错误
ꎮ
2D 这种碳纤维的组成元素为碳 熔点高 不可能是高分子化
理解应用 . ꎬ ꎬ
合物 错误
1 A 物质的结构决定物质的性质 物质的性质反映物质的结 ꎬD ꎮ
. ꎬ 3A 运用激光光谱技术可观测化学反应时分子中原子的运动
构 项正确 物质的结构还包括物质的手性等 项错误 物 . ꎬ
ꎬA ꎻ ꎬB ꎻ 化学反应中最小微粒是原子 无法观察到原子中原子核的内
质的结构不随人们的认识和研究的发展而发生变化 项错 ꎬ
ꎬC 部结构
误 从微观上讲 物质可以是由分子 原子 离子等构成的 ꎮ
ꎻ ꎬ 、 、 ꎬD 4D
项错误 .
ꎮ 5略
2C 熔融 能导电是由于有自由移动的 + - 错误 .
. NaCl Na 、Cl ꎬC ꎮ 6答案 元素 氢原子中只含有一个质子和一个电子 所以最
3D 14 与12 最外层电子数相同 化学性质相似 项错误 . H ꎻ ꎬ
. C C ꎬ ꎬA ꎻ 先产生的元素为
14 的中子数为 14 的中子数为 项错误 同素异形体的 Hꎮ
C 8ꎬ N 7ꎬB ꎻ 7略
研究对象为单质 项错误 14 与12 质子数相同 中子数不 .
同 互为同位素 ꎬC 项正确 ꎻ C C ꎬ 专题2 原子结构与元素性质
ꎬ ꎬD ꎮ
4D 和苯为非极性分子 根据相似相溶规则可知二者相溶
. C60 ꎬ ꎮ
5答案 利用化学反应的原理 通过化学反应实现物质的转 第一单元 原子核外电子的运动
. (1) ꎬ
化 制备人类生活和生产所需要的各种材料 是化学服务于人
ꎬ ꎬ 理解应用
类的重要方式
ꎮ 1B 电子层和形状均相同的原子轨道具有相同的能量 即
利用化学反应实现物质转化 制备人类生活和生产所需要 . ꎬ 3px=
(2) ꎬ 错误
的物质 需要化学家们建立精确有效而又普遍适用的化学反 3py=3pzꎬB ꎮ
ꎬ 2C 第 周期元素中 原子轨道处于半满状态时 含有的未成
应的量子力学理论 . 4 ꎬ ꎬ
ꎮ 对电子数最多 即外围电子排布式为 5 1 则含有的未成对
化学发展的趋势是让反应条件趋向于温和 产率高 速率 ꎬ 3d 4s ꎬ
(3) 、 、 电子数最多为
快 副反应少 污染少 价格低 生产流程简单等 6ꎮ
、 、 、 、 ꎮ 3C
6略 .
. 4C 2-最外层 个电子 电子排布式为 2 2 6 2 6
. S 8 ꎬ 1s 2s 2p 3s 3p ꎬC
错误
第二单元 物质结构研究的范式与方法 ꎮ
5C +电子排布式为 2 2 6 错误 2+电子排布式为
. Na 1s 2s 2p ꎬA ꎻMg
理解应用 2 2 6 错误 -电子排布式为 2 2 6 2 6 10 2 6
1s2s2p ꎬB ꎻBr 1s2s2p 3s3p 3d 4s4p ꎬ
1B 假说是以客观事实材料和科学理论为依据 对所研究的事 错误
. ꎬ D ꎮ
物或现象所提出的一种推测性说明 错误 正确 假说不是 6D 该元素原子中共有 个电子 正确 该原子
ꎬA 、B ꎻ . 2+8+13+2=25 ꎬA ꎻ
幻想 是以客观事实材料和科学理论为依据的 错误 并不
ꎬ ꎬC ꎻ
是所有假说都可以变成科学理论 错误
结构示意图为 有 个电子层 正确 由电子排
ꎬD ꎮ
ꎬ 4 ꎬB ꎻ
2A
.
3D 为微观结构模型
布式可知 最外层有 个电子 正确 该原子 电子层共有
. A、B、C ꎮ
ꎬ 2 ꎬC ꎻ M
4略 5略
. . 个电子 错误
2+6+5=13 ꎬD ꎮ
7D 该基态原子的电子排布式为 2 2 6 2 6 10 2 1
第三单元 物质结构研究的意义 . 1s 2s 2p 3s 3p 3d 4s 4p ꎬ
则第 电子层的电子数为 正确
3 2+6+10=18ꎬD ꎮ
理解应用 8D 项 为 位于第 族 为 位于 族 错误
. A ꎬX Beꎬ ⅡA ꎬY Heꎬ 0 ꎬ ꎻB
1D 理论研究在化学学科中越来越重要 但化学仍然是一门以 项 为 原子 为 + 性质不同 错误 项 的核外电
. ꎬ ꎬX Ne ꎬY Na ꎬ ꎬ ꎻC ꎬX
实验为基础的科学 错误 子排布式可能为 2 2 1 或 2 2 5 可能是 或 元素
ꎬD ꎮ 1s 2s 2p 1s 2s 2p ꎬ B F ꎬY
2略 的核外电子排布式为 2 1 或 2 5 可能为 或
. [Ne]3s 3p [Ne]3s 3p ꎬ Al
3答案 正如人的左右手不能完全重合一样 一对手性异构 元素 则 元素不一定属于同族元素 错误 项 的核
. (1) ꎬ Cl ꎬ X、Y ꎬ ꎻD ꎬX
体在空间上也不能完全重合 因此人们把手性催化合成又称 外电子排布式为 2 2 4 为 元素 的核外电子排布式为
ꎬ 1s 2s 2p ꎬ O ꎬY
为不对称催化合成 2 2 6 2 4 为 元素 和 元素均位于第 族 性质
ꎮ 1s 2s 2p 3s 3p ꎬ S ꎬO S ⅥA ꎬ
手性分子的特殊结构决定了它的特殊性质 一对手性异构 相似 正确
(2) ꎬ ꎬ ꎮ
体 在医药领域 其中的一个可能有疗效 而另一个可能无疗 9答案
ꎬ ꎬ ꎬ . (1)↑↓ ↑↓ ↑↓↑ ↑
效甚至有害 因此 如何合成手性分子的单一光学异构体就
ꎮ ꎬ 1s 2s 2p
成为化学研究领域的热门话题 同时也是化学家面临的巨大
ꎬ (2)↑↓ ↑↓ ↑↓↑↓↑↓ ↑↓ ↑
挑战 1s 2s 2p 3s 3p
ꎮ
4略 (3)↑↓ ↑↓ ↑↓↑↓↑↓ ↑↓ ↑ ↑ ↑
.
综合评价 1s 2s 2p 3s 3p
1C 1 中没有中子 错误 多数原子的中子数和质子数比较 (4)↑↓ ↑↓ ↑ ↑
. 1H ꎬA ꎻ 1s 2s 2p
1
10答案 但 为共价化合物 原子的电子排布式分别为 1
. 1.7ꎬ HF ꎬH、F 1s 、
2 2 5 均差一个电子形成稳定结构 则两原子间形成共
外围电子 1s 2s 2p ꎬ ꎬ
微粒符号 原子序数 电子排布式 价键
排布式 ꎮ
7答案
. (1)C、N、O、Na
2 2 6 2 2 2 2
Si 14 1s 2s 2p 3s 3p 3s 3p (2) ∶ N⋮⋮N ∶
2+ 2 2 6 2 6 (3)O>N>C>Na
Ca 20 1s 2s 2p 3s 3p —
2- 2 2 6 2 6
(4)H2O>NH3
S 16 1s 2s 2p 3s 3p — 综合评价
Zn 30 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 3d 10 4s 2 1 . D A 项 ꎬBr -与 Ar 原子核外电子排布不同 ꎬ 错误 ꎻB 项 ꎬNa + 、
2+ 2 2 6 2 6 6 6 2-核外电子排布均与 相同 错误 项 + -核外电子排
Fe 26 1s 2s 2p 3s 3p 3d 3d O Ne ꎬ ꎻC ꎬK 、Cl
布均与 相同 错误 项 +核外电子排布与 相同 -核
11答案 Ar ꎬ ꎻD ꎬK Ar ꎬF
. K、Cr、Cu 外电子排布与 相同 正确
解析 第四周期元素原子中最外层电子数为 的外围电子 Ne ꎬ ꎮ
1 2C 2-核外电子排布式为 2 2 6 2 6
排布式为 1 5 1 10 1 对应的元素分别为 . S 1s 2s 2p 3s 3p ꎮ
4s 、3d 4s 、3d 4s ꎬ K、Cr、Cuꎮ 3D 项 违背了能量最低原理 应为 10 1 错误 项 违背
. A ꎬ ꎬ 3d 4s ꎬ ꎻB ꎬ
第二单元 元素性质的递变规律 了能量最低原理 应为 5 1 错误 项 违背了能量最低原
ꎬ 3d 4s ꎬ ꎻC ꎬ
理 应先排 再排 应为 8 2 错误
理解应用 ꎬ 4s 3dꎬ 3d 4s ꎬ ꎮ
4C 同主族元素从上到下 金属性增强 第一电离能减小 即
1C 位于同一周期 位于同一主族 原子半径 . ꎬ ꎬ ꎬ
. Na、S ꎬO、S ꎬ Na>S> 错误
正确 元素的非金属性越强 其气态氢化物的稳定性越 K>CsꎬC ꎮ
OꎬA ꎻ ꎬ 5C 由I I I 较小 I 剧增可知 该元素易失去 个电子 即
强 非金属性 则热稳定性 正确 核 . 1、 2、 3 ꎬ 4 ꎬ 3 ꎬ
ꎬ O>S>Pꎬ PH3<H2S<H2OꎬB ꎻ 最外层有
3
个电子
ꎬ
该元素位于
ⅢA
族
ꎮ
外电子层结构相同的离子 核电荷数越大 离子半径越小 则
ꎬ ꎬ ꎬ 6答案
离子半径 + 2+ 3+ 错误 同一周期元素的第一电离 . (1)↑↓ ↑ ↑ ↑
Na >Mg >Al ꎬC ꎻ 2s 2p
能随原子序数的增大而呈增大的趋势 正确
ꎬD ꎮ (2)↑↓ ↑↓↑↓↑
2C 依题意 在元素周期表中相对位置大致为
. ꎬA、B、C、D : 3s 3p
第二周期 (3)↑↓ ↑↓↑ ↑
cC dD 2s 2p
第三周期 bB aA (4)↑↓
3s
说明 与 同周期 与 同周期 且 处于 的下一
A B ꎬC D ꎬ A、B C、D (5)↑↓ ↑
周期 所以 原子半径 原子序数 a b d c 电子层
ꎬ ꎬ :B>A>C>Dꎬ : > > > ꎻ 7答案 3s 3p 违反洪特规则
结构相同 随原子序数增大 离子半径依次减小 离子半径 . (1)BꎬA ꎮ
ꎬ ꎬ ꎬ : 违反能量最低原理
3- - + 2+ 根据同周期主族元素从左到右电负性逐渐增 (2)AꎬB ꎮ
C >D >B >A ꎻ 忽略了能量相同的原子轨道在半充满状态时 体系的
大 同主族元素从上到下电负性逐渐减小 可知元素的电负 (3)AꎬB ꎬ
ꎬ ꎬ 能量较低
性 正确 ꎮ
:D>C>A>BꎻC ꎮ 8答案 2 2 6 2 6 2 2
3B 第一电离能为 n 2n 3 n 2n 4 选项中第一电离能由小到 . (1)Ti 1s 2s 2p 3s 3p 3d 4s
. s p > s p ꎬ
2 2 6 2 6 5 2
大的顺序为 2 4 2 3 2 5 2 6 即最小的为 (2)Mn 1s 2s 2p 3s 3p 3d 4s
2s 2p <2s 2p <2s 2p <2s 2p ꎬ 9答案 2 2 6 2 6 10 2 1 第 周期 族
2 4 正确 . (1)1s 2s 2p 3s 3p 3d 4s 4p 4 ⅢA
2s 2p ꎬB ꎮ
4B 2 为 2 2 为 二者性质不同 错误 层上仅 (2)Ga2O3 GaCl3
. 1s Heꎬ1s 2s Beꎬ ꎬA ꎻM 10答案
有 个电子的 为 元素 层上有 个电子的 为 元 . (1)3 (2)0 (3)2 (4)6
5 X P ꎬN 5 Y As 11答案
素 最外层电子数相同的同主族元素 性质相似 正确 轨 .
ꎬ ꎬ ꎬB ꎻ2p
道只有一个未成对电子的 为 或 轨道上只有一个未 元素
X B Fꎬ3p Na Mg Si P
成对电子的 为 或 性质不一定相似 错误 最外层都 最高正化合价
Y Al Clꎬ ꎬC ꎻ +1 +2 +4 +5
只有一个电子的 原子 可能为 等 化学性
X、Y ꎬ H、Na、K、Cr、Cu ꎬ 氯化物类型
质不一定相似 错误
ꎬD ꎮ 离子化合 离子 离子 共价 共价
5答案 (
. (1)Na Ar 物 共价化 化合物 化合物 化合物 化合物
/
(2)F Cs 合物
和 和 )
(3)As Cr Mn K、Cu Cr Ti
6 . 答案 (1) 氖原子的电子排布式为 1s 2 2s 2 2p 6 ꎬ 达稳定结构 ꎬ 难 专题3 微粒间作用力与物质性质
失电子 所以在同周期中第一电离能最大 磷原子的电子
ꎬ ꎮ (2)
排布式为 2 3 轨道处于半充满状态 是相对稳定的
[Ne]3s 3p ꎬ3p ꎬ 第一单元 金属键 金属晶体
结构 故磷的第一电离能比硫的第一电离能大 原子
ꎬ ꎮ (3)Mg
的电子排布式为 2 2 6 2 失去 个电子成为 2+后 理解应用
1s 2s 2p 3s ꎬ 2 Mg ꎬ1s、
轨道处于全满状态 处于全空状态 是相对稳定的结 1C 金属键无饱和性和方向性 错误 常温下为液态 熔
2s、2p ꎬ3s ꎬ . ꎬA ꎻHg ꎬ
构 的电负性分别为 电负性之差 则形 点低 错误 金属原子脱落下来的价电子形成遍布整块晶体
ꎮ (4)K、F 0.8、4.0ꎬ >1.7ꎬ ꎬB ꎻ
成离子键 的电负性分别为 虽然电负性之差 的 电子气 被所有原子所共用 正确 自由电子把能量传
ꎻH、F 2.1、4.0ꎬ > “ ”ꎬ ꎬC ꎻ
2
教材习题答案
递给金属离子 从而使整块金属达到同样的温度 错误
ꎬ ꎬD ꎮ + 2- +
2A 金属键的形成是通过金属阳离子与自由电子间强烈的相 (3)Na [O] Na
.
互作用 故 正确 解析 是由 +和 -构成的离子化合物 -中
ꎬ A ꎮ (1)NaOH Na OH ꎬOH
3答案 金属晶体中存在着许多自由电子 在外加电场作用下 原子以共价键相结合 为离子化合物 由 2+
. ꎬ H、O ꎮ (2)CaCl2 ꎬ Ca
自由电子定向移动形成电流 而具有导电性 金属晶体中 自 和 -通过离子键结合 是由 + 2-构成的 存在
ꎬ ꎻ ꎬ Cl ꎮ (3)Na2O Na 、O ꎬ
由电子运动时 把能量从温度高的部分传到温度低的部分 因 离子键
ꎬ ꎬ ꎮ
而具有导热性 金属晶体中 金属阳离子与自由电子之间的相 7答案
ꎻ ꎬ . NaCl>KCl>RbCl
互作用没有方向性 原子层滑动时仍能保持这种相互作用 在 解析 离子化合物的熔点与其晶格能有关 晶格能与离子半
ꎬ ꎬ ꎬ
外力的作用下 发生形变 但不会断裂 因而具有延展性 径 所带电荷有关 这几种物质都是离子晶体 阴离子相同 它
ꎬ ꎬ ꎬ ꎮ 、 ꎬ ꎬ ꎬ
4答案 由于 位于同一主族 它们都形成 价离子 们的阳离子半径依次增大 阳离子所带电荷相同 则晶格能依
. K、Na、Li ꎬ +1 ꎬ ꎬ ꎬ
金属离子所带电荷数相同 但由于它们的半径逐渐减小 静电 次减小 其熔点依次降低
ꎬ ꎬ ꎬ ꎮ
8答案
作用不断增强 故金属键不断增强 金属单质的熔点逐渐
ꎬ ꎬ
. XY3Z
升高 解析 晶胞中 位于顶点 个数为 1 位于棱心 个
ꎮ ꎬX ꎬ 8× =1ꎬY ꎬ
5答案 的金属键强于 8
. (1)Cu Kꎮ
原子外围电子排布 原子半径 数为 1 位于体心 个数为 则该化合物的化学式
(2) 、 ꎮ 12× =3ꎬZ ꎬ 1ꎬ
6答案 无 4
. (1)1 ∶ 4 ∶ 2 (2) (3)3 ∶ 1 为
XY3Zꎮ
解析 图 晶胞内金属原子数 1 9答案
(1) aꎬ =8× =1ꎮ . 6 2
8 解析 根据不同位置的微粒的共用情况可知 在晶胞的棱
ꎬA
图 晶胞内金属原子数 1 1 心上 在晶胞的顶点上 晶体中与一个 相紧邻的 有
bꎬ =8× +6× =4ꎮ ꎬB ꎬ B A 6
8 2 个 分别位于 的前 后 左 右 上 下且距离相等 与一个
ꎬ B 、 、 、 、 、 ꎬ A
图 晶胞内金属原子数 1 相紧邻的 有 个 在一条棱上
cꎬ =8× +1=2ꎮ B 2 ꎬ ꎮ
8 10答案
由于金属晶体中的自由电子不属于某个固定原子 而是在 . (1)4 (2)+3
(2) ꎬ 解析 因为晶胞为长方体 所以处于 个面心的 2- 有
整个晶体中自由移动 故自由电子无确切的堆积方式 (1) ꎬ 6 C2 2
ꎬ ꎮ 个距离比另外 个的远 所以 个 2+周围距离最近的 2-
4 ꎬ 1 Ca C2
1 1 数目为
(3)Cu:6× =3ꎬAu:8× =1ꎮ
4ꎮ
2 8
7略 1
. (2)R:8× +1=2ꎻ
8
第二单元 离子键 离子晶体
1 1 1
G:8× +8× +4× +2=8ꎻ
4 4 2
理解应用
1
1C 号 和 号 之间易形成共价键 故 错误 号 和 Q:8× +2=4ꎻ
. 6 C 1 H ꎬ A ꎻ2 He 4
号 之间不形成化学键 故 错误 号 和 号 之间 个数比为 化学式为 由于 为
8 O ꎬ B ꎻ9 F 11 Na R、G、Q 1 ∶ 4 ∶ 2ꎬ RQ2G4ꎬ R +2
易形成离子键 故 正确 号 和 号 之间易形成共价 价 为 价 则 为 价
ꎬ C ꎻ8 O 14 Si ꎬG -2 ꎬ Q +3 ꎮ
键 故 错误
ꎬ D ꎮ
2A 离子化合物中可能含有共价键 如 故 正确 错 第三单元 共价键 共价晶体
. ꎬ NaOHꎬ A 、C
误 共价化合物中一定不含离子键 故 错误 非金属元素的 理解应用
ꎻ ꎬ B ꎻ
原子之间也可能形成离子键 如 故 错误 1A 中只有 键和 键 含有 键而不含
3C 中分别为 二者不
ꎬ
能形
NH
成
4C
离
lꎬ
子化
D
合物
ꎮ
中分别为
.
键 故
CH3C
选
H3
中含
C—C
键 含
C
有
—H
键
ꎬ
和 键
σ
故 不选
π
. A C、Oꎬ ꎻB ꎬ A ꎻN2 NN ꎬ σ π ꎬ B ꎻ
二者不能形成离子化合物 中分别为 可形成 中含有 键和 键 含有 键和 键 故 不选
S、Oꎬ ꎻC Mg、Fꎬ C2H2 C—H CC ꎬ σ π ꎬ C ꎻ
中分别为 二者不能形成离子化合物 中含 键 含有 键和 键 故 不选
MgF2ꎻD Mg、Alꎬ ꎮ CO2 CO ꎬ σ π ꎬ D ꎮ
4B 设每个 -周围最近距离的 2+数目为x 则 2D H 反应物总键能 生成物总键能
. F Ca ꎬ : . Δ = - =(946+436×3-391×
n 2+ n - x 解得x -1 -1 故选
(Ca ) ∶ (F )=1 ∶ 2= ∶ 8ꎬ =4ꎮ 6)kJmol =-92 kJmol ꎬ Dꎮ
3B 氮化硼超硬 耐磨 耐高温 说明它是共价晶体 为分
5B 晶胞中阴 阳离子数之比为 1 1 . 、 、 ꎬ ꎮ C60
. A 、 1 ∶ (8× +6× )= 1 ∶ 4ꎬ 子晶体 金刚石为共价晶体 故 不选 碳化硅 水晶都是共价
8 2 ꎬ ꎬ A ꎻ 、
化合物为 故错误 晶胞中阴 阳离子数之比为 晶体 故 选 水银和铝均为金属 故 不选 硝酸钠为离子晶
M4Nꎬ ꎻB 、 1 ∶ (4× ꎬ B ꎻ ꎬ C ꎻ
体 晶体硅为共价晶体 故 不选
1 化合物为 故正确 晶胞中阴 阳离子数之 ꎬ ꎬ D ꎮ
)=2 ∶ 1ꎬ MN2ꎬ ꎻC 、 4D 双键 三键中都含有 键 其中双键中含有一个 键 三
8 . 、 π ꎬ π ꎬ
键中含有 个 键 正确 原子轨道重叠越多 电子在核间
比为 1 化合物为 故错误 晶胞中 2 π ꎬA ꎻ ꎬ
1 ∶ (3× )= 8 ∶ 3ꎬ M3N8ꎬ ꎻD 出现的概率就越大 所形成的共价键就越牢固 正确 每个
8 ꎬ ꎬB ꎻ
原子所能提供的未成对电子的数目是一定的 共价键的形成
阴 阳离子数之比为 1 化学式为 故 ꎬ
、 1 ∶ (8× )= 1 ∶ 1ꎬ MNꎬ 过程中一个原子含有几个未成对电子 通常就能与几个其他
8 ꎬ
错误 原子的未成对电子配对成共价键 所以与其配对的原子个数
ꎮ ꎬ
也一定 这是共价键的饱和性 正确 轨道的形状是球形对
6答案 + - - 2+ - ꎬ ꎬC ꎻs
. (1)Na [OH] (2)[Cl] Ca [Cl] 称的 它无方向性 错误
ꎬ ꎬD ꎮ
3
5答案 12答案
. (1)1 2 . (1)AgF>AgCl>AgBr>AgI
断开 分子的第一个化学键所需的能量 +
(2)CO CO [(1 072- (2)Cu
-1 -1 比断开 分子中的第一个化
学
74
键
5)
所
kJ
需
的
mo
能
l
量
=327 kJmol ]
-1
N2
-1 小 可 第四单元 分子间作用力 分子晶体
[(946-418)kJmol =528 kJmol ] ꎬ
知 相对更活泼 理解应用
CO
6答案 最外层只有一个电子 它形成稳定结构还需要一 1C 和 为离子晶体 熔点高低与离子键的强弱有关
. (1)H ꎬ . MgO NaCl ꎬ ꎬ
个电子 两个 原子各提供一个电子形成共用电子对而分别 符合题意
ꎬ H C ꎮ
达到稳定结构 所以两个 原子能结合成 原子最外层 2B 硫化钾属于离子晶体 由阴 阳离子通过离子键结合 故
ꎬ H H2ꎬHe
. ꎬ 、 ꎬ A
有 个电子 达到了稳定结构 不需要共用电子 所以两个
正确 干冰属于分子晶体 构成微粒为分子 晶体中微粒间通
2 ꎬ ꎬ ꎬ He
ꎻ ꎬ ꎬ
原子不能结合成 原子最外层只有一个电子 氯原
过范德华力结合 故 错误 金刚石属于共价晶体 构成微粒
He2ꎮ (2)H ꎬ
ꎬ B ꎻ ꎬ
子最外层有 个电子 二者各提供一个电子形成共用电子对
为原子 晶体中微粒间通过共价键结合 故 正确 属于分
7 ꎬ ꎬ
二者都达到稳定结构 所以只能形成 分子
ꎬ ꎬ C ꎻI2
子晶体 分子间通过范德华力结合 故 正确
ꎬ HCl ꎮ
ꎬ ꎬ D ꎮ
7答案 3 . A 水是共价分子 ꎬ 分子间存在范德华力 ꎬ 同时水分子之间还
. (1)BrBr (2)ClPCl (3)HOH 有氢键 所以玻璃态水中也存在范德华力与氢键 故 正确
ꎬ ꎬ A 、C
Cl 错误 玻璃态水是由液态水急速冷却到 时形成的 所以
ꎻ 160 K ꎬ
熔点应该是 而不是 故 错误 玻璃态水无固定形
H 160Kꎬ 0℃ꎬ B ꎻ
状 不存在晶体结构 所以不是分子晶体 故 错误
(4) ∶ N⋮⋮N ∶ (5)HCH ꎬ ꎬ ꎬ D ꎮ
4C 氢键属于分子间作用力 错误 分子内氢键使物质的熔
H . ꎬA ꎻ
解析 溴单质中原子之间形成 对共用电子对 点 沸点降低 错误 溶于水后 分子中的氮原子可
(1) 1 ꎮ (2)PCl3 、 ꎬB ꎻNH3 ꎬNH3
中存在 个 键 原子最外层的 个电子分别与氯原子 以和水分子中的氢原子之间形成氢键 正确 邻羟基苯甲醛
3 P—Cl ꎬP 3 ꎬC ꎻ
形成共用电子对 还有一对孤电子对 水中存在两个氢氧 存在分子内氢键 而对羟基苯甲醛存在分子间氢键 故对羟基
ꎬ ꎮ (3) ꎬ ꎬ
键 氧原子最外层达到 电子稳定结构 个氮原子间形 苯甲醛的熔点高于邻羟基苯甲醛 错误
ꎬ 8 ꎮ (4)2 ꎬD ꎮ
成 对共用电子对 中 原子最外层有 个电子 分 5B 中物质都是离子晶体 阴离子相同 阳离子所带电荷相
3 ꎮ (5)CH4 C 4 ꎬ . A ꎬ ꎬ
别与氢原子形成共用电子对 同 阳离子半径依次减小 则熔点依次升高 故 错误 中物
ꎮ ꎬ ꎬ ꎬ A ꎻB
8答案 的化学式为 的化学式为 的形 质都属于分子晶体且都不含氢键 其相对分子质量依次减小
. YX2 CO2ꎬZX2 SO2ꎬCH4 ꎬ ꎬ
则熔点依次减小 故 正确 水中含有氢键 熔点最高 相对分
H ꎬ B ꎻ ꎬ ꎬ
成过程为 C+4H →H C HꎬH2S 的形成过程为 H+ 子 错 质 误 量 :H2 中 Se 物 >H 质 2S 均 ꎬ 所 为 以 共 熔 价晶 点 体 高低 键 顺 长 序为 H2O>H2Se>H2Sꎬ 所 故
C ꎻD ꎬ C—C<C—Si<Si—Siꎬ
H 以熔点 晶体硅 金刚石 故 错误
: <SiC< ꎬ D ꎮ
S +H →H S Hꎮ 6 . 答案 (1) 离子半径 Mg 2+ <O 2- <K + <Cl - ꎬ 离子所带电荷数 K + =
解析 元素的原子核内有 个质子 故 为 而 与 同 - 2- 2+ 离子晶体的离子半径越小 所带电荷越多 晶
Z 16 ꎬ Z Sꎬ X Z Cl <O =Mg ꎬ ꎬ ꎬ
一主族且为短周期元素 故 为 则 为 与 在 格能越大 则晶体的熔 沸点越高 因此熔 沸点
ꎬ X Oꎬ ZX2 SO2ꎬX Y ꎬ 、 ꎬ 、 MgO<KClꎮ
同一周期 故 核外有 个电子层 且 元素原子最外层电子 的热稳定性依次减弱是因为
ꎬ Y 2 ꎬ Y (2)HF、HCl、HBr、HI H—F、H—Cl、
数是 层所能容纳的电子数的 倍 的最外层有 个电子 的键能逐渐减小 金属键逐渐增强 四
K 2 ꎬY 4 ꎬ H—Br、H—I ꎮ (3) ꎮ (4)
故为 为 种晶体都为分子晶体 组成和结构相似 相对分子质量越大
CꎬYX2 CO2ꎮ ꎬ ꎬ ꎬ
9答案 热稳定性顺序为 分子越稳定 越难分 分子间作用力越大 则 的熔 沸点逐渐升高
. HF>H2O>NH3ꎮ 、 ꎬ F2、Cl2、Br2、I2 、 ꎮ
解 在 时约有 分解 在 时约有 7答案 都是稀有气体 随着相对分子质量的增大 分子间作用
ꎬNH3 300 ℃ 9.7% ꎬH2O 2 000 ℃ . ꎬ ꎬ
分解 在 时仍不分解 说明氢化物分解由易到 力逐渐增大 故熔 沸点逐渐升高 它们与水分子间的作用力
4% ꎬHF 3000 ℃ ꎬ ꎬ 、 ꎻ
难的顺序是 化合物中键能越大 断键所需要的 也逐渐增大 故在水中的溶解度也逐渐增大
NH3<H2O<HFꎬ ꎬ ꎬ ꎮ
能量越高 则越难分解 氢化物分子的分解由易到难的顺序是 8答案 水分子间形成氢键 组成和结构相似的分子
ꎬ ꎬ . (1) ꎮ (2)
则键能由小到大的顺序是 所以 晶体 相对分子质量越大 熔 沸点越高 酒精与水都是极
NH3、H2O、HFꎬ NH3<H2O<HFꎬ ꎬ ꎬ 、 ꎮ (3)
氢化物热稳定性顺序是 性分子 并且酒精与水分子间还可以形成氢键 冰中的氢
NH3<H2O<HFꎮ ꎬ ꎮ (4)
10答案 + + + + 键比液态水中的多 使得水分子很规则地排列 造成体积膨
. NH4、H3O F2、H2 NH3、NH4、H2O、H3O O—H> ꎬ ꎬ
胀 密度变小 低级醇分子间一般可形成氢键
N—H ꎬ ꎮ (5) ꎮ
解析 + 中 提供孤电子对 +提供空轨道 二者能形成 9答案 晶体类型不同 晶体中微粒间的作用力不同
NH4 N ꎬH ꎬ . (1) ꎬ ꎮ
配位键
ꎬH3O
+中
O
提供孤电子对
ꎬH
+提供空轨道
ꎬ
二者能形
(2)
成配位键 其余物质不含配位键 一般情况下 同种元素原
晶体
ꎬ ꎮ ꎬ 金属晶体 离子晶体 共价晶体 分子晶体
子之间形成非极性共价键 不同种元素原子之间形成极性共 类型
ꎬ
价键 所以含有非极性键的微粒有 含有极性键的微粒
ꎬ F2、H2ꎻ 构成 金属离子
有 NH3、NH + 4、H2O、H3O + ꎻ 形成共价键的元素电负性相差越 微粒 自由电子 、 阴 、 阳离子 原子 分子
大 其键的极性越强 的电负性大小为 所以极性键
ꎬ ꎬN、O O>Nꎬ 结 分子间作用
由强到弱的顺序为
O—H>N—Hꎮ 构 微粒 肯定有离子 力 ꎬ 可能有分
11答案 晶体硬度大 共价晶体中共价键的键长越短 键
间作 金属键 键 可能有共 共价键 子内共价键
. CO2 ꎬ ꎬ ꎬ
能越大 硬度就越大 则共价晶体 中化学键键长比 用力 价键 稀有气体除
ꎬ ꎬ CO2 SiO2 (
晶体中化学键键长短 所以 晶体比 晶体硬度大 外
ꎬ CO2 SiO2 ꎮ )
4
教材习题答案
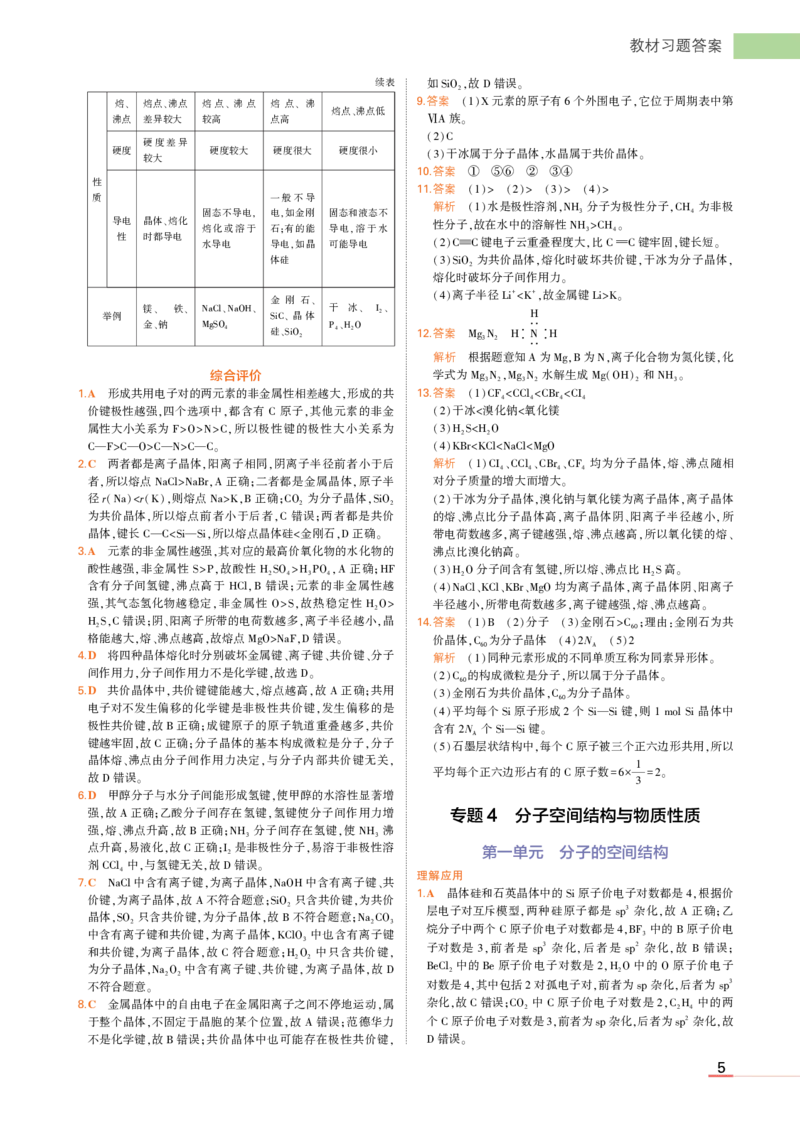
续表 如 故 错误
SiO2ꎬ D ꎮ
熔 熔点 沸点 熔点 沸点 熔 点 沸 9答案 元素的原子有 个外围电子 它位于周期表中第
、 、 、 、 熔点 沸点低 . (1)X 6 ꎬ
沸点 差异较大 较高 点高 、 族
ⅥA ꎮ
硬度差异 (2)C
硬度 硬度较大 硬度很大 硬度很小 干冰属于分子晶体 水晶属于共价晶体
较大 (3) ꎬ ꎮ
10答案
性 . ① ⑤⑥ ② ③④
11答案
质 一般不导 . (1)> (2)> (3)> (4)>
解析 水是极性溶剂 分子为极性分子 为非极
导电 晶体 熔化
固态不导电
ꎬ
电
ꎬ
如金刚 固态和液态不
性分子
(
故
1)
在水中的溶解性
ꎬNH3 ꎬCH4
性 时都 、 导电 熔化或溶于 石 ꎻ 有的能 导电 ꎬ 溶于水 ꎬ NH3>CH4ꎮ
水导电 导电 如晶 可能导电 键电子云重叠程度大 比 键牢固 键长短
ꎬ (2)CC ꎬ CC ꎬ ꎮ
体硅 为共价晶体 熔化时破坏共价键 干冰为分子晶体
(3)SiO2 ꎬ ꎬ ꎬ
熔化时破坏分子间作用力
ꎮ
金 刚 石 (4) 离子半径 Li + <K + ꎬ 故金属键 Li>Kꎮ
镁 铁 、 干 冰
举例 、 、 NaCl、NaOH、 晶体 、 I2、
金 钠 SiC、 H
、 MgSO4 硅
、SiO2
P4、H2O 12
.
答案
Mg3N2 H
N
H
解析 根据题意知 为 为 离子化合物为氮化镁 化
A MgꎬB Nꎬ ꎬ
综合评价 学式为 水解生成 和
Mg3N2ꎬMg3N2 Mg(OH)2 NH3ꎮ
1A 形成共用电子对的两元素的非金属性相差越大 形成的共 13答案
. ꎬ . (1)CF4<CCl4<CBr4<CI4
价键极性越强 四个选项中 都含有 原子 其他元素的非金 干冰 溴化钠 氧化镁
ꎬ ꎬ C ꎬ (2) < <
属性大小关系为 所以极性键的极性大小关系为
F>O>N>Cꎬ (3)H2S<H2O
C—F>C—O>C—N>C—Cꎮ (4)KBr<KCl<NaCl<MgO
2C 两者都是离子晶体 阳离子相同 阴离子半径前者小于后 解析 均为分子晶体 熔 沸点随相
. ꎬ ꎬ (1)CI4、CCl4、CBr4、CF4 ꎬ 、
者 所以熔点 正确 二者都是金属晶体 原子半 对分子质量的增大而增大
ꎬ NaCl>NaBrꎬA ꎻ ꎬ ꎮ
径r r 则熔点 正确 为分子晶体 干冰为分子晶体 溴化钠与氧化镁为离子晶体 离子晶体
(Na)< (K)ꎬ Na>KꎬB ꎻCO2 ꎬSiO2 (2) ꎬ ꎬ
为共价晶体 所以熔点前者小于后者 错误 两者都是共价 的熔 沸点比分子晶体高 离子晶体阴 阳离子半径越小 所
ꎬ ꎬC ꎻ 、 ꎬ 、 ꎬ
晶体 键长 所以熔点晶体硅 金刚石 正确 带电荷数越多 离子键越强 熔 沸点越高 所以氧化镁的熔
ꎬ C—C<Si—Siꎬ < ꎬD ꎮ ꎬ ꎬ 、 ꎬ 、
3A 元素的非金属性越强 其对应的最高价氧化物的水化物的 沸点比溴化钠高
. ꎬ ꎮ
酸性越强 非金属性 故酸性 正确 分子间含有氢键 所以熔 沸点比 高
ꎬ S>Pꎬ H2SO4>H3PO4ꎬA ꎻHF (3)H2O ꎬ 、 H2S ꎮ
含有分子间氢键 沸点高于 错误 元素的非金属性越 均为离子晶体 离子晶体阴 阳离子
ꎬ HClꎬB ꎻ (4)NaCl、KCl、KBr、MgO ꎬ 、
强 其气态氢化物越稳定 非金属性 故热稳定性 半径越小 所带电荷数越多 离子键越强 熔 沸点越高
ꎬ ꎬ O>Sꎬ H2O> ꎬ ꎬ ꎬ 、 ꎮ
错误 阴 阳离子所带的电荷数越多 离子半径越小 晶 14答案 分子 金刚石 理由 金刚石为共
H2SꎬC ꎻ 、 ꎬ ꎬ . (1)B (2) (3) >C60ꎻ :
格能越大 熔 沸点越高 故熔点 错误 价晶体 为分子晶体 N
ꎬ 、 ꎬ MgO>NaFꎬD ꎮ ꎬC60 (4)2 A (5)2
4D 将四种晶体熔化时分别破坏金属键 离子键 共价键 分子 解析 同种元素形成的不同单质互称为同素异形体
. 、 、 、 (1) ꎮ
间作用力 分子间作用力不是化学键 故选 的构成微粒是分子 所以属于分子晶体
ꎬ ꎬ Dꎮ (2)C60 ꎬ ꎮ
5D 共价晶体中 共价键键能越大 熔点越高 故 正确 共用 金刚石为共价晶体 为分子晶体
.
电 子对不发生偏
ꎬ
移的化学键是非
ꎬ
极性共价键
ꎬ
发
A
生偏移
ꎻ
的是
(3)
平均每个 原子形
ꎬ
成
C60
个 键
ꎮ
则 晶体中
ꎬ (4) Si 2 Si—Si ꎬ 1 mol Si
极性共价键 故 正确 成键原子的原子轨道重叠越多 共价 含有 N 个 键
键越牢固 故 ꎬ 正 B 确 分 ꎻ 子晶体的基本构成微粒是分子 ꎬ 分子 石 2 墨 A 层状 S 结 i— 构 Si 中 每 ꎮ 个 原子被三个正六边形共用 所以
ꎬ C ꎻ ꎬ (5) ꎬ C ꎬ
晶体熔 沸点由分子间作用力决定 与分子内部共价键无关
、 ꎬ ꎬ 平均每个正六边形占有的 原子数 1
故 错误 C =6× =2ꎮ
D ꎮ 3
6D 甲醇分子与水分子间能形成氢键 使甲醇的水溶性显著增
. ꎬ
强 故 正确 乙酸分子间存在氢键 氢键使分子间作用力增 专题4 分子空间结构与物质性质
ꎬ A ꎻ ꎬ
强 熔 沸点升高 故 正确 分子间存在氢键 使 沸
ꎬ 、 ꎬ B ꎻNH3 ꎬ NH3
点升高 易液化 故 正确 是非极性分子 易溶于非极性溶 第一单元 分子的空间结构
ꎬ ꎬ C ꎻI2 ꎬ
剂 中 与氢键无关 故 错误
CCl4 ꎬ ꎬ D ꎮ 理解应用
7C 中含有离子键 为离子晶体 中含有离子键 共
. NaCl ꎬ ꎬNaOH 、 1A 晶体硅和石英晶体中的 原子价电子对数都是 根据价
价键 为离子晶体 故 不符合题意 只含共价键 为共价 . Si 4ꎬ
晶体 ꎬ 只含共价 ꎬ 键 A 为分子晶体 ꎻ 故 SiO2 不符合题意 ꎬ 层电子对互斥模型 ꎬ 两种硅原子都是 sp 3 杂化 ꎬ 故 A 正确 ꎻ 乙
ꎬSO2 ꎬ ꎬ B ꎻNa2CO3 烷分子中两个 原子价电子对数都是 中的 原子价电
中
和
含
共
有
价
离
键
子
为
键
离
和
子
共
晶
价
体
键
ꎬ
故
为离
符
子
合
晶
题
体
意
ꎬKClO3
中
中
也
只
含
含
有
共
离
价
子
键
键
子对数是 前
C
者是 3 杂化 后者是
4ꎬB
2
F3
杂化 故
B
错误
3ꎬ sp ꎬ sp ꎬ B ꎻ
为分子晶体 ꎬ 中含 ꎬ 有离 C 子键 共价 ꎻH 键 2O 为 2 离子晶体 故 ꎬ 中的 原子价电子对数是 中的 原子价电子
ꎬNa2O2 、 ꎬ ꎬ D BeCl2 Be 2ꎬH2O O
不符合题意 对数是 其中包括 对孤电子对 前者为 杂化 后者为 3
ꎮ 4ꎬ 2 ꎬ sp ꎬ sp
8C 金属晶体中的自由电子在金属阳离子之间不停地运动 属 杂化 故 错误 中 原子价电子对数是 中的两
. ꎬ ꎬ C ꎻCO2 C 2ꎬC2H4
于整个晶体 不固定于晶胞的某个位置 故 错误 范德华力 个 原子价电子对数是 前者为 杂化 后者为 2 杂化 故
ꎬ ꎬ A ꎻ C 3ꎬ sp ꎬ sp ꎬ
不是化学键 故 错误 共价晶体中也可能存在极性共价键 错误
ꎬ B ꎻ ꎬ D ꎮ
5
2D 杂化前后的轨道数不变 杂化后 轨道的形状发生了改变
. ꎬ ꎬ ꎬ 2Ag~2Na3[Ag(S2O3)2]~1Na2S
故 A 正确 ꎻsp 3 、sp 2 、sp 杂化轨道的空间构型分别是正四面体 、 2 mol 1 mol
平面三角形 直线形 所以其夹角分别为 x
、 ꎬ 109°28′、120°、180°ꎬ 0.0526 mol
故 正确 部分四面体形 三角锥形 形分子的结构都可以 2 mol 1 mol
B ꎻ 、 、V = x
用 3 杂化轨道解释 故 正确 杂化轨道可以部分参与形成 0.0526 mol
sp ꎬ C ꎻ 解得x
化学键 ꎬ 如 NH3 中 N 发生了 sp 3 杂化 ꎬ 形成了 4 个 sp 3 杂化轨 9略 =0.0263 molꎮ
道 但只有 个杂化轨道参与形成化学键 .
ꎬ 3 ꎮ 综合评价
3A 价电子对数 4+1×4 且 分子中不含孤电子对 则 1B 能与血红蛋白中的 2+以配位键结合 使血红蛋白失
. =
2
=4ꎬ SiCl4 ꎬ .
去 输
C
送
O
的能力 从而使人
F
中
e
毒
ꎬ
为正四面体形 正确
O2 ꎬ ꎮ
4
S
D
iCl4
项 和
ꎬ
的
A
空间
ꎮ
结构均为 形 项 + 和
2
.
C
电 荷 NH 根 3 据
不
化
带
合
电
物 ꎬN 中 O 各
-
3
带
元
一
素
个
化
单
合
位
价
负
的
电
代
荷
数 ꎬ 和 Cl 为
-也带
可
一
求
个单位负
. A ꎬSO2 O3 V ꎻB ꎬNH4 CH4 ꎬ 0 ꎮ
的空间结构均为正四面体形 项 和 +的空间结构均 3C 加入 生成 沉淀 c + 降低 平衡正向移动 故
ꎻC ꎬNH3 H3O . KIꎬ AgI ꎬ (Ag ) ꎬ ꎬ A
为三角锥形 项 为直线形 而 为 形 符合题意 不符合题意 加入 与 反应 c 降低 平衡正向
5答案
ꎻD ꎬCO2 ꎬ H2O V ꎬ ꎮ
移动 故 不
ꎻ
符合题
HN
意
O3ꎬ
加入
NH3
c
ꎬ (NH
增
3)
大 平
ꎬ
衡逆向移
. C B D A E 动 故
ꎬ
符
B
合题意 加入
ꎻ
水 生
N
成
H
物
3ꎬ
离
(
子
N
浓
H3
度
)
降低
ꎬ
程度较大 平
6 . 答案 在 ABn 型分子中 A 原子的所有价电子都形成共价键 ꎬ 衡 ꎬ 正向 C 移动 故 ꎻ 不符合题 ꎬ 意 ꎬ
原子没有孤电子对 这样的分子结构对称 正 负电荷重心 ꎬ D ꎮ
A ꎬ ꎬ 、 4C 2+中 2+的配位数为 配位体是 故
重合 为非极性分子 . [Cu(H2O)4] Cu 4ꎬ H2Oꎬ A
ꎬ ꎮ
正确 每个 晶胞中平均含有 2+个数为 1 1
7答案 ∗ ꎻ CaF2 Ca 8× 8 +6× 2 =4ꎬ
. (4)CH3 CH COOH 故 正确 电子云图只表示一个电子在某一区域出现机会的
B ꎻ
NH2 多少 故 错误 晶胞中 原子数目为 1 1 故
8答案 题给物质 中心原子孤电子对数目越多 排斥力 ꎬ C ꎻ Cu 8× +6× =4ꎬ D
. C、N、O ꎬ 8 2
越大 形成的化学键越不稳定 键能就越小 正确
ꎬ ꎬ ꎮ ꎮ
H H H
第二单元 配合物的形成和应用 5答案 3 杂化轨道 2 杂化轨
. H C H 、sp ꎻ CC 、sp
理解应用
H H H
1B 配位化合物一般是指过渡金属元素的原子或离子与含有 道 杂化轨道
. ꎻ H CC H 、sp ꎮ
孤电子对的分子或离子通过配位键结合而形成的化合物 故 6答案 极性分子为 非极性分子为
ꎬ . HF、H2O、NH3ꎻ N2、
正确 配位化合物中还可能含有共价键 离子键 如
A ꎮ 、 ꎬ 7答 CO 案 2、CCl4ꎮ
故 错误 2+中 2+提供空轨 . (1)> (2)>
[Cu(NH3)4]SO4ꎬ B ꎮ [Cu(H2O)6] Cu 8答案
道 中的 原子提供孤电子对 两者结合形成配位键 故 . (1)AgCl+2NH3H2O[Ag(NH3)2]Cl+2H2O
ꎬH2O O ꎬ ꎬ
正确 配合物的应用 生命体中 许多酶与金属离子的配 (2)CuSO4+4NH3H2O[Cu(NH3)4]SO4+4H2O
C ꎮ :① ꎬ
合物有关 科学研究和生产实践中 进行溶解 沉淀或萃取 (3)FeCl3+3KSCNFe(SCN)3+3KCl
ꎻ② ꎬ 、 9答案 将 配成溶液后 加入 酸化的
等操作来达到分离提纯 分析检测等目的 故 正确 . Pd(NH3)2Cl2 ꎬ HNO3
、 ꎬ D ꎮ 溶液 若有沉淀生成 则 -与 2+以离子键结合 若无
2
.
C
CaSO42H2O
属于一般化合物
ꎬ
不属于配合物
ꎮ
A 沉 g 淀 NO 生 3 成
ꎬ
则 ꎬ
Cl
-与
Pd
2+以配 ꎬ 位键 Cl 结合 P
ꎮ
d ꎬ
3 C 固体溶于少量水中 溶液中同时存在黄色的 10答案 平面三角形 三角锥形 直线形
. CuCl2 ꎬ . (1) (2) (3) (4)V
2-和蓝色的 2+ 黄色和蓝色混合物为绿 形 正四面体形 直线形
[CuCl4] [Cu(H2O)4] ꎬ (5) (6)
色 所以得到绿色溶液 故 正确 将 固体溶于大量水 解析 无孤电子对 价电子对数为 原子
ꎬ ꎬ A ꎮ CuCl2 (1)BCl3 ꎬ 3+0=3ꎬB
中
ꎬ
平衡
溶
向
液中
生
加
成
入
[C
少
u
量
(H2O)4]
2
固
+的
体
方
生
向
成
移动
ꎬ
故
沉
B
淀
正确
-
ꎮ
浓
向
度
是
价电
sp
子
2 杂
对
化
数
ꎬ
为
分
3
子
+
为
1=
平
4ꎬ
面
P
三
原
角
子
形
为
ꎮ
s
(
p
2
3
)
杂
P
化
Cl3
ꎬ 分
有
子
一
为
对
三
孤
角
电
锥
子对
形
ꎬ
ꎮ
CuCl2 AgNO3 ꎬ AgCl ꎬCl 无孤电子对 价电子对数为 原子为 杂
减小 平衡正向移动 故 错误 向 溶液中加入 (3)N2O ꎬ 2+0=2ꎬO sp
ꎬ ꎬ C ꎮ CuCl2 NaCl 化 分子为直线形 有两对孤电子对 价电子对数为
固体 -浓度增大 平衡逆向移动 故 正确 ꎬ ꎮ (4)H2O ꎬ
ꎬCl ꎬ ꎬ D ꎮ 原子为 3 杂化 分子为 形 无孤电子
4 . B
内 界
[Co(NH3)3Cl3] 不能电离出 Cl - ꎬ 因为 Cl -位于配合物 2 对 +
ꎬ
2 价 =4 电 ꎬO 子对数为 s
4
p
+0=4ꎬ
ꎬ
Si
原子为 V
sp
3 ꎮ 杂 ( 化 5)
ꎬ
S 分 iH 子 4 为正四面
ꎮ 体形 无孤电子对 价电子对数为 原子
5C 中发生反应 与配合物无关 为 ꎮ 杂 ( 化 6)C 分 2H 子 2 为直线形 ꎬ 2+0=2ꎬC
. C 2FeCl2+Cl2 2FeCl3ꎬ ꎮ sp ꎬ ꎮ
6B 11答案 是非极性分子 它易溶于 这一非极性溶
. . (1)I2 ꎬ CCl4
7答案 配位数 配位原子 剂 而 为极性溶剂
. (1) :2ꎻ :Nꎮ ꎬ H2O ꎮ
配位数 配位原子 2+与 易形成 2+ 而不生成
(2) :6ꎻ :Fꎮ (2)Zn NH3 [Zn(NH3)4] ꎬ Zn(OH)2
配位数 配位原子 沉淀 3+与 不可以形成配合物而可以生成沉淀
(3) :4ꎻ :Nꎮ ꎬFe NH3 ꎮ
配位数 配位原子
(4) :6ꎻ :Oꎮ ∗ 有手性 原子存在 有对映异构体
8答案 (3)CH3 CH COOH C ꎬ ꎬ
. (1)Na2S+2Na3[Ag(S2O3)2]Ag2S↓+4Na2S2O3ꎮ
废定影液中含有 的质量 m -1 OH
(2)1 L Ag =5.68 gL ×1 L= 而 无手性碳原子 故不存在对映异构体
CH3—CH2—COOH ꎬ ꎮ
5.68 gꎮ 12答案 2 6 6 杂化 - 分
. (1)3s 3p 3d (2)sp [ ∶ C⋮⋮N ∶ ] (3)
n 5.68 g 设 的物质的量为x 子晶体
(Ag)= -1≈0.0526 molꎬ Na2S ꎮ (4)1 ∶ 2
108 gmol
6