文档内容
第二章 分子结构与性质
第二节 分子的空间结构
2.3.1共价键的极性
本节是在学习了共价键和分子的立体构型的基础上,进一步来认识分子的一些性质,包括共价
键的极性和非极性,并由此引出一些共价分子的性质及其应用;范德华力、氢键及其对物质性质的
影响,特别是物质的熔沸点及溶解性等;教学时要注意引导学生运用“物质结构决定物质性质,性
质反映结构”的观念来理解和解释分子的性质。
课程目标 学科素养
1.能从共用电子对是否发生偏移的角度认识键的极 a.微观辨识:能从微观角度理解共价键的极
性和分子极性的关系。
性的实质是成键原子分别带正电和负电。
b.模型认知:通过键的极性对物质性质的影
2.知道分子可以分为极性分子和非极性分子。 响的探析,形成“结构决定性质"的认知模
型。
3.知道分子极性和分子中键的极性、分子的空间结
构密切相关。
教学重点:极性分子与非极性分子的判断
教学难点:极性分子与非极性分子的判断
多媒体调试、讲义分发
【复习回顾】
1.共价键的分类
分类标准 类型
共用电子对数 单键、双键、三键
电子云重叠方式 σ键、 π键共用电子对是否偏移 极性键、非极性键
【学生活动】
写出H、O、N、HCl、CO、HO、CH、NH 的电子式和结构式。
2 2 2 2 2 4 3
【设疑】
共用电子对在两原子周围出现的机会是否相同?即共用电子对是否偏移?
【讲解】
有些共用电子对的两个原子由于电负性不同,那么共用电子对在两原子周围出现的机会便不同,即
共用电子对发生偏移。有些共用电子对的两个原子由于电负性相同,那么共用电子对在两原子周围
出现的机会相同,即共用电子对不发生偏移。
根据共用电子对是否偏移,可以将共价键分为极性键和非极性键。
【讲解】
2.键的极性
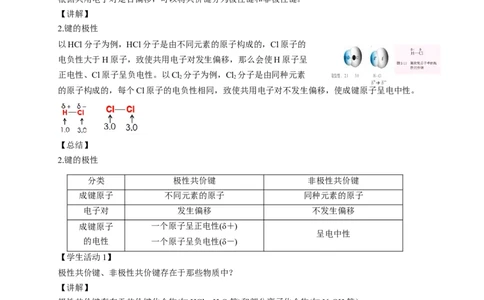
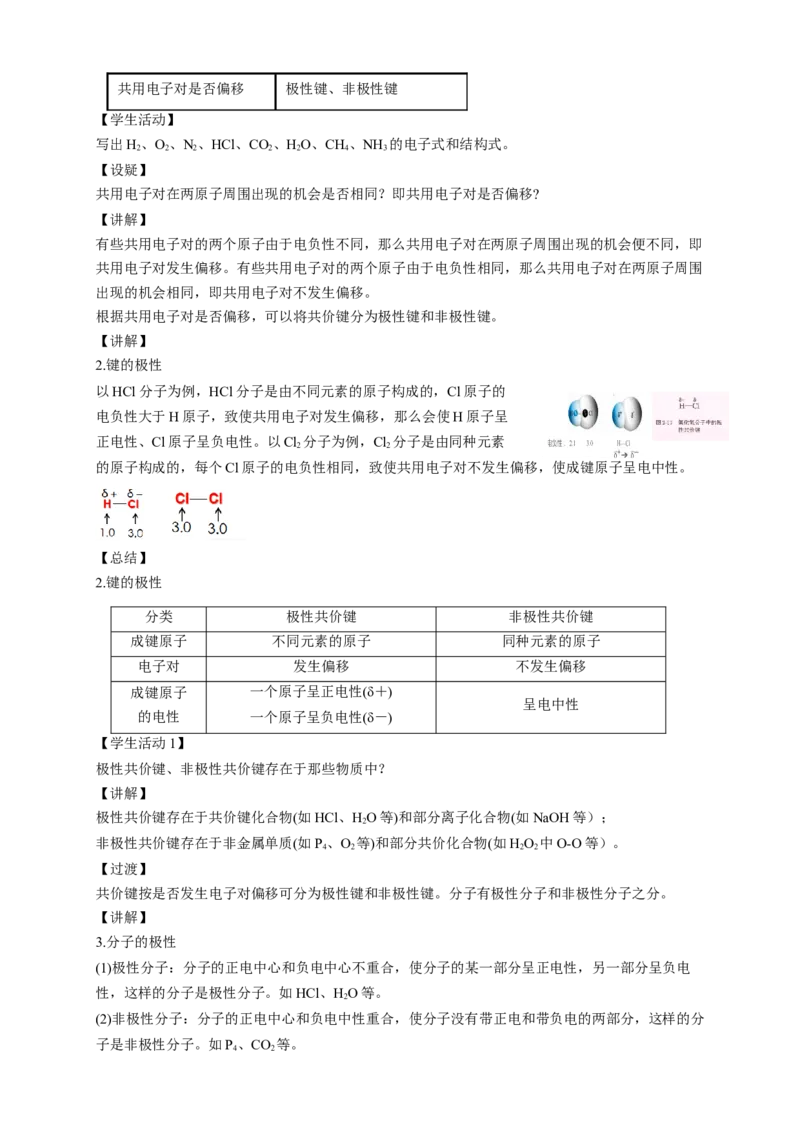
以HCl分子为例,HCl分子是由不同元素的原子构成的,Cl原子的
电负性大于H原子,致使共用电子对发生偏移,那么会使H原子呈
正电性、Cl原子呈负电性。以Cl 分子为例,Cl 分子是由同种元素
2 2
的原子构成的,每个Cl原子的电负性相同,致使共用电子对不发生偏移,使成键原子呈电中性。
【总结】
2.键的极性
分类 极性共价键 非极性共价键
成键原子 不同元素的原子 同种元素的原子
电子对 发生偏移 不发生偏移
成键原子 一个原子呈正电性(δ+)
呈电中性
的电性 一个原子呈负电性(δ-)
【学生活动1】
极性共价键、非极性共价键存在于那些物质中?
【讲解】
极性共价键存在于共价键化合物(如HCl、HO等)和部分离子化合物(如NaOH等);
2
非极性共价键存在于非金属单质(如P、O 等)和部分共价化合物(如HO 中O-O等)。
4 2 2 2
【过渡】
共价键按是否发生电子对偏移可分为极性键和非极性键。分子有极性分子和非极性分子之分。
【讲解】
3.分子的极性
(1)极性分子:分子的正电中心和负电中心不重合,使分子的某一部分呈正电性,另一部分呈负电
性,这样的分子是极性分子。如HCl、HO等。
2
(2)非极性分子:分子的正电中心和负电中性重合,使分子没有带正电和带负电的两部分,这样的分
子是非极性分子。如P、CO 等。
4 2【展示】
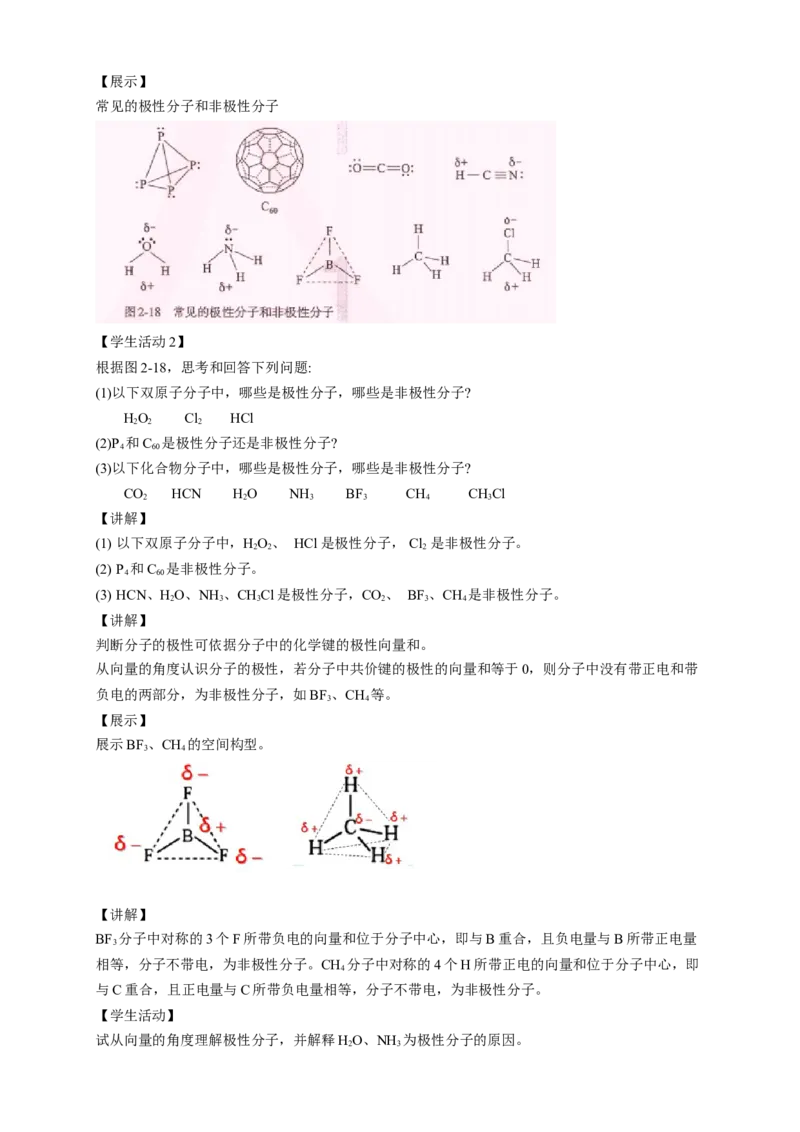
常见的极性分子和非极性分子
【学生活动2】
根据图2-18,思考和回答下列问题:
(1)以下双原子分子中,哪些是极性分子,哪些是非极性分子?
HO Cl HCl
2 2 2
(2)P 和C 是极性分子还是非极性分子?
4 60
(3)以下化合物分子中,哪些是极性分子,哪些是非极性分子?
CO HCN HO NH BF CH CHCl
2 2 3 3 4 3
【讲解】
(1) 以下双原子分子中,HO、 HCl是极性分子,Cl 是非极性分子。
2 2 2
(2) P 和C 是非极性分子。
4 60
(3) HCN、HO、NH 、CHCl是极性分子,CO、 BF、CH 是非极性分子。
2 3 3 2 3 4
【讲解】
判断分子的极性可依据分子中的化学键的极性向量和。
从向量的角度认识分子的极性,若分子中共价键的极性的向量和等于0,则分子中没有带正电和带
负电的两部分,为非极性分子,如BF、CH 等。
3 4
【展示】
展示BF、CH 的空间构型。
3 4
【讲解】
BF 分子中对称的3个F所带负电的向量和位于分子中心,即与B重合,且负电量与B所带正电量
3
相等,分子不带电,为非极性分子。CH 分子中对称的4个H所带正电的向量和位于分子中心,即
4
与C重合,且正电量与C所带负电量相等,分子不带电,为非极性分子。
【学生活动】
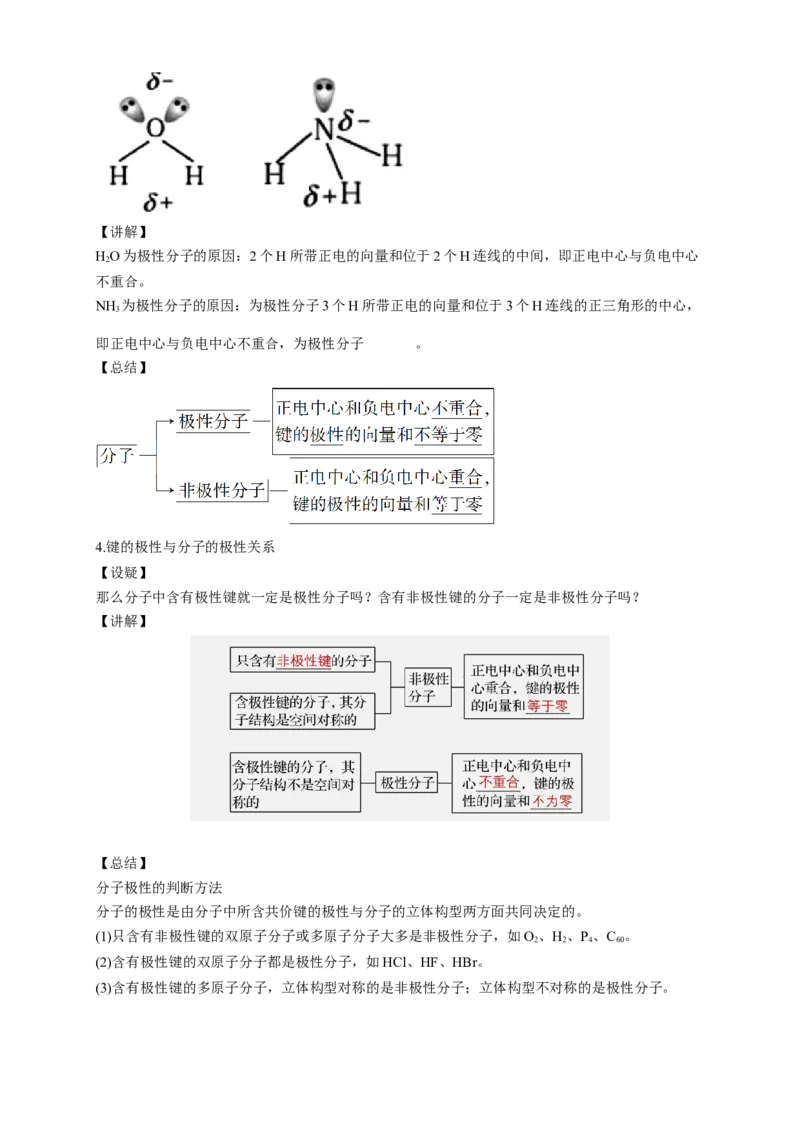
试从向量的角度理解极性分子,并解释HO、NH 为极性分子的原因。
2 3【讲解】
HO为极性分子的原因:2个H所带正电的向量和位于2个H连线的中间,即正电中心与负电中心
2
不重合。
NH 为极性分子的原因:为极性分子3个H所带正电的向量和位于3个H连线的正三角形的中心,
3
即正电中心与负电中心不重合,为极性分子 。
【总结】
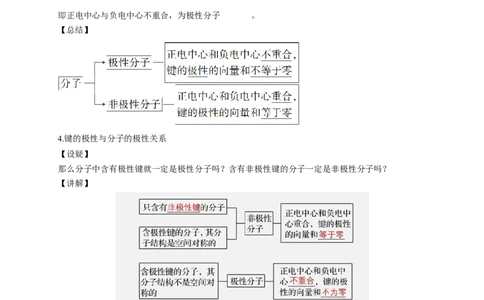
4.键的极性与分子的极性关系
【设疑】
那么分子中含有极性键就一定是极性分子吗?含有非极性键的分子一定是非极性分子吗?
【讲解】
【总结】
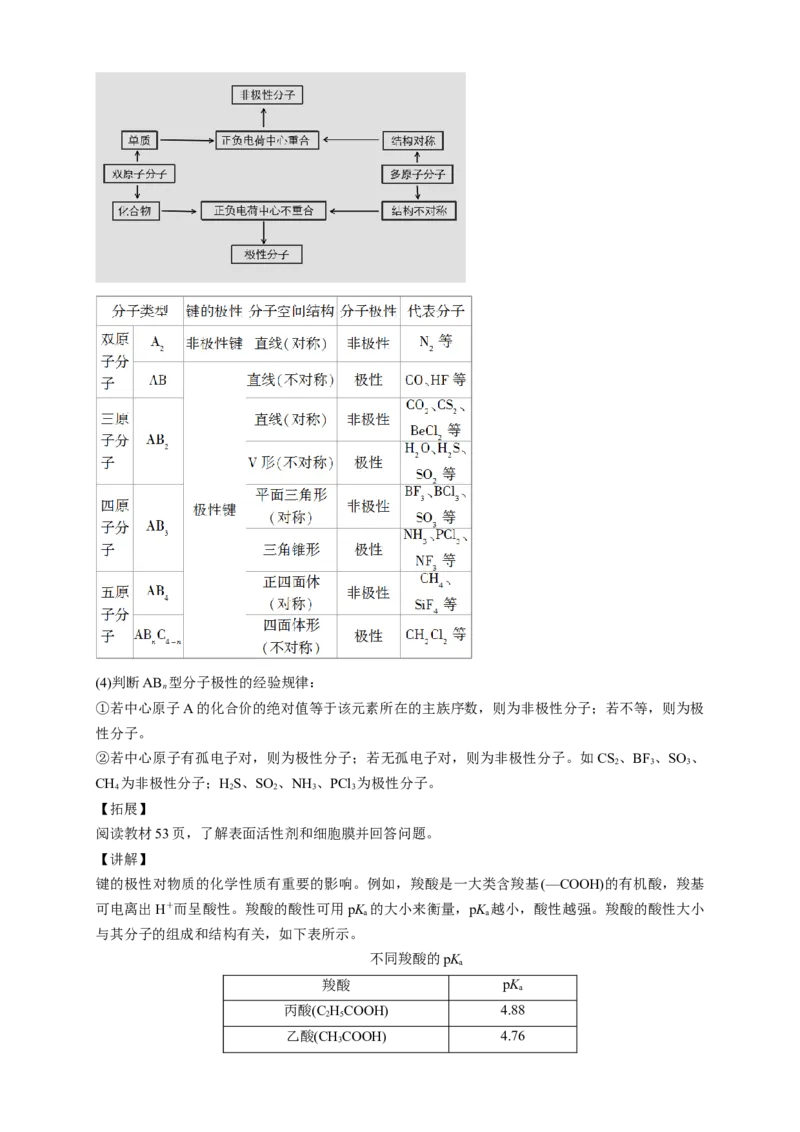
分子极性的判断方法
分子的极性是由分子中所含共价键的极性与分子的立体构型两方面共同决定的。
(1)只含有非极性键的双原子分子或多原子分子大多是非极性分子,如O、H、P、C 。
2 2 4 60
(2)含有极性键的双原子分子都是极性分子,如HCl、HF、HBr。
(3)含有极性键的多原子分子,立体构型对称的是非极性分子;立体构型不对称的是极性分子。(4)判断AB 型分子极性的经验规律:
n
①若中心原子A的化合价的绝对值等于该元素所在的主族序数,则为非极性分子;若不等,则为极
性分子。
②若中心原子有孤电子对,则为极性分子;若无孤电子对,则为非极性分子。如CS 、BF 、SO 、
2 3 3
CH 为非极性分子;HS、SO 、NH 、PCl 为极性分子。
4 2 2 3 3
【拓展】
阅读教材53页,了解表面活性剂和细胞膜并回答问题。
【讲解】
键的极性对物质的化学性质有重要的影响。例如,羧酸是一大类含羧基(—COOH)的有机酸,羧基
可电离出H+而呈酸性。羧酸的酸性可用pK 的大小来衡量,pK 越小,酸性越强。羧酸的酸性大小
a a
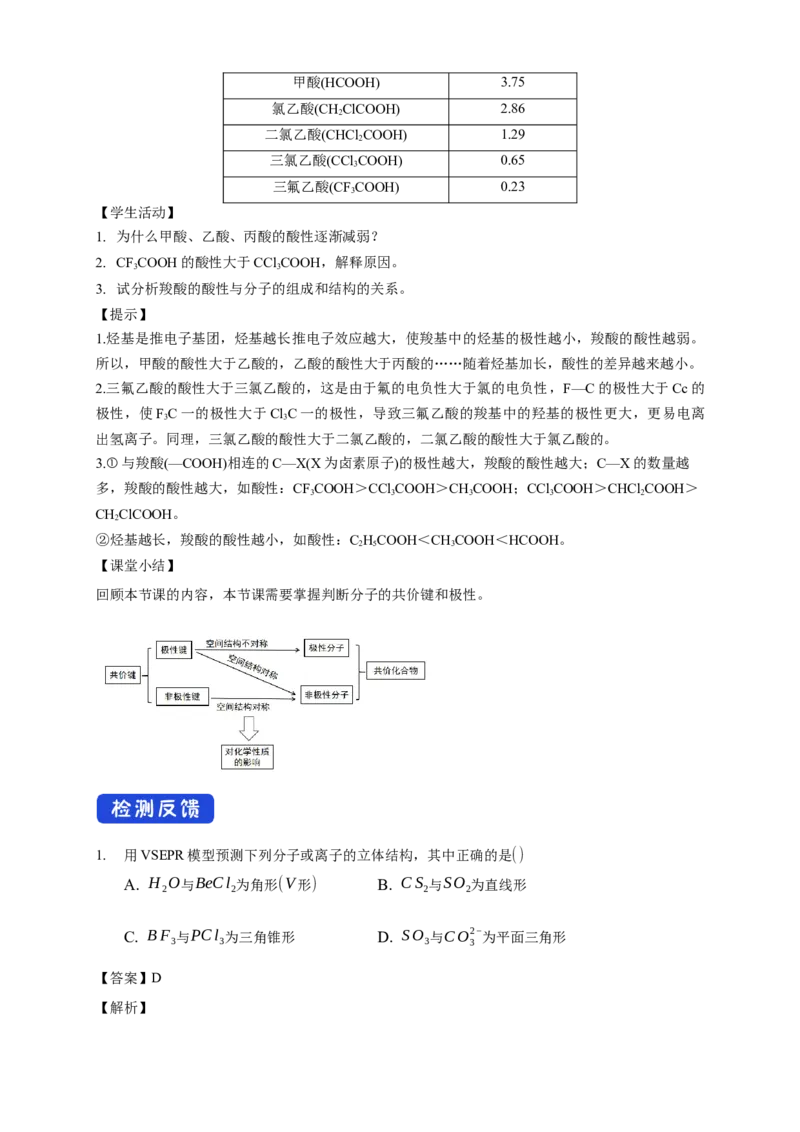
与其分子的组成和结构有关,如下表所示。
不同羧酸的pK
a
羧酸 pK
a
丙酸(C HCOOH) 4.88
2 5
乙酸(CHCOOH) 4.76
3甲酸(HCOOH) 3.75
氯乙酸(CHClCOOH) 2.86
2
二氯乙酸(CHCl COOH) 1.29
2
三氯乙酸(CCl COOH) 0.65
3
三氟乙酸(CFCOOH) 0.23
3
【学生活动】
1. 为什么甲酸、乙酸、丙酸的酸性逐渐减弱?
2. CFCOOH的酸性大于CCl COOH,解释原因。
3 3
3. 试分析羧酸的酸性与分子的组成和结构的关系。
【提示】
1.烃基是推电子基团,烃基越长推电子效应越大,使羧基中的烃基的极性越小,羧酸的酸性越弱。
所以,甲酸的酸性大于乙酸的,乙酸的酸性大于丙酸的……随着烃基加长,酸性的差异越来越小。
2.三氟乙酸的酸性大于三氯乙酸的,这是由于氟的电负性大于氯的电负性,F—C的极性大于Cc的
极性,使FC一的极性大于ClC一的极性,导致三氟乙酸的羧基中的羟基的极性更大,更易电离
3 3
出氢离子。同理,三氯乙酸的酸性大于二氯乙酸的,二氯乙酸的酸性大于氯乙酸的。
3.①与羧酸(—COOH)相连的C—X(X为卤素原子)的极性越大,羧酸的酸性越大;C—X的数量越
多,羧酸的酸性越大,如酸性:CFCOOH>CCl COOH>CHCOOH;CCl COOH>CHCl COOH>
3 3 3 3 2
CHClCOOH。
2
②烃基越长,羧酸的酸性越小,如酸性:C HCOOH<CHCOOH<HCOOH。
2 5 3
【课堂小结】
回顾本节课的内容,本节课需要掌握判断分子的共价键和极性。
1. 用VSEPR模型预测下列分子或离子的立体结构,其中正确的是()
A. H O与BeCl 为角形(V形) B. CS 与SO 为直线形
2 2 2 2
C. BF 与PCl 为三角锥形 D. SO 与CO2− 为平面三角形
3 3 3 3
【答案】D
【解析】1
A.水分子中O原子价层电子对个数=2+ ×(6−2×1)=4,VSEPR模型为正四面体结构,含有2
2
个孤电子对,略去孤电子对后,实际上其空间构型是V形,BeCl 中Be原子的价层电子对个数
2
1
=2+ ×(2−2×1)=2,不含孤电子对,则分子空间构型是直线形,故A错误;
2
B.CS 分子中每个S原子和C原子形成两个共用电子对,所以C原子价层电子对个数是2且不含孤
2
1
电子对,所以为直线形结构,SO 分子中S原子的价层电子对个数=2+ ×(6−2×2)=3且含有1
2 2
对孤电子对,所以为V形结构,故B错误;
1
C.BF 分子中B原子的价层电子对个数=3+ ×(3−3×1)=3且不含有孤电子对,所以其空间构型
3 2
1
为平面三角形,PCl 分子中P原子的价层电子对数=3+ (5−3×1)=4,含孤电子对数为1,杂
3 2
化轨道数4,中心原子采取sp3杂化,分子空间构型为三角锥形,故C错误;
1
D.SO 中S原子价层电子对个数=σ键个数+孤电子对个数=3+ (6−3×2)=3,含孤电子对数为
3 2
0,杂化轨道数3,硫原子采用sp2杂化,分子形状为平面三角形;CO2−
中碳原子价层电子对个数
3
4−3×2+2
=3+ =3,采用sp2杂化,所以CO2− 离子的立体构型为平面三角形,故D正确;
2 3
故选D。
2. 下列说法中正确的是()
A. CH 、C H 、HCN都是含有极性键的非极性分子
4 2 2
B. CO 与SO 的立体构型相似,都是非极性分子
2 2
C. 分子中含有1个手性碳原子
D. 含氧酸可用通式(HO) RO 表示,若m值越大,则含氧酸的酸性越强
m n
【答案】C
【解析】略
3. 已知H O 分子的空间结构可在二面角中如图所示,下列有关H O 结构的说法正确的是()
2 2 2 2A. H O 中有3个σ键、1个π键
2 2
B. H O 为非极性分子
2 2
C. H O 中氧原子为sp杂化
2 2
D. H O 沸点高达158℃,可推测H O 分子间可形成氢键
2 2 2 2
【答案】D
【解析】
A.H O 中有3个σ键,无π键,故A错误;
2 2
B.根据图示,H O 中正负电荷中心不重合,为极性分子,故B错误;
2 2
C.H O 中氧原子为sp3杂化,故C错误;
2 2
D.H O 沸点较高,可推测分子间形成了氢键,故D正确。
2 2
故选D。
4. 关于CS 、SO 、N H 三种物质的说法中正确的是( )
2 2 3
A. CS 在水中的溶解度很小,是由于其属于极性分子
2
B. SO 和N H 均易溶于水,原因之一是它们都是极性分子
2 3
C. CS 和SO 的分子结构相似,均为非极性分子
2 2
D. N H 在水中溶解度很大只是由于N H 分子有极性
3 3
【答案】B
【解析】略
5. 下列有关物质结构与性质的说法正确的是( )
A. CH OH能形成分子内氢键,则CH OH与水以任意比例互溶
3 3
B. C H 、N H 分子组成相同,则它们的分子所有原子共平面
2 4 2 4
C. C 溶于CS 形成红色溶液,则C 是非极性分子
60 2 60
D. 间二甲苯只有一种结构,则苯环不存在单键和双键交替
【答案】C
【解析】A.CH OH能与水分子间形成氢键,则CH OH与水以任意比例互溶,故A错误;
3 3
B.C H (乙烯)是平面结构,分子中所有原子共平面,N H 分子中每个N原子形成3个σ键,有1
2 4 2 4
对孤对电子,价层电子对数为4,则N原子形成的3个σ键构成空间三角锥形,N H 分子中所有
2 4
原子不可能共平面,故B错误;
C.CS 是直线型结构,为非极性分子,由相似相溶的原理可知,C 是非极性分子,故C正确;
2 60
D.邻二甲苯只有一种结构,可说明苯环不存在单键和双键交替,故D错误。
本节是在学习了共价键和分子的立体构型的基础上,进一步来认识分子的极性,能从共用电子
对是否发生偏移的角度认识键的极性的实质是成键原子分别带正电和负电。掌握分子极性和分子中
键的极性、分子的空间结构密切相关。能从微观角度理解共价键的极性和分子极性的关系,培养学
生微观辨识的科学素养,通过键的极性对物质性质的影响的探析,形成“结构决定性质"的认知模
型。