文档内容
第二章 分子结构与性质
第二节 分子的空间结构
2.3.1共价键的极性
一.选择题
1. 下列各项比较中前者高于(或大于或强于)后者的是
A. CH 在水中的溶解度和N H 在水中的溶解度
4 3
B. H Se的热稳定性和H S的热稳定性
2 2
C. I与H形成共价键的极性和F与H形成共价键的极性
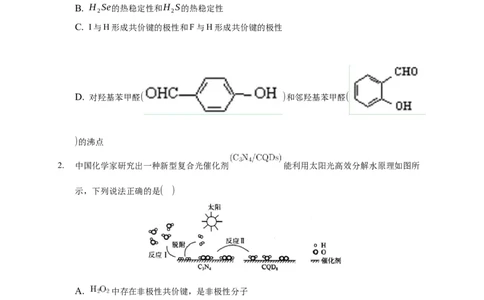
D. 对羟基苯甲醛( )和邻羟基苯甲醛(
)的沸点
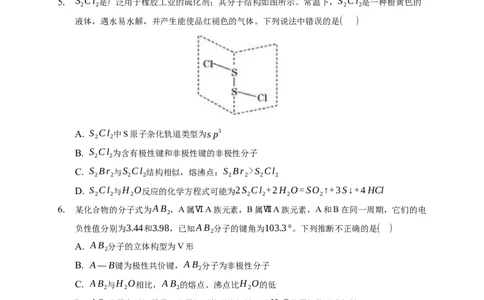
2. 中国化学家研究出一种新型复合光催化剂 能利用太阳光高效分解水原理如图所
示,下列说法正确的是( )
A. 中存在非极性共价键,是非极性分子
B. 反应Ⅰ中涉及极性键的断裂和非极性键的形成
C. 非极性分子中一定有非极性键,极性分子中一定有极性键
D. H O由于是非极性分子而稳定性强
2
3. 下列说法正确的是( )
A. 最外层都只有2个电子的元素原子性质一定相似
B. 同一周期元素中,第一电离能随原子序数增加而增大C. I AsF 晶体中存在I+ 离子,I+ 离子的几何构型为V形
3 6 3 3
D. H O 是一种含有极性键和非极性键的非极性分子
2 2
4. 下列说法正确的是()
A. SO 与 CO 的分子立体构型均为直线形
2 2
B. H O 和 N H 中的分子的极性和共价键的极性均相同
2 3
C. SiO 的键长大于 CO 的键长,所以 SiO 的熔点比 CO 高
2 2 2 2
D. 分子晶体中只存在分子间作用力,不含有其它化学键
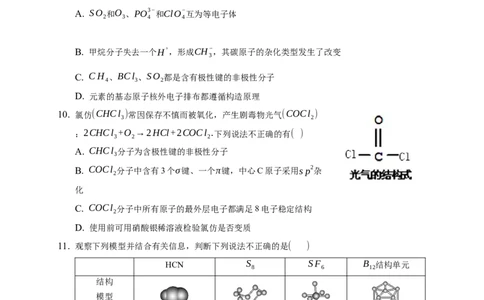
5. S Cl 是广泛用于橡胶工业的硫化剂;其分子结构如图所示。常温下,S Cl 是一种橙黄色的
2 2 2 2
液体,遇水易水解,并产生能使品红褪色的气体。下列说法中错误的是( )
A. S Cl 中S原子杂化轨道类型为sp3
2 2
B. S Cl 为含有极性键和非极性键的非极性分子
2 2
C. S Br 与S Cl 结构相似,熔沸点:S Br >S Cl
2 2 2 2 2 2 2 2
D. S Cl 与H O反应的化学方程式可能为2S Cl +2H O=SO ↑+3S↓+4HCl
2 2 2 2 2 2 2
6. 某化合物的分子式为AB ,A属ⅥA族元素,B属ⅦA族元素,A和B在同一周期,它们的电
2
负性值分别为3.44和3.98,已知AB 分子的键角为103.3°。下列推断不正确的是( )
2
A. AB 分子的立体构型为V形
2
B. A—B键为极性共价键,AB 分子为非极性分子
2
C. AB 与H O相比,AB 的熔点、沸点比H O的低
2 2 2 2
D. AB 分子中无氢原子,分子间不能形成氢键,而H O分子间能形成氢键
2 2
7. 碘单质在水中的溶解度很小,但在CCl 中的溶解度很大,这是因为 ( )
4
A. CCl 与I 的相对分子质量相差较小,而H O与I 的相对分子质量相差较大
4 2 2 2
B. CCl 与I 都是直线形分子,而H O不是直线形分子
4 2 2
C. CCl 和I 都不含氢元素,而H O中含有氢元素
4 2 2
D. CCl 和I 都是非极性分子,而H O是极性分子
4 2 28. 短周期主族元素 W、X、Y、Z的原子序数依次增大,W的简单氢化物可用作制冷剂,Y的原
子半径是所有短周期主族元素中最大的。由 X、Y和 Z三种元素形成的一种盐溶于水后,加
入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生。下列说法不正确的是()
A. 简单氢化物的沸点:X>W>Z
B. 第一电离能:W>X>Z>Y
C. X与 Z形成的化合物均为非极性分子
D. 1molY与足量 X 的单质反应,所得物质中离子总数为 1.5N
2 A
9. 下列说法中正确的是()
A. SO 和O 、PO3− 和ClO− 互为等电子体
2 3 4 4
B. 甲烷分子失去一个H+,形成CH− ,其碳原子的杂化类型发生了改变
3
C. CH 、BCl 、SO 都是含有极性键的非极性分子
4 3 2
D. 元素的基态原子核外电子排布都遵循构造原理
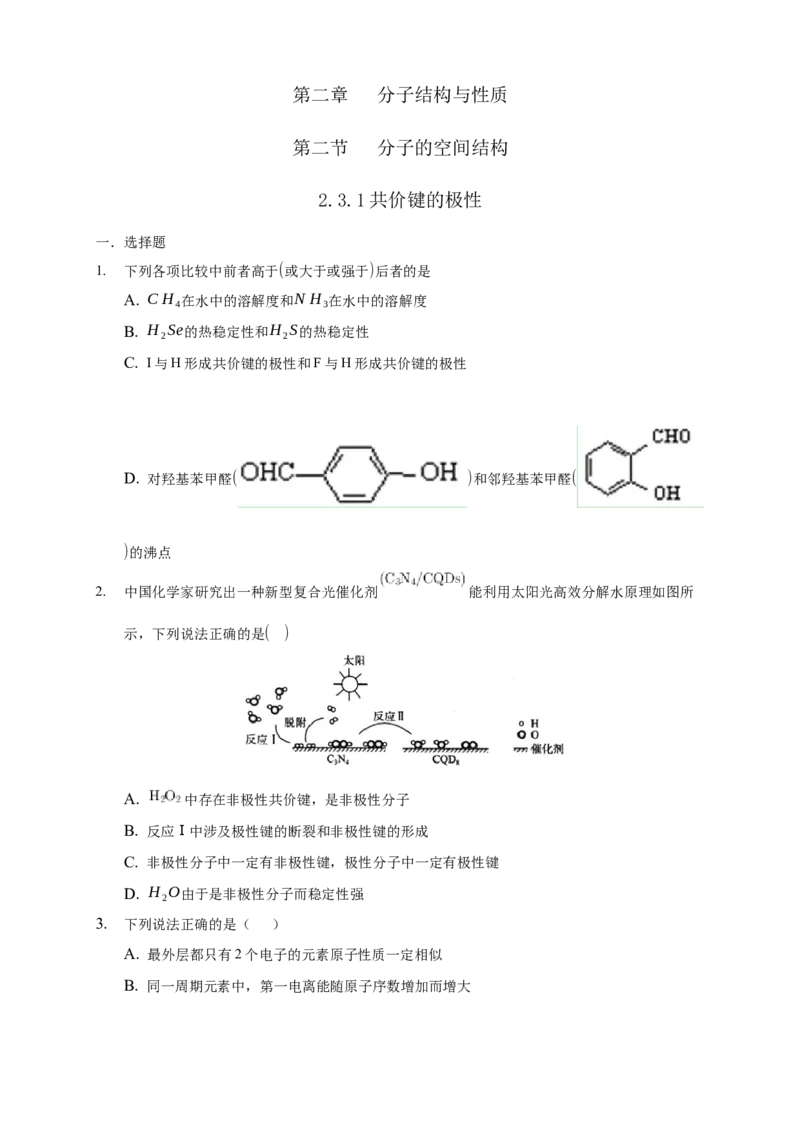
10. 氯仿(CHCl )常因保存不慎而被氧化,产生剧毒物光气(COCl )
3 2
:2CHCl +O →2HCl+2COCl .下列说法不正确的有( )
3 2 2
A. CHCl 分子为含极性键的非极性分子
3
B. COCl 分子中含有3个σ键、一个π键,中心C原子采用sp2杂
2
化
C. COCl 分子中所有原子的最外层电子都满足8电子稳定结构
2
D. 使用前可用硝酸银稀溶液检验氯仿是否变质
11. 观察下列模型并结合有关信息,判断下列说法不正确的是( )
HCN S SF B 结构单元
8 6 12
结构
模型
示意图
备注 — 易溶于CS — 熔点1873K
2
A. HCN的结构式为H —C≡N,分子中含有2个σ键和2个π键
B. 固态硫S 属于原子晶体
8
C. SF 是由极性键构成的非极性分子
6
D. 单质硼属共价晶体,结构单元中含有30个B—B键12. 通常情况下,NCl 是一种油状液体,其分子空间构型与N H 相似。下列对NCl 和N H 的有
3 3 3 3
关叙述正确的是( )
A. NCl 的沸点高于N H 的沸点
3 3
B. 在氨水中,大部分N H 与H O以氢键(用“…”表示)结合形成N H ·H O分子,则
3 2 3 2
N H ·H O的结构式为
3 2
C. NCl 分子是非极性分子
3
D. NBr 比NCl 易挥发
3 3
二、填空题
13. (1)写出 分子的空间结构:___________,它是___________分子(填“极性”或“非极性”
),它的中心原子采用的杂化方式是___________。
(2)甲醛(HCHO)在Ni催化作用下加氢可得甲醇 。甲醇分子内C原子的杂化方式为
___________,甲醇分子内O−C−H的键角___________(填“>”“<”或“=”)甲醛分子内
O−C−H的键角;甲醇极易溶于水,其主要原因是___________。
14. 已知N、P同属元素周期表的ⅤA族元素,N在第二周期,P在第三周期,N H 分子呈三角锥
3
形,N原子位于锥顶,三个H原子位于锥底,N —H键间的夹角是107°。
(1)PH 分子与N H 分子的构型关系是________(填“相同”“相似”或“不相似”),
3 3
________(填“有”或“无”)P—H键,PH 分子是________(填“极性”或“非极性”)分
3
子。
(2)N H 和 PH 相 比 , 热 稳 定 性 更 强 的 是 ________ , 原 因 是
3 3
____________________________________。
(3)N H 和PH 在常温、常压下都是气体,但N H 比PH 易液化,其主要原因是________。
3 3 3 3
A.键的极性N —H比P—H强
B.分子的极性N H 比PH 强
3 3C.相对分子质量PH 比N H 大
3 3
D.N H 分子之间存在特殊的分子间作用力
3
15. 有下列粒子:
①CH ②CH =CH ③CH≡CH④N H ⑤N H+ ⑥BF ⑦H O
4 2 2 3 4 3 2
填写下列空白(填序号):
(1)呈正四面体的是______。
(2)中心原子轨道为sp3杂化的是______,为sp2杂化的是______,为sp杂化的是______。
(3)所有原子共平面的是______,共线的是______。
(4)粒子存在配位键的是______。
(5)含有极性键的极性分子的是______。
16. 在下列物质中:NaCl、NaOH、Na S、H O 、Na S 、(N H ) S、CO 、CCl 、C H
2 2 2 2 2 4 2 2 4 2 4
、SiO 、SiC、晶体硅、金刚石、晶体氩。
2
(1)其中既含有离子键又含有极性共价键的离子晶体是 __________。
(2)其中既含有离子键又含有极性共价键和配位键的离子晶体是 __________。
(3)其中含有极性共价键的非极性分子是 ________。
(4)其中含有极性共价键和非极性共价键的非极性分子是 ________。
(5)其中含有极性共价键和非极性共价键的极性分子是 __________。
(6)其中含有极性共价键的原子晶体是 ________。
17. 含碳元素的物质是化学世界中最庞大的家族。回答下列问题:
(1)碳在形成化合物时,其键型以共价键为主,CH 中的化学键从形成的过程来看属于____(
4
填“σ”或“π”)键,从其极性来看属于__________(填“极性”或“非极性”)键。
(2)CH 和CO 分子中属于非极性分子的是__________;与CH 互为等电子体的阳离子是
4 2 4
__________;与CO 互为等电子体的阴离子是__________。
2
(3)有机物 中含氧官能团的名称为__________,其中含有__________个
手性碳原子。
(4)甲醇与乙烷的相对分子质量和范德华力均相近,但是二者的沸点相差很大,造成该差异的
原因是______________________________。18. 已知A、B、C、D、E为元素周期表中前四周期元素,且原子序数依次增大。A是短周期中原
子半径最大的元素;B元素3p能级半充满,C是所在周期电负性最大的元素;D是第四周期未
成对电子最多的元素;E元素位于元素周期表的第11列。试回答下列有关的问题:
(1)写出基态D原子的价电子排布式:________,E元素位于元素周期表________。
(2)A、B、C三种元素的第一电离能最大的是________(用元素符号表示)。这三种元素最高价
氧化物的水化物形成的溶液,物质的量浓度相同时,pH由大到小的顺序是_______(写化学式)
。
(3)D可形成化合物[D(H O) ](NO ) 。
2 6 3 3
①[D(H O) ](NO ) 中配位体的VSEPR模型名称是________。该化合物中阴离子的中心原
2 6 3 3
子的轨道杂化类型为________。
②1个[D(H O) ] 3+ 中含有的σ键数目为________。
2 6
(4)已知B、C两种元素形成的化合物通常有两种。这两种化合物中________(填化学式)为非极
性分子,另一种化合物的电子式为________。