文档内容
第二章 分子结构与性质
第三节 分子结构与物质性质
2.3.2分子间的作用力 分子的手性
一.选择题
1. 下列关于氢键的说法正确的是
A. 由于氢键的作用,使 、 、HF的沸点反常,且沸点高低顺序为
B. 氢键只能存在于分子间,不能存在于分子内
C. 没有氢键就没有生命
D. 相同量的水在气态、液态和固态时均有氢键,且氢键的数目依次增多
【答案】C
【解析】
A. “反常”是指它们在本族元素的氢化物沸点排序中的现象,三种物质的沸点高低顺序可由事实得
出,常温下只有水是液体,水的沸点最高,故A错误;
B. 氢键存在于不直接相连但相邻的H、 或N、 原子间,所以分子内也可能存在氢键,如邻
羟基苯甲醛分子内含有氢键,故B错误;
C. 因为氢键的存在使常温常压下的水呈液态,而液态水是生物体营养传递的基础,故C正确;
D. 水在气态时,分子间距离大,分子之间没有氢键,故D错误。
故选C。
2. 下列对分子性质的解释中,正确的是
A. 极易溶于水而 难溶于水只是因为 是极性分子, 是非极性分子
B. 乳酸 具有光学活性,因为其分子中含有一个手性碳原子
C. 水很稳定 以上才会部分分解 是因为水分子间存在大量的氢键D. 已知酸性: ,因为 的氧原子数大于HClO的氧原子数
【答案】B
【解析】
A. 与水分子之间存在氢键,使氨气易溶于水,所以 极易溶于水的原因为 是极性分
子和氨气与水分子间存在氢键,故A错误;
B. 中间碳原子上连有四个不一样的基团:氢原子、甲基、羧基和羟基,是手性碳原
子,存在对映异构即手性异构体,故B正确;
C.水很稳定 以上才会部分分解 是因为水中含有的 键非常稳定,与存在氢键无关,
故C错误;
D. 的非羟基氧原子数比HClO的多,含氧酸中非羟基氧原子数越多,酸性越强,所以磷酸的
酸性强于次氯酸,故D错误;
故选:B。
3. 若不断地升高温度,会实现“雪花 水 水蒸气 氧气和氢气”的转化。在转化的各阶段被
破坏的主要作用依次是
A. 氢键、分子间作用力、非极性键 B. 氢键、氢键、极性键
C. 氢键、极性键、分子间作用力 D. 分子间作用力、氢键、非极性键
【答案】B
【解析】
固态水中和液态水中都含有氢键,“雪花 水 水蒸气”主要是氢键被破坏,属于物理变化,共
价键没有被破坏,“水蒸气 氧气和氢气”为化学变化,破坏的是极性共价键。
综上所述,B项正确。
故选B。
4. 现有T、A、B、C、D、E、F七种前四周期元素,原子序数依次增大。T的原子半径在周期表
中最小,基态A原子s能级上电子总数是p能级上电子总数的2倍,基态C原子的价电子排布
式为 ,D、E位于同主族,且未成对电子数均为0,基态F原子为前四周期元素中未成
对电子数最多的元素,根据以上信息下列说法正确的是
A. 基态F原子占有15种能量不同的原子轨道B. T、A、B可组成一种直线形分子,其中 键和 键数目之比为
C. 分解温度
D. A、B、C的简单氢化物中,最稳定的是C的氢化物,沸点最高的也是C的氢化物
【答案】D
【解析】
T、A、B、C、D、E、F七种前四周期元素中,原子序数依次增大;T的原子半径在周期表中最
小,T为氢元素;基态C原子的价电子排布式为 , ,所以核电荷数为8,C为氧元
素;基态A原子s能级上电子总数是p能级上电子总数的2倍,A为碳元素;D、E位于同主族,且
未成对电子数均为0,D为镁元素,E为钙元素;基态F原子为前四周期元素中未成对电子数最多
的元素,F为铬元素;由于A为碳元素,C为氧元素,所以B为氮元素,
A.基态铬原子核外电子排布式为 ,占有15种原子轨道,但是同一能级的轨道
能量相同,故A错误;
B.T、A、B可组成一种直线形分子HCN,结构式为 ,其中 键和 键数目之比为
,故B错误;
C.碳酸盐的热分解是由于晶体中的阳离子结合碳酸根离子中的氧离子,使碳酸根离子分解为二氧化
碳分子。镁离子半径小于钙离子半径,所以与氧离子形成的离子键较强,晶格能较大,因此碳酸镁
的热分解温度较低,故C错误;
D.A、B、C的简单氢化物分别为 、 、 ;元素的非金属性越强,则对应的氢化物越
稳定,非金属性: ,因此 最稳定;由于水分子间存在氢键,且数目大于氨气,因
此沸点最高,故D正确;
故选D。
5. 液氨是富氢物质,是氢能的理想载体。下列说法不正确的是
A. 分子中氮原子的杂化方式为 杂化
B. 中, 分子是配体
C. 相同压强下, 的沸点比 的沸点低
D. 与 、 、 互为等电子体【答案】C
【解析】
A.氨气分子中氮原子价层电子对个数 ,所以N原子采用 杂化,故A
正确;
B.在 离子中, 提供空轨道,N原子提供孤电子对,所以N原子是配位原子,
分子是配体,故B正确;
C. 和 结构相似且都属于分子晶体,分子晶体的熔沸点随着其相对分子质量的增大而增
大,但氢键能增大物质的沸点,氨气存在分子间氢键,所以相同压强时, 和 比较,氨气
沸点高,故C错误;
D.等电子体为原子数相等和价电子数相等的原子团, 与 、 、 均含有5个原子
团,且价电子数均为8,为等电子体,故D正确;
故选C。
6. 固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。下
图为少量HCl气体分子在 冰表面吸附和溶解过程的示意图。下列叙述错误的是
A. 冰表面第一层中,HCl以分子形式存在
B. 冰表面第二层中, 浓度为 设冰的密度为
C. 冰表面第三层中,冰的氢键网络结构保持不变
D. 冰表面各层之间,均存在可逆反应
【答案】D【解析】
A.由图可知,冰表面第一层中存在HCl分子,则HCl以分子形式存在,故A正确;
B.冰表面第二层中, : :1,设水的体积为1L,溶液体积近似为1L,则 浓度
为 ,故B正确;
C.冰表面第三层中,仍存在 分子,则冰的氢键网络结构保持不变,故C正确;
D.由图可知,只有第二层存在HCl气体分子在冰表面吸附和离解过程,第一、三层不存在,故D错
误。
故选D。
7. 下列说法不正确的是
A. HClO、 、 、 的酸性依次增强
B. 苹果酸 含有1个手性碳原子
C. HCl、 、 均易溶于水的原因之一是与 分子均形成氢键
D. 以极性键结合的分子不一定是极性分子
【答案】C
【解析】
A. HClO、 、 、 分子中非羟基氧原子数依次为:0、1、2、3,含氧酸中非羟
基氧原子个数越多,酸性越强,则HClO、 、 、 的酸性依次增强,故A正
确;
B.苹果酸 中连接羟基的碳原子上连接有4个不同的原子或原子团,是手
性碳原子,故B正确;
C.HCl与水分子之间不能形成氢键,故C错误;
D.含有极性键的分子可能为极性分子,也可为非极性分子,如甲烷是由极性键构成的非极性分子,
故D正确。
故选C。8. 下列关于 、 、 三种物质的说法正确的是
A. 在水中的溶解度很小,是由于其属于极性分子
B. 和 均易溶于水,原因之一是它们都是极性分子
C. 为非极性分子,所以在三种物质中熔、沸点最低
D. 在水中的溶解度很大只是由于 分子为极性分子
【答案】B
【解析】
根据“相似相溶”规律,水是极性分子, 是非极性分子, 和 都是极性分子,故
C 在水中的溶解度很小, 和 均易溶于水,A项错误、B项正确;
C. 在常温下是液体, 和 在常温下是气体,故三种物质中 的熔、沸点最高,C项
错误;
D. 在水中的溶解度很大,除了与 分子为极性分子有关外,还与 分子和 分子之
间可形成氢键有关,D项错误。
9. 某化合物的分子式为 ,A属ⅥA族元素,B属ⅦA族元素,A和B在同一周期,它们的
电负性值分别为 和 ,已知 分子的键角为 。下列推断不正确的是
A. 分子的立体构型为V形
B. 键为极性共价键, 分子为非极性分子
C. 与 相比, 的熔点、沸点比 的低
D. 分子中无氢原子,分子间不能形成氢键,而 分子间能形成氢键
【答案】B
【解析】
根据各元素在周期表中的位置可知,A为O元素,B为F元素,该分子为 ,
A. 分子键角为 ,为V形结构,故A正确;
B. 键为极性共价键, 为V形结构,正负电荷中心不重合,为极性分子,故B错误;
C. 分子之间存在氢键,熔、沸点较高,故C正确;
D. 分子之间存在氢键, 分子中不含有H原子,分子间不能形成氢键,故D正确。
故选B。
10. 胆矾 可写为 ,其结构示意图如下:下列有关胆矾的说法正确的是
A. 的价电子排布式为
B. 所有氧原子都采取 杂化
C. 胆矾中含有的粒子间作用力有离子键、极性键、配位键和氢键
D. 胆矾所含元素中,H、O、S的半径及电负性依次增大
【答案】C
【解析】
A.Cu是29号元素,原子核外电子数为29,Cu原子的核外电子排布式为 ,
失去4s、3d能级上各一个电子生成铜离子,故铜离子价电子电子排布式 ,故A错误;
B.氧原子并不都是 杂化,该结构中的氧原子部分饱和,部分不饱和,杂化方式不同。从现代物
质结构理论出发,硫酸根离子中S和非羟基O之间除了形成1个 键之外,还形成了反馈 键。形
成 键的电子不能处于杂化轨道上,O必须保留未经杂化的p轨道,就不可能都是 杂化,故B
错误;
C.胆矾为离子化合物,含有离子键, 中原子间为极性键, 分子之间有氢键, 和
之间为配位键,故C正确;
D.胆矾所含元素中,H、O、S的半径依次增大,但电负性 ,故D错误。
故选C。
11. 下列关于N、B所形成化合物的结构和性质的叙述正确的是
A. 中N和B的杂化方式不同
B. 熔点: 原子晶体 原子晶体C. 含大 键,形成的大 键的电子由N、B提供
D. 的沸点明显高于 的原因是 分子间形成的氢键更强
【答案】 D
【解析】
A. 中N和B的杂化方式相同,都是 杂化,故A错误;
B.原子半径 ,故原子晶体熔点: 原子晶体 原子晶体 ,故B错误;
C. 含大 键,形成的大 键的电子由每个N原子提供一对电子,B原子不提供电
子,故C错误;
D. 和 都存在分子间氢键,但 分子间氢键更强,故 沸点更高,故D正确。
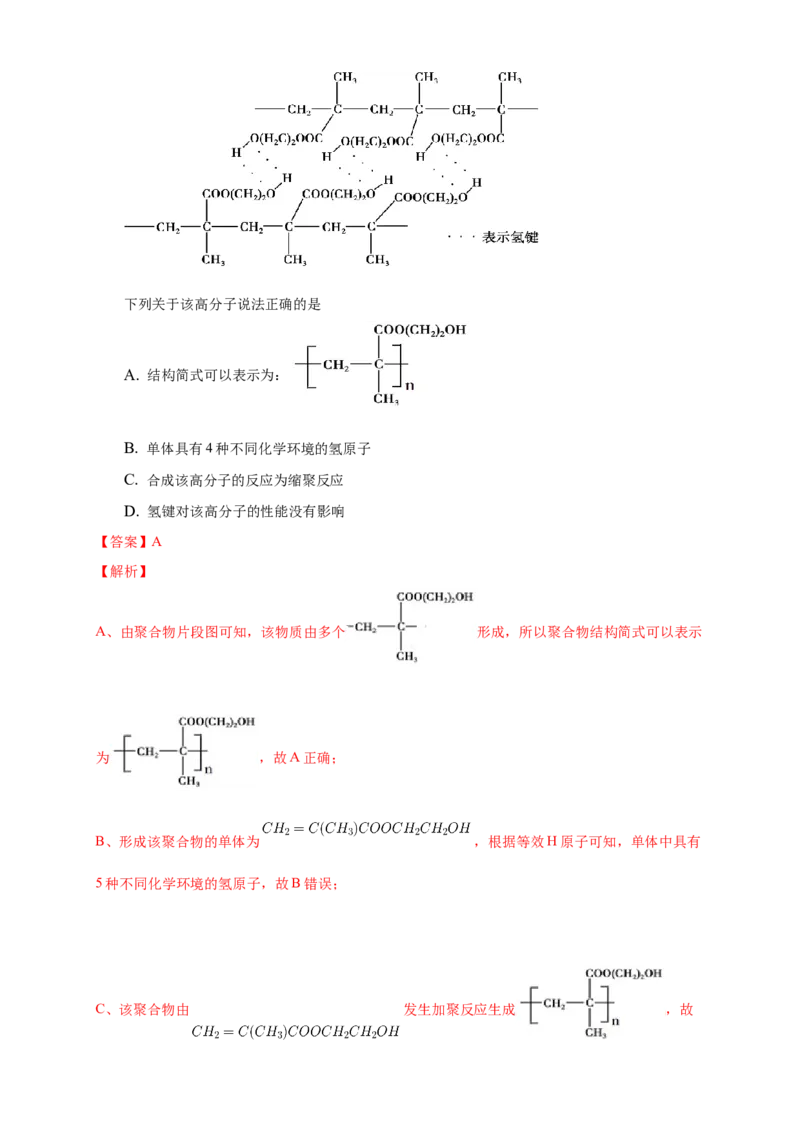
12. 某种用于隐形眼镜材料的聚合物片段如下:下列关于该高分子说法正确的是
A. 结构简式可以表示为:
B. 单体具有4种不同化学环境的氢原子
C. 合成该高分子的反应为缩聚反应
D. 氢键对该高分子的性能没有影响
【答案】A
【解析】
A、由聚合物片段图可知,该物质由多个 形成,所以聚合物结构简式可以表示
为 ,故A正确;
B、形成该聚合物的单体为 ,根据等效H原子可知,单体中具有
5种不同化学环境的氢原子,故B错误;
C、该聚合物由 发生加聚反应生成 ,故C错误;
D、氢键影响高分子的物理性质,如溶解性、熔沸点等,故D错误。
13. “类推”是一种常用的学习方法,但有时会产生错误的结论,下列类推结论中正确的是
A. 沸点高低: ;则沸点高低:
B. 稳定性强弱: ;则稳定性强弱:
C. 干冰 是分子晶体;则 也是分子晶体
D. 晶体中有阴离子,必有阳离子:则晶体中有阳离子,必有阴离子
【答案】B
【解析】
A、因第ⅥA族中,O的非金属性最强,且水中分子之间存在氢键,则水的熔、沸点比其他元素氢
化物的高,故A错误;
B.元素的非金属性越强,稳定性越大,同周期元素从左到右元素的非金属性逐渐增强,则对应的氢
化物的稳定性逐渐增强,故B正确;
C.干冰 是分子晶体,而 为原子晶体,故C错误。
D.金属晶体组成微粒为金属阳离子和自由电子,不含阴离子,故D错误;
故选:B。
二、填空题
14. 已知N、P同属元素周期表的ⅤA族元素,N在第二周期,P在第三周期, 分子呈三角锥
形,N原子位于锥顶,三个H原子位于锥底, 键间的夹角是 。
分子与 分子的构型关系是________ 填“相同”“相似”或“不相似” ,
________ 填“有”或“无” 键, 分子是________ 填“极性”或“非极性” 分
子。
和 相比,热稳定性更强的是________,原因是
____________________________________。和 在常温、常压下都是气体,但 比 易液化,其主要原因是________。
A.键的极性 比 强
B.分子的极性 比 强
C.相对分子质量 比 大
D. 分子之间存在特殊的分子间作用力
【答案】 相似;有;极性;
; 分子中 键键能比 分子中的 键键能大;
。
【解析】
分子中N原子形成3个 键,N原子有1对孤对电子对,空间构型为三角锥型,氮
原子和磷原子结构相似,所以分子的构型关系为相似, 键为极性键, 分子空间构型为
三角锥型,正负电荷重心不重合,是极性分子,故答案为:相似;有;极性;
氮的原子半径比磷的原子半径小, 键长比 键长短,键能更大,分子更稳定,所以
热稳定性更强,故答案为: ; 分子中 键键能比 分子中的 键键能
大;
比 易液化,其主要原因是 分子之间存在氢键, 分子之间为范德华力,氢键
作用比范德华力强,与键的极性、相对分子质量无关,故答案为:D。
15. 含碳元素的物质是化学世界中最庞大的家族。回答下列问题:
碳在形成化合物时,其键型以共价键为主, 中的化学键从形成的过程来看属于____
填“ ”或“ ” 键,从其极性来看属于__________ 填“极性”或“非极性” 键。
和 分子中属于非极性分子的是__________;与 互为等电子体的阳离子是
__________;与 互为等电子体的阴离子是__________。有机物 中含氧官能团的名称为__________,其中含有__________个
手性碳原子。
甲醇与乙烷的相对分子质量和范德华力均相近,但是二者的沸点相差很大,造成该差异的
原因是______________________________。
【答案】 ;极性
、 ; ; 羧基;1
甲醇分子间存在氢键,因此其沸点远高于乙烷
【解析】
个 分子中含有四个 共价键,单键为 键,从共价键的极性来看属于极性键。故答
案为: ;极性;
和 结构对称,分子中正负电荷重心重叠,都为非极性分子; 的原子总数为5、价
电子总数为8,用替代法,与 互为等电子体的阳离子为 ; 的原子总数为3、价电子
总数为16,用替代法,与 互为等电子体的阴离子为 等。故答案为: 、 ;
; ;
有机物 中含氧官能团的名称为羧基,连有四个不同基团的碳原子形象地
称为手性碳原子 常以 标记手性碳原子 ,根据结构简式可知,该化合物中含有1个手性碳原子;
故答案为:羧基;1;
甲醇分子间存在氢键,会使其沸点远高于乙烷,这样虽然甲醇与乙烷的相对分子质量和范德华
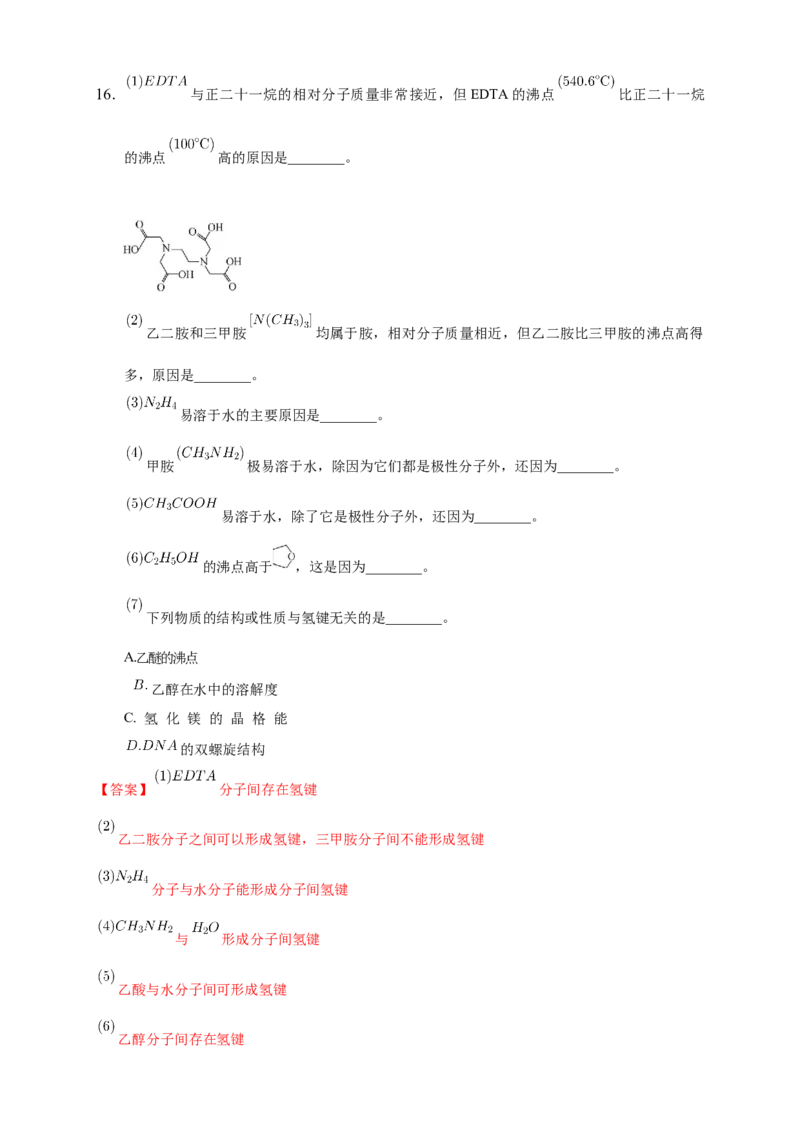
力均相近,但是二者的沸点相差很大;故答案为:甲醇分子间存在氢键,因此其沸点远高于乙烷。16. 与正二十一烷的相对分子质量非常接近,但EDTA的沸点 比正二十一烷
的沸点 高的原因是________。
乙二胺和三甲胺 均属于胺,相对分子质量相近,但乙二胺比三甲胺的沸点高得
多,原因是________。
易溶于水的主要原因是________。
甲胺 极易溶于水,除因为它们都是极性分子外,还因为________。
易溶于水,除了它是极性分子外,还因为________。
的沸点高于 ,这是因为________。
下列物质的结构或性质与氢键无关的是________。
A.乙醚的沸点
乙醇在水中的溶解度
C. 氢 化 镁 的 晶 格 能
的双螺旋结构
【答案】 分子间存在氢键
乙二胺分子之间可以形成氢键,三甲胺分子间不能形成氢键
分子与水分子能形成分子间氢键
与 形成分子间氢键
乙酸与水分子间可形成氢键
乙醇分子间存在氢键【解析】 羧基中的羟基之间可以形成氢键,故而沸点提高。
乙二胺中有和N原子相连的H原子,能形成分子间氢键,而三甲胺 不能形成分子间
氢键
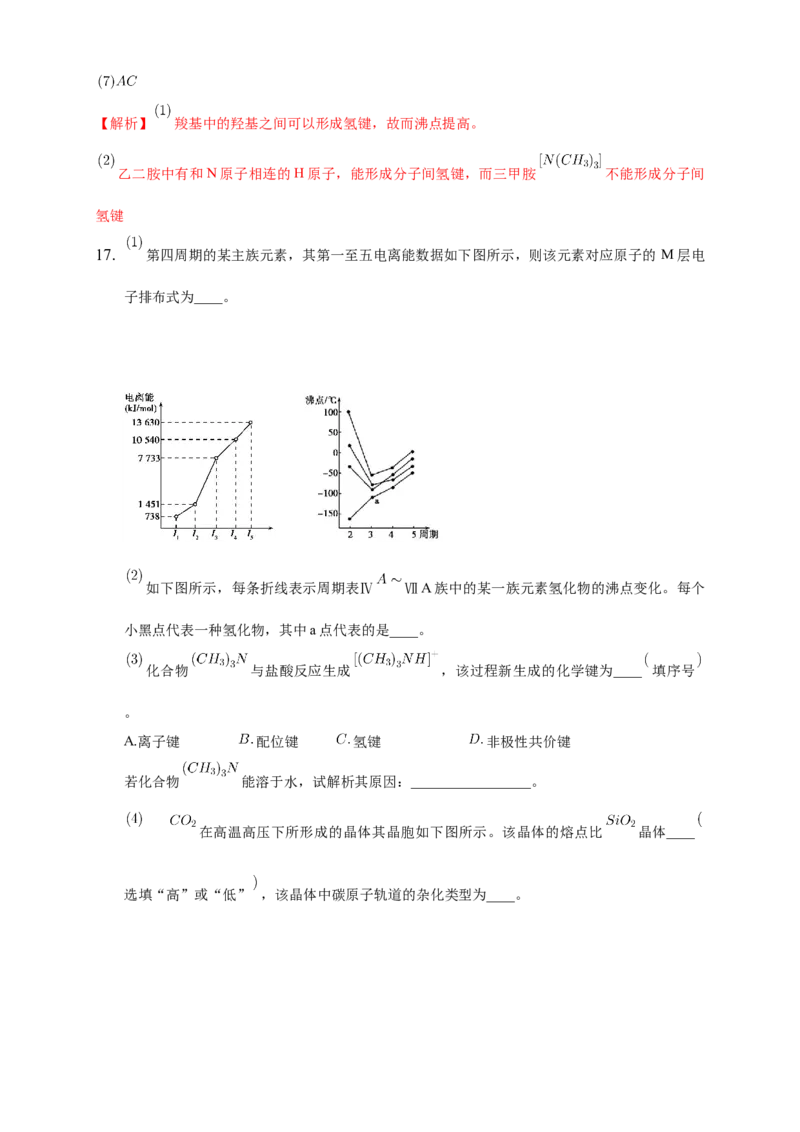
17. 第四周期的某主族元素,其第一至五电离能数据如下图所示,则该元素对应原子的 M层电
子排布式为____。
如下图所示,每条折线表示周期表Ⅳ ⅦA族中的某一族元素氢化物的沸点变化。每个
小黑点代表一种氢化物,其中a点代表的是____。
化合物 与盐酸反应生成 ,该过程新生成的化学键为____ 填序号
。
A.离子键 配位键 氢键 非极性共价键
若化合物 能溶于水,试解析其原因:_________________。
在高温高压下所形成的晶体其晶胞如下图所示。该晶体的熔点比 晶体____
选填“高”或“低” ,该晶体中碳原子轨道的杂化类型为____。等的水合离子是否有颜色与原子结构有关,且存在一定的规律。试推断 的水合
离子为__________ 填“有”或“无” 色离子,依据是__________________。
离子
水合离子颜色 无色 紫红色浅绿色 蓝色 无色
【答案】
;化合物 为极性分子且可与水分子间形成氢键
高; 杂化
有; 的3d轨道上有未成对电子
【解析】略