文档内容
第三章 晶体结构与性质
第二节 金属晶体与离子晶体
第一课时 金属晶体
一.选择题
1.关于金属性质和原因的描述不正确的是( )
A. 金属一般具有银白色光泽,是物理性质,与金属键没有关系
B. 金属具有良好的导电性,是因为在金属晶体中共享了金属原子的价电子,形成了“电子气”,
在外电场的作用下自由电子定向移动便形成了电流,所以金属易导电。
C. 金属具有良好的导热性能,是因为自由电子在受热后,加快了运动速率,自由电子通过与金属
离子发生碰撞,传递了能量
D. 金属晶体具有良好的延展性,是因为金属晶体中的原子层可以滑动而不破坏金属键
2.闪烁着银白色光泽的金属钛( Ti)因具有密度小、强度大、无磁性等优良的机械性能,被广泛地应
22
用于军事、医学等领域,号称“崛起的第三金属”。已知钛有 48Ti、49Ti、50Ti等同位素,下列关于
金属钛的叙述中不正确的是( )
A.上述钛原子中,中子数不可能为22
B.钛元素在周期表中处于第4周期
C.钛的不同同位素在周期表中处于不同的位置
D.钛元素是d区的过渡元素
3.下列关于合金的叙述不正确的是( )
A. 合金的熔点一般比它的各成分金属的熔点低
B. 合金的硬度一般比它的各成分金属的大
C. 合金的性质一般是各成分金属性质的总和
D. 合金在工业上的用途比纯金属更广
4.铝镁合金因坚硬、轻巧、美观、洁净、易于加工而成为新型建筑装潢材料,主要用于制作窗框、
卷帘门、防护栏等。下列性质与这些用途无关的是( )
A. 不易生锈
B. 导电性好
C. 密度小
D. 强度高
5.物质结构理论推出:金属键越强,其金属的硬度越大,熔、沸点越高。且研究表明,一般来说,
金属阳离子半径越小,所带电荷越多,则金属键越强,由此判断下列说法错误的是( )
A. 硬度:Mg>Al B. 熔点:Mg>Ca
C. 硬度:Mg>K D. 熔点:Ca>K6.金属键的强弱与金属原子价电子数的多少有关,价电子数越多金属键越强;与金属阳离子的半径
大小也有关,金属阳离子的半径越大,金属键越弱。据此判断下列选项中金属的熔点逐渐升高的是
( )
A. Li Na K B. Na Mg Al C. Li Be Mg D. Li Na Mg
7.下列金属晶体中,金属键最弱的是( )
A. K B. Na C. Mg D. Al
8.金属键的实质是( )
A. 自由电子与金属阳离子之间的相互作用
B. 金属原子与金属原子间的相互作用
C. 金属阳离子与阴离子的吸引力
D. 自由电子与金属原子之间的相互作用
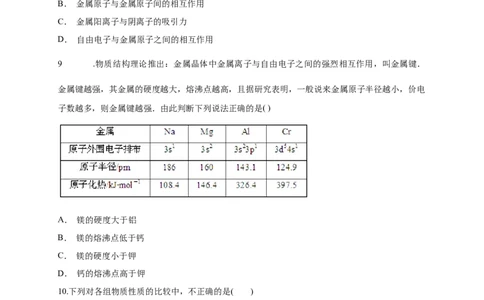
9 .物质结构理论推出:金属晶体中金属离子与自由电子之间的强烈相互作用,叫金属键.
金属键越强,其金属的硬度越大,熔沸点越高,且据研究表明,一般说来金属原子半径越小,价电
子数越多,则金属键越强.由此判断下列说法正确的是( )
A. 镁的硬度大于铝
B. 镁的熔沸点低于钙
C. 镁的硬度小于钾
D. 钙的熔沸点高于钾
10.下列对各组物质性质的比较中,不正确的是( )
A. 熔点:Li>Na>K
B. 导电性:Ag>Cu>Al>Fe
C. 密度:Na﹤Mg﹤Al
D. 空间利用率:体心立方堆积<六方最密堆积<面心立方最密堆积
11.构成金属晶体的微粒是( )
A. 原子 B. 分子 C. 金属阳离子 D. 金属阳离子和自由电子
12.金属晶体的熔沸点之间的差距是由于( )
A. 金属键的强弱不同B. 金属的化合价的不同
C. 金属的晶体中电子数的多少不同
D. 金属的阳离子的半径大小不同
13.下图是金属晶体内部的电气理论示意图
仔细观察并用电气理论解释金属导电的原因是
A. 金属能导电是因为含有金属阳离子
B. 金属能导电是因为含有的自由电子在外电场作用下做定向运动
C. 金属能导电是因为含有电子且无规则运动
D. 金属能导电是因为金属阳离子和自由电子的相互作用
14.两种金属A和B,已知A,B常温下为固态,且A,B属于质软的轻金属,由A,B熔合而成的
合金不可能具有的性质有( )
A. 导电、导热、延展性较纯A或纯B金属强
B. 常温下为液态
C. 硬度较大,可制造飞机
D. 有固定的熔点和沸点
15.金属晶体能传热的原因( )
A. 因为金属晶体的紧密堆积
B. 因为金属键是电子与电子之间的作用
C. 金属晶体中含自由移动的电子
D. 金属晶体中的自由移动的阳离子