文档内容
第三章 晶体结构与性质
第二节 金属晶体与离子晶体
第一课时 金属晶体
在学习了分子晶体、原子晶体之后,本节介绍了有关金属晶体的知识,引导学生比较分子晶
体、原子晶体在晶体结构上的区别和性质上的差异,从晶体结构的微观视角去解释物质的物理性
质。感受科学的魅力。
课程目标 学科素养
1.认识金属晶体的结构和性质。 a. 宏观辨识与微观探析:能从微观的视角来解
释金属晶体的导电性、导热性、延展性等宏观性
2.能利用金属键、“电子气理论”解释金属的
质。
一些物理性质。
教学重点:金属晶体的结构特点与性质之间的关系
教学难点:金属晶体的结构特点与性质之间的关系
多媒体调试、讲义分发
【新课导入】
日常生活中我们一定见过很多金属制品
【设问】
金属都是晶体吗?
【学生回答】
金属(除汞外)在常温下都是晶体。
【讲解】
一、金属晶体
1. 定义:金属原子间通过金属键相互结合形成的
2. 组成微粒:金属阳离子和自由电子
3. 微粒间的作用力:金属键
4. 分类:金属(除汞外)
【点拨】①在金属晶体中,不存在单个分子或原子,金属单质或合金(晶体锗、灰锡除外)属于金属晶体。
②金属晶体是一个“巨分子”。
【过渡】
金属的结构就好像很多硬球一层一层很紧密地堆积,每一个金属原子的周围有较多相同的原子围绕
着。在金属晶体中,原子之间以金属键相互结合。那么,金属键的本质是什么呢?
二、金属键
1.定义:在金属单质晶体中原子之间以金属阳离子与自由电子之间强烈的相互作用。
2.成键粒子:金属阳离子和自由电子。
3.成键条件:金属单质或合金。
4.成键本质
电子气理论:金属原子脱落下来的价电子形成遍布整块晶体的“电子气”,被所有原子共用,从而
把所有金属原子维系在一起,形成像共价晶体一样的“巨分子”。
5.金属键的特征
金属键无方向性和饱和性。
【学生活动】
金属钠的熔点较低、硬度较小,钨是熔点最高的金属、铬是硬度最大的金属, 解释Na、Mg、Al
的熔点依次升高、硬度依次增大的原因。解释原因。
【讲解】
Na、Mg、Al的熔点依次升高、硬度依次增大的原因Na+、Mg2+、Al3+电荷数依次增大,半径依次减
小,金属键依次增强。
【小结】
影响金属键强弱的因素
离子所带的电荷和离子半径,离子所带的电荷越多,离子半径越小,金属键越强,熔沸点越高,硬
度越大。
【学生活动】
有阳离子一定有阴离子?若有阴离子,一定存在阳离子?
【讲解】
在金属晶体中有阳离子,但没有阴离子,所以,晶体中有阳离子不一定有阴离子,若有阴离子,则
一定有阳离子。
【学生活动】
金属有哪些通性?为什么金属具有这些共同的性质?用电子气理论解释金属的物理性质?
【展示】
用多媒体课件展示金属晶体的电子气理论示意图。
【讲解】
金属具有光泽、导电性、导热性、延展性等。金属的通性与金属的结构有关。
电子气理论解释金属的物理性质
(1)金属延展性的解释当金属受到外力作用时,晶体中的各原子层就会发生回相对滑动,但排列方式不变,弥散在金属原
子间的电子气可以起到类似轴承中滚珠之间润滑剂的作用,所以金属有良好的延展性。
【学生活动】
解释合金性能发生变化的原因
当向金属晶体中掺入不同的金属或非金属原子时,就像滚珠之间掺入细小而坚硬的沙土或碎石一
样,会使金属的延展性甚至硬度发生改变。
(2)金属导电性的解释
在金属晶体中,充满着带负电的“电子气”(自由电子),这些电子气的运动是没有一定方向的,
但在外加电场的条件下,自由电子定向运动形成电流,所以金属容易导电。不同的金属导电能力不
同,导电性最强的三中金属是:Ag、Cu、Al。
电子气中的自由电子在热的作用下与金属原子频繁碰撞解释金属的电导率随温度升高而下降。
(3)金属导热性的解释
自由电子移运动时与金属离子相互碰撞,在碰撞过程中发生能量交换。当金属的某一部分受热时,
从区域获得能量的电子会向别处运动并发生碰撞,将能量从温度高的区域传递到温度低的区域,最
后使整块金属的温度趋于一致。金属的导热性可以解释生活中常见的些现象。比如,在冬天我们感
觉金属制品比木制品更凉,原因是当人接触到金属时,金属很快将人体的热量传递出去,因为木制
品不易导热所以当人接触到木制品时,身体的热量不易散失。
(4)有金属光泽的解释
金属晶体内部存在自由电子,当光线投射到金属表面时,自由电子吸收可见光,然后又把各种波长
的光大部分再反射出来,这就使绝大多数金属呈现银灰色或银白色光泽。而金属在粉末状态时,金
属原子的取向杂乱,排列不规则,吸收可见光后不能再反射出来,所以金属粉末常呈暗灰色或黑色
【知识点拨】
①温度越高,金属的导电能力越弱。②合金的熔、沸点比其各成分金属的熔、沸点低。
【本节小结】
本节课掌握金属晶体及电子气理论,并且能够用电子气理论解释金属的通性。
三种晶体类型与性质的比较
晶体类型 原子晶体 分子晶体 金属晶体
构成晶体的粒子 原子 分子 金属阳离子和自由电子分子间作用力(范德华
作用力 共价键 金属键
力和氢键)
组成和结构相似、无
确定作用力强弱
键长(原子半径) 氢键时,比较相对分 原子半径、价电子数
的一般判断方法
子质量
差别较大(汞常温下呈液态,钨
熔沸点 高 低
物 熔点为3 410 ℃)
理
硬度 大 较小 差别较大
性
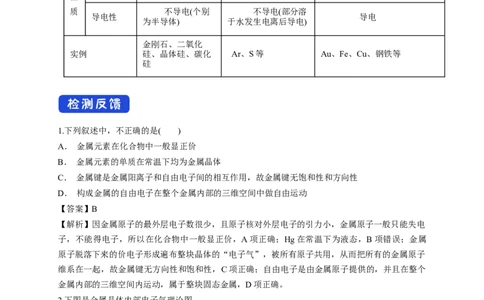
质 不导电(个别 不导电(部分溶
导电性 导电
为半导体) 于水发生电离后导电)
金刚石、二氧化
实例 硅、晶体硅、碳化 Ar、S等 Au、Fe、Cu、钢铁等
硅
1.下列叙述中,不正确的是( )
A. 金属元素在化合物中一般显正价
B. 金属元素的单质在常温下均为金属晶体
C. 金属键是金属阳离子和自由电子间的相互作用,故金属键无饱和性和方向性
D. 构成金属的自由电子在整个金属内部的三维空间中做自由运动
【答案】B
【解析】因金属原子的最外层电子数很少,且原子核对外层电子的引力小,金属原子一般只能失电
子,不能得电子,所以在化合物中一般显正价,A项正确;Hg在常温下为液态,B项错误;金属
原子脱落下来的价电子形成遍布整块晶体的“电子气”,被所有原子共用,从而把所有的金属原子
维系在一起,故金属键无方向性和饱和性,C项正确;自由电子是由金属原子提供的,并且在整个
金属内部的三维空间内运动,属于整块固态金属,D项正确。
2.下图是金属晶体内部电子气理论图
电子气理论可以用来解释金属的性质,其中正确的是( )
A. 金属能导电是因为金属阳离子在外加电场作用下定向移动
B. 金属能导热是因为自由电子在热的作用下相互碰撞,从而发生热的传导
C. 金属具有延展性是因为在外力的作用下,金属阳离子各层间会出现相对滑动,但自由电子可以
起到润滑的作用,使金属不会断裂D. 合金与纯金属相比,由于增加了不同的金属或非金属,使电子数目增多,所以合金的延展性比
纯金属强,硬度比纯金属小
【答案】C
【解析】金属能导电是因为自由电子在外加电场作用下定向移动,A项错误;金属能导热是因为自
由电子在热的作用下与金属阳离子碰撞,从而发生热的传导,B项错误;合金与纯金属相比,由于
增加了不同的金属或非金属,相当于填补了金属阳离子之间的空隙,所以一般情况下合金的延展性
比纯金属弱,硬度比纯金属大,D项错误。
3.金属晶体具有延展性的原因( )
A. 金属键很微弱
B. 金属键没有饱和性
C. 密堆积层的阳离子容易发生滑动,但不会破坏密堆积的排列方式,也不会破坏金属键
D. 金属阳离子之间存在斥力
【答案】C
【解析】金属键没有方向性,当金属受外力作用时,金属原子之间发生相对滑动,各层金属原子之
间仍保持金属键的作用。因此,在一定强度的外力作用下,金属可以发生形变,表现出良好的延展
性。
4.金属晶体的形成是因为晶体中存在( )
①金属原子 ②金属阳离子 ③自由电子 ④阴离子
A. 只有① B. 只有③ C. ②③ D. ②④
【答案】C
【解析】形成金属晶体的粒子是金属阳离子和自由电子。
5.下列叙述正确的是( )
A. 金属受外力作用时常常发生变形而不易折断,是由于金属原子之间有较 强的作用
B. 通常情况下,金属里的自由电子会发生定向移动而形成电流
C. 金属是借助自由电子的运动,把能量从温度高的部分传到温度低的部分
D. 金属的导电性随温度的升高而减弱
【答案】D
【解析】 金属受外力作用时常常发生变形而不易折断,是因为金属晶体中金属阳离子与自由电子
存在较强作用各原子层会发生相对滑动,但不会改变原来的排列方式,故A项不正确;金属里的自
由电子要在外力作用下才能发生定向移动产生电流,故B项不正确;金属的导热性是由于自由电子
碰撞金属离子将能量进行传递,故C项不正确。
本节课学生掌握金属晶体的结构和性质。能够利用金属键、“电子气理论”解释金属的一些物
理性质。提升学生宏观辨识与微观探析的科学素养。