文档内容
3.3.2 离子晶体、过渡晶体与混合型晶体(导学案)
1. 知道介于典型晶体之间的过渡晶体及混合型晶体。
2. 了解晶体类型的比较与判断方法。
重点:过渡晶体与混合型晶体的结构与物理性质。
难点:过渡晶体与混合型晶体的结构与物理性质。
1.过渡晶体与混合型晶体
(1)过渡晶体
典型晶体包括分子晶体、共价晶体、金属晶体和离子晶体。事实上,纯粹的典型晶体
是 ,大多数晶体是它们之间的 ,当某晶体中的离子键成分大于共价键成
分时,通常当作 来处理,当离子键成分小于共价键成分时,通常当作 来
处理,当离子键成分接近于共价键成分时我们称之为过渡晶体;四类晶体都有 。
(2)混合型晶体——石墨
石墨的结构特点及晶体类型
石墨晶体中,既有共价键,又有类似 的作用力,还有 ,属于
。
1.判断正误,正确的画“√”,错误的画“×”。
(1)纯粹的典型晶体是没有的( )
(2)离子键成分的百分数是依据电负性的差值计算出来的,差值越大,离子键成分的百分数越小( )
(3)在共价晶体中可以认为共价键贯穿整个晶体,而在分子晶体中共价键仅限于晶体微
观空间的一个个分子中( )
(4)四类晶体都有过渡型( )
(5)石墨的二维结构内,每个碳原子的配位数为3( )
(6)石墨的导电只能沿石墨平面的方向进行( )
(7)石墨晶体层与层之间距离较大,所以石墨的熔点不高( )
2.下列说法中正确的是( )
A.形成离子键的阴、阳离子间只存在静电吸引力
B.第ⅠA族元素与第ⅦA族元素形成的化合物一定是离子化合物
C.离子晶体的熔点一定比共价晶体的熔点高
D.离子晶体中可能只含有非金属元素
3.下列关于氯化铯晶体的叙述不正确的是 ( )
A.1 mol氯化铯中有6.02×1023个CsCl分子
B.氯化铯晶体中,每个Cs+周围与它最近且等距离的Cs+有6个
C.氯化铯晶体中,Cs+和Cl-的配位数都是8
D.每个晶胞中平均含有1个Cs+和1个Cl-
4. 石墨晶体是层状结构(如图)。以下有关石墨晶体的说法正确的一组是( )
①石墨中存在两种作用力;②石墨是混合型晶体;③石墨中的C为sp2杂
化;④石墨的熔、沸点都比金刚石低;⑤石墨中碳原子数和C—C键数之
比为1∶2;⑥石墨和金刚石的硬度相同;⑦石墨层内导电性和层间导电
性不同;⑧每个六元环完全占有的碳原子数是2
A.全对 B.除⑤外
C.除①④⑤⑥外 D.除⑥⑦⑧外
5.同类晶体物质熔、沸点的变化是有规律的,试分析下列两组物质熔点规律性变化的原
因:
A组物质 NaCl KCl CsCl
熔点/K 1074 1049 918
B组物质 Na Mg Al
熔点/K 370 922 933
晶体熔、沸点的高低,取决于组成晶体微粒间的作用力的大小。A组物质是________晶
体,晶体中微粒之间通过________相连。B组物质是________晶体,价层电子数由少到多
的顺序是________,粒子半径由大到小的顺序是________。考点1过渡晶体
1.石墨晶体的结构
石墨晶体具有层状结构(如图所示),每个碳原子用sp2杂化轨道与邻
近的3个碳原子以共价键相结合,形成无限的六边形平面网状结构;每个
碳原子还有1个与碳环平面垂直的未参与杂化的2p轨道,并含有1个未
成对电子,因此能够形成遍及整个平面的大π键。正是由于电子可以在整
个六边形网状平面上运动,因此石墨的大π键具有金属键的性质,这就是石墨沿层的平行
方向导电性强的原因。这些网络状的平面结构以范德华力结合形成层状结构,这样,石墨
晶体中既有共价键,又有范德华力,同时还有类似金属键的作用力。因此石墨晶体是一种
混合型晶体。
在石墨晶体中,每个碳原子参与了3个C—C键的形成,每个C—C键被2个碳原子共
用,每个碳原子被3个正六边形共用,故每个正六边形平均占有的碳原子数为6×=2,碳
原子个数与C—C键键数之比为1∶(3×)=2∶3。
2.石墨晶体独特的性质
(1)导电性:石墨有导电性,而且由于相邻碳原子平面相隔较远,电子不能从一个平面
跳跃到另一个平面,所以石墨的导电性只能沿着石墨平面的方向。
(2)润滑性:石墨晶体层与层之间存在范德华力,结合力弱,层与层之间可发生相对滑
动,使之具有润滑性。可用作润滑剂、铅笔笔芯等。
(3)石墨的熔、沸点很高,石墨的熔点比金刚石还高。
中科院的科学家已研制出一种高性能超级电容器电极材料——氮掺杂有序介孔石墨
烯,该材料可用作电动车的“超强电池”,充电只需7秒钟,即可续航35公里。下面有关
石墨晶体的说法错误的是( )
A.石墨晶体中既有共价键又有分子间作用力
B.石墨晶体熔、沸点很高,硬度很大
C.石墨晶体中每个六边形平均含2个完整碳原子D.石墨晶体中,每个C原子被3个六元环共用
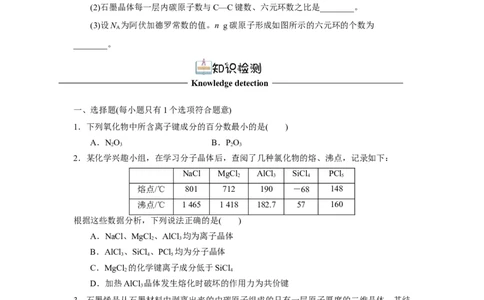
石墨的片层结构如图所示,请回答下列问题。
(1)一个六元环实际含有________个碳原子。
(2)石墨晶体每一层内碳原子数与C—C键数、六元环数之比是________。
(3)设N 为阿伏加德罗常数的值。n g碳原子形成如图所示的六元环的个数为
A
________。
一、选择题(每小题只有1个选项符合题意)
1.下列氧化物中所含离子键成分的百分数最小的是( )
A.NO B.PO
2 3 2 3
2.某化学兴趣小组,在学习分子晶体后,查阅了几种氯化物的熔、沸点,记录如下:
NaCl MgCl AlCl SiCl PCl
2 3 4 5
熔点/℃ 801 712 190 -68 148
沸点/℃ 1 465 1 418 182.7 57 160
根据这些数据分析,下列说法正确的是( )
A.NaCl、MgCl 、AlCl 均为离子晶体
2 3
B.AlCl 、SiCl 、PCl 均为分子晶体
3 4 5
C.MgCl 的化学键离子成分低于SiCl
2 4
D.加热AlCl 晶体发生熔化时破坏的作用力为共价键
3
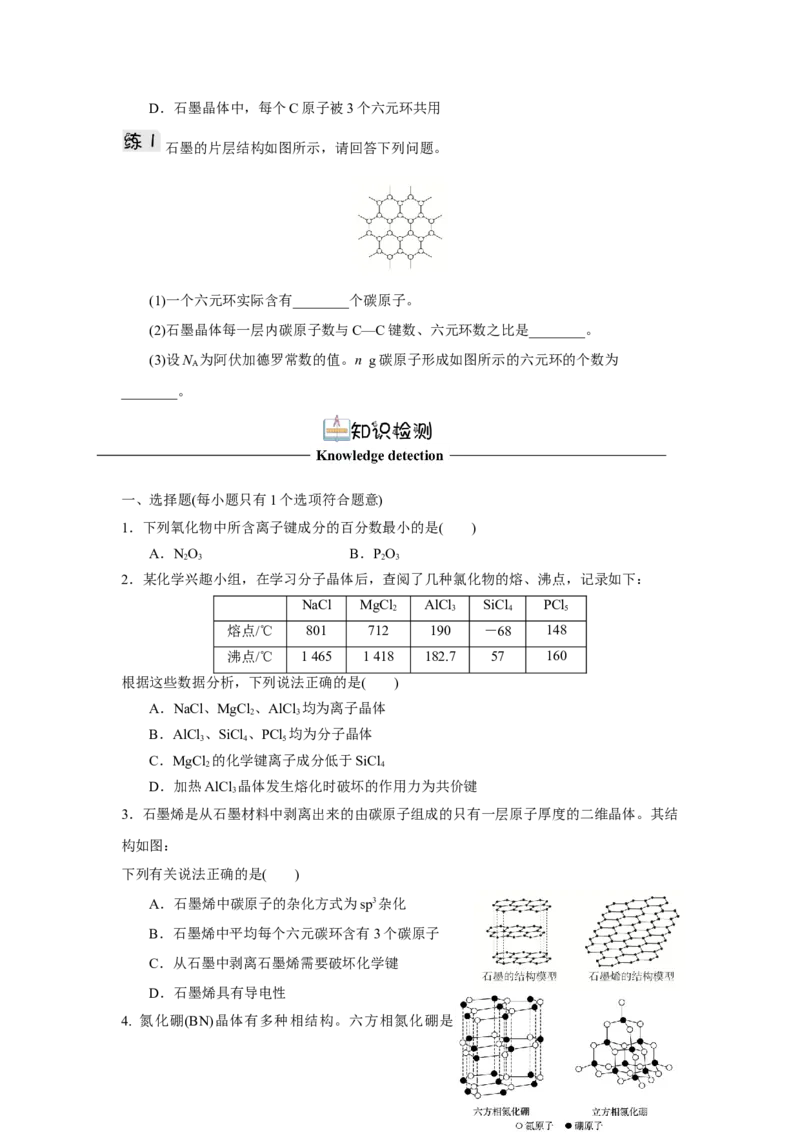
3.石墨烯是从石墨材料中剥离出来的由碳原子组成的只有一层原子厚度的二维晶体。其结
构如图:
下列有关说法正确的是( )
A.石墨烯中碳原子的杂化方式为sp3杂化
B.石墨烯中平均每个六元碳环含有3个碳原子
C.从石墨中剥离石墨烯需要破坏化学键
D.石墨烯具有导电性
4. 氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂;立方相氮化硼是超硬
材料,有优异的耐磨性。它们的晶体结构如图所示,下列关于这两种晶体的说法正确的是(
)
A.六方相氮化硼与石墨一样可以导电
B.立方相氮化硼含有σ键和π键,所以硬度大
C.两种晶体均为分子晶体
D.六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间结构为平面三角形
5.下表给出几种氯化物的熔点和沸点:
NaCl AlCl SiCl
3 4
熔点/℃ 801 190 -70
沸点/℃ 1413 180 57.57
有关表中所列三种氯化物的性质,以下叙述正确的是( )
①氯化铝在加热时能升华
②四氯化硅在晶态时属于分子晶体
③氯化钠晶体中粒子之间以范德华力结合
④氯化铝晶体属于离子晶体
A.②③ B.③④
C.①② D.①②③④
6. 石墨烯是只由一层碳原子所构成的平面薄膜,其结构模型如图所 示。
下列有关说法错误的是( )
A.晶体中碳原子间全部是碳碳单键
B.石墨烯与石墨都是碳的同素异形体
C.石墨烯中所有碳原子可以处于同一个平面
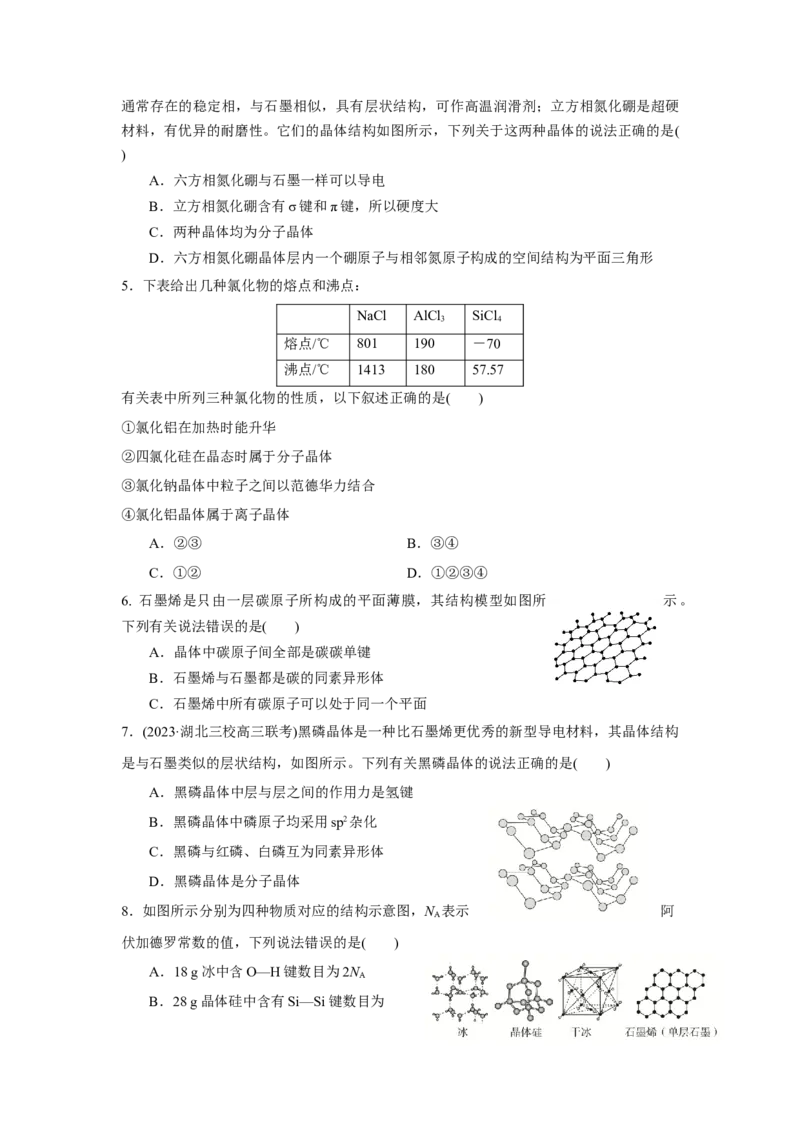
7.(2023·湖北三校高三联考)黑磷晶体是一种比石墨烯更优秀的新型导电材料,其晶体结构
是与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是( )
A.黑磷晶体中层与层之间的作用力是氢键
B.黑磷晶体中磷原子均采用sp2杂化
C.黑磷与红磷、白磷互为同素异形体
D.黑磷晶体是分子晶体
8.如图所示分别为四种物质对应的结构示意图,N 表示 阿
A
伏加德罗常数的值,下列说法错误的是( )
A.18 g冰中含O—H键数目为2N
A
B.28 g晶体硅中含有Si—Si键数目为2N
A
C.44 g干冰中含有N 个晶胞结构单元
A
D.石墨烯是碳原子单层片状新材料,12 g石墨烯中含C—C键数目为1.5N
A
9.经X射线研究证明,PCl 在固体时,由空间结构分别是正四面体和正八面体的两种离子
5
构成,下列关于PCl 的推断正确的是( )
5
A.PCl 固体是分子晶体
5
B.PCl 晶体由PCl和PCl构成,且离子数目之比为1∶1
5
C.PCl 晶体具有良好的导电性
5
D.PCl 晶体由PCl和PCl构成,且离子数目之比为1∶1
5
二、非选择题
10.碳元素的单质有多种形式,如图所示,依次是C 、石墨和金刚石的结构图:
60
回答下列问题:
(1)金刚石、石墨、C 、碳纳米管等都是碳元素的单质形式,它们互为__________。
60
(2)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为________、________。
(3)C 属于________晶体,石墨属于________晶体。
60
(4)石墨晶体中,层内C—C键的键长为142 pm,而金刚石中C—C键的键长为154
pm。其原因是金刚石中只存在C—C间的________共价键,而石墨层内的C—C间不仅存
在________共价键,还有________键。
11.填写下列空白:
(1)GaF 的熔点高于1000 ℃,GaCl 的熔点为77.9 ℃,其原因是
3 3
________________________________。
(2)A、B、C、D为原子序数依次增大的四种短周期元素,A2-和B+具有相同的电子层
结构;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个
未成对电子。回答下列问题:
①单质A有两种同素异形体,其中沸点较高的是________(填分子式),原因是
______________________________________;
②A和B的氢化物所属的晶体类型分别为________和________;二者熔点高低顺序为________(化学式);
③B与D形成化合物的晶体类型是______________。
12.近年来,新能源汽车不断得到推广,其所用能源为锂电池。其中钴酸锂、磷酸铁锂等
正极材料研究不断在发展。回答下列问题:
(1)基态钴原子价层电子排布式为________。
(2)PO中心原子的价层电子对数为__________、杂化轨道类型为________,PO的空间
结构为________。
(3)H O与NH 的键角比较:HO________NH(填“>”“<”或“=”),分析原因:
2 3 2 3
__________________________________________________________________________
。
(4)以下表格中的氧化物的熔点缺乏数据:
氧化物 PO SO LiO MgO
4 6 2 2
熔点/℃
请根据所学知识比较它们的熔点相对大小,并解释表中氧化物之间熔点差异的原因:
_____________________________________________________________
_______________________________________________________________________________
____________________________________________。
(5)Li O具有反萤石结构,晶胞如图所示。已知晶胞参数为466.5 pm,设阿伏加德罗常
2
数的值为N ,则LiO的密度为____________________g·cm-3(列出计算式)。
A 2