文档内容
第三章 晶体结构与性质
第四节 配合物与超分子
一.选择题
1.若X、Y两种粒子之间可形成配位键,则下列说法正确的是( )
A. X、Y只能是分子
B. X、Y只能是离子
C. 若X提供空轨道,则Y至少要提供一对孤电子对
D. 若X提供空轨道,则配位键表示为X→Y
【答案】C
【解析】形成配位键的两种微粒可以均是分子或者均是离子,还可以一种是分子、一种是离子,但
必须是一种微粒提供空轨道、另一种微粒提供孤电子对,A、B项错误,C项正确;配位键中箭头
应该指向提供空轨道的X,D项错误。
2.某溶液显红色,则该溶液中含有大量的( )
A. [Cu(NH )]2+ B. Fe(SCN) C. [Al(OH)]- D. [Ag(NH )]OH
3 4 3 4 3 2
【答案】B
【解析】[Cu(NH ) ]2+在溶液中呈深蓝色,[Al(OH) ]-、[Ag(NH ) ]OH在溶液中均无色,B
3 4 4 3 2
项正确。
3.酞菁钴近年来被广泛应用于光电材料、非线性光学材料、催化剂等方面。酞菁钴的熔点约为 163
℃,其结构如图所示(部分化学键未画明)。下列说法正确的是( )
A. 酞菁钴中三种非金属元素的电负性大小顺序为N>H>C
B. 酞菁钴中碳原子的杂化方式有sp2杂化和sp3杂化两种
C. 与Co(Ⅱ)通过配位键结合的是2号和4号N原子
D. 酞菁钴一定是离子晶体
【答案】C
【解析】电负性大小顺序为N>C>H,A项错误;酞菁钴中碳原子均形成3个σ键,没有孤电子对,
均采取sp2杂化,B项错误;N原子形成3个共价键即可达到8电子稳定结构,所以2号和4号N原
子与Co(Ⅱ)通过配位键结合,C项正确;从酞菁钴的熔点来看,酞菁钴应该属于分子晶体,D项错误。
4.下列关于[Cr(H O) Br ]Br·2H O的说法正确的是( )
2 4 2 2
A. 配体为水分子,外界为Br-
B. 中心离子的配位数为6
C. 中心离子采取sp3杂化
D. 中心离子的化合价为+2
【答案】B
【解析】[Cr(H O) Br ]Br·2H O中内界为[Cr(H O) Br ]+,Cr3+为中心离子,配体为HO、Br-,配位
2 4 2 2 2 4 2 2
数为6,外界为Br-,Cr3+提供的空轨道数为6,中心离子没有采取sp3杂化。
5.0.01 mol氯化铬(CrCl ·6H O)在水溶液中用过量的AgNO 处理,产生0.01 mol AgCl沉淀,此氯化
3 2 3
铬最可能是( )
A. [Cr(H O) ]Cl B. [Cr(H O) Cl]Cl ·H O
2 6 3 2 5 2 2
C. [Cr(H O) Cl]Cl·2HO D. [Cr(H O) Cl]·3H O
2 4 2 2 2 3 3 2
【答案】C
【解析】0.01 mol氯化铬(CrCl ·6H O)在水溶液中用过量的AgNO 处理,产生0.01 mol AgCl沉淀,
3 2 3
说明1 mol氯化铬(CrCl ·6H O)中有1 mol氯离子在外界,其余在内界,而正三价铬为六配位,则此
3 2
氯化铬最可能是[Cr(H O) Cl]Cl·2HO,C正确。
2 4 2 2
6.配位化合物的数量巨大,组成和结构形形色色。配合物[Cu(NH )](OH) 的中心离子、配体、中心
3 4 2
离子的化合价和配位数分别为( )
A. Cu2+、NH 、+2、4 B. Cu+、NH 、+1、4
3 3
C. Cu2+、OH-、+2、2 D. Cu2+、NH 、+2、2
3
【答案】A
【解析】配合物[Cu(NH )](OH) 中,Cu2+为中心离子,化合价为+2,配体为NH ,配位数为4。
3 4 2 3
7.已知某紫色配合物的组成为CoCl ·5NH ·H O,其水溶液显弱酸性,加入强碱加热至沸腾有NH 放
3 3 2 3
出,同时产生Co O 沉淀;向一定量该配合物溶液中加过量AgNO 溶液,有AgCl沉淀生成,待沉
2 3 3
淀完全后过滤,再加过量AgNO 溶液于滤液中,无明显变化,但加热至沸腾又有AgCl沉淀生成,
3
且第二次沉淀量为第一次沉淀量的二分之一。则该配合物的化学式最可能为( )
A. [CoCl (NH )]Cl·NH ·H O B. [Co(NH )(H O)]Cl
2 3 4 3 2 3 5 2 3
C. [CoCl(NH )(H O)]Cl ·2NH D. [CoCl(NH )]Cl ·H O
3 3 2 2 3 3 5 2 2
【答案】D
【解析】CoCl ·5NH ·H O的水溶液显弱酸性,加入强碱加热至沸腾有 NH 放出,说明NH 均在内
3 3 2 3 3
界,向该配合物溶液中加过量AgNO 溶液,有AgCl沉淀生成,说明该配合物外界有Cl-,过滤后
3
再加过量AgNO 溶液于滤液中无变化,但加热至沸腾又有AgCl沉淀生成,且第二次沉淀量为第一
3次沉淀量的二分之一,说明该配合物内界也含有Cl-,且外界的Cl-与内界的Cl-个数之比为2∶1。
综上分析,D项最有可能。
8.向盛有少量CuCl 溶液的试管中滴入少量NaOH溶液,再滴入适量浓氨水,下列叙述不正确的是(
2
)
A. 开始生成蓝色沉淀,加入适量浓氨水后,形成无色溶液
B. Cu(OH) 溶于浓氨水的离子方程式是:Cu(OH) +4NH ===[Cu(NH )]2++2OH-
2 2 3 3 4
C. 开始生成蓝色沉淀,加入适量浓氨水后,沉淀溶解形成深蓝色溶液
D. 开始生成Cu(OH) ,之后生成更稳定的配合物
2
【答案】A
【解析】向CuCl 溶液中加入少量NaOH溶液,发生反应Cu2++2OH-===Cu(OH) ↓,Cu(OH) 沉淀
2 2 2
为蓝色,再加入适量浓氨水,发生反应Cu(OH) +4NH ===[Cu(NH )]2++2OH-,形成深蓝色溶液,
2 3 3 4
故A错误。
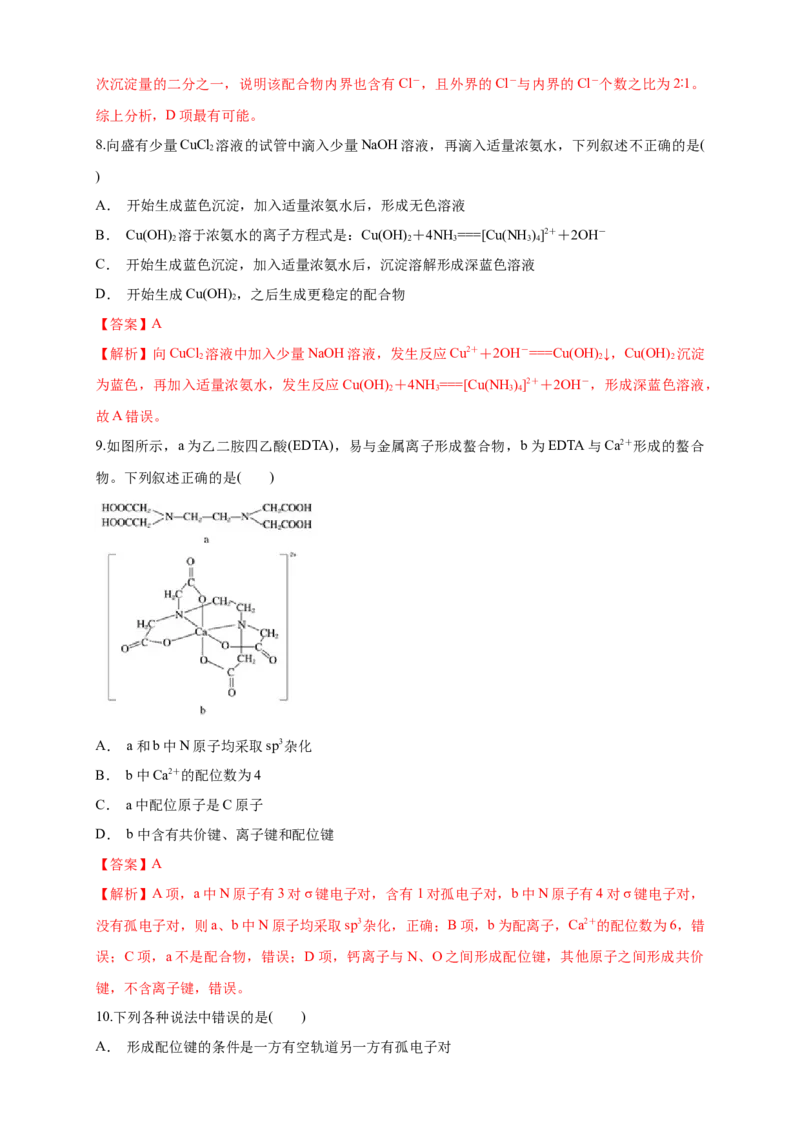
9.如图所示,a为乙二胺四乙酸(EDTA),易与金属离子形成螯合物,b为EDTA与Ca2+形成的螯合
物。下列叙述正确的是( )
A. a和b中N原子均采取sp3杂化
B. b中Ca2+的配位数为4
C. a中配位原子是C原子
D. b中含有共价键、离子键和配位键
【答案】A
【解析】A项,a中N原子有3对σ键电子对,含有1对孤电子对,b中N原子有4对σ键电子对,
没有孤电子对,则a、b中N原子均采取sp3杂化,正确;B项,b为配离子,Ca2+的配位数为6,错
误;C项,a不是配合物,错误;D项,钙离子与N、O之间形成配位键,其他原子之间形成共价
键,不含离子键,错误。
10.下列各种说法中错误的是( )
A. 形成配位键的条件是一方有空轨道另一方有孤电子对B. 配位键是一种特殊的共价键
C. NH NO 、HSO 都含有配位键
4 3 2 4
D. 共价键的形成条件是成键原子必须有未成对电子
【答案】D
【解析】配位键是成键的两个原子一方提供孤电子对,另一方提供空轨道而形成的共价键,可见成
键双方都不存在未成对电子,故A,B对,D错;NH NO 、HSO 中的NH、SO含有配位键,故C
4 3 2 4
对。
11.对配合物[Cu(NH )]SO 的叙述,错误的是( )
3 4 4
A. Cu2+和NH 之间以配位键结合
3
B. [Cu(NH )]2+和SO 2-之间以离子键结合
3 4 4
C. Cu2+和NH 之间以离子键结合
3
D. [Cu(NH )]SO 在水中全部电离成[Cu(NH )]2+和SO 2-
3 4 4 3 4 4
【答案】C
【解析】A.该配合物中氮原子提供孤电子对,所以氨气分子是配位体,铜离子提供空轨道,
Cu2+和NH 之间以配位键结合,故A正确;
3
B.[Cu(NH )]SO 中外界是SO 2﹣,內界是[Cu(NH )]2+,以离子键结合,故B正确;
3 4 4 4 3 4
C.该配合物中,铜离子提供空轨道,是中心离子,氮原子提供孤电子对,氨气分子是配位体,
Cu2+和NH 之间以配位键结合,故C错误;
3
D.[Cu(NH )]SO 中外界是 SO 2﹣,內界是[Cu(NH )]2+,以离子键结合,水中全部电离成
3 4 4 4 3 4
[Cu(NH )]2+和SO 2﹣,故D正确;
3 4 4
12..下列不属于配合物的是( )
A. [Cu(HO)]SO •H O B. [Ag(NH )]OH
2 4 4 2 3 2
C. KAl(SO )•12H O D. Na[Al(OH)]
4 2 2 4
【答案】C
【解析】A.该物质中,铜离子提供空轨道、水分子中氧原子提供孤电子对而形成配位键,所以该
物质属于配合物,故A不选;
B.该物质中,银离子提供空轨道、NH3中氮原子提供孤电子对而形成配位键,所以该物质属于配
合物,故B不选;
C.KAl(SO ) •12H O属于一般化合物,不含配体,所以 KAl(SO ) •12H O不属于配合物,故
4 2 2 4 2 2
C选;
D.Na[Al(OH) ]中铝原子提供空轨道,氢氧根离子提供孤电子对,所以该物质属于配合
4
物,故D不选;13.向下列配合物的水溶液中加入AgNO 溶液不能生成AgCl沉淀的是( )
3
A. [Co(NH )Cl]Cl B. [Co(NH )Cl]
3 4 2 3 3 3
C. [Co(NH )]Cl D. [Co(NH )Cl]Cl
3 6 3 3 5 2
【答案】B
【解析】A.[Co(NH )Cl]Cl中有阴离子氯离子,所以能和硝酸银反应生成氯化银沉淀,故 A错
3 4 2
误;
B.[Co(NH )Cl]中没有阴离子氯离子,所以不能和硝酸银反应生成氯化银沉淀,故B正确;
3 3 3
C.[Co(NH )]Cl 中有阴离子氯离子,所以能和硝酸银反应生成氯化银沉淀,故C错误;
3 6 3
D.[Co(NH )Cl]Cl 中有阴离子氯离子,所以能和硝酸银反应生成氯化银沉淀,故D错误.
3 5 2
二、填空题
14.回答下列问题:
(1)若BCl 与XY 通过B原子与X原子间的配位键结合形成配合物,则该配合物提供孤电子对的
3 n
原子是 。
(2)NH 与BF 可以通过配位键形成NH ·BF , 原子提供孤电子对, 原子提供空轨
3 3 3 3
道。写出NH ·BF 的结构式,并用“→”表示出配位键 。
3 3
(3)肼(NH )分子可视为NH 分子中的一个氢原子被—NH (氨基)取代形成的另一种氮的氢
2 4 3 2
化物。肼能与硫酸反应生成NHSO 。NHSO 晶体类型与硫酸铵相同,则NHSO 的晶体内存在
2 6 4 2 6 4 2 6 4
(填序号)。
a.离子键 b.配位键 c.共价键
(4)向盛有硫酸铜溶液的试管中滴加氨水,先生成难溶物,继续滴加氨水,难溶物溶解,得到深
蓝色透明溶液。下列对此现象的说法正确的是 。
A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
B.沉淀溶解后,生成深蓝色的配离子[Cu(NH )]2+
3 4
C.[Cu(NH )]2+的立体构型为正四面体形
3 4
D.在[Cu(NH )]2+配离子中,Cu2+给出孤电子对,NH 提供空轨道
3 4 3
(5)向氯化铜溶液中加入过量浓氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH ) ]Cl
3 4 2
晶体,深蓝色晶体中含有的化学键除普通的共价键外,还有 和 。
【答案】(1)X (2)N B
(3)abc (4)B (5)离子键 配位键【解析】(1)BCl 分子中的B原子的1个2s轨道和2个2p轨道进行sp2杂化形成3个sp2杂化轨道。
3
B原子还有1个空轨道(未杂化的2p轨道),所以B原子与X形成配位键时,X应提供孤电子对。
(2)NH 中N原子为sp3杂化,N原子上有一对孤电子对,BF 中B原子为sp2杂化,杂化轨道与F
3 3
原子形成3个共价键,故有一个2p空轨道,与NH 形成配位键。
3
(3)(NH ) SO 中,NH 存在配位键、共价键,表示为 ,SO 与NH 之
4 2 4
间 以 离 子 键 结 合 。 故 NHSO 中 , NH 存 在 配 位 键 、 共 价 键 , 表 示 为
2 6 4 2
,SO 与NH 之间以离子键结合。
2
(4)
(5)Cu2+中存在空轨道,NH 中N原子上有孤电子对,N与Cu2+之间以配位键结合、[Cu(NH )
3 3
]2+与Cl-间以离子键结合。
4
15.(1)[Fe(HO) ]2+与NO反应生成的[Fe(NO)(H O) ]2+中,NO以N原子与Fe2+形成配位键。请在
2 6 2 5
[Fe(NO)(H O) ]2+结构示意图的相应位置补填缺少的配体。
2 5
(2)向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成红色,该反应在有的教材中用方程式FeCl +3KSCN===Fe(SCN) +3KCl表示,经研究表明Fe(SCN) 是配合物,Fe3+与SCN-不仅能
3 3 3
以1∶3的个数比配合,还可以以其他个数比配合。
请按要求填空:
①Fe3+与SCN-反应时,Fe3+提供__________,SCN-提供__________,二者通过配位键结合。
②所得Fe3+与SCN-的配合物中,主要是Fe3+与SCN-以个数比1∶1配合,所得离子显红色,含该离
子的配合物化学式是__________________________________________________。
【答案】(1)
(2)①空轨道 孤电子对 ②[Fe(SCN)]Cl
2
【解析】(1)根据化学式,缺少的配体是NO和HO,NO中N为配位原子,HO中O上有孤电子对,
2 2
O为配位原子。(2)①Fe3+与SCN-反应生成的配合物中,Fe3+提供空轨道,SCN-提供孤电子对;
②Fe3+与SCN-以个数比1∶1配合所得离子为[Fe(SCN)]2+,所以FeCl 与KSCN在水溶液中反应生成
3
[Fe(SCN)]Cl 与KCl。
2
16.配位化学创始人维尔纳发现,取CoCl ·6NH (黄色)、CoCl ·5NH (紫红色)、CoCl ·4NH (绿色)和
3 3 3 3 3 3
CoCl ·4NH (紫色)四种化合物各1 mol,分别溶于水,加入足量硝酸银溶液,立即产生氯化银,沉淀
3 3
的物质的量分别为3 mol、2 mol、1 mol和1 mol。
(1)请根据实验事实用配合物的形式写出它们的化学式。
CoCl ·6NH :______________________________________________________________,
3 3
CoCl ·5NH :______________________________________________________________,
3 3
CoCl ·4NH (绿色和紫色):___________________________________________________。
3 3
(2)CoCl ·4NH (绿色)和CoCl ·4NH (紫色)的组成相同而颜色不同的原因是
3 3 3 3
________________________________________________________________________。
(3)上述配合物中,中心离子的配位数都是__________。
【答案】(1)[Co(NH )]Cl [Co(NH )Cl]Cl
3 6 3 3 5 2
[Co(NH )Cl]Cl (2)它们互为同分异构体 (3)6
3 4 2
【解析】沉淀的物质的量分别为3 mol、2 mol、1 mol和1 mol,可知物质的量分别为1 mol的四
种配合物,能电离出来的Cl-(即外界Cl-)的物质的量分别为3 mol、2 mol、1 mol、1 mol,故它
们的化学式分别为[Co(NH )]Cl 、[Co(NH )Cl]Cl 、[Co(NH )Cl]Cl、[Co(NH )Cl]Cl。
3 6 3 3 5 2 3 4 2 3 4 2
17.配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一提供空轨道的粒子结合.
如NH +就是由NH (氮原子提供电子对)和H+(提供空轨道)通过配位键形成的.据此,回答下
4 3
列问题:(1)下列粒子中可能存在配位键的是
A.COB.HO+C.CHD.[Ag(NH )]+
2 3 4 3 2
(2)向硫酸铜溶液中滴加氨水,会有蓝色沉淀产生,继续滴加,沉淀溶解,溶液变成深蓝色.请
写出沉淀溶解的离子方程式 .
(3)配位化学创始人维尔纳发现,将各为1mol的CoCl •6NH(黄色)、CoCl •5NH(紫红色)、
3 3 3 3
CoCl •4NH (绿色)、CoCl •4NH (紫色)四种配合物溶于水,加入足量硝酸银溶液,生成氯化银
3 3 3 3
沉淀分别为3mol、2mol、1mol、和1mol.已知上述配合物中配离子的配位数均为6.请根据实验
事实用配合物的形式写出它们的化学式.
①CoCl •5NH ②CoCl •4NH(紫色)
3 3 3 3
【答案】(1)BD;(2)Cu(OH) +4NH•H O=[Cu(NH ) ]2++2OH﹣+4H O;(3)[Co(NH )
2 3 2 3 4 2 3
Cl]Cl ; [Co(NH )Cl]Cl.
5 2 3 4 2
【解析】(1)含有孤电子对和含有空轨道的原子之间易形成配位键,
A.CO 中没有孤电子对和空轨道,所以没有配位键,故错误;
2
B.HO+中一个H原子含有空轨道、O原子含有孤电子对,所以该微粒中含有配位键,故正确;
3
C.CH 中没有孤电子对和空轨道,所以没有配位键,故错误;
4
D.[Ag(NH )]+中银离子含有空轨道、N原子含有孤电子对,所以该微粒中含有配位键,故正确;
3 2
(2)硫酸铜和氨水反应生成铵根离子和氢氧化铜沉淀,氢氧化铜和氨水继续反应生成铜氨络合物,
离子方程式为Cu(OH)+4NH•H O=[Cu(NH )]2++2OH﹣+4H O,
2 3 2 3 4 2
(3)1mol的CoCl •6NH (黄色)、CoCl •5NH (紫红色)、CoCl •4NH (绿色)、CoCl •4NH
3 3 3 3 3 3 3 3
(紫色)四种配合物溶于水,加入足量硝酸银溶液,生成氯化银沉淀分别为 3mol、2mol、1mol、
和1mol,说明这几种配合物的外界中氯离子个数分别是3、2、1、1,剩余氯离子为配体,
①CoCl •5NH 的外界中含有2个氯离子,则另外一个氯原子为配体,该化合物的配合物是 6,则氨
3 3
气分子都是配体,则其化学式为[Co(NH )Cl]Cl ,
3 5 2
②CoCl •4NH 中氯离子个数是1,则另外两个氯原子为配体,其配位数是6,则氨气分子都是配体,
3 3
则该化学式为[Co(NH )Cl]Cl。
3 4 2
18.配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一缺电子的粒子结合。如:
NH就是由NH (氮原子提供孤电子对)和H+(缺电子)通过配位键形成的。据此,回答下列问题:
3
(1)下列粒子中可能存在配位键的是________。
A.COB.HO+C.CHD.HSO
2 3 4 2 4
(2)硼酸(H BO)溶液呈酸性,试写出其电离方程式:
3 3
________________________________________________________________________。
(3)科学家对 HO 结构的认识经历了较为漫长的过程,最初,科学家提出了两种观点:甲:
2 2、乙:H—O—O—H,式中O→O表示配位键,在化学反应中O→O键遇到还原剂时易
断裂。化学家Baeyer和Villiyer为研究HO 的结构,设计并完成下列实验:
2 2
a.将C HOH与浓HSO 反应生成(C H)SO 和水;
2 5 2 4 2 5 2 4
b.将制得(C H)SO 与HO 反应,只生成A和HSO ;
2 5 2 4 2 2 2 4
c.将生成的A与H 反应(已知该反应中H 作还原剂)。
2 2
①如果HO 的结构如甲所示,实验c中化学反应方程式为_____________________________
2 2
________________________________________________________________________(A写结构简式)。
②为了进一步确定 HO 的结构,还需要在实验 c后添加一步实验 d,请设计 d的实验方案:
2 2
________________________________________________________________________
________________________________________________________________________。
【答案】 (1)BD
(2)H BO+HO H++B(OH)
3 3 2
(3)①
②用无水CuSO 检验实验c的反应产物中有没有水(或其他合理答案)
4
【解析】形成配位键的条件:一方能够提供孤电子对,另一方具有能够接受孤电子对的空轨道,常
见能形成电负性强的元素N、O、F