文档内容
第四节 配合物与超分子
一、配合物
1.配位键
(1)概念:成键原子一方提供孤电子对,另一方提供空轨道形成的共价键。
【注】配位键是一种特殊的共价键。配位键中的共用电子对是由成键单方
提供的,而其他的共价键的共用电子对是由成键双方提供的。
(2)配位键的形成条件
①成键原子一方能提供孤电子对。如分子有 NH 、H O、HF、CO等;离子
3 2
有Cl-、OH-、CN-、SCN-等。
②成键原子另一方能提供空轨道。如 H+、Al3+、B及过渡金属的原子或离
子。
(3)配位键同样具有饱和性和方向性。一般来说,多数过渡金属的原子或离
子形成配位键的数目是基本不变的,如 Ag+形成2个配位键;Cu2+形成4个配
位键等。
2.配位化合物
(1)配合物的概念:把金属离子或原子(称为中心离子或原子)与某些分子或离
子(称为配体或配位体)以配位键结合形成的化合物称为配位化合物,简称配合
物。如[Cu(NH ) ]SO 、[Ag(NH ) ]OH、NH Cl等均为配合物。
3 4 4 3 2 4
(2)配合物的形成
实验操作 实验现象 有关离子方程式
Cu 2 + +
滴加氨水后,试管中首
2NH ·H O == = Cu(OH) ↓ +
3 2 2
先出现蓝色沉淀,氨水
2NH 、 Cu(OH) +
过量后沉淀逐渐溶解, 2
4NH == = [Cu(NH ) ] 2 + + 2OH -
滴加乙醇后析出深蓝色 3 3 4
1晶体[Cu(NH ) ]SO ·H O
3 4 4 2
溶液变血红色 Fe 3 + + 3SCN - == = Fe(SCN)
3
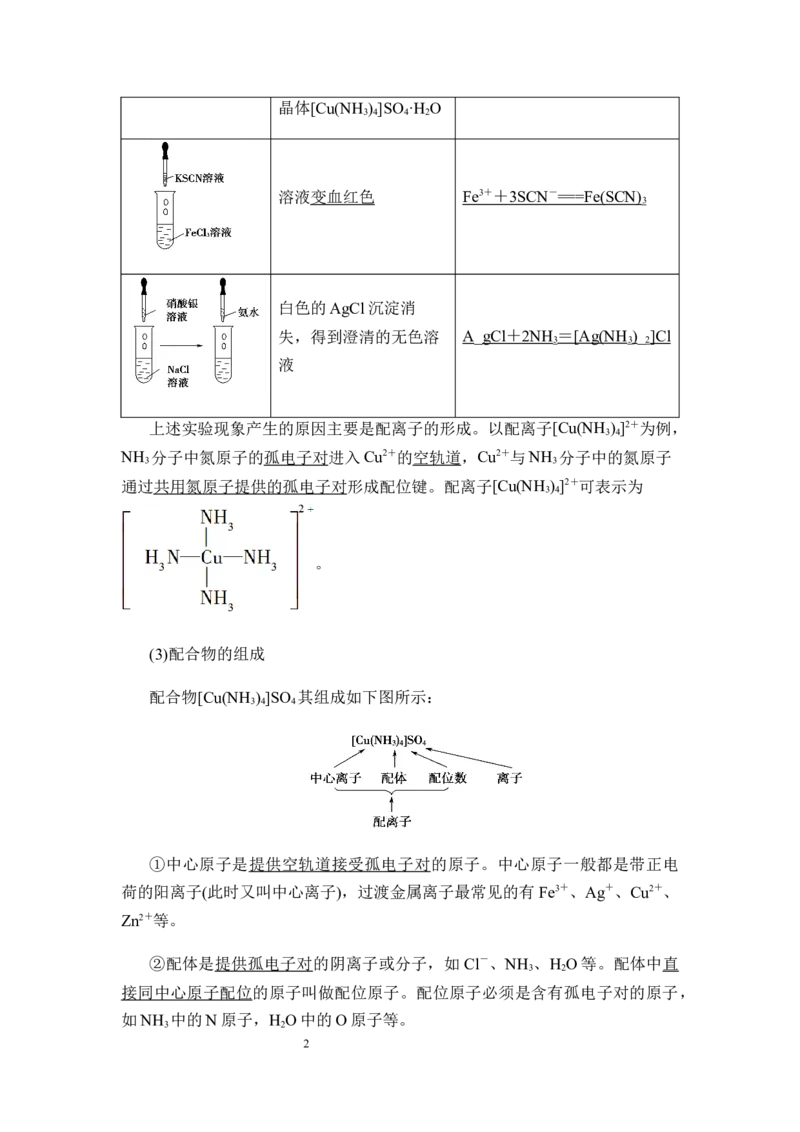
白色的AgCl沉淀消
失,得到澄清的无色溶 A_ gCl + 2NH = [Ag(NH )_ ]Cl
3 3 2
液
上述实验现象产生的原因主要是配离子的形成。以配离子[Cu(NH ) ]2+为例,
3 4
NH 分子中氮原子的孤电子对进入Cu2+的空轨道,Cu2+与NH 分子中的氮原子
3 3
通过共用氮原子提供的孤电子对形成配位键。配离子[Cu(NH ) ]2+可表示为
3 4
。
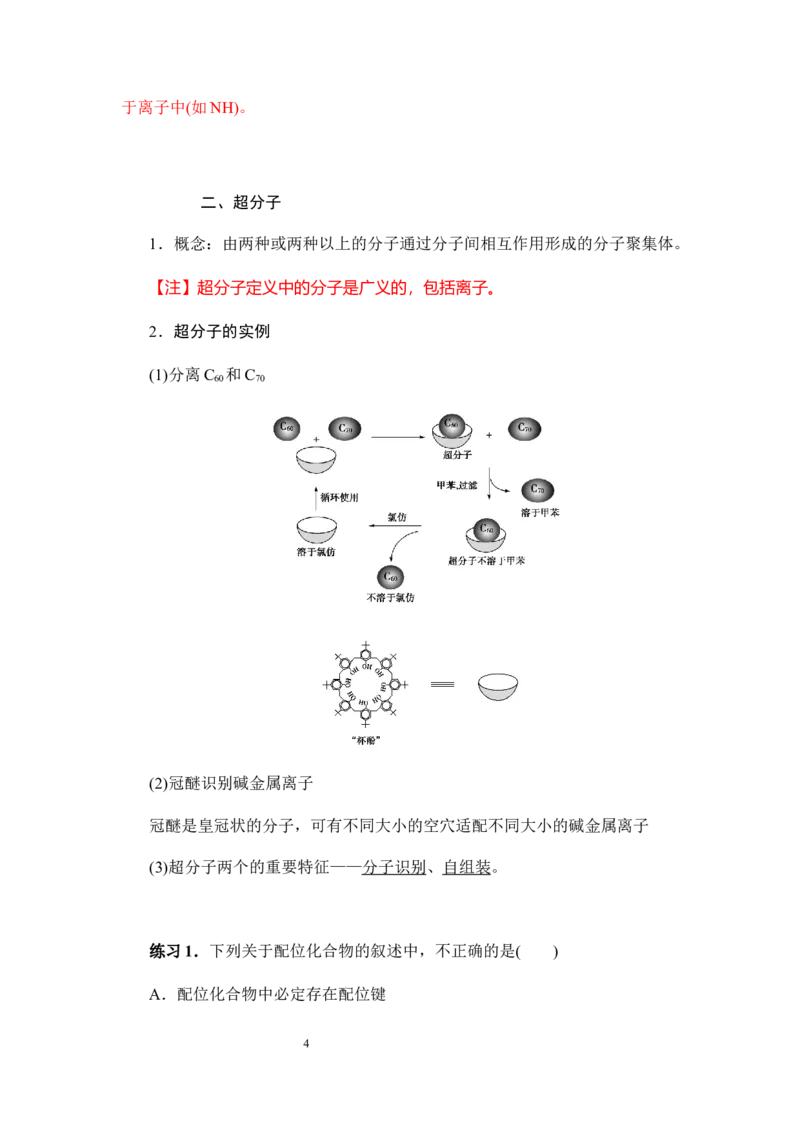
(3)配合物的组成
配合物[Cu(NH ) ]SO 其组成如下图所示:
3 4 4
①中心原子是提供空轨道接受孤电子对的原子。中心原子一般都是带正电
荷的阳离子(此时又叫中心离子),过渡金属离子最常见的有Fe3+、Ag+、Cu2+、
Zn2+等。
②配体是提供孤电子对的阴离子或分子,如Cl-、NH 、H O等。配体中直
3 2
接同中心原子配位的原子叫做配位原子。配位原子必须是含有孤电子对的原子,
如NH 中的N原子,H O中的O原子等。
3 2
2③配位数是直接与中心原子形成的配位键的数目。如[Fe(CN) ]4-中配位数
6
为6。
3.配合物的形成对物质性质的影响
(1)溶解性的影响:一些难溶于水的金属氯化物、溴化物、碘化物、氰化物,
可以依次溶于含过量Cl-、Br-、I-、CN-和氨的溶液中,形成可溶性的配合物。
(2)颜色的改变:当简单离子形成配离子时,颜色常发生变化,根据颜色的
变化可以判断是否有配离子生成。如 Fe3+与SCN-在溶液中可生成配位数为1~
6的配离子,这种配离子的颜色是血红色的,反应的离子方程式如下: Fe3++
nSCN-===[Fe(SCN) ]3-n(n=1~6)。
n
(3)稳定性增强:配合物具有一定的稳定性,配合物中的配位键越强,配合
物越稳定。当作为中心原子的金属离子相同时,配合物的稳定性与配体的性质
有关。如血红素中的Fe2+与CO分子形成的配位键比Fe2+与O 分子形成的配位
2
键强,因此血红素中的Fe2+与CO分子结合后,就很难再与O 分子结合,使血
2
红蛋白失去输送O 的功能,从而导致人体CO中毒。
2
4.配合物内界中共价键数目的判断
若配体为单核离子如Cl-等,可以不予计入,若为分子,需要用配体分子内
的共价键数乘以该配体的个数,此外,还要加上中心原子与配体形成的配位键,
这也是σ键。例如:配合物[Co(NH ) Cl ]Cl的共价键数为3×4+4+2=18。
3 4 2
【拓展】配位键与共价键的关系
①形成过程不同:配位键实质上是一种特殊的共价键,在配位键中一方提
供孤电子对,另一方具有能够接受孤电子对的空轨道。普通共价键的共用电子
对是由成键原子双方共同提供的。
②配位键与普通共价键的实质相同。它们都被成键原子双方共用,如在 NH
中有三个普通共价键、一个配位键,但四者是完全相同的。
③同普通共价键一样,配位键可以存在于分子中[如Ni(CO) ],也可以存在
4
3于离子中(如NH)。
二、超分子
1.概念:由两种或两种以上的分子通过分子间相互作用形成的分子聚集体。
【注】超分子定义中的分子是广义的,包括离子。
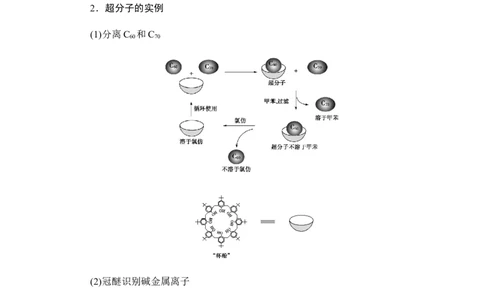
2.超分子的实例
(1)分离C 和C
60 70
(2)冠醚识别碱金属离子
冠醚是皇冠状的分子,可有不同大小的空穴适配不同大小的碱金属离子
(3)超分子两个的重要特征——分子识别、自组装。
练习1.下列关于配位化合物的叙述中,不正确的是( )
A.配位化合物中必定存在配位键
4B.配位化合物中只有配位键
C.[Cu(H O) ]2+中的Cu2+提供空轨道,H O中的氧原子提供孤电子对形成
2 4 2
配位键
D.配位化合物在半导体等尖端技术、医学科学、催化反应和材料化学等领
域都有着广泛的应用
答案 B [含有配位键的化合物就是配位化合物,但配位化合物还会含有共
价键、离子键等,B错误。]
练习2.(1)Zn的氯化物与氨水反应可形成配合物[Zn(NH ) ]Cl ,1 mol该配
3 4 2
合物中含有σ键的数目为________。
(2)关于配合物[Zn(NH ) ]Cl 的说法正确的是________。
3 4 2
A.配位数为6
B.配体为NH 和Cl-
3
C.[Zn(NH ) ]2+为内界
3 4
D.Zn2+和NH 以离子键结合
3
[解析] (1)[Zn(NH ) ]Cl 中[Zn(NH ) ]2+与 Cl-形成离子键,而 1 个
3 4 2 3 4
[Zn(NH ) ]2+中含有4个N→Zn键(配位键)和12个N—H键,共16个σ键,故1
3 4
mol该配合物中含有16 mol σ键,即16N 。
A
(2)Zn2+的配位原子个数是4,所以其配位数是4,故A错误;该配合物中氮
原子提供孤电子对,所以 NH 是配体,故 B 错误;[Zn(NH ) ]Cl 中外界是 Cl
3 3 4 2
-,内界是[Zn(NH ) ]2+,故C正确;该配合物中,锌离子提供空轨道,氮原子
3 4
提供孤电子对,所以 Zn2+和NH 以配位键结合,属于特殊共价键,不属于离子
3
键,故D错误。
[答案] (1)16N (2)C
A
5练习3.(1)在[Ni(NH ) ]2+中Ni2+与NH 之间形成的化学键称为________,
3 6 3
提供孤电子对的成键原子是________。
(2)CaF 难溶于水,但可溶于含Al3+的溶液中,原因是_________。 (用离子
2
方程式表示,已知AlF在溶液中可稳定存在)。
(3)配合物[Cr(H O) ]3+中,与Cr3+形成配位键的原子是_____(填元素符号)。
2 6
[解析] (1)Ni2+与NH 之间形成共价键时Ni2+提供空轨道,N提供孤电子
3
对,形成配位键。(2)CaF 中存在沉淀溶解平衡:CaF (s) Ca2+(aq)+
2 2
2F-(aq),溶液中的F-与Al3+形成配位离子AlF,使沉淀溶解平衡向右移动,导
致氟化钙溶解。(3)H O分子中的O原子有孤电子对,能与Cr3+形成配位键。
2
[答案] (1)配位键 N (2)3CaF +Al3+===3Ca2++AlF (3) O
2
6