文档内容
2021-2022 学年高二化学重难点专题突破
模块二 分子结构与性质
专题 05 分子的空间结构及中心原子杂化轨道类型的判断方法
一.选择题
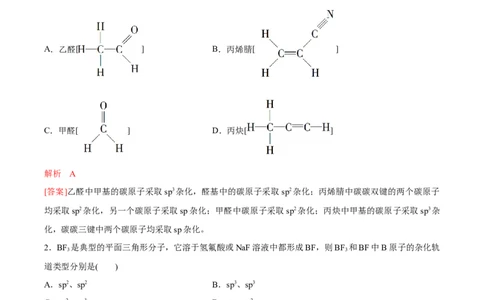
1.下列分子所含原子中,既有sp3杂化,又有sp2杂化的是( )
A.乙醛[ ] B.丙烯腈[ ]
C.甲醛[ ] D.丙炔[ ]
解析 A
[答案]乙醛中甲基的碳原子采取sp3杂化,醛基中的碳原子采取sp2杂化;丙烯腈中碳碳双键的两个碳原子
均采取sp2杂化,另一个碳原子采取sp杂化;甲醛中碳原子采取sp2杂化;丙炔中甲基的碳原子采取sp3杂
化,碳碳三键中两个碳原子均采取sp杂化。
2.BF 是典型的平面三角形分子,它溶于氢氟酸或NaF溶液中都形成BF,则BF 和BF中B原子的杂化轨
3 3
道类型分别是( )
A.sp2、sp2 B.sp3、sp3
C.sp2、sp3 D.sp、sp2
解析 C
[答案]BF 中B原子的价层电子对数为3,所以为sp2杂化,BF中B原子的价层电子对数为4,所以为sp3杂
3
化。
3.在BrCH===CHBr分子中,C—Br采用的成键轨道是( )
A.sp—p B.sp2—s
C.sp2—p D.sp3—p解析 C
[答案]BrCH===CHBr分子中的两个碳原子都采取sp2杂化,溴原子的价层电子排布为4s24p5,4p轨道上有一
个未成对电子,与碳原子的一个sp2杂化轨道成键,C项正确。
4.氨分子的空间结构是三角锥形,而甲烷是正四面体形,这是因为( )
A.两种分子的中心原子杂化轨道类型不同,NH 为sp2杂化,而CH 是sp3杂化
3 4
B.NH 分子中N原子形成三个杂化轨道,CH 分子中C原子形成4个杂化轨道
3 4
C.NH 分子中有一个未成键的孤电子对,它对成键电子对的排斥作用较强
3
D.氨气分子是极性分子而甲烷是非极性分子
解析 C
[答案]氨分子中的N原子和甲烷分子中的C原子都是sp3杂化,C原子的四个杂化轨道全部参与成键,而N
原子的杂化轨道中有3个参与成键,还有一个孤电子对,孤电子对对成键电子对的排斥作用较强,从而使
得两种分子的结构不同,C项正确。
5.下列分子或离子中,VSEPR模型与粒子的空间结构一致的是( )
A.SO B.HCHO
2
C.NCl D.HO+
3 3
[答案] B
解析 当中心原子没有孤电子对时,VSEPR模型与分子的空间结构就是一致的,SO 、NCl 、HO+的中心
2 3 3
原子均有孤电子对,A、C、D项错误。
6.下列关于NH、NH 、NH三种粒子的说法不正确的是( )
3
A.三种粒子所含有的电子数相等
B.三种粒子中氮原子的杂化方式相同
C.三种粒子的空间构型相同
D.键角大小关系:NH>NH >NH
3
[答案] C
解析NH、NH 、NH含有的电子数均为10,A正确;NH、NH 、NH三种粒子中氮原子的杂化方式均为sp3
3 3
杂化,B正确;NH空间结构为正四面体形,NH 为三角锥形,NH为V形,C错误;NH、NH 、NH三种
3 3
粒子的键角大小关系为NH>NH >NH,D正确。
3
7.氯的含氧酸根离子有ClO-、ClO、ClO、ClO等,关于它们的说法不正确的是( )
A.ClO的中心Cl原子采取sp3杂化
B.ClO的空间结构为三角锥形
C.ClO的空间结构为直线形D.ClO-中Cl原子的杂化类型与ClO相同
解析 C
[答案]ClO的中心原子Cl的孤电子对数为0,与中心Cl原子结合的O原子数为4,则Cl原子采取sp3杂化,
A正确;ClO的中心原子Cl的价层电子对数为3+=4,且含有1个孤电子对,空间结构为三角锥形,B正
确;ClO的中心原子Cl的价层电子对数为2+=4,且含有2个孤电子对,空间结构为V形,C错误;ClO
-中Cl原子的孤电子对数为3,与Cl原子结合的O原子数为1,Cl原子采取sp3杂化,ClO中Cl原子的孤
电子对数为2,与Cl原子结合的O原子数为2,Cl原子采取sp3杂化,D正确。
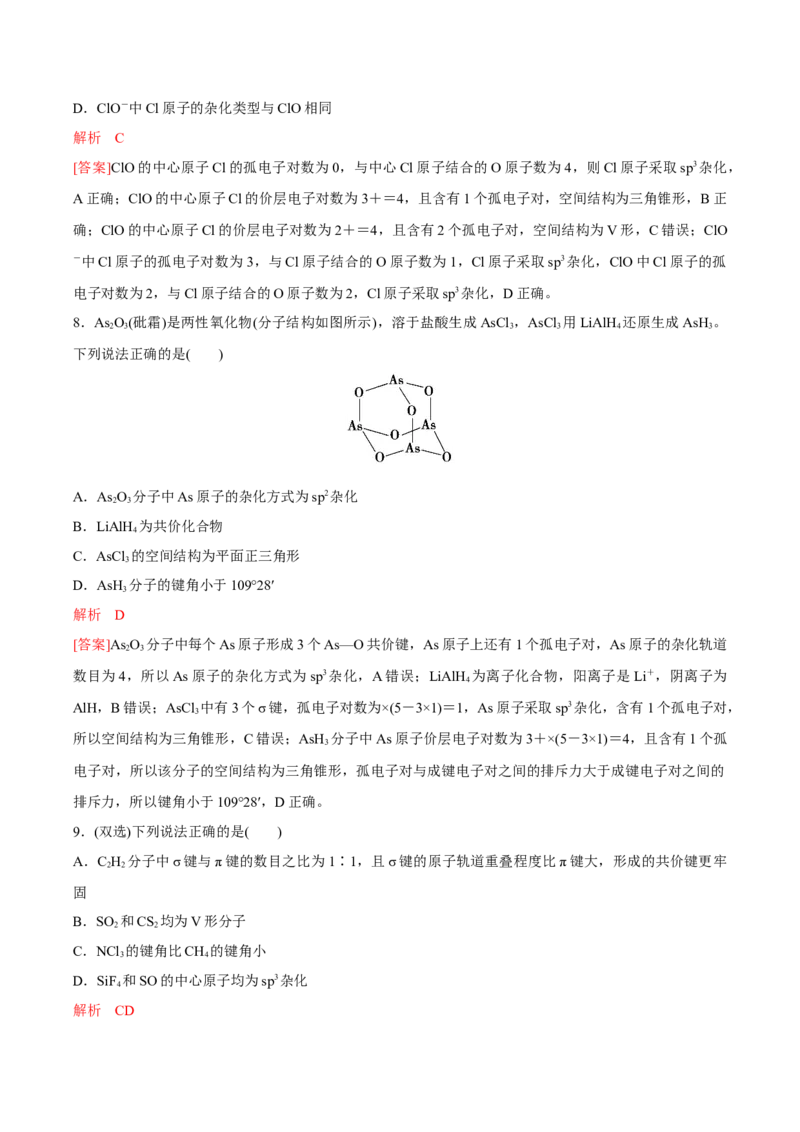
8.As O(砒霜)是两性氧化物(分子结构如图所示),溶于盐酸生成AsCl ,AsCl 用LiAlH 还原生成AsH 。
2 3 3 3 4 3
下列说法正确的是( )
A.As O 分子中As原子的杂化方式为sp2杂化
2 3
B.LiAlH 为共价化合物
4
C.AsCl 的空间结构为平面正三角形
3
D.AsH 分子的键角小于109°28′
3
解析 D
[答案]As O 分子中每个As原子形成3个As—O共价键,As原子上还有1个孤电子对,As原子的杂化轨道
2 3
数目为4,所以As原子的杂化方式为sp3杂化,A错误;LiAlH 为离子化合物,阳离子是Li+,阴离子为
4
AlH,B错误;AsCl 中有3个σ键,孤电子对数为×(5-3×1)=1,As原子采取sp3杂化,含有1个孤电子对,
3
所以空间结构为三角锥形,C错误;AsH 分子中As原子价层电子对数为3+×(5-3×1)=4,且含有1个孤
3
电子对,所以该分子的空间结构为三角锥形,孤电子对与成键电子对之间的排斥力大于成键电子对之间的
排斥力,所以键角小于109°28′,D正确。
9.(双选)下列说法正确的是( )
A.C H 分子中σ键与π键的数目之比为1∶1,且σ键的原子轨道重叠程度比π键大,形成的共价键更牢
2 2
固
B.SO 和CS 均为V形分子
2 2
C.NCl 的键角比CH 的键角小
3 4
D.SiF 和SO的中心原子均为sp3杂化
4
解析 CD[答案]C H 分子中σ键与π键数目比为3∶2,A错误。CS 中中心原子C的价层电子对数=2+×(4-2×2)=
2 2 2
2,中心原子C为sp杂化,且无孤电子对,所以CS 为直线形分子,B错误。NCl 、CH 的中心原子均采取
2 3 4
sp3杂化,且N原子上有1个孤电子对,孤电子对与成键电子对间的排斥力较大,所以 NCl 的键角比CH
3 4
的键角小,C正确。SiF 中中心原子Si的价层电子对数=4+×(4-4×1)=4,SO中中心原子S的价层电子
4
对数=3+×(6+2-3×2)=4,所以SiF 和SO的中心原子均为sp3杂化,D正确。
4
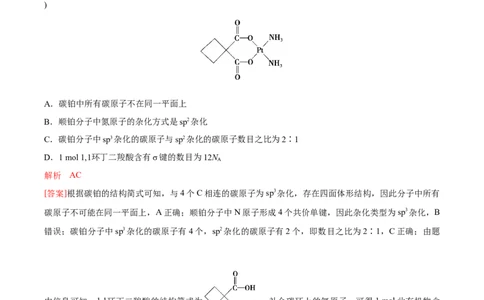
10.(双选)顺铂[Pt(NH )Cl]是1969年发现的第一种具有抗癌活性的金属配合物;碳铂是 1,1环丁二羧酸二
3 2 2
氨合铂(Ⅱ)的简称,属于第二代铂族抗癌药物,结构如图所示,其毒副作用低于顺铂。下列说法正确的是(
)
A.碳铂中所有碳原子不在同一平面上
B.顺铂分子中氮原子的杂化方式是sp2杂化
C.碳铂分子中sp3杂化的碳原子与sp2杂化的碳原子数目之比为2∶1
D.1 mol 1,1环丁二羧酸含有σ键的数目为12N
A
解析 AC
[答案]根据碳铂的结构简式可知,与4个C相连的碳原子为sp3杂化,存在四面体形结构,因此分子中所有
碳原子不可能在同一平面上,A正确;顺铂分子中N原子形成4个共价单键,因此杂化类型为sp3杂化,B
错误;碳铂分子中sp3杂化的碳原子有4个,sp2杂化的碳原子有2个,即数目之比为2∶1,C正确;由题
中信息可知,1,1环丁二羧酸的结构简式为 ,补全碳环上的氢原子,可得1 mol此有机物含
有σ键的数目为18N ,D错误。
A
11.第ⅤA族元素的原子(以R表示)与A原子结合形成RA 气态分子,其空间结构为三角锥形。PCl 在气
3 5
态和液态时,分子结构如图所示,下列关于PCl 分子的说法中不正确的是( )
5A.每个原子都达到最外层8电子稳定结构
B.Cl—P—Cl的键角有120°、90°、180°三种
C.PCl 受热后会分解生成分子空间结构呈三角锥形的PCl
5 3
D.分子中5个P—Cl的键能不都相同
解析 A
[答案]P原子的最外层有5个电子,形成5个共用电子对,所以PCl 中P的最外层不满足8电子稳定结构,
5
A错误;由图可知,三角双锥上下两个顶点Cl原子与中心P原子形成的Cl—P—Cl的键角为180°,中间为
平面三角形,其中两个顶点Cl原子与中心P原子形成的Cl—P—Cl的键角为120°,通过中间的三角形所在
的平面将三角双锥截为两个完全相同的三角锥,在上面的三角锥中 Cl—P—Cl的键角为90°,所以Cl—P—
Cl的键角有90°、120°、180°三种,B正确;PCl =====PCl +Cl↑,则PCl 受热后会分解生成分子空间结
5 3 2 5
构呈三角锥形的PCl ,C正确;键长越短,键能越大,因分子中P—Cl的键长不都相同,所以键能不都相
3
同,D正确。
12.下列说法正确的是( )
A.CHCl 分子的空间结构为正四面体形
2 2
B.HO分子中氧原子的杂化轨道类型为sp2,分子的立体构型为V形
2
C.CO 分子中碳原子的杂化轨道类型为sp,分子的立体构型为直线形
2
D.SO的空间结构为平面三角形
解析 C
[答案]CH 中4个共价键完全相同,为正四面体形,CHCl 分子的4个共价键不完全相同,所以分子的空间
4 2 2
结构不是正四面体形,A错误;HO分子中O原子的价层电子对数=2+×(6-1×2)=4,为sp3杂化,含有
2
2个孤电子对,分子的空间结构为V形,B错误;CO 中C原子的价层电子对数=2+×(4-2×2)=2,为sp
2
杂化,分子的空间结构为直线形,C正确;SO中S原子的价层电子对数=3+×(6+2-3×2)=4,为sp3杂
化,含1对孤电子对,分子的空间结构为三角锥形,D错误。
二.填空题
13.硼砂是含结晶水的四硼酸钠。以硼砂为原料,可以得到BF、BN和硼酸等重要化合物,请根据下列信
3
息回答有关问题:图1 图2
(1)硼砂中阴离子Xm-(含B、O、H三种元素)的球棍模型如图1所示,则在Xm-中,2号硼原子的杂化类型
为________;m=________(填数字)。
(2)BN中B的化合价为________,请解释原因:_______________________。
(3)BF 和过量 NaF 作用可生成 NaBF ,BF 的空间结构为________________;NaBF 的电子式为
3 4 4
______________________。
[解析] (1)根据图示可知,2号B原子的价层电子对数为3,且无孤电子对,故采取sp2杂化;根据图示可
知,该阴离子的化学式为[H B O]m-,其中H显+1价,B显+3价、O显-2价,所以m=2。(2)由于电负
4 4 9
性:N>B,所以 BN 中 B 显+3 价。(3)BF 的空间结构为正四面体形,NaBF 的电子式为
4
。
[答案] (1)sp2 2
(2)+3 N的电负性大于B的电负性
(3)正四面体形
14.目前工业上制备丙烯腈(CH===CHC≡N)有乙炔法、丙烯氨氧化法等。
2
乙炔法:
H—C≡C—H+HCN―――――――――――→CH===CHCN
2
丙烯氨氧化法:
CH===CHCH+NH +O催化CH===CHCN+3HO
2 3 3 2剂 2 2(1)下列说法正确的是__________(填序号)。
a.NH的空间结构为正四面体形
b.CH===CHCN分子中只有碳、氢原子位于同一平面上
2
c.C H、HCN分子中所有原子均位于同一直线上
2 2
(2)1 mol丙烯腈分子中含有σ键的数目为__________。
[解析] (1)NH中N原子的价层电子对数=σ键数+孤电子对数=4+×(5-4×1-1)=4,则N原子采取sp3
杂化,NH的空间结构为正四面体形,a正确;CH===CH—C≡N分子相当于一个碳碳双键和一个碳氮三键
2
通过一个碳碳单键相连,所有原子都处在同一平面上,b错误;C H 、HCN分子中都含有一个三键,碳原
2 2
子均为sp杂化,则分子中所有原子均位于同一直线,c正确。
(2)每个单键、双键、三键都含有1个σ键,所以1 mol丙烯腈分子中含有σ键的物质的量为6 mol,数目为
6N 。
A
[答案] (1)ac (2)6N (或6×6.02×1023)
A
15.目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍行业发展蕴藏着巨大潜力。
Ⅰ.(1)硫酸镍溶于氨水形成[Ni(NH )]SO 蓝色溶液。
3 6 4
①基态Ni2+的核外电子排布式为__________。
②在[Ni(NH )]2+中存在的化学键有__________(填序号)。
3 6
A.离子键 B.共价键 C.氢键
D.σ键 E.π键
Ⅱ.丁二酮肟是一种较灵敏地检验Ni2+的试剂。
(2)丁二酮肟( )分子中C原子轨道杂化类型为__________,1 mol丁二酮肟分子所
含σ键的数目为__________(设N 为阿伏加德罗常数的值)。
A
[解析] Ⅰ.(1)①Ni是28号元素,根据原子核外电子排布规律可知,基态 Ni2+的核外电子排布式为
1s22s22p63s23p63d8。
②[Ni(NH )]2+中Ni2+与NH 之间形成配位键,NH 中N、H原子形成N—H共价键,两者都是σ键。
3 6 3 3
Ⅱ.(2)丁二酮肟( )分子中甲基上碳原子的价层电子对数是4,且不含孤电子对,
为sp3杂化,连接甲基的碳原子的价层电子对数是3,且不含孤电子对,为sp2杂化;已知丁二酮肟的结构简式为 ,分子中含有13个单键和2个双键,则共含有15个σ键,所以1 mol丁二
酮肟分子中含有σ键的数目为15N 。
A
[答案] Ⅰ.(1)①1s22s22p63s23p63d8 ②BD
Ⅱ.(2)sp3和sp2 15N
A
16.(1)比较下列物质中键角的大小(填“>”“=”或“<”)。
①CH______P。
4 4
②NH ______PH ______AsH 。
3 3 3
③PF ______PCl 。
3 3
④光气(COCl )中∠Cl—C==O______∠Cl—C—Cl。
2
[答案] ①> ②> > ③< ④>
(2)下列分子或离子中键角由大到小排列正确的是( )
①BCl ②NH ③HO ④PCl ⑤BeCl
3 3 2 2
A.⑤④①②③ B.④①②⑤③
C.⑤①④②③ D.③②④①⑤
[答案] C
解析
VSEPR
中心原子上孤电 中心原子上价 杂化轨
微粒 空间结构 键角
子对数 层电子对数 道类型
模型名称
平面 平面
①BCl ×(3-3×1)=0 3 sp2 120°
3
三角形 三角形
②NH ×(5-3×1)=1 4 四面体形 sp3 三角锥形 107°
3
③HO ×(6-2×1)=2 4 四面体形 sp3 V形 105°
2
正四面 正四面
④PCl ×(5-1-4×1)=0 4 sp3 109°28′
体形 体形
⑤BeCl ×(2-2×1)=0 2 直线形 sp 直线形 180°
2
键角由大到小的顺序为⑤①④②③。倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育