文档内容
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
2021-2022 学年高二化学重难点专题突破
模块三 晶体结构与性质
专题 08 离子键、配位键与金属键
一.选择题
1.氯化钠是日常生活中人们常用的调味品。下列性质可以证明氯化钠中一定存在离子键的是( )
A.具有较高的熔点 B.熔融状态能导电
C.水溶液能导电 D.常温下能溶于水
[答案]B
[解析]NaCl在熔融状态能导电,说明NaCl=====Na++Cl-,即说明NaCl中存在离子键。
2.下列关于配合物的说法中不正确的是( )
A.许多过渡金属离子对多种配体具有很强的结合力,因而过渡金属配合物远比主族金属配合物多
B.配合物中,中心离子与配体间、配离子与酸根离子间都以配位键结合
C.配离子中,中心离子提供空轨道,配体提供孤电子对
D.中心离子所结合配体的个数称为配位数,不同离子的配位数可能不同
[答案]B
[解析]许多过渡金属的离子对多种配体具有很强的结合力,因而过渡金属配合物远比主族金属的配合
物多,A正确;配合物中,中心离子与配体间以配位键结合,配离子与酸根离子间以离子键结合,B错误;
配合物中,中心离子提供空轨道,配体提供孤电子对,C正确;配位数是指形成配离子时配体的个数,不
同离子的配位数可能相同也可能不同,D正确。
3.下列配合物的配位数是6的是( )
A.K[Co(SCN) ] B.Fe(SCN)
2 4 3
C.Na[AlF ] D.[Cu(NH )]Cl
3 6 3 4 2
[答案]C
[解析]K[Co(SCN) ]中Co2+的配位数是4,A不符合题意;Fe(SCN) 中Fe3+的配位数是3,B不符合题
2 4 3
意;Na[AlF ]中Al3+的配位数是6,C符合题意;[Cu(NH )]Cl 中Cu2+的配位数是4,D不符合题意。
3 6 3 4 2
4.(双选)下列关于金属及金属键的说法正确的是 ( )
A.金属键跟共价键不同,它不具有方向性和饱和性
B.金属键是金属阳离子与“自由电子”间的相互作用
C.金属导电是因为在外加电场作用下金属内部产生了“自由电子”
D.金属具有光泽是因为金属阳离子吸收并放出可见光
【答案】AB
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
【解析】金属键是金属阳离子和“自由电子”之间的一种作用力,没有方向性和饱和性,A、B项正确;金属中
的“自由电子”并不是在外加电场的作用下产生的,金属导电是因为在外加电场作用下“自由电子”发生了
定向移动,C项不正确;金属具有光泽是因为“自由电子”能够吸收并放出可见光,D项不正确。
5.下列各组元素的所有组合中,既可形成离子化合物,又可形成共价化合物的是( )
A.H、C、O、K B.H、Na、O、S
C.H、N、O D.H、O、S
[答案]C
[解析]A、B项都含活泼金属元素,所有元素组合只能形成离子化合物,D项中全部为非金属元素,
所有元素组合只能形成共价化合物,特殊的是C项中的N元素,它既可与H元素组成NH,又可与O元素
组成NO,所以既可形成离子化合物NH NO ,又可形成共价化合物HNO。
4 3 3
6.下列关于化学键的各种叙述正确的是( )
A.含有金属元素的化合物一定是离子化合物
B.共价化合物中一定不存在离子键
C.由多种非金属元素组成的化合物一定是共价化合物
D.由不同种元素组成的多原子分子中,一定只存在极性键
[答案]B
[解析]含有金属元素的化合物,可能为共价化合物,如氯化铝,A项错误;含离子键的化合物一定为
离子化合物,则共价化合物中一定不存在离子键,B项正确;由多种非金属元素组成的化合物,可能为离
子化合物,如铵盐,C项错误;由不同种元素组成的多原子分子中可存在极性键和非极性键,如HO 中存
2 2
在极性键和非极性键,D项错误。
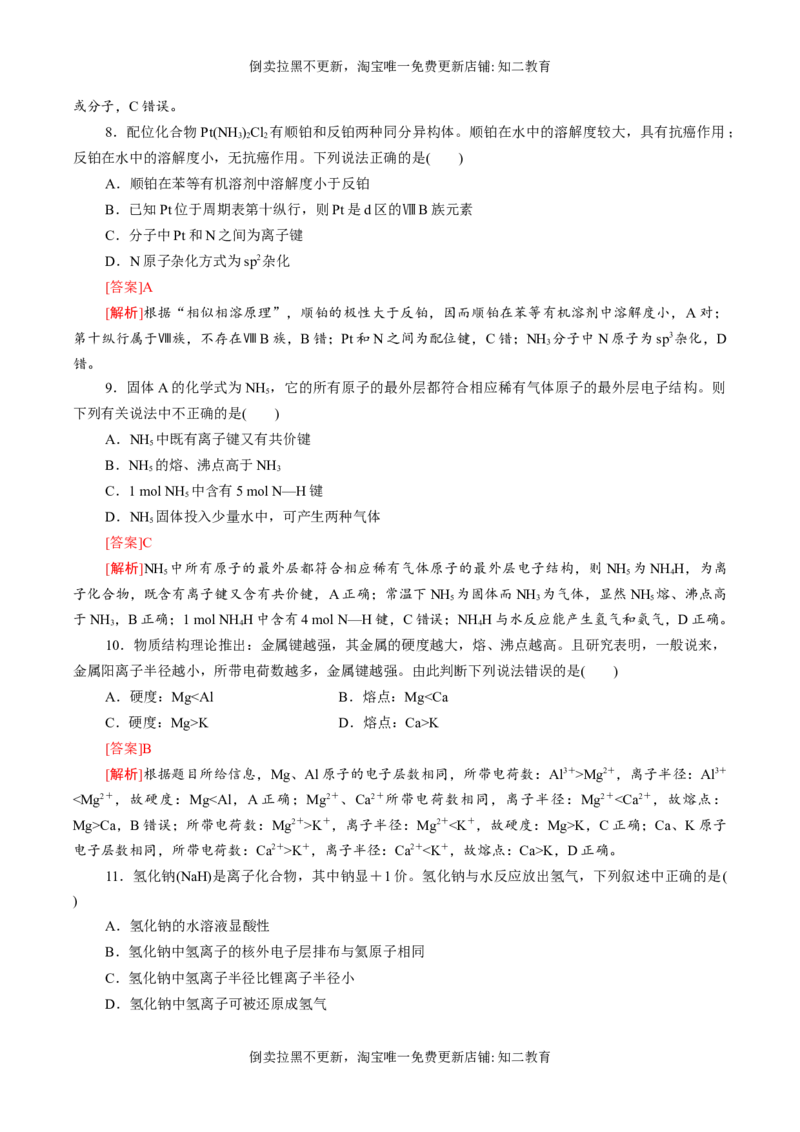
7.如图所示是卟啉配合物叶绿素的结构示意图(部分),下列有关叙述正确的是( )
A.该叶绿素只含有H、Mg、C元素
B.该叶绿素是配合物,中心离子是镁离子
C.该叶绿素是配合物,其配体是N元素
D.该叶绿素不是配合物,而是高分子化合物
[答案]B
[解析]该化合物还含有氧元素和氮元素,A错误;Mg的最高化合价为+2,而化合物中镁原子与4个
氮原子作用,由此可以判断该化合物中镁原子与氮原子间形成配位键,该物质为配合物,B正确,D错误;
该化合物中配位原子为氮原子,不能称氮原子为配体,同样也不能称氮元素为配体,因为配体一般为离子
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
或分子,C错误。
8.配位化合物Pt(NH )Cl 有顺铂和反铂两种同分异构体。顺铂在水中的溶解度较大,具有抗癌作用;
3 2 2
反铂在水中的溶解度小,无抗癌作用。下列说法正确的是( )
A.顺铂在苯等有机溶剂中溶解度小于反铂
B.已知Pt位于周期表第十纵行,则Pt是d区的ⅧB族元素
C.分子中Pt和N之间为离子键
D.N原子杂化方式为sp2杂化
[答案]A
[解析]根据“相似相溶原理”,顺铂的极性大于反铂,因而顺铂在苯等有机溶剂中溶解度小,A对;
第十纵行属于Ⅷ族,不存在ⅧB族,B错;Pt和N之间为配位键,C错;NH 分子中N原子为sp3杂化,D
3
错。
9.固体A的化学式为NH ,它的所有原子的最外层都符合相应稀有气体原子的最外层电子结构。则
5
下列有关说法中不正确的是( )
A.NH 中既有离子键又有共价键
5
B.NH 的熔、沸点高于NH
5 3
C.1 mol NH 中含有5 mol N—H键
5
D.NH 固体投入少量水中,可产生两种气体
5
[答案]C
[解析]NH 中所有原子的最外层都符合相应稀有气体原子的最外层电子结构,则NH 为NH H,为离
5 5 4
子化合物,既含有离子键又含有共价键,A正确;常温下NH 为固体而NH 为气体,显然NH 熔、沸点高
5 3 5
于NH ,B正确;1 mol NH H中含有4 mol N—H键,C错误;NH H与水反应能产生氢气和氨气,D正确。
3 4 4
10.物质结构理论推出:金属键越强,其金属的硬度越大,熔、沸点越高。且研究表明,一般说来,
金属阳离子半径越小,所带电荷数越多,金属键越强。由此判断下列说法错误的是( )
A.硬度:MgK D.熔点:Ca>K
[答案]B
[解析]根据题目所给信息,Mg、Al原子的电子层数相同,所带电荷数:Al3+>Mg2+,离子半径:Al3+
Ca,B错误;所带电荷数:Mg2+>K+,离子半径:Mg2+K,C正确;Ca、K原子
电子层数相同,所带电荷数:Ca2+>K+,离子半径:Ca2+K,D正确。
11.氢化钠(NaH)是离子化合物,其中钠显+1价。氢化钠与水反应放出氢气,下列叙述中正确的是(
)
A.氢化钠的水溶液显酸性
B.氢化钠中氢离子的核外电子层排布与氦原子相同
C.氢化钠中氢离子半径比锂离子半径小
D.氢化钠中氢离子可被还原成氢气
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
[答案]B
[解析]NaH+HO===NaOH+H↑,故其水溶液显碱性;H-与He原子核外电子层排布都为1s2;H-与
2 2
Li+电子层数相同,但H-原子核内只有一个质子,对核外电子吸引力小于 Li+,故H-的半径大于Li+,
NaH中氢离子可被氧化成氢气。
12.向下列配合物的水溶液中加入AgNO 溶液,不能生成AgCl沉淀的是( )
3
A.[Co(NH )Cl]Cl B.[Co(NH )Cl]
3 4 2 3 3 3
C.[Co(NH )]Cl D.[Co(NH )Cl]Cl
3 6 3 3 5 2
[答案]B
[解析]配合物中由配位键结合的几乎不电离的稳定部分为配合物的内界,通过离子键与内界结合的部
分为配合物的外界,只要外界存在Cl-,加入AgNO 溶液即有AgCl沉淀生成。配合物[Co(NH )Cl]中,
3 3 3 3
Co3+、NH 、Cl-全部处于内界,在溶液中很难电离出 Cl-,加入AgNO 溶液不生成AgCl沉淀,B项符合
3 3
题意。
13.许多过渡金属离子对多种配体有很强的结合力,能形成种类繁多的配合物。下列说法正确的是(
)
A.向配合物[TiCl(H O) ]Cl ·H O溶液中加入足量的AgNO 溶液,所有的Cl-均被完全沉淀
2 5 2 2 3
B.[Pt(NH )]2+和[PtCl ]2-中,其中心离子的化合价都是+2价
3 6 4
C.配合物[Cu(NH )]SO ·H O的配体为NH 和SO
3 4 4 2 3
D.配合物[Ag(NH)]OH的配位数为6
3 2
[答案]B
[解析]加入足量的AgNO 溶液,外界Cl-与Ag+反应生成AgCl沉淀,内界配体Cl-不能电离出来,A
3
错误;[Pt(NH )]2+中,NH 可以看为一个整体,显0价,[PtCl ]2-中,Cl元素显-1价,故两者的中心离子
3 6 3 4
的化合价都是+2价,B正确;配合物[Cu(NH )]SO ·H O的配体为NH ,C错误;配合物[Ag(NH)]OH的
3 4 4 2 3 3 2
配体为NH ,配位数为2,D错误。
3
14.20世纪60年代初,化学家巴特列特用PtF(六氟化铂)与等物质的量的氧气在室温下制得了一种
6
深红色的固体,经实验确认,该化合物的化学式为OPtF 。这是人类第一次制得O的盐。巴特列特经过类
2 6
比和推理,考虑到稀有气体Xe(氙)和O 的第一电离能几乎相等,断定XePtF 也应存在。巴特列特立即动
2 6
手实验,结果在室温下轻而易举地制得了XePtF 黄色固体。根据以上叙述判断下列说法不正确的是( )
6
A.OPtF 可能是离子化合物
2 6
B.XePtF 可能存在离子键
6
C.PtF 具有强氧化性
6
D.Xe元素的化合价一定为零
[答案]D
[解析]A项,抓住“这是人类第一次制得O的盐”,故OPtF 为离子化合物,A正确。XePtF 是巴特
2 6 6
列特类推后制得的,可以推断它的结构类似于OPtF ,也应是一种离子化合物,离子化合物中存在离子键,
2 6
B正确。得电子的是PtF,说明PtF 具有氧化性,C正确。稀有气体原子的最外层有2个或8个电子,属于
6 6
稳定结构,但稀有气体也可以参与反应,形成具有共价键或离子键的化合物,单质Xe的化合价为零,在
其形成的化合物XePtF 中,它的化合价不为零,D错误。
6
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
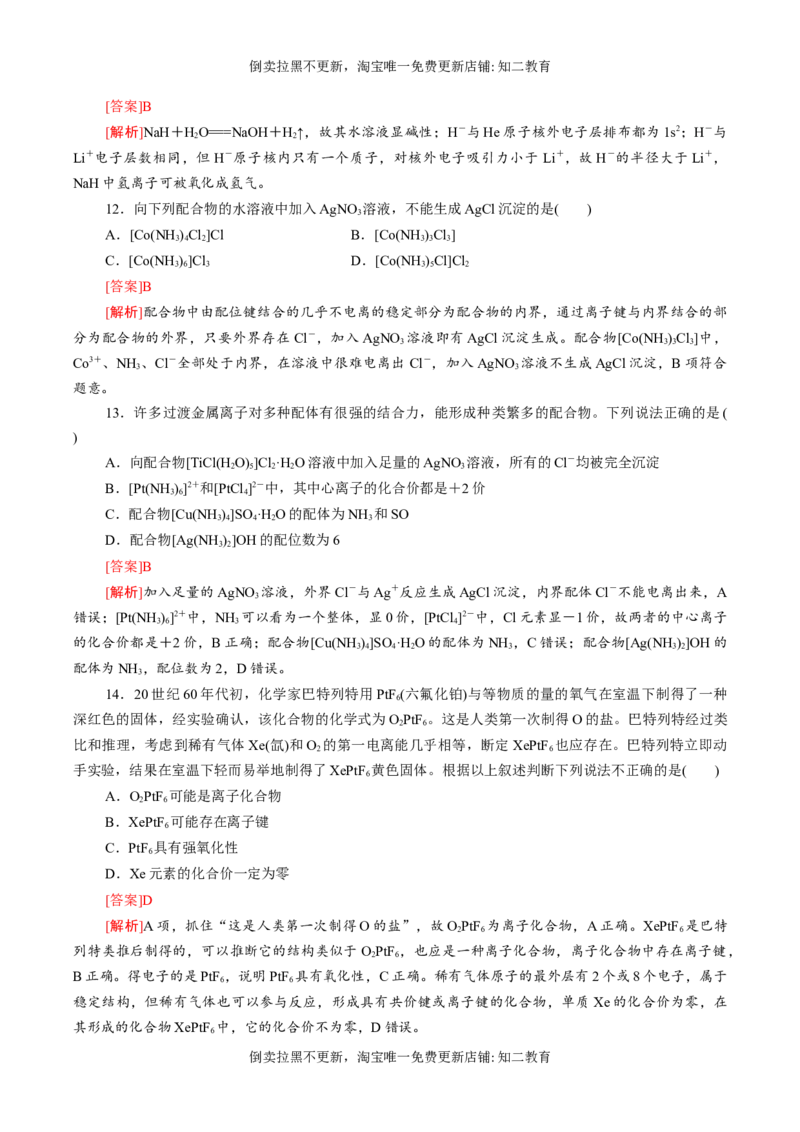
15.已知[Co(NH )]3+的空间结构如图所示,其中数字处的小圆圈表示 NH 分子,且各相邻的NH 分
3 6 3 3
子间的距离相等,Co3+位于八面体的中心。若其中两个NH 被Cl取代,所形成的[Co(NH )Cl]+同分异构
3 3 4 2
体的种数有( )
A.2种 B.3种 C.4种 D.5种
[答案]A
[解析]该配离子的结构为正八面体,正八面体的六个顶点的位置是等效的,选取其中一个取代,剩余
位置有两种,所以二元取代产物为2种。
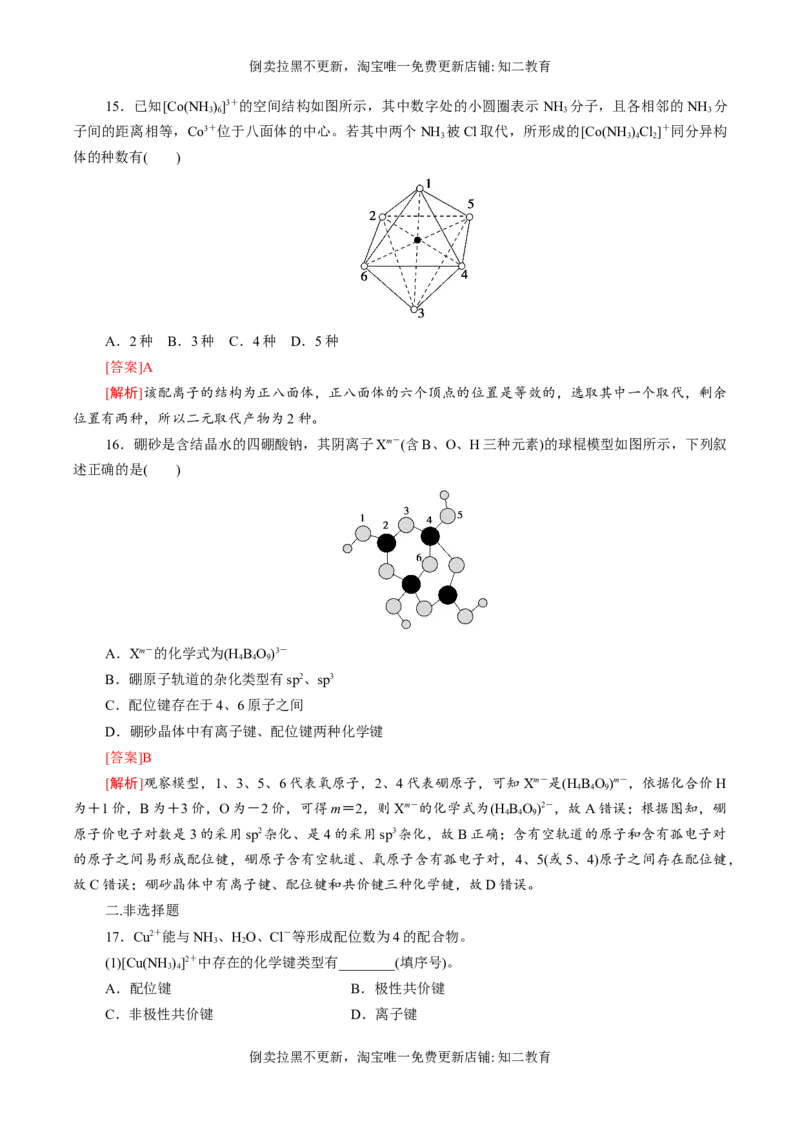
16.硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示,下列叙
述正确的是( )
A.Xm-的化学式为(H B O)3-
4 4 9
B.硼原子轨道的杂化类型有sp2、sp3
C.配位键存在于4、6原子之间
D.硼砂晶体中有离子键、配位键两种化学键
[答案]B
[解析]观察模型,1、3、5、6代表氧原子,2、4代表硼原子,可知Xm-是(H B O)m-,依据化合价H
4 4 9
为+1价,B为+3价,O为-2价,可得m=2,则Xm-的化学式为(H B O)2-,故A错误;根据图知,硼
4 4 9
原子价电子对数是3的采用sp2杂化、是4的采用sp3杂化,故B正确;含有空轨道的原子和含有孤电子对
的原子之间易形成配位键,硼原子含有空轨道、氧原子含有孤电子对,4、5(或5、4)原子之间存在配位键,
故C错误;硼砂晶体中有离子键、配位键和共价键三种化学键,故D错误。
二.非选择题
17.Cu2+能与NH 、HO、Cl-等形成配位数为4的配合物。
3 2
(1)[Cu(NH )]2+中存在的化学键类型有________(填序号)。
3 4
A.配位键 B.极性共价键
C.非极性共价键 D.离子键
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
(2)[Cu(NH )]2+具有对称的空间结构,[Cu(NH )]2+中的两个NH 被两个Cl-取代,能得到两种不同结
3 4 3 4 3
构的产物,则[Cu(NH )]2+的空间结构为________。
3 4
(3)某种含Cu2+的化合物可催化丙烯醇制备丙醛的反应:HOCH CH=== CH―→CHCHCHO。在丙烯
2 2 3 2
醇分子中发生某种方式杂化的碳原子数,是丙醛分子中发生同样方式杂化的碳原子数的2倍,则这类碳原
子的杂化方式为________。
[解析] (1)[Cu(NH )]2+中铜离子与氨分子之间的化学键是配位键,氨分子内部的化学键是极性键。
3 4
(2)[Cu(NH )]2+是平面正方形。
3 4
(3)HOCHCH===CH 中的C原子,有一个采取sp3杂化,两个采取sp2杂化。CHCHCHO中的C原子
2 2 3 2
有两个采取sp3杂化,一个采取sp2杂化。
[答案] (1)AB (2)平面正方形 (3)sp2
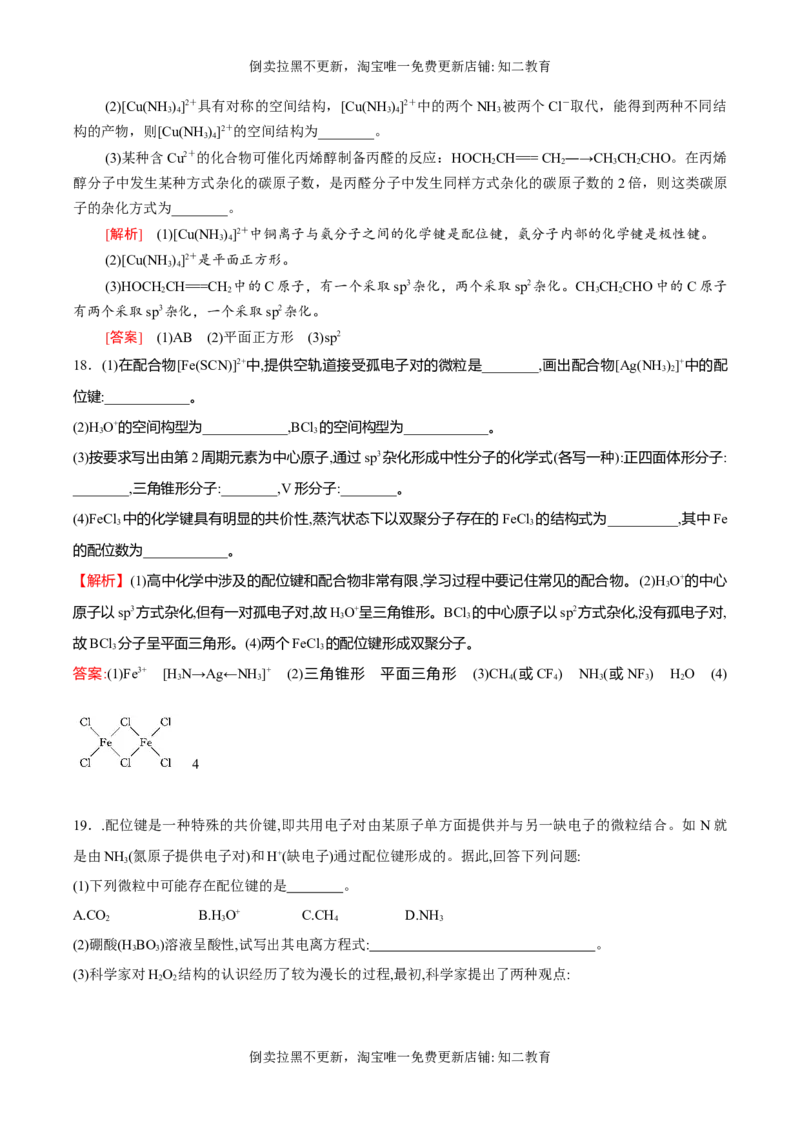
18.(1)在配合物[Fe(SCN)]2+中,提供空轨道接受孤电子对的微粒是________,画出配合物[Ag(NH)]+中的配
3 2
位键:____________。
(2)H O+的空间构型为____________,BCl 的空间构型为____________。
3 3
(3)按要求写出由第2周期元素为中心原子,通过sp3杂化形成中性分子的化学式(各写一种):正四面体形分子:
________,三角锥形分子:________,V形分子:________。
(4)FeCl 中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl 的结构式为__________,其中Fe
3 3
的配位数为____________。
【解析】(1)高中化学中涉及的配位键和配合物非常有限,学习过程中要记住常见的配合物。(2)H O+的中心
3
原子以sp3方式杂化,但有一对孤电子对,故HO+呈三角锥形。BCl 的中心原子以sp2方式杂化,没有孤电子对,
3 3
故BCl 分子呈平面三角形。(4)两个FeCl 的配位键形成双聚分子。
3 3
答案:(1)Fe3+ [H N→Ag←NH ]+ (2)三角锥形 平面三角形 (3)CH (或CF) NH (或NF ) HO (4)
3 3 4 4 3 3 2
4
19..配位键是一种特殊的共价键,即共用电子对由某原子单方面提供并与另一缺电子的微粒结合。如 N就
是由NH (氮原子提供电子对)和H+(缺电子)通过配位键形成的。据此,回答下列问题:
3
(1)下列微粒中可能存在配位键的是 。
A.CO B.H O+ C.CH D.NH
2 3 4 3
(2)硼酸(H BO)溶液呈酸性,试写出其电离方程式: 。
3 3
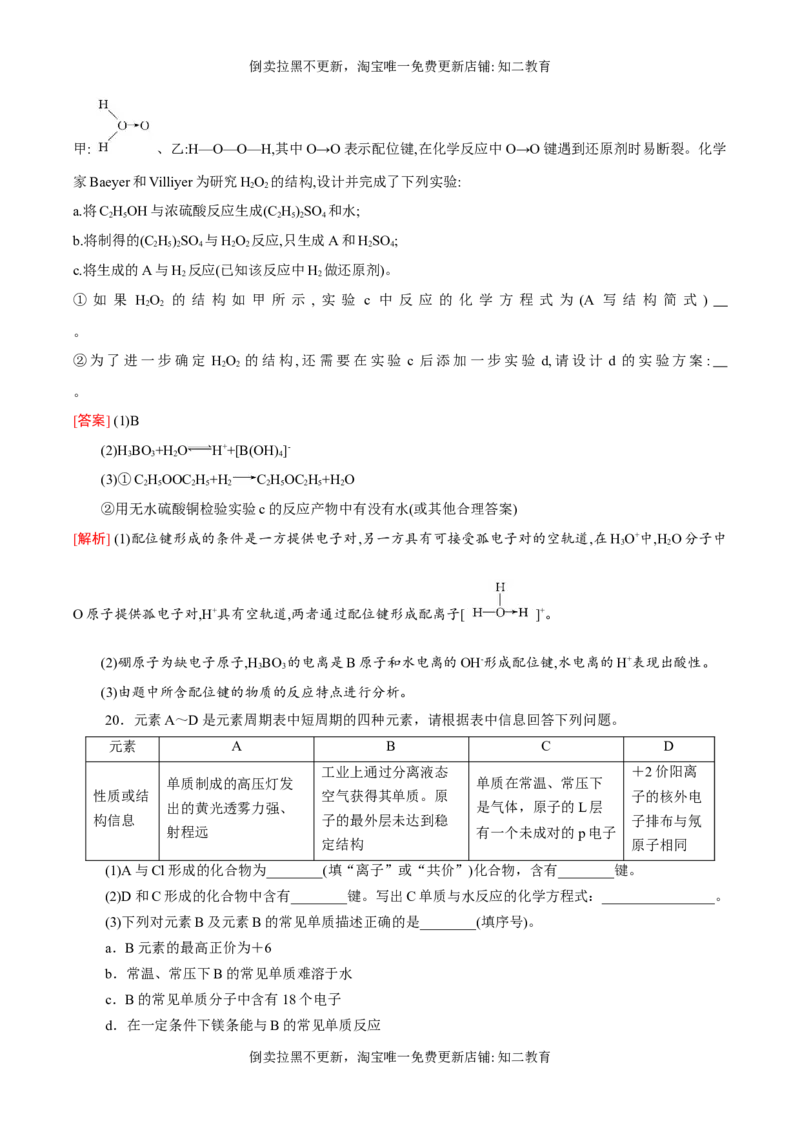
(3)科学家对HO 结构的认识经历了较为漫长的过程,最初,科学家提出了两种观点:
2 2
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
甲: 、乙:H—O—O—H,其中O→O表示配位键,在化学反应中O→O键遇到还原剂时易断裂。化学
家Baeyer和Villiyer为研究HO 的结构,设计并完成了下列实验:
2 2
a.将C HOH与浓硫酸反应生成(C H)SO 和水;
2 5 2 5 2 4
b.将制得的(C H)SO 与HO 反应,只生成A和HSO ;
2 5 2 4 2 2 2 4
c.将生成的A与H 反应(已知该反应中H 做还原剂)。
2 2
① 如 果 HO 的 结 构 如 甲 所 示 , 实 验 c 中 反 应 的 化 学 方 程 式 为 (A 写 结 构 简 式 )
2 2
。
②为了进一步确定 HO 的结构,还需要在实验 c 后添加一步实验 d,请设计 d 的实验方案:
2 2
。
[答案] (1)B
(2)H BO+H O H++[B(OH) ]-
3 3 2 4
(3)①C HOOC H+H C HOC H+H O
2 5 2 5 2 2 5 2 5 2
②用无水硫酸铜检验实验c的反应产物中有没有水(或其他合理答案)
[解析] (1)配位键形成的条件是一方提供电子对,另一方具有可接受孤电子对的空轨道,在HO+中,H O分子中
3 2
O原子提供孤电子对,H+具有空轨道,两者通过配位键形成配离子[ ]+。
(2)硼原子为缺电子原子,H BO 的电离是B原子和水电离的OH-形成配位键,水电离的H+表现出酸性。
3 3
(3)由题中所含配位键的物质的反应特点进行分析。
20.元素A~D是元素周期表中短周期的四种元素,请根据表中信息回答下列问题。
元素 A B C D
工业上通过分离液态 +2价阳离
单质制成的高压灯发 单质在常温、常压下
性质或结 空气获得其单质。原 子的核外电
出的黄光透雾力强、 是气体,原子的L层
构信息 子的最外层未达到稳 子排布与氖
射程远 有一个未成对的p电子
定结构 原子相同
(1)A与Cl形成的化合物为________(填“离子”或“共价”)化合物,含有________键。
(2)D和C形成的化合物中含有________键。写出C单质与水反应的化学方程式:________________。
(3)下列对元素B及元素B的常见单质描述正确的是________(填序号)。
a.B元素的最高正价为+6
b.常温、常压下B的常见单质难溶于水
c.B的常见单质分子中含有18个电子
d.在一定条件下镁条能与B的常见单质反应
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
(4)若B与H能形成BH,则B为________元素,BH中含有的化学键为________。
(5)A和D两元素中金属性较强的是________(写元素符号),写出能证明该结论的一个实验事实:
__________________________。
[解析] 由四种元素为短周期元素可知,A、B、C、D的原子序数均不大于18。由A单质的用途可知,
A为Na元素;由B单质的工业制法及原子结构特点可知,B为N元素或O元素;由C原子的电子排布特
点可知C可能为B元素或F元素,又由其物理性质可推断出C为F元素;由D的+2价阳离子的结构特点
可知,D为Mg元素。(3)O元素或N元素均无+6价,故a项错误;由于B的常见单质为N 或O ,O 、N
2 2 2 2
在常温常压下均难溶于水,故b项正确;O 分子中含有16个电子,N 分子中含有14个电子,故c项错误;
2 2
2Mg+O 2MgO,3Mg+N MgN ,故d项正确。(4)由题意知B为N元素,NH中含有的化学键为
2 2 3 2
共价键和配位键。(5)比较金属性强弱的依据有:①与水(或酸)反应的剧烈程度;②最高价氧化物对应水化
物的碱性强弱;③金属间的置换反应等。
[答案] (1)离子 离子
(2)离子 2F+2HO===4HF+O
2 2 2
(3)bd
(4)N 共价键、配位键
(5)Na 钠与水反应比镁与水反应剧烈(或氢氧化钠的碱性比氢氧化镁强,答案合理即可)
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育