文档内容
2021-2022 学年高二化学重难点专题突破
模块二 分子结构与性质
专题 07 化学键、范德华力和氢键的判断与应用
一.选择题
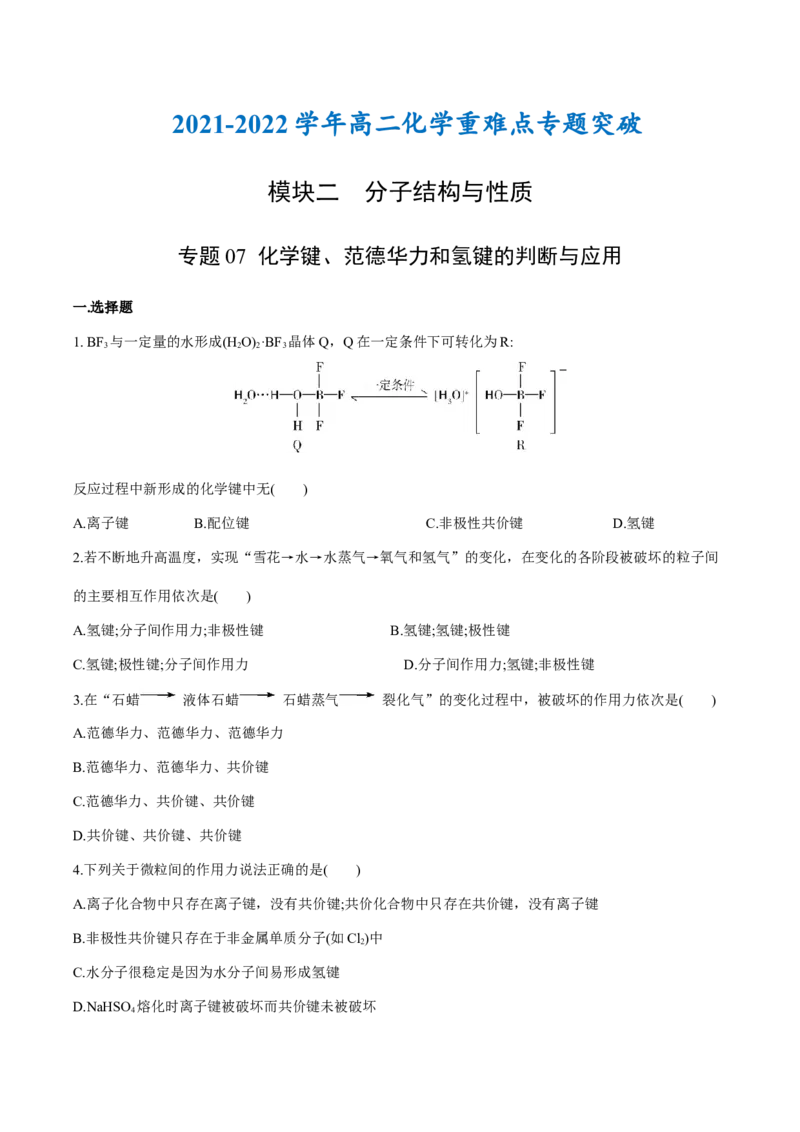
1. BF 与一定量的水形成(H O) ·BF 晶体Q,Q在一定条件下可转化为R:
3 2 2 3
反应过程中新形成的化学键中无( )
A.离子键 B.配位键 C.非极性共价键 D.氢键
2.若不断地升高温度,实现“雪花→水→水蒸气→氧气和氢气”的变化,在变化的各阶段被破坏的粒子间
的主要相互作用依次是( )
A.氢键;分子间作用力;非极性键 B.氢键;氢键;极性键
C.氢键;极性键;分子间作用力 D.分子间作用力;氢键;非极性键
3.在“石蜡 液体石蜡 石蜡蒸气 裂化气”的变化过程中,被破坏的作用力依次是( )
A.范德华力、范德华力、范德华力
B.范德华力、范德华力、共价键
C.范德华力、共价键、共价键
D.共价键、共价键、共价键
4.下列关于微粒间的作用力说法正确的是( )
A.离子化合物中只存在离子键,没有共价键;共价化合物中只存在共价键,没有离子键
B.非极性共价键只存在于非金属单质分子(如Cl)中
2
C.水分子很稳定是因为水分子间易形成氢键
D.NaHSO 熔化时离子键被破坏而共价键未被破坏
45.下列有关作用力的说法不正确的是( )
A.酒精易溶于水主要是因为酒精分子与水分子之间能形成氢键
B.含极性键的分子不一定是极性分子
C.NHCl受热分解时只破坏离子键
4
D.HCl、HBr、HI的熔点和沸点依次升高与范德华力大小有关
6. 2018年1月26日,中国科技大学的教授们将水置于一个20 ℃、足够强的电场中,水瞬间凝固形成“暖
冰”。则关于“暖冰”的判断正确的是( )
A.“暖冰”中存在离子键
B.“暖冰”中水分子的O—H键是非极性键
C.“暖冰”有良好的导电性和导热性
D.水凝固形成20 ℃时的“暖冰”所发生的变化是物理变化
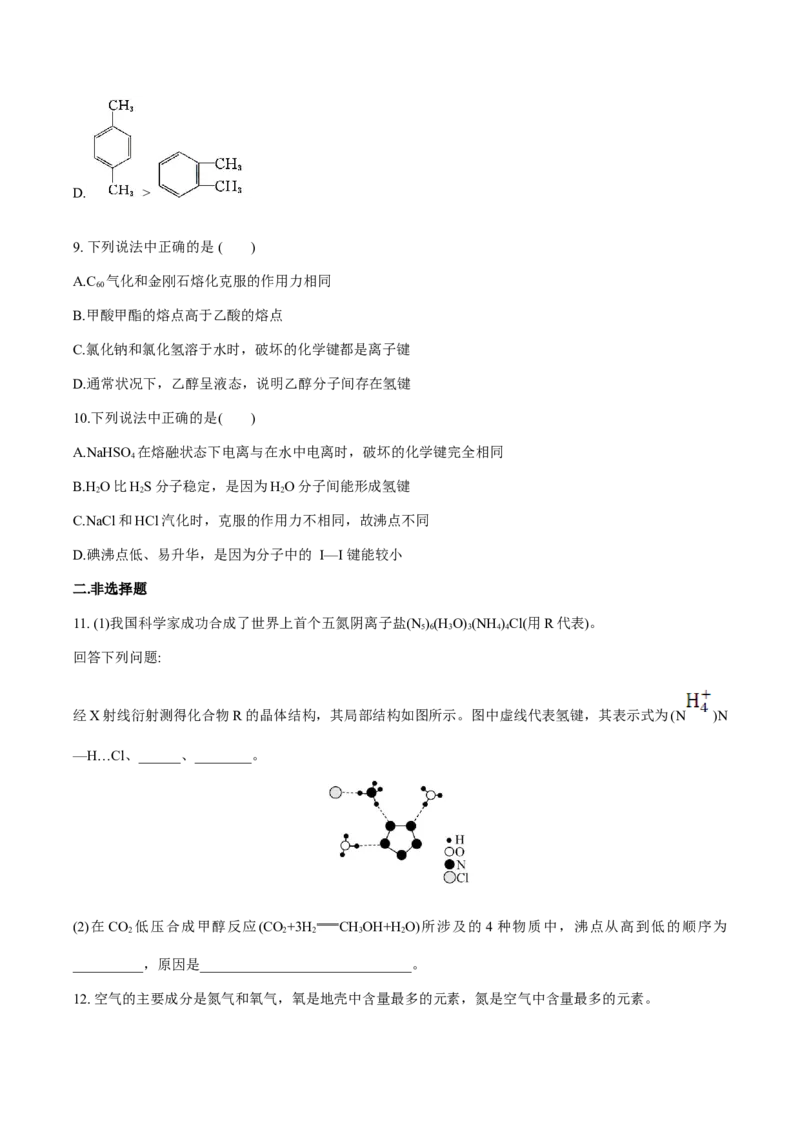
7.(双选)如图是元素周期表的一部分,所列字母分别代表一种化学元素。下列说法正确的是( )
A.b的第一电离能小于c的第一电离能
B.d在c的常见单质中燃烧,产物中既含有离子键也含有共价键
C.e与a组成的化合物沸点比水低,原因是水分子之间可形成氢键
D.f元素的基态原子失去4s能级上的所有电子后所形成的离子最稳定
8. 下列有关范德华力的强弱对比正确的是 ( )
A.CH>CH CH
4 3 3
B.CH CHCHCHCH>
3 2 2 2 3
C.SO
9. 下列说法中正确的是( )
A.C 气化和金刚石熔化克服的作用力相同
60
B.甲酸甲酯的熔点高于乙酸的熔点
C.氯化钠和氯化氢溶于水时,破坏的化学键都是离子键
D.通常状况下,乙醇呈液态,说明乙醇分子间存在氢键
10.下列说法中正确的是( )
A.NaHSO 在熔融状态下电离与在水中电离时,破坏的化学键完全相同
4
B.H O比HS分子稳定,是因为HO分子间能形成氢键
2 2 2
C.NaCl和HCl汽化时,克服的作用力不相同,故沸点不同
D.碘沸点低、易升华,是因为分子中的 I—I 键能较小
二.非选择题
11. (1)我国科学家成功合成了世界上首个五氮阴离子盐(N )(H O) (NH )Cl(用R代表)。
5 6 3 3 4 4
回答下列问题:
经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。图中虚线代表氢键,其表示式为(N )N
—H…Cl、______、________。
(2)在 CO 低压合成甲醇反应(CO+3H CHOH+H O)所涉及的 4 种物质中,沸点从高到低的顺序为
2 2 2 3 2
__________,原因是______________________________。
12. 空气的主要成分是氮气和氧气,氧是地壳中含量最多的元素,氮是空气中含量最多的元素。(1)水在常温情况下,其组成的化学式可用(H O) 表示,为什么?____________ ____________。
2 m
(2)从氨合成塔里分离H、N、NH 的混合物,采用____________方法,为什么?__________________。
2 2 3
(3)N、P、As都属于第ⅤA族元素,形成简单氢化物的沸点由高到低的顺序为_______>_______>_______。
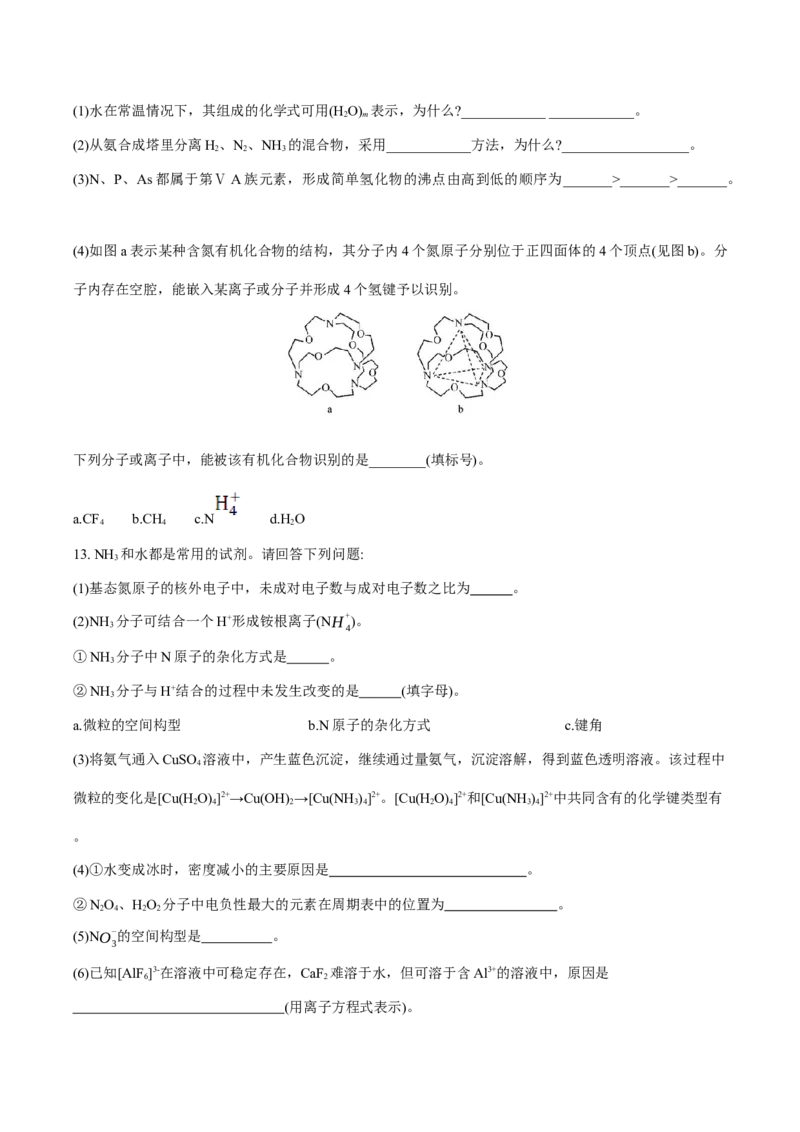
(4)如图a表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图b)。分
子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。
下列分子或离子中,能被该有机化合物识别的是________(填标号)。
a.CF b.CH c.N d.H O
4 4 2
13. NH 和水都是常用的试剂。请回答下列问题:
3
(1)基态氮原子的核外电子中,未成对电子数与成对电子数之比为 。
(2)NH 分子可结合一个H+形成铵根离子(NH+)。
3 4
①NH 分子中N原子的杂化方式是 。
3
②NH 分子与H+结合的过程中未发生改变的是 (填字母)。
3
a.微粒的空间构型 b.N原子的杂化方式 c.键角
(3)将氨气通入CuSO 溶液中,产生蓝色沉淀,继续通过量氨气,沉淀溶解,得到蓝色透明溶液。该过程中
4
微粒的变化是[Cu(H O) ]2+→Cu(OH) →[Cu(NH )]2+。[Cu(H O) ]2+和[Cu(NH )]2+中共同含有的化学键类型有
2 4 2 3 4 2 4 3 4
。
(4)①水变成冰时,密度减小的主要原因是 。
②NO、HO 分子中电负性最大的元素在周期表中的位置为 。
2 4 2 2
(5)NO-的空间构型是 。
3
(6)已知[AlF ]3-在溶液中可稳定存在,CaF 难溶于水,但可溶于含Al3+的溶液中,原因是
6 2
(用离子方程式表示)。(7)F 通入稀NaOH溶液中可生成OF ,OF 分子的空间构型为 ,其中氧原子的杂化方式为
2 2 2
。
14.海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。
(1)在光照条件下,氯气和氢气反应过程如下:
①Cl Cl+Cl ②Cl+H HCl+H
2 2
③H+Cl HCl+Cl……
2
反应②中形成的化合物的电子式为 ;反应③中被破坏的化学键属于 键(填“极性”或“非极
性”)。
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是 (用元素符号表
示)。与氯元素同周期且金属性最强的元素位于周期表的第 周期 族。
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是 。
a.卤化银的颜色按AgCl、AgBr、AgI的顺序依次加深
b.卤化氢的键长按H—F、H—Cl、H—Br、H—I键的顺序依次减小
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d.卤素单质与氢气化合按F、Cl、Br 、I 的顺序由难变易
2 2 2 2
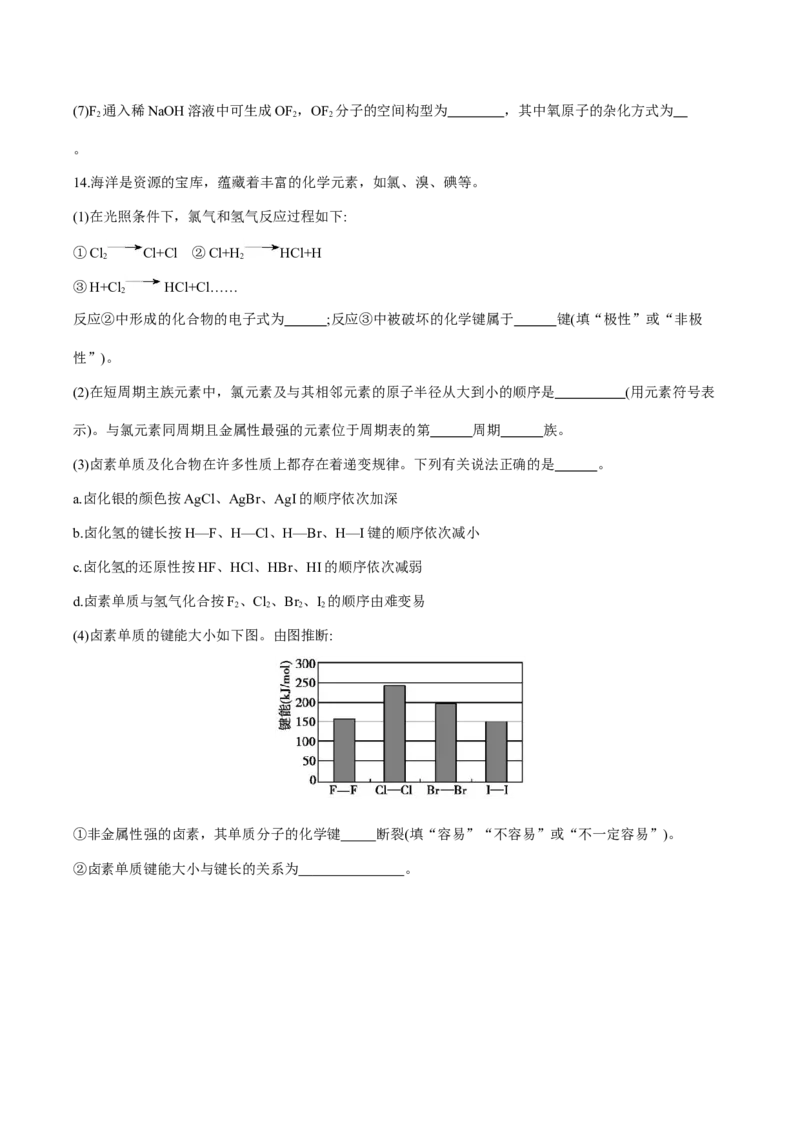
(4)卤素单质的键能大小如下图。由图推断:
①非金属性强的卤素,其单质分子的化学键 断裂(填“容易”“不容易”或“不一定容易”)。
②卤素单质键能大小与键长的关系为 。倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育