文档内容
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
2021-2022 学年高二化学重难点专题突破
模块三 晶体结构与性质
专题 09 四类典型晶体的比较及应用
一.选择题
1.下面的排序不正确的是( )
A.熔点由高到低:Na>Mg>Al
B.硬度由大到小:金刚石>碳化硅>晶体硅
C.晶体熔点由低到高:CF碳化硅>硅
2.下列晶体熔、沸点由高到低的顺序正确的是( )
①SiC ②Si ③HCl ④HBr ⑤HI ⑥CO ⑦N ⑧H
2 2
A.①②③④⑤⑥⑦⑧ B.①②⑤④③⑥⑦⑧
C.①②⑤④③⑦⑥⑧ D.⑥⑤④③②①⑦⑧
3.下列物质的熔沸点高低顺序正确的是( )
A.金刚石>晶体硅>二氧化硅>碳化硅
B.CI >CBr >CCl >CH
4 4 4 4
C.MgO>H O>N>O
2 2 2
D.金刚石>生铁>纯铁>钠
4.下列物质性质的变化规律,与共价键的键能大小有关的是( )
A.F、Cl、Br 、I 的熔点、沸点逐渐升高
2 2 2 2
B.HF、HCl、HBr的熔、沸点顺序为HF>HBr>HCl
C.金刚石的硬度、熔点、沸点都高于晶体硅
D.NaF、NaCl、NaBr、NaI的熔点依次降低
5.下列各组物质中,按熔点由低到高的顺序排列正确的是( )
①O、I、Hg ②CO、KCl、SiO
2 2 2
③Na、K、Rb ④Na、Mg、Al
A.①③ B.①④
C.②③ D.②④
6.下列各物质的晶体中,晶体类型相同的是( )
A.O 和SiO B.NaI和I
2 2 2
C.CO 和HO D.CCl 和NaCl
2 2 4
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
7.根据下列几种物质的熔点和沸点数据,判断下列有关说法中,错误的是( )
NaCl MgCl AlCl SiCl 单质B
2 3 4
熔点/℃ 810 710 190 -68 2 300
沸点/℃ 1 465 1 418 182.7 57 2 500
A.SiCl 是分子晶体
4
B.单质B是原子晶体
C.AlCl 加热能升华
3
D.MgCl 所含离子键的强度比NaCl大
2
8.X和Y两种元素的核电荷数之和为22,X的原子核外电子数比Y的少6个。下列说法中不正确的
是( )
A.X的单质固态时为分子晶体
B.Y的单质为共价晶体
C.X与Y形成的化合物固态时为分子晶体
D.X与碳形成的化合物为分子晶体
9.下列各组物质中,化学键类型相同、晶体类型也相同的是( )
A.CaCl 和NaOH B.碘、氖
2
C.CO 和HO D.CCl 和KCl
2 2 4
10.下列说法中正确的是( )
A.固态时能导电的物质一定是金属晶体
B.熔融状态能导电的晶体一定是离子晶体
C.水溶液能导电的晶体一定是离子晶体
D.固态不导电而熔融态导电的晶体一定是离子晶体
二.非选择题
11.分析下列物质的物理性质,判断其晶体类型。
(1)碳化铝,黄色晶体,熔点2 200 ℃,熔融态不导电:________。
(2)溴化铝,无色晶体,熔点98 ℃,熔融态不导电:________。
(3)五氟化矾,无色晶体,熔点19.5 ℃,易溶于乙醇、氯仿、丙酮等:________。
(4)溴化钾,无色晶体,熔融时或溶于水中都能导电:________。
(5)SiI:熔点120.5 ℃,沸点287.4 ℃,易水解:________。
4
(6)硼:熔点2 300 ℃,沸点2 550 ℃,硬度大:________。
(7)硒:熔点217 ℃,沸点685 ℃,溶于氯仿:________。
(8)锑:熔点630.74 ℃,沸点1 750 ℃,导电:________。
12.现有几组物质的熔点(℃)数据:
A组 B组 C组 D组
金刚石:3 550 ℃ Li:181 ℃ HF:-83 ℃ NaCl:801 ℃
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
硅晶体:1 410 ℃ Na:98 ℃ HCl:-115 ℃ KCl:776 ℃
硼晶体:2 300 ℃ K:64 ℃ HBr:-89 ℃ RbCl:718 ℃
二氧化硅:1 723 ℃ Rb:39 ℃ HI:-51 ℃ CsCl:645 ℃
据此回答下列问题:
(1)A组属于________晶体,其熔化时克服的微粒间的作用力是________。
(2)B组晶体共同的物理性质是________(填序号)。
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于______________________。
(4)D组晶体可能具有的性质是________(填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)D 组 晶 体 的 熔 点 由 高 到 低 的 顺 序 为 NaCl>KCl>RbCl>CsCl , 其 原 因 为
_______________________________________。
13.氯酸钾熔化,粒子间克服了 ;二氧化硅熔化,粒子间克服了 ;碘的升华,粒子间克服了
。三种晶体的熔点由高到低的顺序是 。
(2)下列六种晶体:①CO,②NaCl,③Na,④Si,⑤CS,⑥金刚石,它们的熔点从低到高的顺序为 (填序号)。
2 2
(3)在H、(NH )SO 、SiC、CO、HF中,五种物质的熔点由低到高的顺序是 。
2 4 2 4 2
(4)A、B、C、D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS,不溶于水
2
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3 500 ℃
试推断它们的晶体类型:A ;B ;C ;D 。
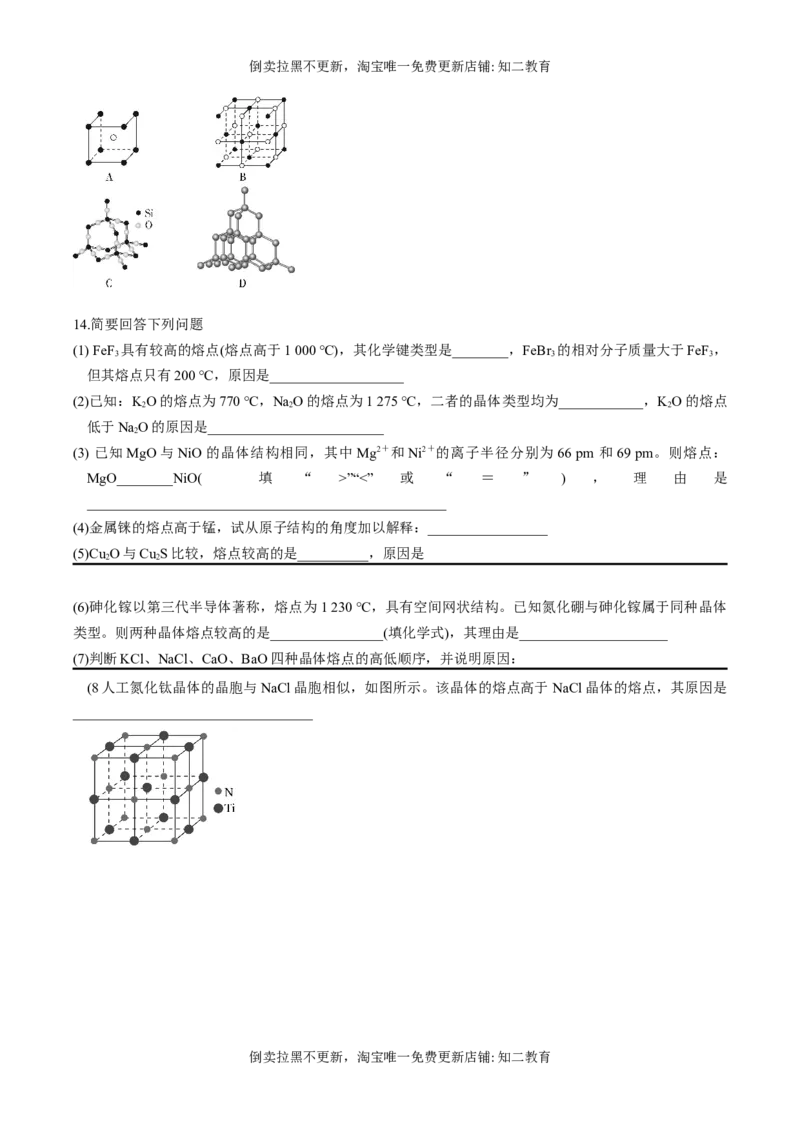
(5)如图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:A ;B
;C ;D 。
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
14.简要回答下列问题
(1) FeF 具有较高的熔点(熔点高于1 000 ℃),其化学键类型是________,FeBr 的相对分子质量大于FeF ,
3 3 3
但其熔点只有200 ℃,原因是___________________
(2)已知:KO的熔点为770 ℃,NaO的熔点为1 275 ℃,二者的晶体类型均为____________,KO的熔点
2 2 2
低于NaO的原因是_________________________
2
(3) 已知MgO与NiO的晶体结构相同,其中Mg2+和Ni2+的离子半径分别为66 pm 和69 pm。则熔点:
MgO________NiO( 填 “ >”“<” 或 “ = ” ) , 理 由 是
___________________________________________________
(4)金属铼的熔点高于锰,试从原子结构的角度加以解释:_________________
(5)Cu O与Cu S比较,熔点较高的是__________,原因是
2 2
(6)砷化镓以第三代半导体著称,熔点为1 230 ℃,具有空间网状结构。已知氮化硼与砷化镓属于同种晶体
类型。则两种晶体熔点较高的是________________(填化学式),其理由是_____________________
(7)判断KCl、NaCl、CaO、BaO四种晶体熔点的高低顺序,并说明原因:
(8人工氮化钛晶体的晶胞与NaCl晶胞相似,如图所示。该晶体的熔点高于NaCl晶体的熔点,其原因是
__________________________________
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育
倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育