文档内容
第一章 物质及其变化
第一节 物质的分类和转化
第2课时 物质的转化
(1)能对酸、碱、盐、氧化物及它们之间的反应进行描述和符号表征。
(2)通过归纳相关物间的化学反应关系,建立物质转化模型,认识物质的变化规律。
【内容分析】
根据课程标准的要求,以及初、高中化学教学衔接的实际需要,本节安排了两部分内容:物质的分类,
物质的转化。
在物质分类的基础上,教材以“思考与讨论”的形式,引导学生复习酸、碱、盐的主要化学性质,如
列举反应实例,说明反应类型等。这样安排的主要目的是通过学生活动的形式进一步巩固初中化学的就知
识,加深学生对物质间建化学反球律的认识,为介绍物质之间的转化作准备。
教材指岀,考虑如何实现物质之间的转化时最基本的依据是化学变化过程中元素不会改变,这是化学
的基本观念之一。随后通过“思考与讨论”,以含Ca、C元素的物质为例,引导学生认识不同类别物质之
间的转化关系及反应规律。同时强调,物质转化的价值在于制备人类生活和生产所需要的新物质,并指出
工业生产中制取某种物质时要考虑的因素,目的是培养学生综合考虑问题的意识。
本节内容的特点是源于初中,高于初中。在编排思路上,教材注意与初中化学相关知识的合理衔接,
以物质的转化为线索,复习和巩固旧知识,适当引入新知识。在科学方法和科学观念方面,教材突出强调
物质转化的价值。这样编排,既可以减轻学生进入高中化学学习的不适感,有利于激发学生的学习兴趣;又
能够使学生站在更高的角度学习化学,有利于发展化学学科核心素养。【教学重点和难点】
重点:建立各类物质的转化关系模型。
难点:各类物质间的转化关系。
【教学流程】
【学习任务一】酸、碱、盐的化学性质
【初高中知识链接】
【活动一】同类物质往往具有相似的性质,请同学们完成P10思考与讨论。
【设计意图】以“思考与讨论”的形式,引导学生复习酸、碱、盐的主要化学性质,主要目的是通过学生
活动的形式进一步巩固初中化学的重点知识,加深学生对物质间发生化学反应规律的认识,为介绍物质之
间的转化作准备。
【活动二】讨论为什么不同的酸 (或碱 )具有相似的化学性质?
【设计意图】从宏观辨识到微观探析,加深学生对反应本质的认识。
【学习任务二】物质的转化
根据物质的组成和性质,通过化学变化可以实现物质之间的转化。在化学变化过程中,元素是不会改变的,这
是考虑如何实现物质之间的转化时最基本的依据。
【活动一】请同学们完成P11思考与讨论
【设计意图】引导学生认识不同类别物质之间的转化关系及反应规律。
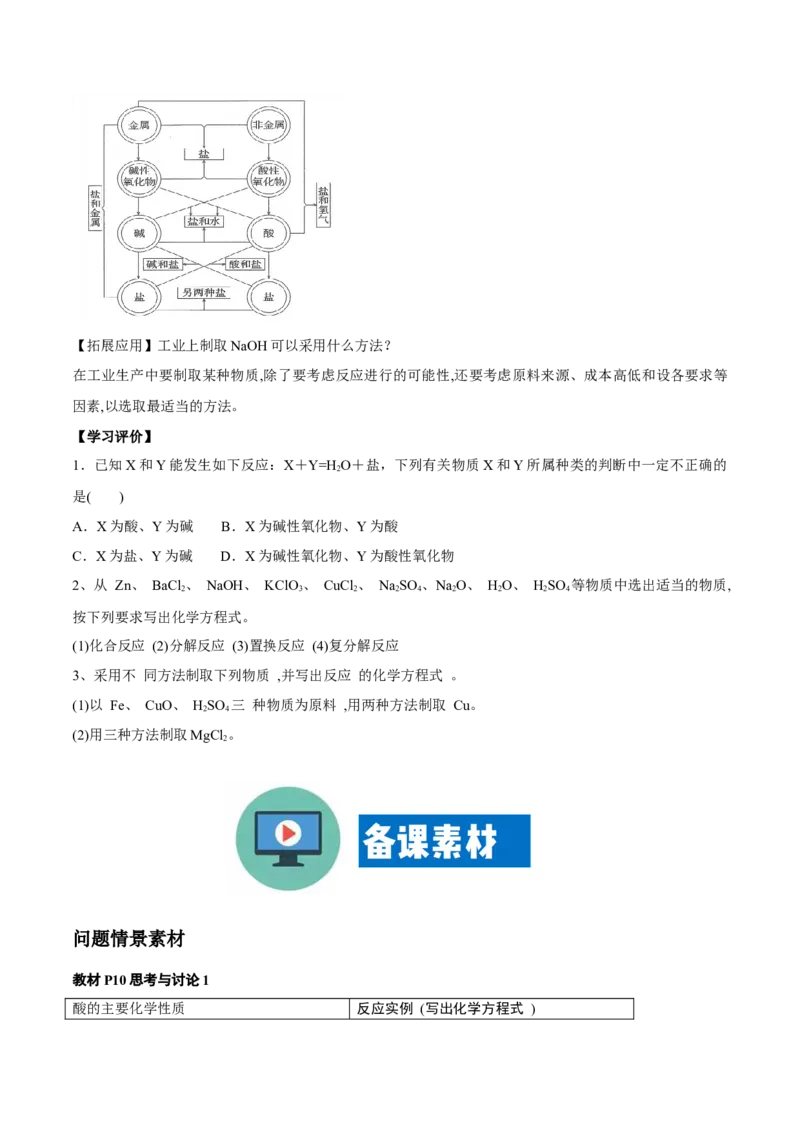
归纳总结:从物质的分类角度小结物质转化关系
【活动二】根据上面的转化过程,写出由金属单质Na到NaCO、非金属单质S到对应盐CuSO 的转化过
2 3 4
程。
讨论两个物质系列之间可能发生的反应。
【设计意图】各类物质之间的反应规律对学习理解具体反应具有指导意义,为后续课程中关于元素化合物
知识的学习奠定基础。两个物质系列之间的反应关系可以概括为“化学性质’对立’的物质之间容易发生
反应”。掌握了这样的规律就能帮助学生增强判断力,扩大知识视野,提高学习效率。【拓展应用】工业上制取NaOH可以采用什么方法?
在工业生产中要制取某种物质,除了要考虑反应进行的可能性,还要考虑原料来源、成本高低和设各要求等
因素,以选取最适当的方法。
【学习评价】
1.已知X和Y能发生如下反应:X+Y=HO+盐,下列有关物质X和Y所属种类的判断中一定不正确的
2
是( )
A.X为酸、Y为碱 B.X为碱性氧化物、Y为酸
C.X为盐、Y为碱 D.X为碱性氧化物、Y为酸性氧化物
2、从 Zn、 BaCl 、 NaOH、 KClO 、 CuCl 、 NaSO 、NaO、 HO、 HSO 等物质中选出适当的物质,
2 3 2 2 4 2 2 2 4
按下列要求写出化学方程式。
(1)化合反应 (2)分解反应 (3)置换反应 (4)复分解反应
3、采用不 同方法制取下列物质 ,并写出反应 的化学方程式 。
(1)以 Fe、 CuO、 HSO 三 种物质为原料 ,用两种方法制取 Cu。
2 4
(2)用三种方法制取MgCl 。
2
问题情景素材
教材P10思考与讨论1
酸的主要化学性质 反应实例 (写出化学方程式 )酸与活泼金属反应
酸与碱性氧化物反应
酸与碱反应
酸与某些盐反应
(2)请分别归纳碱和盐这两类物质的主要化学性质。
(3)讨论:酸、碱、盐的主要化学性质中,涉及哪些反应类型?
【使用建议】
1、复习回顾酸、碱、盐的化学性质。
2、列举实例并要求学生写出化学方程式。
3、分析酸碱盐性质反应的反应类型,总结酸、碱、盐相互之间反应属于复分解反应。
教材P10思考与讨论2
(1)写出下列物质之间转化的化学方程式 ,体会由金属单质到盐、非金属单质到盐的转化关系。
Ca→CaO→ Ca(OH) →CaSO
2 4
C—>CO -→ H CO-→ CaCO
2 2 3 3
(1) 对于上述转化关系,从物质分类的角度看 ,你发现了什么规律?将你的想法与同学交流。
【使用建议】
1、从物质分类的角度构建转化规律认知模型
2、进一步引导学生将物质分为酸性物质和碱性物质,两个“化学性质’对立’的物质之间容易发生反
应”,掌握了这样的规律就能帮助学生增强判断力,扩大知识视野,提高学习效率。
练习与应用(教材P12)
5.从 Zn、 BaC1 、 NaOH、 KClO、CuC1 、NaSO 、Na0、 H0、 HSO 等物质中,选出适当的物质,按
2 3 2 2 4 2 2 2 4
下列要求写出化学方程式。
(1)化合反应
(2)分解反应
(3)置换反应
(4)复分解反应6.写出下列物质之间转化的化学方程式。
(1)Cu→CuO→CuSO → Cu(OH) 、 → CuSO -→ Cu。
4 2 4
(2)C→ CO → CaCO → CaO→ Ca(OH) → CaCl
2 3 2 2
7、采用不同方法制取下列物质 ,并写出反应的化学方程式 。
(1)以 Fe、 CuO、 HSO 三 种物质为原料 ,用两种方法制取 Cu。
2 4
(2)用三种方法制取MgC1 。
2
8.许多食品包装袋中常有一个小纸袋,内盛白色固体物质,标有 “干燥剂”字样,其主要成分为生石灰。
(1)写出生石灰的化学式。生石灰属于哪一类别的物质?
(2)生石灰为什么可用作干燥剂 (用化学方程式表示 )?
(3)生石灰可以与哪些类别的物质发生化学反应?请列举两例,并写出反应的化学方程式。
(4)在你学过的物质中,还有哪些物质可用作干燥剂?
答案
5. (1)化合反应:NaO+HO=2NaOH
2 2
(2)分解反应:
(3) 置换反应:Zn+CuCl =ZnCl +Cu Zn+H SO =ZnSO +H ↑
2 2 2 4 4 2
(4)复分解反应:BaCl +Na SO =BaSO ↓+2NaClBaCl +H SO =BaSO ↓+2HCl
2 2 4 4 2 2 4 4
2NaOH+CuC1 =Cu(OH) ↓ +2NaCl 2NaOH+HSO =Na SO +2H O Na O+HSO =Na SO +H O
2 2 2 4 2 4 2 2 2 4 2 4 2
6. (1) CuO+HSO =CuSO+H O CuSO +2NaOH=Cu(OH) ↓+Na SO
2 4 4 2 4 2 2 4
Cu(OH) +H SO =CuSO+2H O
2 2 4 4 2
CuSO +Zn=Cu+ZnSO
4 4
(2) CO+CaO=CaCO CaO+H O=Ca(OH) Ca(OH)+2HCl=CaCl +2H O
2 3 2 2 2 2 2
7.(1)方法①:CuO+HSO =CuSO+H O Fe+CuSO =FeSO+Cu
2 4 4 2 4 4
方法②:Fe+H SO =FeSO+H ↑
2 4 4 2
(2 )方法①: Mg+2HCl=MgCl +H ↑
2 2
方法②:MgO+2HCl=MgCl +H O
2 2
方法③:Mg(OH) +2HCl=MgCl +2H O
2 2 2
8.(1)CaO碱性氧化物、金属氧化物
【解析】按照不同的标准,一种物质可以分属不同类型。
(2) CaO+H O=Ca(OH)
2 2(3) 酸、酸性氧化物、水。如 CaO+2HCl=CaCl +H O
2 2
CaO+H O=Ca(OH)
2 2
【解析】应从碱性氧化物的共性出发进行预测。
(4) 浓硫酸、五氧化二磷、硅胶、无水氯化钙