文档内容
第 12 讲 化学电池
知识导航
知识精讲
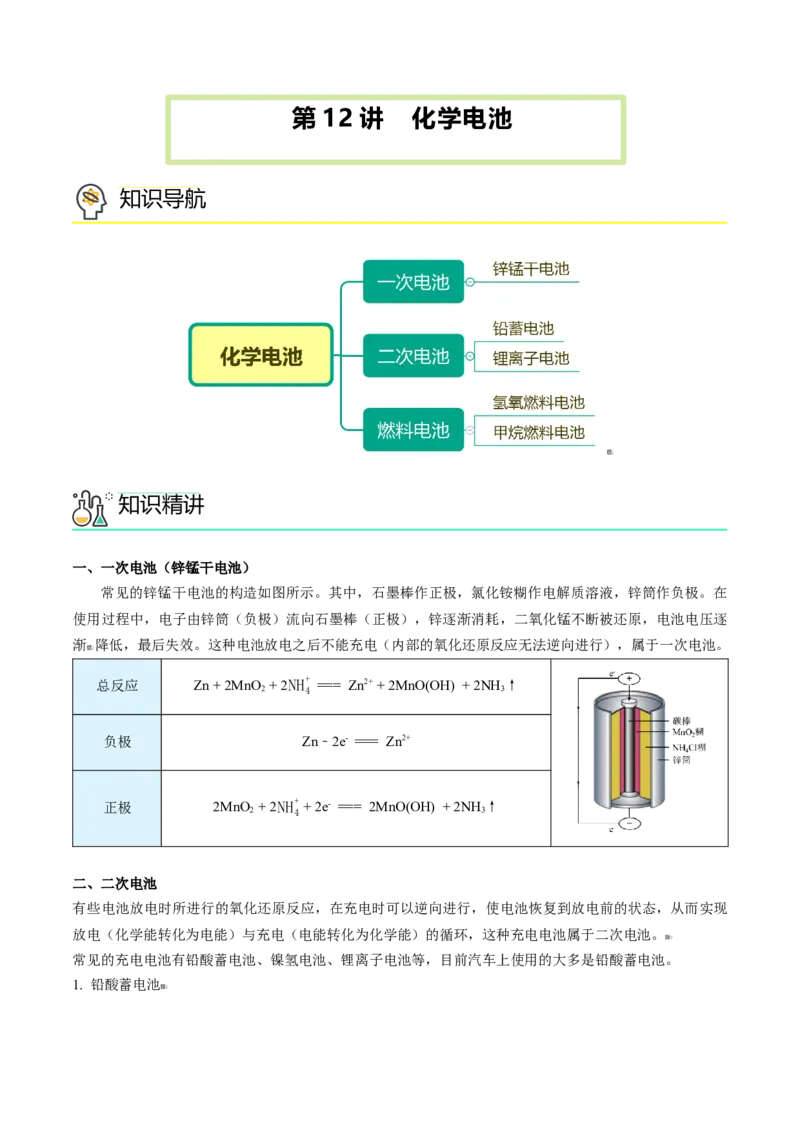
一、一次电池(锌锰干电池)
常见的锌锰干电池的构造如图所示。其中,石墨棒作正极,氯化铵糊作电解质溶液,锌筒作负极。在
使用过程中,电子由锌筒(负极)流向石墨棒(正极),锌逐渐消耗,二氧化锰不断被还原,电池电压逐
渐 降低,最后失效。这种电池放电之后不能充电(内部的氧化还原反应无法逆向进行),属于一次电池。
总反应 Zn + 2MnO + 2NH+ === Zn2+ + 2MnO(OH) + 2NH ↑
2 4 3
负极 Zn﹣2e- === Zn2+
正极 2MnO + 2NH+ + 2e- === 2MnO(OH) + 2NH ↑
2 4 3
二、二次电池
有些电池放电时所进行的氧化还原反应,在充电时可以逆向进行,使电池恢复到放电前的状态,从而实现
放电(化学能转化为电能)与充电(电能转化为化学能)的循环,这种充电电池属于二次电池。
常见的充电电池有铅酸蓄电池、镍氢电池、锂离子电池等,目前汽车上使用的大多是铅酸蓄电池。
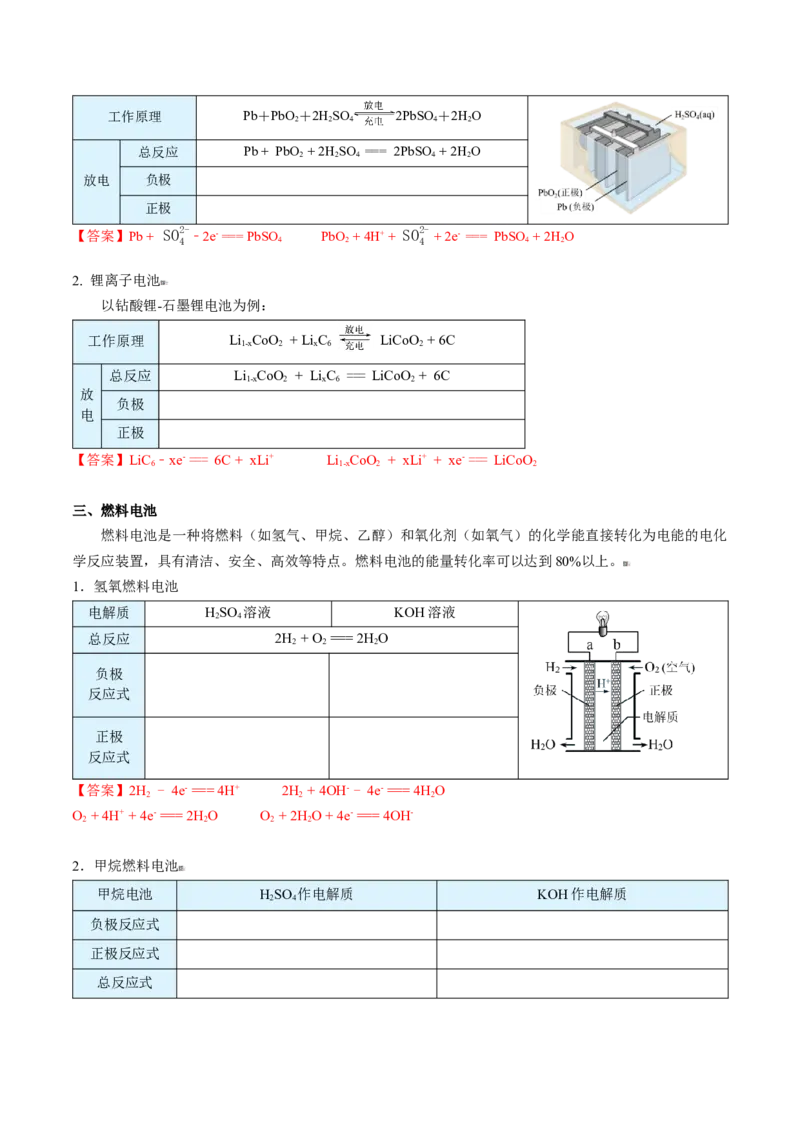
1. 铅酸蓄电池工作原理 Pb+PbO+2HSO 2PbSO+2HO
2 2 4 4 2
总反应 Pb + PbO + 2HSO === 2PbSO + 2HO
2 2 4 4 2
放电 负极
正极
【答案】Pb +
SO2-
﹣2e- === PbSO PbO + 4H+ +
SO2-
+ 2e- === PbSO + 2HO
4 4 2 4 4 2
2. 锂离子电池
以钻酸锂-石墨锂电池为例:
工作原理 Li CoO + Li C LiCoO + 6C
1-x 2 x 6 2
总反应 Li CoO + LiC === LiCoO + 6C
1-x 2 x 6 2
放
负极
电
正极
【答案】LiC ﹣xe- === 6C + xLi+ Li CoO + xLi+ + xe- === LiCoO
6 1-x 2 2
三、燃料电池
燃料电池是一种将燃料(如氢气、甲烷、乙醇)和氧化剂(如氧气)的化学能直接转化为电能的电化
学反应装置,具有清洁、安全、高效等特点。燃料电池的能量转化率可以达到80%以上。
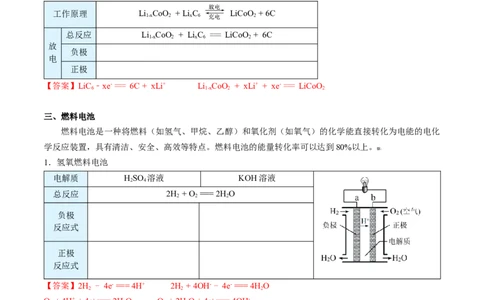
1.氢氧燃料电池
电解质 HSO 溶液 KOH溶液
2 4
总反应 2H +O === 2H O
2 2 2
负极
反应式
正极
反应式
【答案】2H - 4e- === 4H+ 2H +4OH- - 4e- === 4H O
2 2 2
O + 4H+ + 4e- === 2H O O +2HO + 4e- === 4OH-
2 2 2 2
2.甲烷燃料电池
甲烷电池 HSO 作电解质 KOH作电解质
2 4
负极反应式
正极反应式
总反应式【答案】CH + 2H O - 8e- === CO + 8H+ CH + 10OH- - 8e- === + 7H O
4 2 2 4 CO2- 2
3
2O +8H+ + 8e- === 4HO 2O + 8e- + 4HO === 8OH-
2 2 2 2
CH + 2O === CO + 2H O CH + 2O + 2OH- === + 3H O
4 2 2 2 4 2 CO2- 2
3
经典例题
题型一:化学电池的分类及特点
【变1】下列化学电池属于高效、环境友好电池的是
A.镍镉电池 B.锌锰电池
C.铅蓄电池 D.氢氧燃料电池
【答案】D
【详解】
A.镍镉电池中含有镍镉重金属,对环境有污染,故A错误;
B.锌锰电池中含有锌、锰元素,对环境有污染,故B错误;
C.铅蓄电池中含有铅重金属,对环境有污染,故C错误;
D.氢氧燃料电池最终生成水,水对环境无污染,故D正确;
故选:D。
题型二:一次电池
【变2】碱性锌锰电池的总反应为: 。下列关于该电池的说法中
正确的是
A.Zn为负极, 为正极
B.工作时KOH没有发挥作用
C.工作时电子由 经外电路流向Zn
D.Zn发生还原反应, 发生氧化反应
【答案】A
【解析】
【分析】
由电池总反应可知,锌为碱性锌锰电池的负极,碱性条件下锌做负极失去电子发生氧化反应生成氢氧化锌,
电极反应式为Zn—2e—+2OH—=Zn(OH) ,二氧化锰是电池的正极,在水分子作用下,二氧化锰做正极得到
2电子发生还原反应生成碱式氧化锰和氢氧根离子,电极反应式为MnO +e—+H O=MnO(OH)+OH—。
2 2
【详解】
A.由分析可知,锌为碱性锌锰电池的负极,二氧化锰是电池的正极,故A正确;
B.碱性锌锰电池的电解质为氢氧化钾,电池工作时,电离出的离子向两极移动构成闭合回路,同时氢氧
根离子还参与电极反应,故B错误;
C.由分析可知,锌为碱性锌锰电池的负极,二氧化锰是电池的正极,电池工作时,电子由锌经外电路流
向二氧化锰,故C错误;
D.由分析可知,碱性条件下锌做负极失去电子发生氧化反应生成氢氧化锌,在水分子作用下,二氧化锰
做正极得到电子发生还原反应生成碱式氧化锰和氢氧根离子,故D错误;
故选A。
【例4】锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质
LiClO 溶于混合有机溶剂中,Li+ 通过电解质迁移入MnO 晶格中,生成LiMnO 。下列说法错误的是
4 2 2
A.电极a为电池的负极
B.外电路的电流方向是由电极b流向电极a
C.电极b上的反应式为:MnO +e-+Li+=LiMnO
2 2
D.可用水代替电池中的混合有机溶剂
【答案】D
【详解】
A.电池工作时,锂失电子发生氧化反应,电极a为电池的负极,故A正确;
B.a是负极、b是正极,外电路的电流方向是由电极b流向电极a,故B正确;
C.电池工作时,b是正极,Li+通过电解质迁移入MnO 晶格中,电极b上的反应式为:MnO +e-+Li+
2 2
=LiMnO ,故C正确;
2
D.锂能与水反应,所以不能用水代替电池中的混合有机溶剂,故D错误;
选D。
题型三:二次电池
【变5】目前汽车上使用的铅蓄电池如图所示,根据图示回答下列问题:(1)铅蓄电池的负极是___________,铅蓄电池的正极是___________。
(2)铅蓄电池的总反应式为Pb+PbO +2HSO =2PbSO+2HO,则负极发生___________(填“氧化”或“还
2 2 4 4 2
原”)反应,由___________生成___________;正极发生___________(填“氧化”或“还原”)反应,由
___________生成___________。
(3)电解质溶液是HSO ,那么在铅蓄电池中H+向___________(填“正”或“负”)极移动, 向
2 4
___________(填“正”或“负”)极移动。
【答案】 Pb PbO 氧化 Pb PbSO 还原 PbO PbSO
2 4 2 4
正 负
【解析】
【分析】
从铅蓄电池的总反应式Pb+PbO +2HSO =2PbSO+2HO可以看出,Pb失电子,则Pb作负极;PbO 得电
2 2 4 4 2 2
子生成PbSO ,则PbO 作正极。
4 2
【详解】
(1)由总反应式可以看出,铅蓄电池的负极是Pb,铅蓄电池的正极是PbO 。答案为:Pb;PbO ;
2 2
(2)铅蓄电池的总反应式为Pb+PbO +2HSO =2PbSO+2HO,则负极Pb生成PbSO ,失电子发生氧化反
2 2 4 4 2 4
应,由Pb生成PbSO ;正极PbO 生成PbSO ,得电子发生还原反应,由PbO 生成PbSO 。答案为:氧化;
4 2 4 2 4
Pb;PbSO ;还原;PbO ;PbSO ;
4 2 4
(3)铅蓄电池属于原电池,在原电池中,阳离子向正极移动,阴离子向负极移动,电解质溶液是HSO ,那
2 4
么在铅蓄电池中H+向正极移动, 向负极移动。答案为:正;负。
【变6】锂/氟化碳电池稳定性很高。电解质溶液为 的乙二醇二甲醚( )溶液,总
反应为 ,放电产物 沉积在正极,工作原理如图所示:
下列说法正确的是
A.外电路电子由b流向a
B.离子交换膜为阴离子交换膜
C.电解质溶液可用 的乙醇溶液代替D.正极的电极反应式为
【答案】D
【分析】
电解质为LiClO 的乙二醇二甲醚溶液,总反应为xLi+CF═xLiF+C,负极为Li,负极上Li失电子生成
4 x
Li+,正极为CF,正极反应为CF+xe-+xLi+═xLiF+C,据此分析解答。
x x
【详解】
A.由上述分析可知,负极为Li,电子由负极流向正极,即a流向b,故A错误;
B.Li+通过离子交换膜在正极上形成LiF,所以交换膜为阳离子交换膜,故B错误;
C.Li是活泼金属能与乙醇反应,所以不能乙醇溶液代替,故C错误;
D.由分析可知,正极的电极反应为: ,故D正确。
答案选D。
题型四:燃料电池
【变7】燃料电池是一种高效、环境友好的发电装置,某氢氧燃料电池的构造示意图如下,该电池工作时,
下列说法正确的是
A.O 在b电极上发生氧化反应
2
B.电解质溶液中OH-向正极移动
C.该装置实现了电能到化学能的转化
D.氢氧燃料电池是一种具有应用前景的绿色电源
【答案】D
【解析】
【详解】
A.O 在b电极上得到电子发生还原反应,A错误;
2
B.该燃料电池工作时,电解质溶液中OH-向正电荷较多的负极移动,B错误;
C.该装置通过两个电极分别发生氧化反应、还原反应,实现了化学能到电能的转化,C错误;
D.氢氧燃料电池反应产物水不会对环境造成污染,且水又是生产燃料H 的原料,比H 直接燃烧能量利用
2 2
率大大提高,因此是一种具有应用前景的绿色电源,D正确;
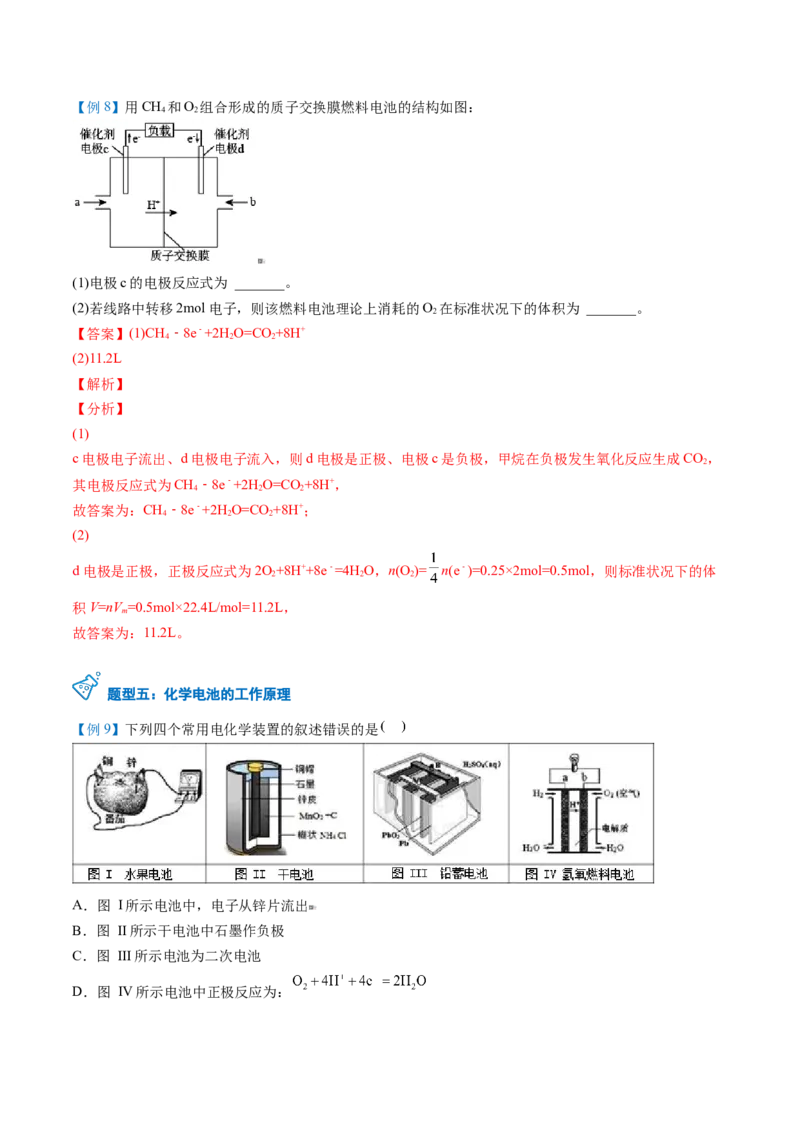
故合理选项是D。【例8】用CH 和O 组合形成的质子交换膜燃料电池的结构如图:
4 2
(1)电极c的电极反应式为 _______。
(2)若线路中转移2mol电子,则该燃料电池理论上消耗的O 在标准状况下的体积为 _______。
2
【答案】(1)CH ﹣8e﹣+2H O=CO+8H+
4 2 2
(2)11.2L
【解析】
【分析】
(1)
c电极电子流出、d电极电子流入,则d电极是正极、电极c是负极,甲烷在负极发生氧化反应生成CO,
2
其电极反应式为CH﹣8e﹣+2H O=CO+8H+,
4 2 2
故答案为:CH﹣8e﹣+2H O=CO+8H+;
4 2 2
(2)
d电极是正极,正极反应式为2O+8H++8e﹣=4H O,n(O )= n(e﹣)=0.25×2mol=0.5mol,则标准状况下的体
2 2 2
积V=nV =0.5mol×22.4L/mol=11.2L,
m
故答案为:11.2L。
题型五:化学电池的工作原理
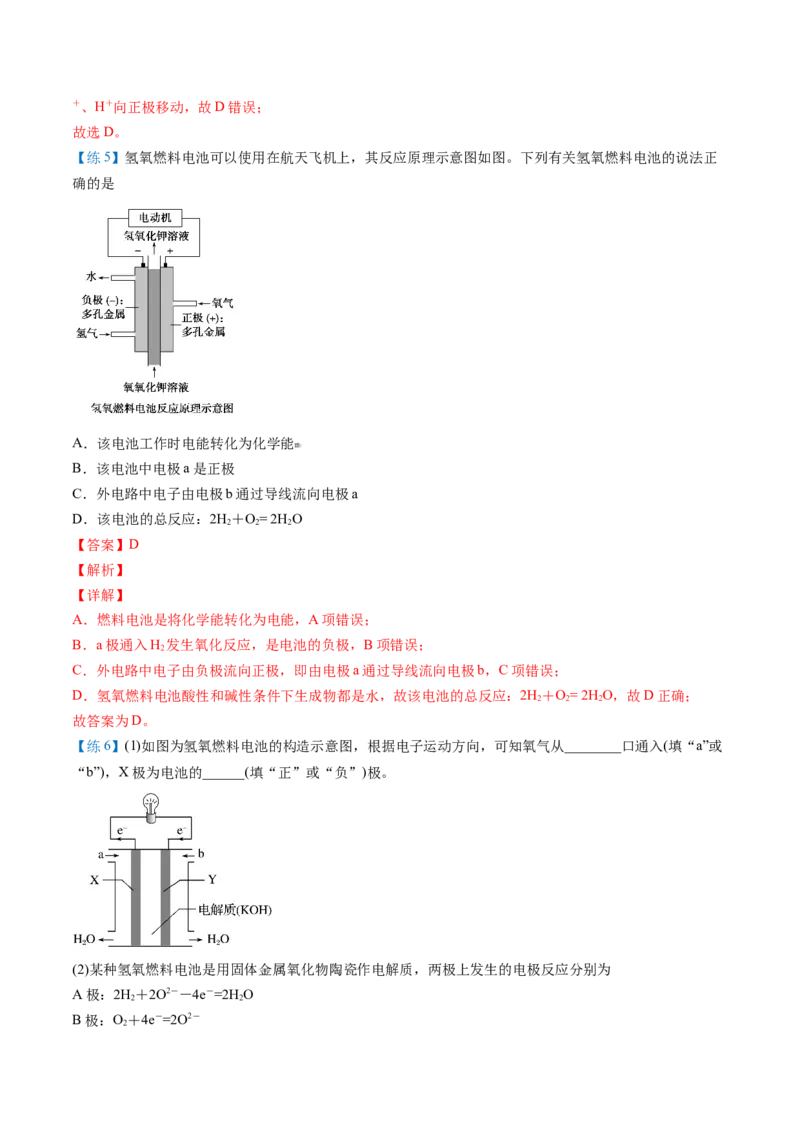
【例9】下列四个常用电化学装置的叙述错误的是
A.图 I所示电池中,电子从锌片流出
B.图 II所示干电池中石墨作负极
C.图 III所示电池为二次电池
D.图 IV所示电池中正极反应为:【答案】B
【详解】
A. 原电池工作时,电子从负极流出,图 I所示电池中,锌为负极,则电子从锌片流出,A正确;
B. 图 II所示干电池中石墨作正极、锌作负极,B错误;
C. 铅蓄电池对外供电时,铅作负极、二氧化铅作正极,当充电时,铅作阴极,二氧化铅作阳极,可反复
使用,故图 III所示电池为二次电池,C正确;
D. 图 IV所示电池为氢氧燃料电池,其中,氧气在正极得到电子发生还原反应,正极反应为:
,D正确;
答案选B。
【变9】下列有关装置的说法正确的是
A.装置I中 为原电池的负极
B.装置IV工作时,电子由锌通过导线流向碳棒
C.装置III可构成原电池
D.装置II为一次电池
【答案】B
【详解】
A.Al能够与NaOH溶液反应,而Mg不能反应,所以装置I中 为原电池的正极,Al为原电池的负极,
A错误;
B.由于电极活动性Zn比C强,所以Zn为负极,碳棒为正极,故装置IV工作时,电子由负极锌通过导线
流向正极碳棒,B正确;
C.装置III中2个电极都是Zn,没有活动性不同的电极,因此不可构成原电池,C错误;
D.装置II可充电,为电解池;也可放电,为原电池,故装置II电池为二次电池,D错误;
故合理选项是B。
【变10】电化学在生产生活中都具有重要的作用和意义。
(1)研究人员最近发明了一种“水”电池,这种电池能利用淡水与海水之间含盐量的差别进行发电,在海水
中电池反应可表示为:5MnO +2Ag+2NaCl=Na MnO +2AgCl
2 2 5 10
①该电池的负极反应式为___________;
②在电池中,Na+不断移动到“水”电池的___________极(填“正”或“负”);
③外电路每通过4 mol电子时,生成NaMnO 的物质的量是___________;
2 5 10(2)中国科学院应用化学研究所在二甲醚(CHOCH )燃料电池技术方面获得新突破。二甲醚燃料电池的工作
3 3
原理如图所示。
①该电池工作时,b口通入的物质为___________;
②该电池负极的电极反应式为___________;
③工作一段时间后,当9.2 g二甲醚完全反应生成CO 时,有___________ 个电子转移。
2
【答案】(1) Ag-e-+Cl-=AgCl 正 2 mol
(2) 二甲醚(CHOCH ) CHOCH -12e-+3H O=2CO+12H+ 2.4N
3 3 3 3 2 2 A
【解析】
(1)
①由总方程式分析可知:Ag在反应中失电子作原电池的负极,电极反应为Ag-e-+Cl-=AgCl;
②在电池中,阳离子向负电荷较多的正极移动,故Na+移向电池的正极;
③根据①可知负极电极反应为Ag-e-+Cl-=AgCl,故反应中转移4 mol电子,消耗4 mol Ag,由总反应方程可
知:每生成1 mol的NaMnO ,反应转移2 mol电子,则现在反应转移4 mol电子,因此生成NaMnO
2 5 10 2 5 10
的物质量为2 mol;
(2)
①在原电池反应中阳离子向负电荷较多的正极移动。根据图示可知H+移向右侧电极,说明右侧电极为正极,
左侧电极为负极。故该电池工作时。b口通入的物质是燃料二甲醚;
②在负极上燃料失去电子发生氧化反应产生CO、H+,故负极的电极反应式为:CHOCH -12e-
2 3 3
+3H O=2CO+12H+;
2 2
③9.2 g二甲醚的物质的量n(二甲醚)= ,根据负极反应式可知:每有1 mol二甲醚发生反应,
转移12 mol电子,则当有9.2 g(即有0.2 mol)二甲醚发生反应时转移电子的物质的量为n(e-)=0.2 mol×12=2.4
mol,则反应过程中转移的电子数目为N(e-)=2.4 mol ×N /mol=2.4N 。
A A
提分特训
【题1】新冠肺炎最明显的症状就是出现发热,体温枪能快速检测人体体温。该体温枪所用的电池为一种
银锌电池(如下图所示),该电池的总反应式为: 。下列关于该电池的说法正确的是
A.Ag O电极作正极,发生氧化反应
2
B.该电池放电时溶液中的K+向Zn电极移动
C.电池工作时,电流从Ag O电极经过隔板流向Zn电极
2
D.该电池的负极反应为:
【答案】D
【详解】
A.根据总反应方程式分析Ag O化合价降低,得到电子,作原电池正极,发生还原反应,故A错误;
2
B.Zn化合价升高,是原电池负极,Ag O化合价降低,得到电子,作原电池正极,根据原电池“同性相
2
吸”,得到该电池放电时溶液中的K+向Ag O电极移动,故B错误;
2
C.电池工作时,电流从Ag O电极经过外电路流向Zn电极,故C错误;
2
D.根据B分析得到Zn为负极,根据总反应式得到该电池的负极反应为: ,故D
正确。
综上所述,答案为D。
【题2】下列图示都是原电池原理在化学电源中的应用。
下列有关说法中正确的是
A.铅蓄电池在放电时,其负极是铅电极
B.氢氧燃料电池中, 所在电极发生的反应为
C.氢氧燃料电池中,通入 的一极为负极
D.铅蓄电池放电后, 极质量减小
【答案】A【详解】
A.铅蓄电池在放电时,铅是负极,由铅变成硫酸铅,A正确;
B.氢氧燃料电池中,电解质溶液为酸性,所以H 所在电极发生的反应为H-2e-=2H+,B错误;
2 2
C.氢氧燃料电池中,通入O 的一极为正极,C错误;
2
D.铅蓄电池放电后,PbO 极变成PbSO ,质量增重,D错误;
2 4
故选A。
【题3】铅酸蓄电池、镍镉碱性电池都是重要的二次电池。已知镍镉碱性电池放电时,正极反应为:
,负极反应为: 。下列有关说法不
正确的是
A.铅酸蓄电池放电时, 在两个电极上生成
B.若用铅酸蓄电池为镍镉碱性电池充电,则 电极与Cd电极相连接且两电极附近的pH值均增大
C.镍镉碱性电池在充电时的反应为
D.放电一段时间后镍镉碱性电池内 变大
【答案】B
【解析】
【详解】
A.铅酸蓄电池负极电极反应为:Pb+SO -2e-=PbSO,正极电极反应为:PbO +4H++SO +2e-
4 2
=PbSO+2H O,由此可知,硫酸铅在两个电极上产生,A正确;
4 2
B.若用铅酸蓄电池为镍镉碱性电池充电,则铅酸蓄电池的 电极为正极,应与镍镉碱性电池的正极相
连,而不是Cd电极,B错误;
C.由题意可知,镍镉碱性电池在放电时的反应为: ,则充
电时的反应为: ,C正确;
D.镍镉碱性电池在放电时的反应为: ,反应过程中消耗水,
使得电解液浓度增大,氢氧根离子浓度变大,D正确;
答案选B。
【题4】某固体酸燃料电池以CaHSO 固体为电解质传递H+,其基本结构见图,下列有关说法错误的是
4A.H+在固体酸膜中由a极流向b极
B.b极上的电极反应式为:O+2H O+4e-=4OH-
2 2
C.电池总反应可表示为:2H+O =2H O
2 2 2
D.电路中每转移1mol电子,b极消耗16gO
2
【答案】D
【解析】
【分析】
根据燃料电池中,通入燃料的一极为负极,故通入氢气的一极为电池的负极,发生氧化反应,反应为H-
2
2e-═2H+,通入氧气的一极为电池的正极,发生还原反应,反应为O+4e-+4H+=2H O;电池工作时,电子通
2 2
过外电路从负极流向正极,即从a极流向b极,电解质溶液中阳离子向正极移动,即H+由a极通过固体酸
电解质传递到b极;每转移0.1mol电子,消耗0.05mol的H,标准状况下的体积为1.12L,据此分析答题。
2
【详解】
A.由分析可知,电解质溶液中阳离子向正极移动,即H+由a极通过固体酸电解质传递到b极,A正确;
B.由分析可知,b极上的电极反应式为:O+2H O+4e-4OH-,B正确;
2 2
C.由分析可知,负极反应式为H-2e-═2H+,正极反应式为:O+2H O+4e-4OH-,故电池总反应可表示为:
2 2 2
2H+O =2H O,C正确;
2 2 2
D.根据电子守恒可知,电路中每转移1mol电子,b极消耗O 为 =8g,D错误;
2
故答案为:D。
【题5】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。
高铁电池的总反应为3Zn+2K FeO+8H O 3Zn(OH) +2Fe(OH) +4KOH,下列叙述正确的是
2 4 2 2 3
A.放电时正极附近溶液的pH减小
B.充电时阳极反应为:Fe(OH) -3e-+ 5 OH- = + 4H O
3 2
C.放电时每转移3 mol电子,正极有1mol KFeO 被氧化
2 4
D.放电时负极反应为:Zn-2e- +2OH-= Zn(OH)
2
【答案】BD
【解析】
【分析】根据电池的总反应可知,高铁电池放电时必定是锌在负极失去电子,电极反应式为Zn-2e-+2OH-
=Zn(OH) ,高铁酸钠在正极得到电子,电极反应式为FeO2+4H O+3e-=Fe(OH) +5OH-,根据电极反应式可
2 4 2 3
判断电子转移的物质的量与反应物之间的关系,负极上消耗OH-离子,碱性要减弱,以此解答该题。
【详解】
A.放电时正极附近发生得电子的还原反应,FeO2+4H O+3e-=Fe(OH) +5OH-,生成氢氧根离子,所以碱性
4 2 3
增强,故A错误;
B.充电时,铁离子失去电子,发生Fe(OH) 转化为FeO2-的反应,电极反应为Fe(OH) -3e-+ 5 OH- =
3 4 3
+ 4H O,故B正确;
2
C.放电时Zn元素失去电子,正极Fe元素得到电子,转移电子数为1mol×(6-3)=3mol,放电时每转移3
mol电子,正极有1 mol KFeO 被还原,故C错误;
2 4
D.根据电池的总反应可知,高铁电池放电时必定是锌在负极失去电子,电极反应式为Zn-2e-+2OH-
=Zn(OH) ,故D正确。
2
答案选BD。
【题6】磷酸铁锂电池是以磷酸铁锂为正极材料的一种锂离子二次电池,电池总反应为M Fe PO +LiC
1-x x 4 6
LiM Fe PO +6C,其原理如图所示,下列说法正确的是
1-x x 4
A.放电时,石墨电极的电势更高
B.充电时,Li+移向磷酸铁锂电极
C.充电时,磷酸铁锂电极应与电源正极相连
D.放电时,正极反应式为M Fe PO +e-+Li+=LiFe PO +(1-x)M
1-x x 4 x 4
【答案】C
【分析】
从电池总反应式可以分析出,放电时LiC 变为Li+和6C,Li元素化合价升高被氧化,所以石墨电极是负极,
6
另一侧磷酸铁锂电极为正极,放电过程电解质中Li+向磷酸铁锂电极方向移动;
【详解】
A.根据分析,石墨电极为负极,故电势更低,描述错误,不符题意;
B.根据分析,放电时Li+移向磷酸铁锂电极,而充电时离子移动方向相反,向石墨电极移动,描述错误,
不符题意;
C.放电时,磷酸铁锂电极是正极,电子流入,充电时,该极需输出电子,故要和电源正极相连,描述正
确,符合题意;
D.根据电池模型,可以看到,放电时正极电极反应式应是M Fe PO +e-+Li+=LiM Fe PO ,描述错误,不
1-x x 4 1-x x 4符题意;
综上,本题选C。
【题7】酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是碳粉、MnO 、ZnCl 和
2 2
NH Cl等组成的糊状填充物,该电池在放电过程产生MnOOH,回收处理该废电池可得到多种化工原料,
4
有关数据表所示:
溶解度/(g/100g水)
温度/℃
0 20 40 60 80 100
化合物
NH Cl 29.3 37.2 45.8 55.3 65.6 77.3
4
ZnCl 343 395 452 488 541 614
2
回答下列问题:
(1)该电池的正极反应式为 ___________。
(2)维持电流强度为0.5A,电池工作五分钟,理论上消耗Zn___________g.(已知Q=It,F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl 和NH Cl,二者可通过___________分离回收。
2 4
(4)滤渣的主要成分是MnO 、___________和___________,欲从中得到较纯的MnO ,最简便的方法是
2 2
___________,其原理是___________。
【答案】 MnO +e-+H+=MnOOH 0.05g 加热浓缩、冷却结晶 碳粉
2
MnOOH 在空气中加热 碳粉转变为CO,MnOOH氧化为MnO
2 2
【解析】
【分析】
【详解】
(1)该电池的正极发生还原反应,MnO 被还原生成MnOOH,电极方程式为MnO +H++e-=MnOOH,负极锌
2 2
被氧化生成Zn2+,电池总反应式为2MnO +Zn+2H+=2MnOOH+Zn2+,故答案为MnO +H++e-=MnOOH;
2 2
(2)电池工作5分钟,通过的电量Q=0.5A×5min×60s/min=150C,因此通过电子的物质的量n(e-)=Q/F=
150C/96500C/mol=1.554×10-3mol,则理论消耗Zn的质量是m(Zn)=1.554×10-3mol/2×65g/mol=0.05g,故
答案为0.05。
(3)由于ZnCl 的溶解度受温度影响较大,而NH Cl的溶解度受温度影响较小,所以可采用加热浓缩、冷却
2 4
结晶的方法分离氯化锌和氯化铵混合物;故答案为:加热浓缩、冷却结晶;
(4)根据废电池糊状填充物中碳粉和MnO 及正极放电产生的MnOOH都不溶于水,可确定滤渣的主要成分;
2
碳粉在足量氧气中燃烧转变为CO,MnOOH在足量氧气中燃烧转变为MnO ,因此得到较纯的二氧化锰最
2 2
简便的方法是在足量空气或氧气中燃烧滤渣,故答案为:碳粉;MnOOH;在空气中加热;碳粉转变为
CO,MnOOH氧化为MnO 。
2 2提分作业
【练1】下列电池工作时能量转化形式与其它三个不同的是
A.锌锰碱性电池 B.硅太阳能电池
C.铅蓄电池 D.银锌纽扣电池
【答案】B
【详解】
A.锌锰碱性电池是将化学能转化为电能的装置;
B.硅太阳能电池是将太阳能转化为电能的装置;
C.铅蓄电池是将化学能转化为电能的装置;
D.银锌纽扣电池是将化学能转化为电能的装置;
可见只有选项B中硅太阳能电池能量转化形式与其它选项不同,故合理选项是B。
【练2】碱性锌锰干电池的总反应为: 。下列关于该电池的说法
中正确的是
A.Zn为负极, 为正极 B.工作时电子由 经由外电路流向Zn
C.工作时OH-移向正极 D.电池放电过程中,溶液的酸碱性一定不变
【答案】A
【详解】
A.由碱性锌锰电池的总反应 可知,正极MnO 得电子被还原,
2
负极是金属锌失电子被氧化,故A正确;
B.工作时外电路电子由负极流向正极,即电子由Zn经由外电路流向MnO ,故B错误;
2
C.电池工作时阴离子OH-向负极锌电极移动,故C错误;
D.碱性锌锰电池中的电解质为KOH,由碱性锌锰电池的总反应
可知,电池放电过程中,KOH物质的量不变,但反应消耗水,溶液OH-浓度增大,则碱性增强,故D错误;
答案为A。
【练3】下列有关化学电池装置的叙述中,不正确的是图Ⅰ碱性锌锰电池 图Ⅱ铅-硫酸蓄电池 图Ⅲ原电池 图Ⅳ银锌纽扣电池
A.图Ⅰ所示电池工作时,锌粉失电子
B.图Ⅱ所示电池放电过程中,电解质溶液中的 移向 极
C.图Ⅱ所示装置工作过程中,电解质溶液的质量增大
D.图Ⅳ所示电池中, 是氧化剂,电池工作过程中被还原为
【答案】C
【详解】
A.碱性锌锰电池中,锌作负极,失电子,发生氧化反应,故A正确;
B.原电池中,阳离子向正极移动,铅-硫酸蓄电池中PbO 极为正极,电解质溶液中的H+移向PbO 极,故
2 2
B正确;
C.铜-铁-硫酸铜原电池中铁为负极,溶解,铜为正极,析出铜,电池反应为Fe+ Cu2+ =Fe2+ + Cu,工作过
程中,电解质溶液的质量减小,故C错误;
D.银锌纽扣电池中Ag O为正极,得电子,作氧化剂,电池工作过程中被还原为Ag,故D正确;
2
故选C。
【练4】银锌电池广泛用作各种电子仪器的电源,其电极分别为Ag O和Zn,电解质溶液为KOH溶液,总
2
反应式为Ag O+Zn+H O=2Ag+Zn(OH) ,下列说法中不正确的是
2 2 2
A.工作时,正极上发生反应的物质是Ag O
2
B.负极发生的反应是Zn+2OH--2e-=Zn(OH)
2
C.工作时,负极区溶液c(OH-)减小
D.溶液中OH-向正极移动,K+、H+向负极移动
【答案】D
【解析】
【分析】
【详解】
A.Ag O中Ag化合价降低,发生还原反应,在正极反应,故A正确;
2
B.Zn在负极上失电子,电解质溶液为KOH溶液,所以负极反应为Zn+2OH−−2e−=Zn(OH) ,故B正确;
2
C.负极发生反应Zn+2OH--2e-=Zn(OH) ,消耗氢氧根离子,因此负极c(OH-)减小,故C正确;
2
D.原电池原理中,阳离子移向正极,阴离子移向负极,因此放电时,电解质溶液中OH-向负极移动,K+、H+向正极移动,故D错误;
故选D。
【练5】氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图。下列有关氢氧燃料电池的说法正
确的是
A.该电池工作时电能转化为化学能
B.该电池中电极a是正极
C.外电路中电子由电极b通过导线流向电极a
D.该电池的总反应:2H+O= 2H O
2 2 2
【答案】D
【解析】
【详解】
A.燃料电池是将化学能转化为电能,A项错误;
B.a极通入H 发生氧化反应,是电池的负极,B项错误;
2
C.外电路中电子由负极流向正极,即由电极a通过导线流向电极b,C项错误;
D.氢氧燃料电池酸性和碱性条件下生成物都是水,故该电池的总反应:2H+O= 2H O,故D正确;
2 2 2
故答案为D。
【练6】(1)如图为氢氧燃料电池的构造示意图,根据电子运动方向,可知氧气从________口通入(填“a”或
“b”),X极为电池的______(填“正”或“负”)极。
(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为
A极:2H+2O2--4e-=2H O
2 2
B极:O+4e-=2O2-
2则A极是电池的______极;电子从该极________(填“流入”或“流出”)。
(3)微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag O和Zn,电解质溶液为
2
KOH溶液,电极反应为:
Zn+2OH--2e-=ZnO+HO
2
Ag O+HO+2e-=2Ag+2OH-
2 2
总反应为Ag O+Zn=ZnO+2Ag
2
①Zn是_______极,Ag O发生________反应。
2
②电子由_____极流向_____极(填“Zn”或“Ag O”),当电路通过1 mol电子时,负极消耗物质的质量是
2
________g。
③在使用过程中,电解质溶液中KOH的物质的量_____(填“增大”“减小”或“不变”)。
【答案】 b 负 负 流出 负 还原 Zn Ag O
2
32.5 不变
【解析】
【详解】
(1)氢氧燃料电池中,电子从负极向正极移动, X是负极;Y是正极,氧气得电子,氧气应通入正极。
(2)根据电极反应可知,A极发生氧化反应,应该是电池的负极,电子从该极流出。
(3)①根据电极反应可知Zn失电子被氧化而溶解,Ag O得电子被还原发生还原反应。
2
②发生原电池反应时,电子由负极经外电路到正极,即电子从Zn极经外电路到Ag O极,当通过电路1
2
mol时,负极消耗Zn的质量是32.5 g。
③根据电极反应式,电池中KOH只起到增强导电的作用,不参与反应,故电池使用过程中KOH的量不变。倒卖拉黑不更新,淘宝唯一免费更新店铺: 知二教育