文档内容
《化学反应速率与化学平衡》单元测试(基础巩固)
学校:___________姓名:___________班级:___________考号:___________
一、单选题(共45分)
1.(本题3分) 下列说法正确的是
A.活化分子的每一次碰撞都能够发生化学反应
B.能够发生有效碰撞的分子叫做活化分子
C.反应物用量增加后,有效碰撞次数增多,反应速率增大
D.催化剂能提高活化分子的活化能,从而加快反应速率
2.(本题3分) 对于 反应,反应速率最快的是
A. B.
C. D.
3.(本题3分) 一定温度下,向2L恒容密闭容器中充入0.4molNH 和0.5molO 发生反应4NH (g)+5O(g)
3 2 3 2
4NO(g)+6H O(g)。4min后,NO的浓度为0.06mol·L-1。下列有关说法错误的是( ) ⇌
2
A.4min末,用NO表示的反应速率为0.03mol·L-1·min-1
B.4min末,NH 的浓度为0.14mol·L-1
3
C.0~4min内,生成的水的质量为3.24g
D.0~4min内,O 的物质的量减少了0.15mol
2
4.(本题3分) O 在水中易分解,一定条件下,O 的浓度减少一半所需的时间(t)如表所示。
3 3
pH
t/min 3.0 4.0 5.0 6.0
T/℃
20 301 231 169 58
30 158 108 48 15
50 31 26 15 7
据表中的递变规律,推测O 分别在条件①40℃、pH=3.0,②10℃、pH=4.0,③30℃、pH=7.0下,分解速
3
率依次增大的顺序为A.①②③ B.③②① C.②①③ D.③①②
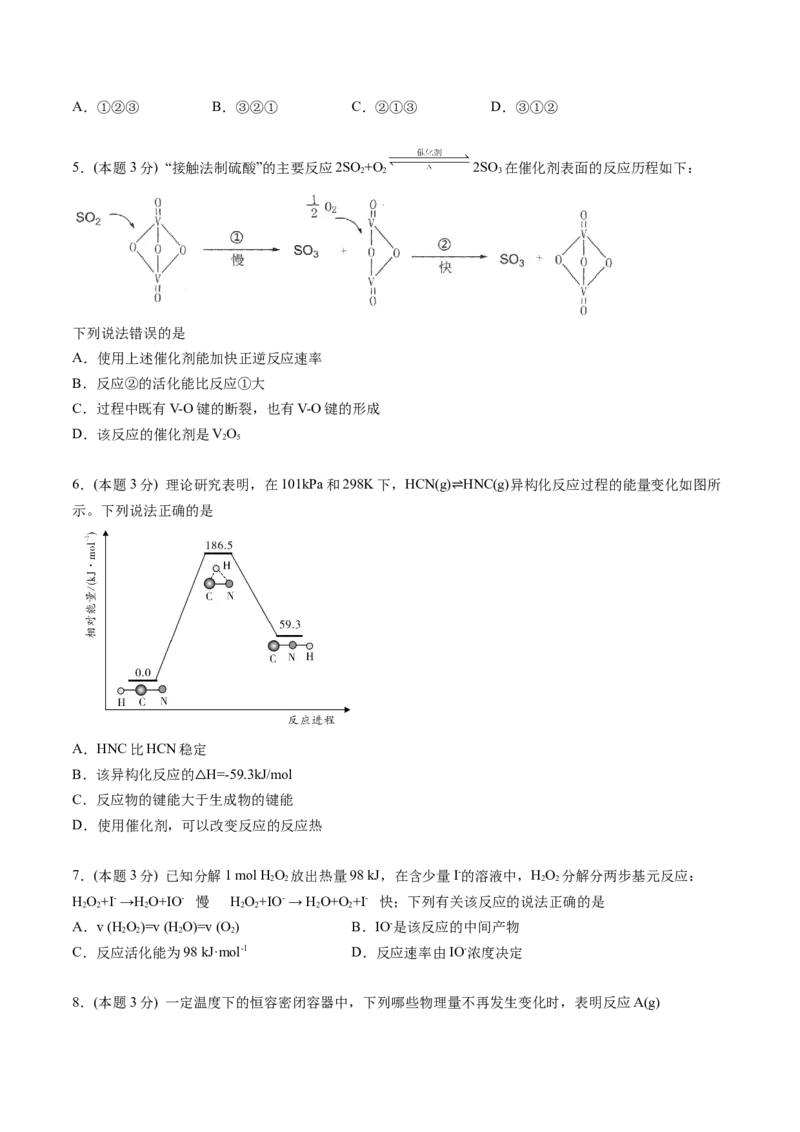
5.(本题3分) “接触法制硫酸”的主要反应2SO +O 2SO 在催化剂表面的反应历程如下:
2 2 3
下列说法错误的是
A.使用上述催化剂能加快正逆反应速率
B.反应②的活化能比反应①大
C.过程中既有V-O键的断裂,也有V-O键的形成
D.该反应的催化剂是VO
2 5
6.(本题3分) 理论研究表明,在101kPa和298K下,HCN(g) HNC(g)异构化反应过程的能量变化如图所
示。下列说法正确的是
⇌
A.HNC比HCN稳定
B.该异构化反应的 H=-59.3kJ/mol
C.反应物的键能大于生成物的键能
△
D.使用催化剂,可以改变反应的反应热
7.(本题3分) 已知分解1 mol H O 放出热量98 kJ,在含少量I-的溶液中,HO 分解分两步基元反应:
2 2 2 2
HO+I- →HO+IO- 慢 HO+IO- → H O+O+I- 快;下列有关该反应的说法正确的是
2 2 2 2 2 2 2
A.v (H O)=v (H O)=v (O ) B.IO-是该反应的中间产物
2 2 2 2
C.反应活化能为98 kJ·mol-1 D.反应速率由IO-浓度决定
8.(本题3分) 一定温度下的恒容密闭容器中,下列哪些物理量不再发生变化时,表明反应A(g)+2B(g) C(g)+D(g)已达到化学平衡状态
①混合气体的压强②混合气体的密度③B的物质的量浓度④混合气体的总物质的量⑤混合气体的平均相对
⇌
分子质量⑥混合气体的总质量
A.①②③④⑤⑥ B.①③④⑤ C.①②③④⑤ D.②⑥
9.(本题3分) 在密闭容器中,给一氧化碳和水蒸气的气体混合物加热,在催化剂存在下发生反应:CO(g)
+H O(g) H(g)+CO (g)。在500℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.2
2 2 2
mol/L,则在此条件下CO的转化率为
⇌
A.25% B.50% C.75% D.80%
10.(本题3分) 已知反应 2NH N+3H ,在某温度下的平衡常数为0.25,在此条件下,氨的合成反应
3 2 2
N + 3H 2NH 的平衡常数为
2 2 3
A.4 B.2 C.1 D.0.5
11.(本题3分) 下列关于化学平衡常数的说法中错误的是
A.某特定反应的平衡常数只与温度有关
B.催化剂不能改变平衡常数的大小
C.平衡常数发生改变,化学平衡必发生改变
D.化学平衡移动时,平衡常数必改变
12.(本题3分) T℃时,气体物质A、B、C发生反应。反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保
持其他条件不变,温度分别为T 和T 时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是
1 2
A.反应方程式为:2A+B 3C
B.T>T,正反应为吸热反应
1 2
C.T<T,正反应为放热反应
1 2
D.保持容器总压强不变,通入稀有气体,平衡向逆反应方向移动
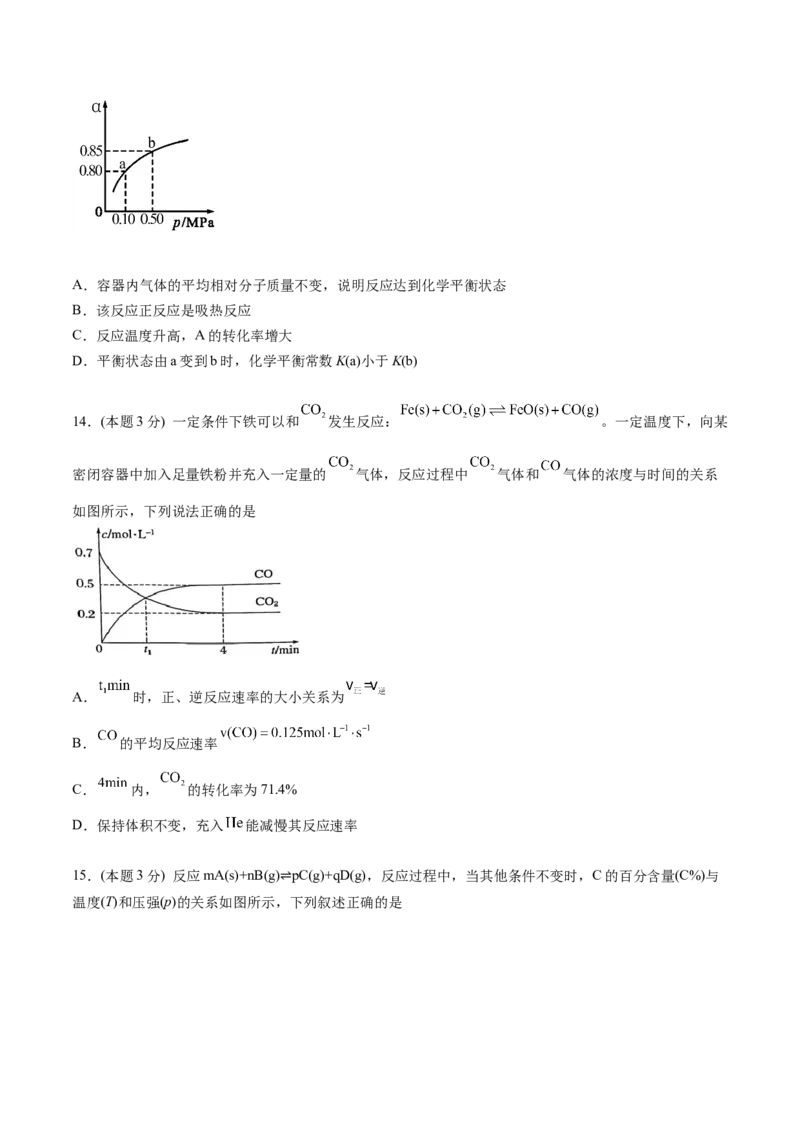
13.(本题3分) 已知 ,在密闭容器中进行,K(300℃)>K(350℃),某温度下,A的平衡
转化率(a)与体系总压强(P)的关系如图所示。下列说法正确的是A.容器内气体的平均相对分子质量不变,说明反应达到化学平衡状态
B.该反应正反应是吸热反应
C.反应温度升高,A的转化率增大
D.平衡状态由a变到b时,化学平衡常数K(a)小于K(b)
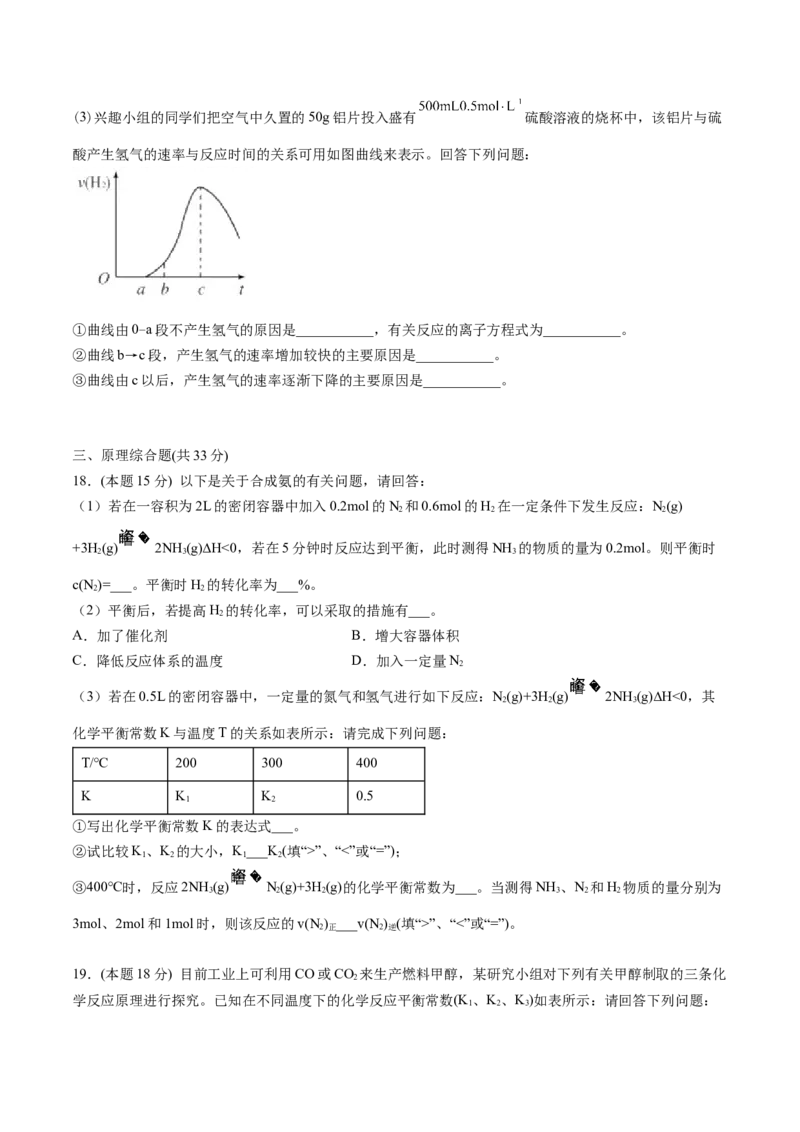
14.(本题3分) 一定条件下铁可以和 发生反应: 。一定温度下,向某
密闭容器中加入足量铁粉并充入一定量的 气体,反应过程中 气体和 气体的浓度与时间的关系
如图所示,下列说法正确的是
A. 时,正、逆反应速率的大小关系为
B. 的平均反应速率
C. 内, 的转化率为71.4%
D.保持体积不变,充入 能减慢其反应速率
15.(本题3分) 反应mA(s)+nB(g) pC(g)+qD(g),反应过程中,当其他条件不变时,C的百分含量(C%)与
温度(T)和压强(p)的关系如图所示,下列叙述正确的是
⇌A.达到平衡后,加入催化剂,C%增大
B.达到平衡后,若升温,平衡向左移动
C.化学方程式中n<p+q
D.达到平衡后,增加A的量有利于平衡向右移动
二、填空题(共22分)
16.(本题8分) (1)在下列事实中,什么因素影响了化学反应的速率?
①石灰石煅烧时要粉碎成细小的矿粒_______;
②熔化的KClO 放出气泡很慢,撒入少量MnO ,则很快产生气体_______;
3 2
③同样大小的石灰石分别在0.1mol·L-1的盐酸和1mol·L-1的盐酸中反应速率不同_______;
④夏天的食品易霉变,冬天就不易发生该现象_______;
(2)依据实验数据,写出下列反应的热化学方程式。
①1molC H(g)与适量O(g)反应,生成CO(g)和HO(1),放出1411kJ热量_______。
2 4 2 2 2
②2molAl(s)与适量O(g)发生反应,生成Al O(s),放出1669.8kJ热量_______。
2 2 3
③若适量的N 和O 完全反应,每生成23gNO 需要吸收16.95kJ热量,则表示该反应的热化学方程式为
2 2 2
_______。
④在25℃、101kPa时,4gH 在足量O 中完全燃烧生成HO(1)放出571.6kJ的热量,则表示H 燃烧热的热
2 2 2 2
化学方程式为_______。
17.(本题14分) 研究化学反应的能量变化和速率变化是研究化学反应的重要角度。
(1)化学反应中能量变化的主要原因是旧的化学键断裂会___________(填“放出”或“吸收”)能量;新的
化学键形成会___________(填“放出”或“吸收”)能量。
(2)工业上高炉炼铁,其反应为: ,属于放热反应,反应物的总能量
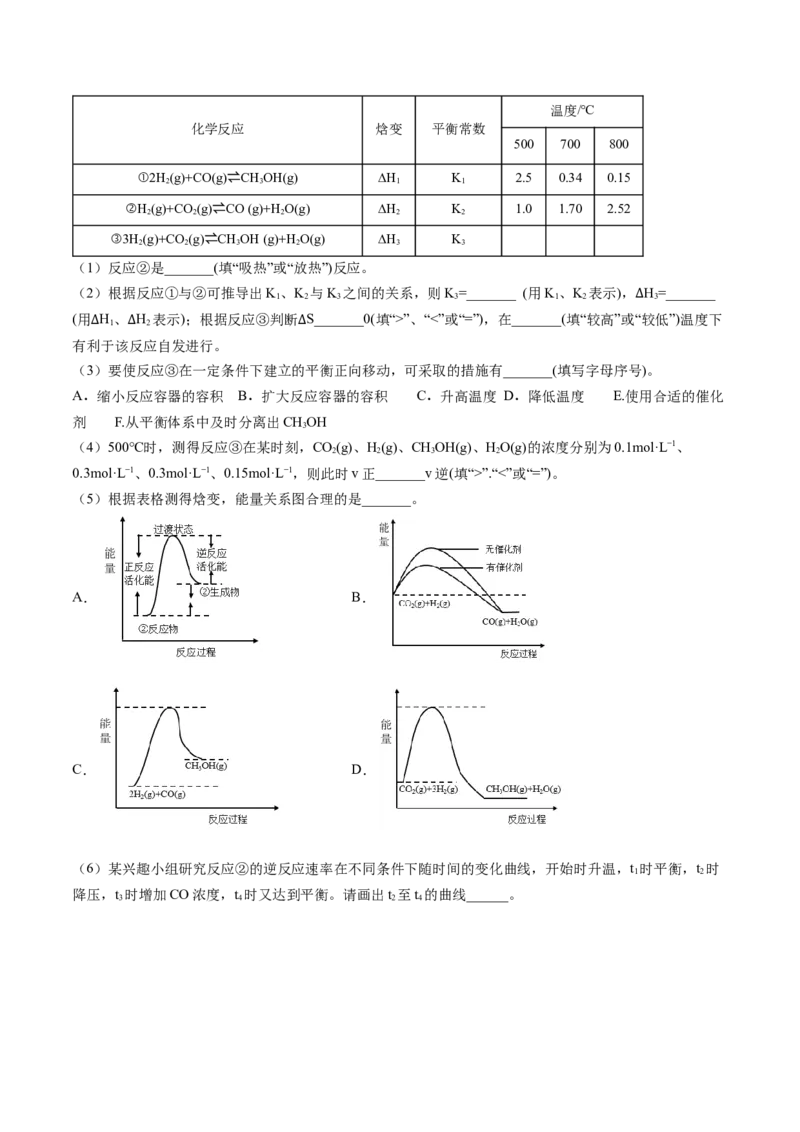
___________(填“>”、“=”或“<”)生成物的总能量。(3)兴趣小组的同学们把空气中久置的50g铝片投入盛有 硫酸溶液的烧杯中,该铝片与硫
酸产生氢气的速率与反应时间的关系可用如图曲线来表示。回答下列问题:
①曲线由0-a段不产生氢气的原因是___________,有关反应的离子方程式为___________。
②曲线b→c段,产生氢气的速率增加较快的主要原因是___________。
③曲线由c以后,产生氢气的速率逐渐下降的主要原因是___________。
三、原理综合题(共33分)
18.(本题15分) 以下是关于合成氨的有关问题,请回答:
(1)若在一容积为2L的密闭容器中加入0.2mol的N 和0.6mol的H 在一定条件下发生反应:N(g)
2 2 2
+3H (g) 2NH (g)∆H<0,若在5分钟时反应达到平衡,此时测得NH 的物质的量为0.2mol。则平衡时
2 3 3
c(N)=___。平衡时H 的转化率为___%。
2 2
(2)平衡后,若提高H 的转化率,可以采取的措施有___。
2
A.加了催化剂 B.增大容器体积
C.降低反应体系的温度 D.加入一定量N
2
(3)若在0.5L的密闭容器中,一定量的氮气和氢气进行如下反应:N(g)+3H(g) 2NH (g)∆H<0,其
2 2 3
化学平衡常数K与温度T的关系如表所示:请完成下列问题:
T/℃ 200 300 400
K K K 0.5
1 2
①写出化学平衡常数K的表达式___。
②试比较K、K 的大小,K___K(填“>”、“<”或“=”);
1 2 1 2
③400℃时,反应2NH (g) N(g)+3H(g)的化学平衡常数为___。当测得NH 、N 和H 物质的量分别为
3 2 2 3 2 2
3mol、2mol和1mol时,则该反应的v(N ) ___v(N ) (填“>”、“<”或“=”)。
2 正 2 逆
19.(本题18分) 目前工业上可利用CO或CO 来生产燃料甲醇,某研究小组对下列有关甲醇制取的三条化
2
学反应原理进行探究。已知在不同温度下的化学反应平衡常数(K 、K、K)如表所示:请回答下列问题:
1 2 3温度/℃
化学反应 焓变 平衡常数
500 700 800
①2H(g)+CO(g)⇌CHOH(g) ∆H K 2.5 0.34 0.15
2 3 1 1
②H(g)+CO(g)⇌CO (g)+HO(g) ∆H K 1.0 1.70 2.52
2 2 2 2 2
③3H(g)+CO(g)⇌CHOH (g)+HO(g) ∆H K
2 2 3 2 3 3
(1)反应②是_______(填“吸热”或“放热”)反应。
(2)根据反应①与②可推导出K、K 与K 之间的关系,则K=_______ (用K、K 表示), H=_______
1 2 3 3 1 2 3
(用 H、 H 表示);根据反应③判断 S_______0(填“>”、“<”或“=”),在_______(填“较高”或“较低”)温度下
1 2 ∆
有利于该反应自发进行。
∆ ∆ ∆
(3)要使反应③在一定条件下建立的平衡正向移动,可采取的措施有_______(填写字母序号)。
A.缩小反应容器的容积 B.扩大反应容器的容积 C.升高温度 D.降低温度 E.使用合适的催化
剂 F.从平衡体系中及时分离出CHOH
3
(4)500℃时,测得反应③在某时刻,CO(g)、H(g)、CHOH(g)、HO(g)的浓度分别为0.1mol·L−1、
2 2 3 2
0.3mol·L−1、0.3mol·L−1、0.15mol·L−1,则此时v正_______v逆(填“>”.“<”或“=”)。
(5)根据表格测得焓变,能量关系图合理的是_______。
A. B.
C. D.
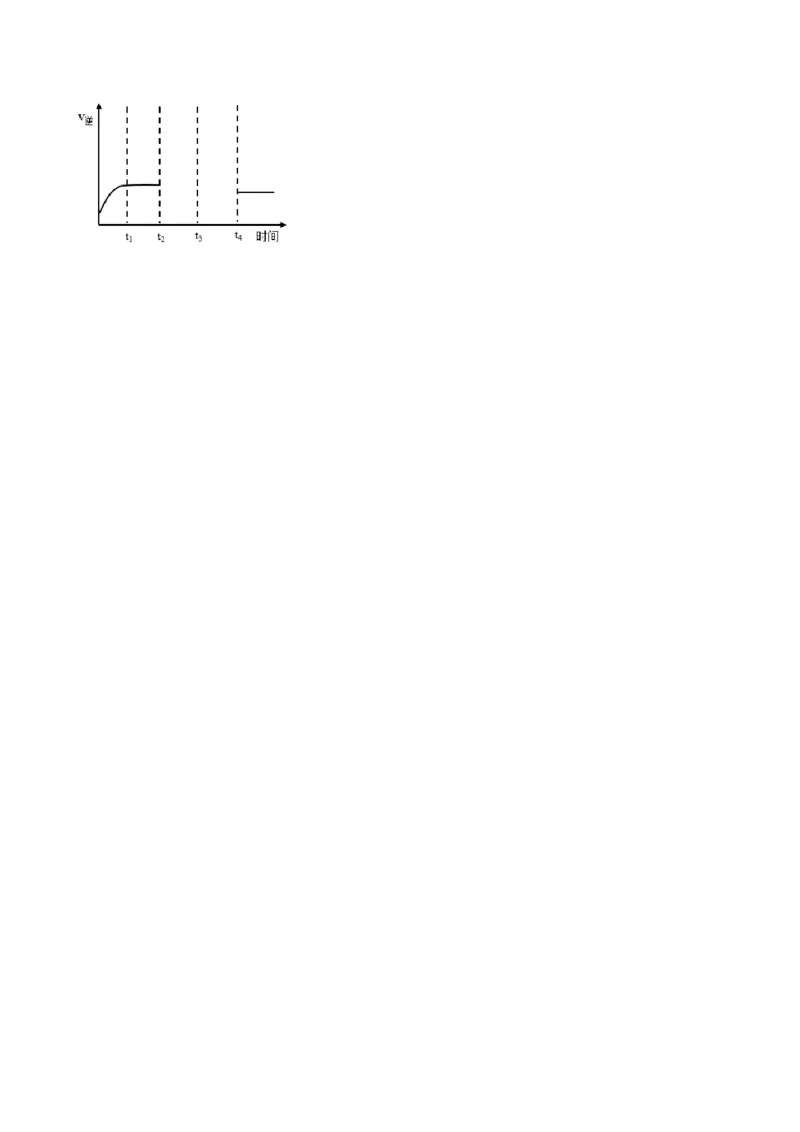
(6)某兴趣小组研究反应②的逆反应速率在不同条件下随时间的变化曲线,开始时升温,t 时平衡,t 时
1 2
降压,t 时增加CO浓度,t 时又达到平衡。请画出t 至t 的曲线______。
3 4 2 4倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育