文档内容
zxxk.com
化学用语—提高篇课后练习
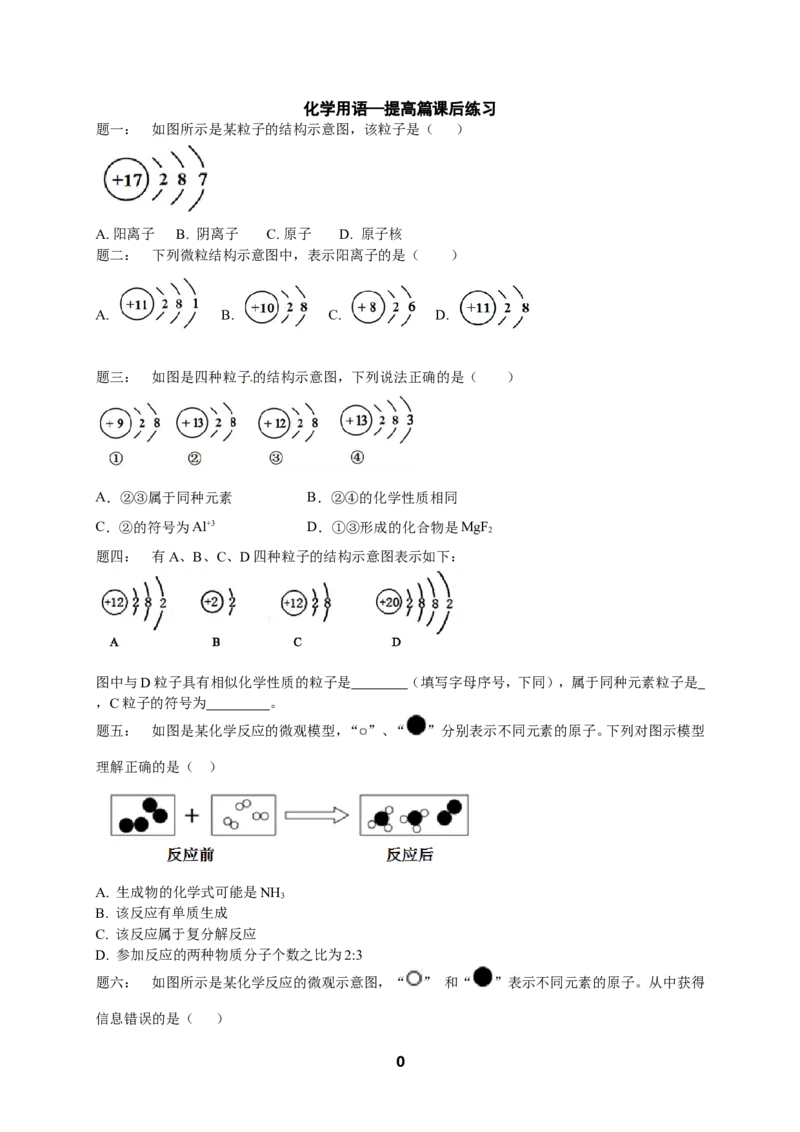
题一: 如图所示是某粒子的结构示意图,该粒子是( )
A. 阳离子 B. 阴离子 C. 原子 D. 原子核
题二: 下列微粒结构示意图中,表示阳离子的是( )
A. B. C. D.
题三: 如图是四种粒子的结构示意图,下列说法正确的是( )
A.②③属于同种元素 B.②④的化学性质相同
C.②的符号为Al+3 D.①③形成的化合物是MgF
2
题四: 有A、B、C、D四种粒子的结构示意图表示如下:
图中与D粒子具有相似化学性质的粒子是 (填写字母序号,下同),属于同种元素粒子是
,C粒子的符号为 。
题五: 如图是某化学反应的微观模型,“ ”、“ ”分别表示不同元素的原子。下列对图示模型
理解正确的是( )
A. 生成物的化学式可能是NH
3
B. 该反应有单质生成
C. 该反应属于复分解反应
D. 参加反应的两种物质分子个数之比为2:3
题六: 如图所示是某化学反应的微观示意图,“ ” 和“ ”表示不同元素的原子。从中获得
信息错误的是( )
0zxxk.com
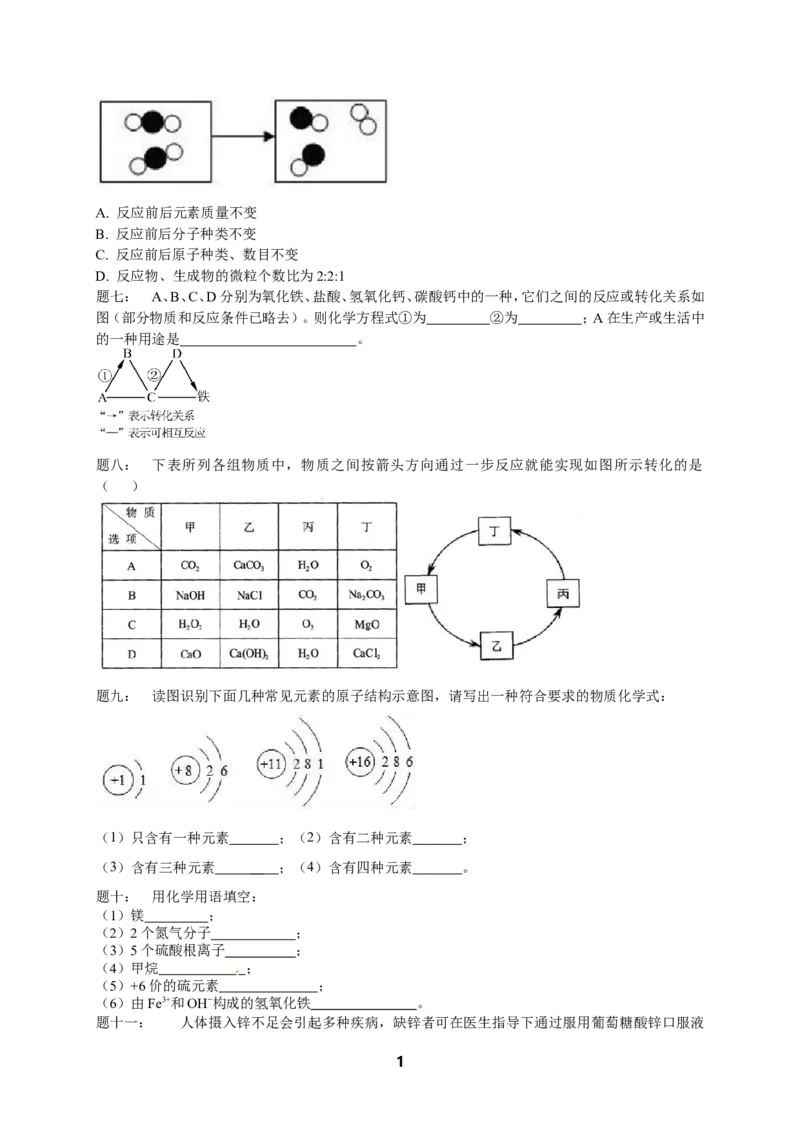
A. 反应前后元素质量不变
B. 反应前后分子种类不变
C. 反应前后原子种类、数目不变
D. 反应物、生成物的微粒个数比为2:2:1
题七: A、B、C、D分别为氧化铁、盐酸、氢氧化钙、碳酸钙中的一种,它们之间的反应或转化关系如
图(部分物质和反应条件已略去)。则化学方程式①为 ②为 ;A在生产或生活中
的一种用途是 。
题八: 下表所列各组物质中,物质之间按箭头方向通过一步反应就能实现如图所示转化的是
( )
题九: 读图识别下面几种常见元素的原子结构示意图,请写出一种符合要求的物质化学式:
(1)只含有一种元素 ;(2)含有二种元素 ;
(3)含有三种元素 _ _ ;(4)含有四种元素 。
题十: 用化学用语填空:
(1)镁 ;
(2)2个氮气分子 ;
(3)5个硫酸根离子 ;
(4)甲烷 ;
(5)+6价的硫元素 ;
(6)由Fe3+和OH构成的氢氧化铁 。
题十一: 人体摄入锌不足会引起多种疾病,缺锌者可在医生指导下通过服用葡萄糖酸锌口服液
1zxxk.com
来补锌。已知葡萄糖酸锌的化学式为C H O Zn。填空:
12 22 14
(1)葡萄糖酸锌中属于微量元素的是 ;
(2)葡萄糖酸锌的相对分子质量为 ;
(3)葡萄糖酸锌中锌元素的质量分数为 (计算结果精确到0.1%)。
题十二: 下图是某种氮肥包装标签上的部分文字:
请回答下列问题:
(1)该肥料由________________种元素组成,原子个数比为________________。
(2)硝酸铵中氮元素的质量分数应为________________(精确到小数点后一位),则该肥料的实际纯
度是________________。
题十三: 化学就在我们身边。
(1)土豆是我们喜爱的一种食品,如图所示是“家乡味土豆片”的主要营养成分。它能为人体提供的
营养素是 。多食用土豆和牛奶有利于身体健康,理由是 。
(2)土豆等农作物的生长需要化肥。下列化肥中属于氮肥的是 。
A. NH Cl B. KCO C. CO(NH) D. Ca (PO )
4 2 3 2 2 3 4 2
(3)贵阳市家用燃料的下列变迁,让我们认识了化学的重要价值。
充分燃烧1kg天然气和煤所产生的CO 和SO 的质量如下图所示。为此,改用天然气作燃料的优点是
2 2
。天然气(主要成分CH)燃烧的化学方程式为 。
4
(4)固体氢化镁(化学式为MgH )可作为氢动力汽车的能源提供剂。提供能源时氢化镁与水反应生成
2
一种碱和氢气,反应的化学方程式为 。
题十四: 汽车是现代生活中不可缺少的代步工具。请回答下列问题:
(1)汽车制造需要大量的钢铁。工业上用一氧化碳和赤铁矿(主要成分是Fe O)炼铁,发生反应的化
2 3
学方程式为 。
2zxxk.com
(2)下列汽车配件及用品中,属于有机合成材料的是 (填编号)。
a. 钢铁外壳 b. 合成纤维材质的安全气囊 c. 橡胶轮胎 d. 羊毛座垫
(3)钢铁易生锈。汽车在喷漆前可用盐酸溶液“酸洗”,以除去钢铁表面的铁锈(铁锈主要成分是
Fe O )。除锈过程中观察到溶液变黄,有无色气泡逸出。写出溶液变黄的化学方程式
2 3
。
(4)高级轿车配置的安全气囊内有硝酸铵(NH NO )。当汽车在高速行驶中受到猛烈撞击时,硝酸铵
4 3
会迅速发生分解,产生大量的水蒸气和一氧化二氮气体充满气囊。气囊填补在驾驶员与挡风玻璃、方
向盘之间,达到保护驾乘人员的目的。
①已知硝酸铵中铵根离子( )的化合价为+1价,则铵根中氮元素的化合价为 。
[来源:Zxxk.Com]
②写出硝酸铵受撞击发生分解反应的化学方程式 。
(5)酒驾会带来危害。交警在查酒驾时,先请司机打开车窗,若闻到酒精气味,则要求司机必须接受酒
精含量的测试。交警能闻到酒精的气味是因为 。
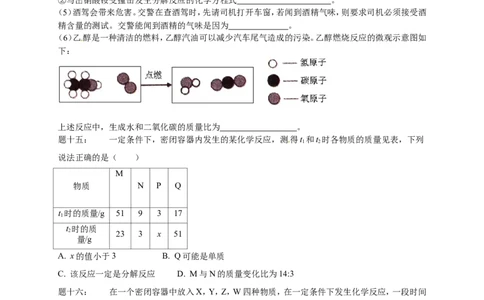
(6)乙醇是一种清洁的燃料,乙醇汽油可以减少汽车尾气造成的污染。乙醇燃烧反应的微观示意图如
下:
上述反应中,生成水和二氧化碳的质量比为 。
题十五: 一定条件下,密闭容器内发生的某化学反应,测得t 和t 时各物质的质量见表,下列
1 2
说法正确的是( )
M
[来
物质 N P Q
t 时的质量/g 51 9 3 17
1
t 时的质
2 23 3 x 51
量/g
[来源:学+科+网]
A. x的值小于3 B. Q可能是单质
C. 该反应一定是分解反应 D. M与N的质量变化比为14:3
题十六: 在一个密闭容器中放入X,Y,Z,W四种物质,在一定条件下发生化学反应,一段时间
后,测得相关数据如下表,下列关于此反应的认识,正确的是( )
物 质 X Y Z W
反应前的质量/g 10 m 8 7
反应后的质量/g 2 3 30 25
A.若W为水,则X或Y必定为酸或碱
B.若X为化合物,Y为单质,则该反应一定为置换反应
C.m的数值为32
D.参加反应的X与Y的质量比为1:4
3zxxk.com
4zxxk.com
化学用语—提高篇
课后练习参考答案
题一: C
详解:图中粒子的核内质子数等于核外电子总数,表明该粒子是原子。所以本题应该选C。
题二: D
详解:在原子中:质子数=核电荷数=核外电子数,化学上习惯用圆圈表示原子核,里面的数字表示质
子数(即核电荷数),核外电子分层排布,弧线表示电子层,弧线上的数字表示该层上的电子数,A、B、
C中质子数=核外电子数,为原子;D中质子数11大于核外电子数10,带正电荷,表示阳离子,本题应
选D。
题三: D
详解:A. 元素是具有相同质子数(即核电荷数)的一类原子的总称,②、③粒子的核内质子数不同,因
此不属于同种元素,A项说法错误;
B. 决定元素化学性质的是最外层电子数,②、④粒子的最外层电子数不同,因而不具有相同的化学性
质,B项说法错误;
C. ②粒子的核内质子数(13)比核外电子数(10)多3,则②粒子为带3个单位正电荷的铝离子,其离
子符号为Al3+,C项符号表示错误;
D. 镁原子的最外层电子数为2,在化学反应中易失去2个电子而形成带2个单位正电荷的阳离子,镁
元素在化合物中的化合价通常为+2价;氟原子的最外层电子数为7,在化学反应中易得到1个电子而
形成带1个单位负电荷的阴离子,氟元素在化合物中的化合价通常为﹣1价;则镁、氟组成化合物的
化学式为MgF ,D项说法正确。因此本题答案为D。
2
题四: A AC Mg2+
详解:元素的化学性质取决于原子的最外层电子数,A、D粒子的最外层电子数都为2,因此具有相似
的化学性质,注意B粒子的最外层电子数尽管也为2,但第一电子层上的2个电子却是相对稳定结构,
因而B与A、D的化学性质有较大差异;A、C具有相同的质子数,属于同种元素;C粒子为Mg2+。
题五: A
详解:A. 若“ ”、“ ”分别表示氢、氮元素的原子,则生成物“ ”的化学式可能是NH ,A项
3
正确;
B. 该反应的生成物只有“ ”一种,“ ”分子由不同种元素的原子构成,属于化合物,B项错
误;
C. 该反应符合“多变一”的特点,属于化合反应,C项错误;
D. 反应后, 剩余一个,所以参加反应的两种物质分子个数之比为1:3,D项错误。本题答案为A。
题六: B
详解:化学反应的过程是构成反应物的分子分解成原子、原子再重新组合成新物质分子的过程,在该
过程中,原子的种类不变、原子的数目不变、原子的质量不变,因而反应前后元素质量不变,A、C项均
正确;反应前后分子种类一定发生变化,B项错误;从图中可直观看出反应物、生成物的微粒个数比
为2:2:1,D项正确。本题答案为B。
题七: ①Ca(OH) +CO =CaCO ↓+H O ( 或 Ca(OH) +Na CO=CaCO↓+2NaOH )
2 2 3 2 2 2 3 3
②Fe O+6HCl=2FeCl +3H O 改良酸性土壤(或作建筑材料、配制农药波尔多液等)
2 3 3 2
详解:从图中可以看出,C能与A、B、D及铁发生反应,可知C为盐酸;上述物质中能转化生成铁的物
质只有氧化铁,则D为氧化铁,反应②的化学方程式为:Fe O+6HCl==2FeCl +3H O;A、B分别为氢
2 3 3 2
氧化钙、碳酸钙中的一种,氢氧化钙与二氧化碳或可溶性碳酸盐反应可转化生成碳酸钙,而碳酸钙不
5zxxk.com
能直接转化生成氢氧化钙,则 A 为氢氧化钙、B为碳酸钙,则反应①的化学方程式为:
Ca(OH) +CO =CaCO ↓+H O或Ca(OH) +Na CO==CaCO↓+2NaOH等;氢氧化钙俗称熟石灰、消石灰,
2 2 3 2 2 2 3 3
常用作建筑材料、改良酸性土壤,配制农药波尔多液等。
题八: A
详解:解题的方法是结合图示转化关系逐项推断筛选。
A项中二氧化碳与氢氧化钙溶液可生成碳酸钙和水。碳酸钙与盐酸反应可生成氯化钙、二氧化碳和水。
水通电分解生成氧气和氢气。碳在充足的氧气中完全燃烧生成二氧化碳,满足图示转化关系;
B项中的氯化钠不能通过一步反应生成二氧化碳;
C项中的氧化镁不能通过一步反应生成过氧化氢;
D项中的水不能通过一步反应生成氯化钙。本题应选A。
题九: (1)H (2)HO (3)HSO (4)NaHSO
2 2 2 4 4
详解:图示分别是氢、氧、钠和硫的原子结构示意图,分别属于氢元素、氧元素、钠元素和硫元素。
(1)只含一种元素的纯净物是单质,如氢气(H)、氧气(O)、钠(Na)和硫(S);(2)含有两种元素的
2 2
化合物有水(HO)、过氧化氢(HO)、氧化钠(NaO)、硫化钠(NaS)、二氧化硫(SO )、三氧化硫
2 2 2 2 2
(SO )等;
3
(3)含有三种元素的化合物有氢氧化钠(NaOH)、硫酸(HSO )、硫酸钠(NaSO )等;
2 4 2 4
(4)含有四种元素的化合物有硫酸氢钠(NaHSO)。
4
题十: (1)Mg (2)2N (3) (4)CH (5) (3)Fe(OH)
2 4 3
详解:解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,以及在化学符号前或
其它位置加上适当的计量数来完整地表达其意义。
(1)镁是由原子直接构成的物质,其化学式用镁元素符号表示;
(2)化学式前面加数字表示分子的个数;
(3)离子符号前面加数字表示离子的个数;
(4)甲烷的化学式为CH;
4
(5)硫元素的化合价应标注在元素符号的上面;
(6)氢氧化铁中Fe元素和OH的化合价分别为+3和1价,根据化合物中正负化合价代数和为0书
写氢氧化铁的化合式。
题十一: (1)锌 (2)455 (3)14.3%
详解:(1)锌在人体中的含量小于0.01%,属于微量元素;
(2)葡萄糖酸锌(C H O Zn)的相对分子质量=12×12+1×22+16×14+65=455;
12 22 14
(3)葡萄糖酸锌中锌元素的质量分数= ≈14.3%。
题十二: (1)三 2:4:3 (2)35.0% 98%
详解:(1)硝酸铵(NH NO )由氮、氢、氧三种元素组成;氮、氢、氧的原子个数比为2:4:3;
4 3
(2)硝酸铵中氮元素的质量分数= ×100%=35.0%;设该肥料的实际纯度(该肥
料中硝酸铵的质量分数)为x,则有如下关系: ,解得:x=98%。
题十三: (1)糖类、蛋白质、油脂、维生素 营养丰富、均衡
(2)AC (3)防止形成酸雨,保护环境 CH+2O CO+2H O
4 2 2 2
(4)MgH +2H O==Mg(OH) ↓+2H ↑
2 2 2 2
详解:(1)从题图中能够看出,土豆中富含蛋白质、糖类、油脂和维生素等营养素,由于土豆和牛奶中
6zxxk.com
含有多种营养素,利于均衡营养,所以多食用有利于身体健康;
(2)NH Cl、CO(NH) 属于氮肥、KCO 属于钾肥、Ca (PO ) 属于磷肥;
4 2 2 2 3 3 4 2
(3)分析题图能够看出:燃烧相同质量的天然气和煤所产生的CO 相近,但燃烧甲烷几乎不产生SO ,
2 2
而燃烧煤产生的SO 却非常多,SO 溶于水生成酸性物质使雨水显酸性,形成酸雨,故改用天然气作
2 2
燃料能够防止形成酸雨,有利于保护环境;
(4)根据原子守恒定律,可以推断出反应生成的碱是Mg(OH) ,进一步依据反应物和生成物完成氢化
2
镁与水反应的化学方程式,并注意化学方程式的配平。
题十四: (1)Fe O+3CO高温 2Fe+3CO (2)bc (3)Fe O+6HCl=2FeCl +3H O
2 3 2 2 3 3 2
(4)①3价 ②NH NO NO↑+2H O↑ (5)分子在不断运动 (6)27:44
4 3 2 2
详解:(1)在高温条件下,一氧化碳能和氧化铁反应生成铁和二氧化碳,由此写出反应的化学方程式;
(2)钢铁属于金属材料,合成纤维、合成橡胶属于有机合成材料,羊毛属于天然有机材料,故选bc;
(3)铁锈的主要成分氧化铁能和盐酸反应生成黄色的氯化铁溶液和水,铁锈除去后,露出的铁继续和
盐酸反应生成氯化亚铁和氢气,本题要求写出溶液变黄的化学方程式,因此写出第一个反应的化学方
程式即可:Fe O+6HCl=2FeCl +3H O;
2 3 3 2
(4)①铵根中氢元素的化合价为+1价,设铵根中氮元素的化合价为x,则x+(+1) 4=+1,解得x=
3;②根据提供的信息可知硝酸铵撞击后会生成水蒸气和一氧化二氮,根据一写、二配、三注的步骤
即可写出反应的化学方程式;
(5)闻到气味是因为分子在不断运动;
(6)根据反应的微观示意图可写出乙醇燃烧的化学方程式为:C HOH+3O 3HO+2CO,反应
2 5 2 2 2
中生成水和二氧化碳的质量比为:
= 。
题十五: D
详解:A. 依据各物质在化学反应前后的质量变化可以确定M、N是反应物,Q是生成物,在t~t 时间
1 2
段内参加反应的M、N的质量分别为5123=28 g、93=6 g,反应物质
量减少了28+6=34 g。生成Q的质量为5117=34 g,所以P的质量没有变化,因而x的值为3,所以P
既不是反应物也不是生成物,A项错误;
B.该反应可表示为M+N=Q,该反应具有“多变一”的特点,属于化合反应,则Q一定属于化合物,
B、C项均错误;
[来源:Z*xx*k.Com]
D. 参加反应的M、N的质量比为28g:6g=14:3,D项正确。所以本题答案为D。
题十六: D
详解:A. 由表中数据分析可知,反应前后,X的质量减少了10 g2 g=8 g,故X是反应物,参加反应
的X的质量为8 g;Z的质量增加了30 g-8 g=22 g,Z是生成物,生成Z的质量为22 g;W的质量增
加了25 g7 g=18 g,W是生成物,生成的W的质量为18 g;由质量守恒定律,Y应是反应物,且参
加反应的Y的质量为22 g+18 g8 g=32 g,故m的数值为32 g+3 g=35 g。综上所述,该反应的反应
物为X和Y,生成物是Z和W。若W为水,则X或Y不一定为酸或碱,如酒精等有机物燃烧也能生成
水,A错误;若X为化合物,Y为单质,无法确定Z和W的类别,该反应不一定为置换反应,B错误;
根据上面的分析m的数值应为35 g,C错误;参加反应的X与Y的质量比为8g:32g=1:4,D正确。本
题答案为D。
7