文档内容
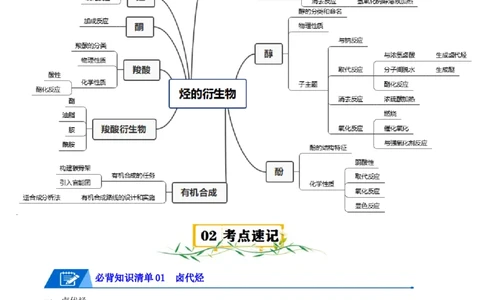
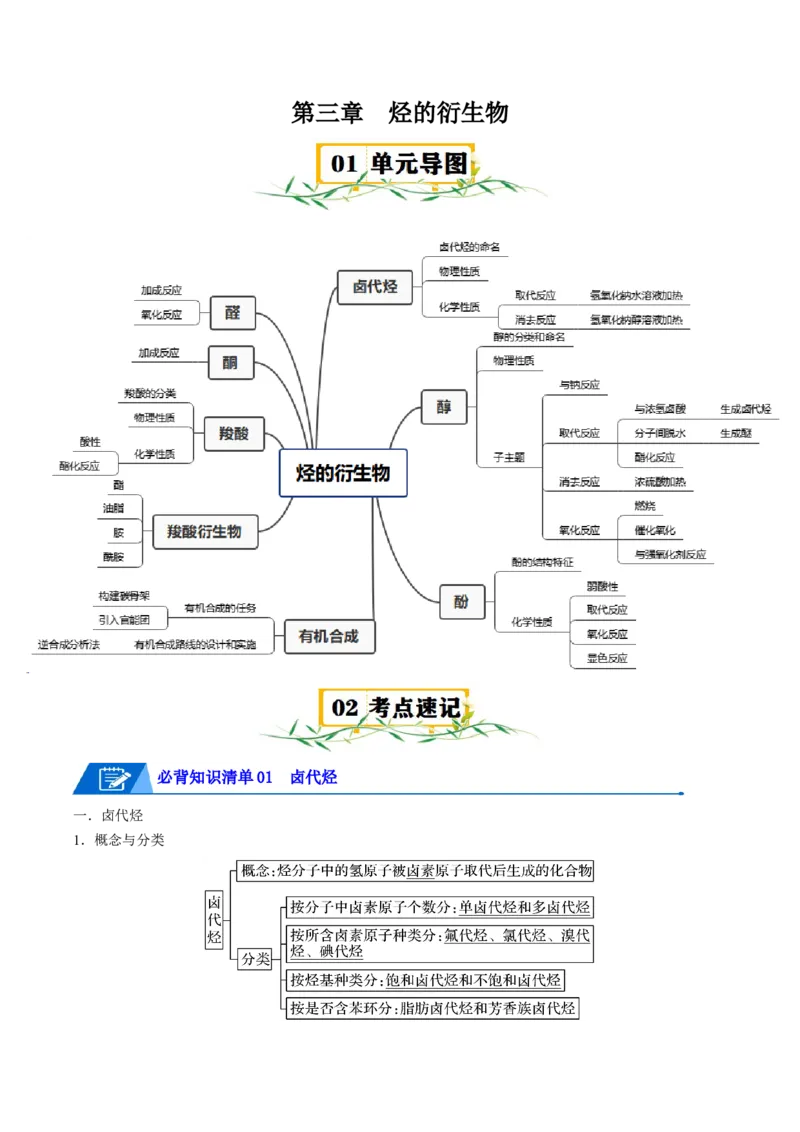
第三章 烃的衍生物
必背知识清单01 卤代烃
一.卤代烃
1.概念与分类2.卤代烃的命名
卤代烃的命名一般用系统命名法,与烃类的命名相似。例如:
、CH==CH—Cl、
2
2-氯丁烷 氯乙烯 1,2-二溴乙烷
3.物理性质
二.取代反应 消去反应
1.取代反应(水解反应)
实验装置
①中溶液分层
实验现象 ②中有机层厚度减小,直至消失
④中有淡黄色沉淀生成
实验解释 溴乙烷与NaOH溶液共热产生了 Br -
(1)溴乙烷与氢氧化钠溶液共热时断裂的是C—Br,水中的羟基与碳原子形成C—O,断下的Br与水中的H
结合成HBr。
(2)溴乙烷与NaOH溶液共热反应的化学方程式为CHCHBr+NaOH――→CHCHOH+NaBr。
3 2 3 2
反应类型为取代反应。
2.消去反应
实验装置 实验现象
反应产生的气体经水洗后,使酸性KMnO 溶液褪
4
色
生成的气体分子中含有碳碳不饱和键
(1)1-溴丁烷与氢氧化钠的乙醇溶液共热反应后,化学方程式为
CHCHCHCHBr+NaOH――→CHCHCH==CH ↑+NaBr+HO。
3 2 2 2 3 2 2 2
(2)消去反应:有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如HO、HX等),
2而生成含不饱和键的化合物的反应。
(3)问题讨论:①实验中盛有水的试管的作用是为了除去挥发出来的乙醇, 原因是乙醇也能使酸性高锰酸
钾溶液褪色,干扰丁烯的检验。
②除酸性高锰酸钾溶液外还可以用溴的四氯化碳溶液来检验丁烯,此时气体还用先通入水中吗?
不用,理由是乙醇与溴不反应,不会干扰丁烯的检验。
必背知识清单02 醇
一.醇的概述
1.醇的概念、分类及命名
(1)概念
醇是羟基与饱和碳原子相连的化合物。
饱和一元醇通式为C H OH 或C H O(n≥1,n为整数)。
n 2n+1 n 2n+2
(2)分类
(3)命名
CHCHCHOH 1- 丙醇 ; 2- 丙醇 ; 1,2,3- 丙三醇 。
3 2 2
③注意:用系统命名法命名醇,确定最长碳链时不能把—OH看作链端,只能看作取代基,但选择的最长
碳链必须连有—OH。
2.物理性质
(1)沸点
①相对分子质量相近的醇和烷烃相比,醇的沸点远远高于烷烃。
②饱和一元醇,随分子中碳原子个数的增加,醇的沸点升高。
③碳原子数相同时,羟基个数越多,醇的沸点越高。
(2)溶解性:甲醇、乙醇、丙醇、乙二醇、丙三醇等低级醇可与水以任意比例混溶。
(3)密度:醇的密度比水的密度小。
3.几种重要的醇
名称 结构简式 性质 用途
无色透明、易挥发的液体;能
与水及多种有机溶剂混溶;有
甲醇 CHOH 毒、误服少量(10 mL)可致人 化工原料、燃料
3
失明,多量(30 mL)可致人死
亡无色、黏稠的液体,有甜味、 发动机防冻液的主要化学
乙二醇 能与水混溶,能显著降低水的 成分,也是合成涤纶等高
凝固点 分子化合物的主要原料
吸水能力——配制印泥、
无色、黏稠、具有甜味的液
丙三醇 化妆品;凝固点低——作
体,能与水以任意比例混溶,
(甘油) 防冻剂;三硝酸甘油酯俗
具有很强的吸水能力
称硝化甘油——作炸药等
二.醇的化学性质——以乙醇为例
乙醇发生化学反应时,可断裂不同的化学键。如
1.与钠反应
分子中a 键断裂,化学方程式为2CHCHOH+2Na―→2CHCH ONa + H ↑。
3 2 3 2 2
2.消去反应
分子中 b 、 d 键断裂,化学方程式为CHCHOH―――→CH==CH ↑+HO。
3 2 2 2 2
3.取代反应
(1)与HX发生取代反应
分子中b 键断裂,化学方程式为C HOH+HX――→C H X + H O。
2 5 2 5 2
(2)分子间脱水成醚
一分子中a 键断裂,另一分子中b 键断裂,化学方程式为
2CHCHOH―――→CHCHOCH CH+HO。
3 2 3 2 2 3 2
4.氧化反应
(1)燃烧反应:C H OH + 3O ――→ 2CO + 3H O。
2 5 2 2 2
(2)催化氧化
乙醇在铜或银作催化剂加热的条件下与空气中的氧气反应生成乙醛,分子中 a 、 c 键断裂,化学方程式为
2CHCH OH + O ―――→ 2CH CHO + 2H O 。
3 2 2 3 2
(3)醇被酸性KMnO 溶液或酸性KCr O 溶液氧化CH3CH2OH――→CH3CHO――→CH3COOH。
4 2 2 7
必背知识清单03 酚
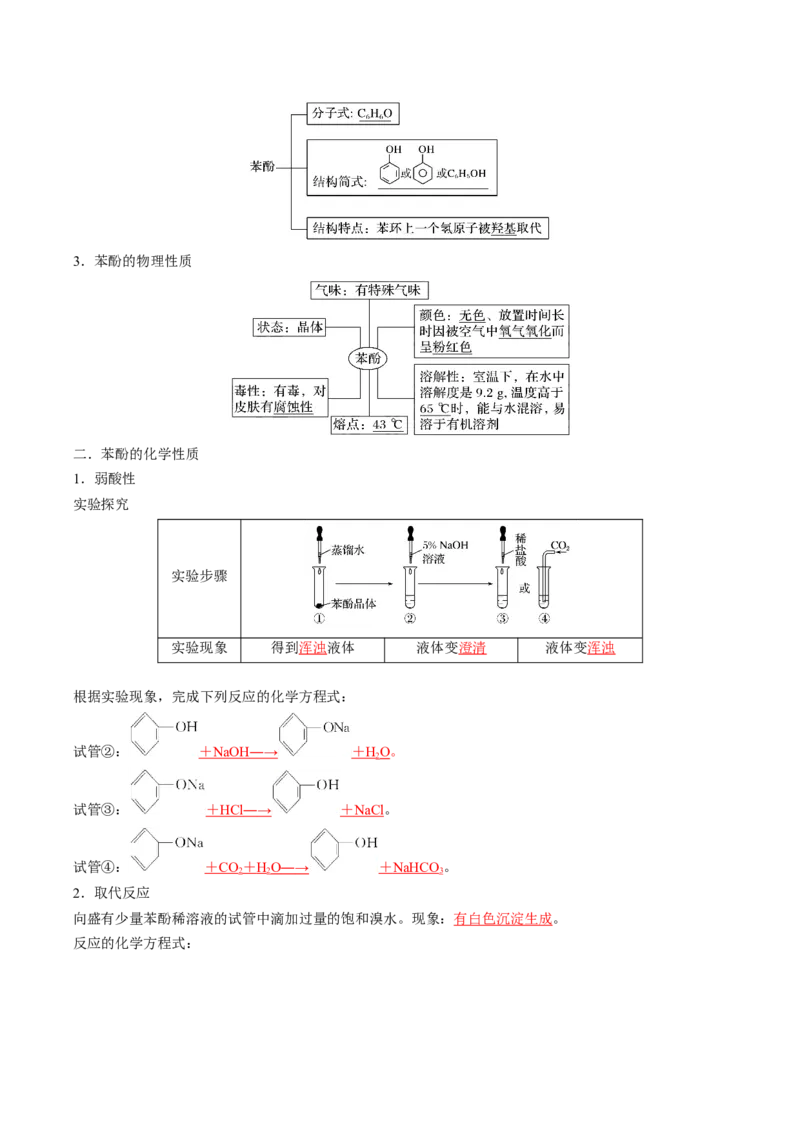
一.酚的概念及其代表物的结构
1.酚的概念
酚是羟基与苯环直接相连而形成的化合物。
如: 、 和
2.苯酚的分子结构3.苯酚的物理性质
二.苯酚的化学性质
1.弱酸性
实验探究
实验步骤
实验现象 得到浑浊液体 液体变澄清 液体变浑浊
根据实验现象,完成下列反应的化学方程式:
试管②: + NaOH ― → + H O。
2
试管③: + HC l ― → + NaC l。
试管④: + CO + H O ― → + NaHCO 。
2 2 3
2.取代反应
向盛有少量苯酚稀溶液的试管中滴加过量的饱和溴水。现象:有白色沉淀生成。
反应的化学方程式:+3Br ―→ +3HBr
2
3.显色反应
在少量苯酚溶液中滴加氯化铁溶液。现象:溶液显紫色。
4.氧化反应
苯酚是无色晶体,但放置时间过长往往显粉红色,其原因是部分苯酚被空气中的氧气氧化。
必背知识清单04 醛 酮
一.乙醛的性质
1.醛的概念及结构特点
醛是由烃基(或氢原子)与醛基相连而构成的化合物。醛类官能团的结构简式是 — CHO ,饱和一元醛的通式
为C H O( n ≥1) 或C H CHO。
n 2n n 2n+1
2.乙醛的结构与物理性质
3.乙醛的化学性质
(1)加成反应
①催化加氢(还原反应)
乙醛中的碳氧双键和烯烃中的碳碳双键性质类似,也能与氢气发生加成反应,化学方程式为
CHCHO+H――→CHCHOH。
3 2 3 2
②与HCN加成
在醛基的碳氧双键中,由于氧原子的电负性较大,碳氧双键中的电子偏向氧原子,使氧原子带部分负电
荷,碳原子带部分正电荷,从而使醛基具有较强的极性。乙醛能和一些极性试剂例如氰化氢(HCN)发生加
成反应: +H—CN―→ (2-羟基丙腈)。
(2)氧化反应
①可燃性
乙醛燃烧的化学方程式:2CH CHO + 5O ――→ 4CO + 4H O。
3 2 2 2
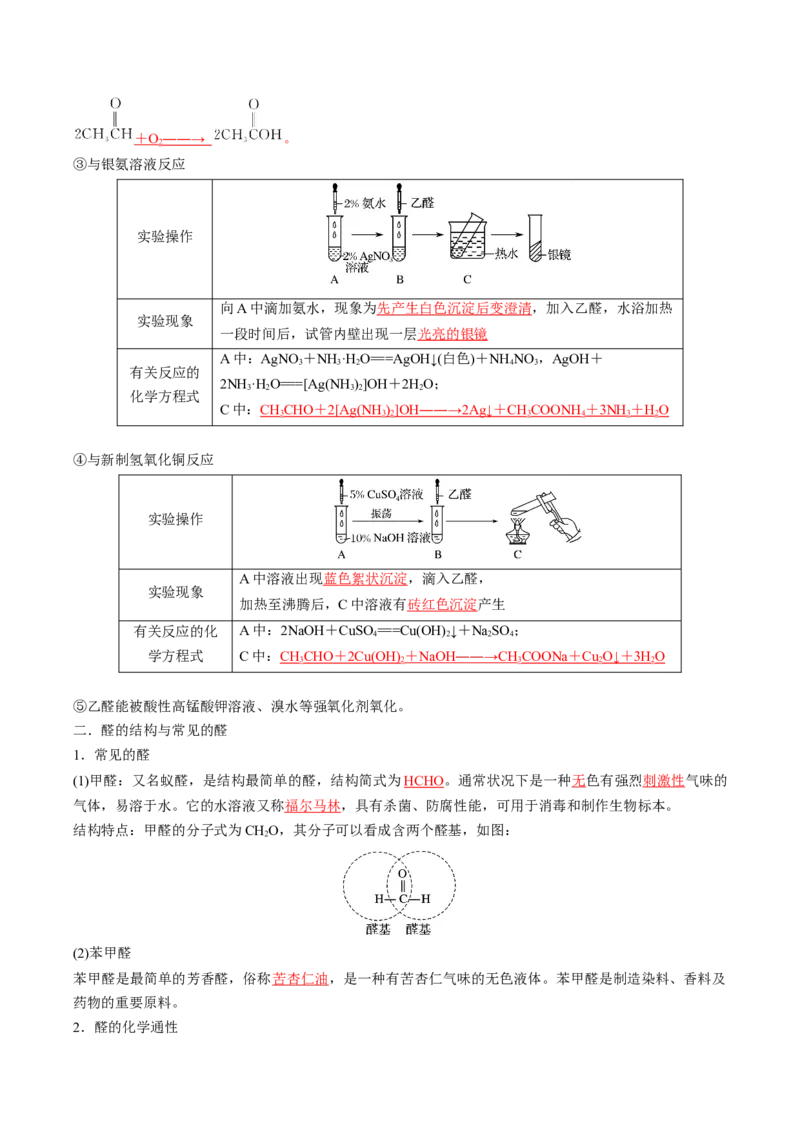
②催化氧化
乙醛在一定温度和催化剂作用下,能被氧气氧化为乙酸的化学方程式:+ O ――→ 。
2
③与银氨溶液反应
实验操作
向A中滴加氨水,现象为先产生白色沉淀后变澄清,加入乙醛,水浴加热
实验现象
一段时间后,试管内壁出现一层光亮的银镜
A中:AgNO+NH ·H O===AgOH↓(白色)+NH NO ,AgOH+
3 3 2 4 3
有关反应的
2NH ·H O===[Ag(NH )]OH+2HO;
3 2 3 2 2
化学方程式
C中:CH CHO + 2[Ag(NH ) ]OH ――→ 2Ag↓ + CH COONH + 3NH + H O
3 3 2 3 4 3 2
④与新制氢氧化铜反应
实验操作
A中溶液出现蓝色絮状沉淀,滴入乙醛,
实验现象
加热至沸腾后,C中溶液有砖红色沉淀产生
有关反应的化 A中:2NaOH+CuSO ===Cu(OH) ↓+NaSO ;
4 2 2 4
学方程式 C中:CH CHO + 2Cu(OH) + NaOH ――→ CH COONa + Cu O↓ + 3H O
3 2 3 2 2
⑤乙醛能被酸性高锰酸钾溶液、溴水等强氧化剂氧化。
二.醛的结构与常见的醛
1.常见的醛
(1)甲醛:又名蚁醛,是结构最简单的醛,结构简式为HCHO。通常状况下是一种无色有强烈刺激性气味的
气体,易溶于水。它的水溶液又称福尔马林,具有杀菌、防腐性能,可用于消毒和制作生物标本。
结构特点:甲醛的分子式为CHO,其分子可以看成含两个醛基,如图:
2
(2)苯甲醛
苯甲醛是最简单的芳香醛,俗称苦杏仁油,是一种有苦杏仁气味的无色液体。苯甲醛是制造染料、香料及
药物的重要原料。
2.醛的化学通性(1)醛可被氧化为羧酸,也可被氢气还原为醇,因此醛既有氧化性,又有还原性,其氧化、还原的关系为R
—CHOH ――→ 。
2
(2)有机物的氧化、还原反应
①氧化反应:有机物分子中失去氢原子或加入氧原子的反应,即加氧去氢。
②还原反应:有机物分子中加入氢原子或失去氧原子的反应,即加氢去氧。
③醛基的检验:在洁净的试管中加入新制银氨溶液和少量试样后,水浴加热,有银镜生成,或在洁净的试
管中加入少量试样和新制的Cu(OH) ,加热煮沸,有砖红色沉淀生成。
2
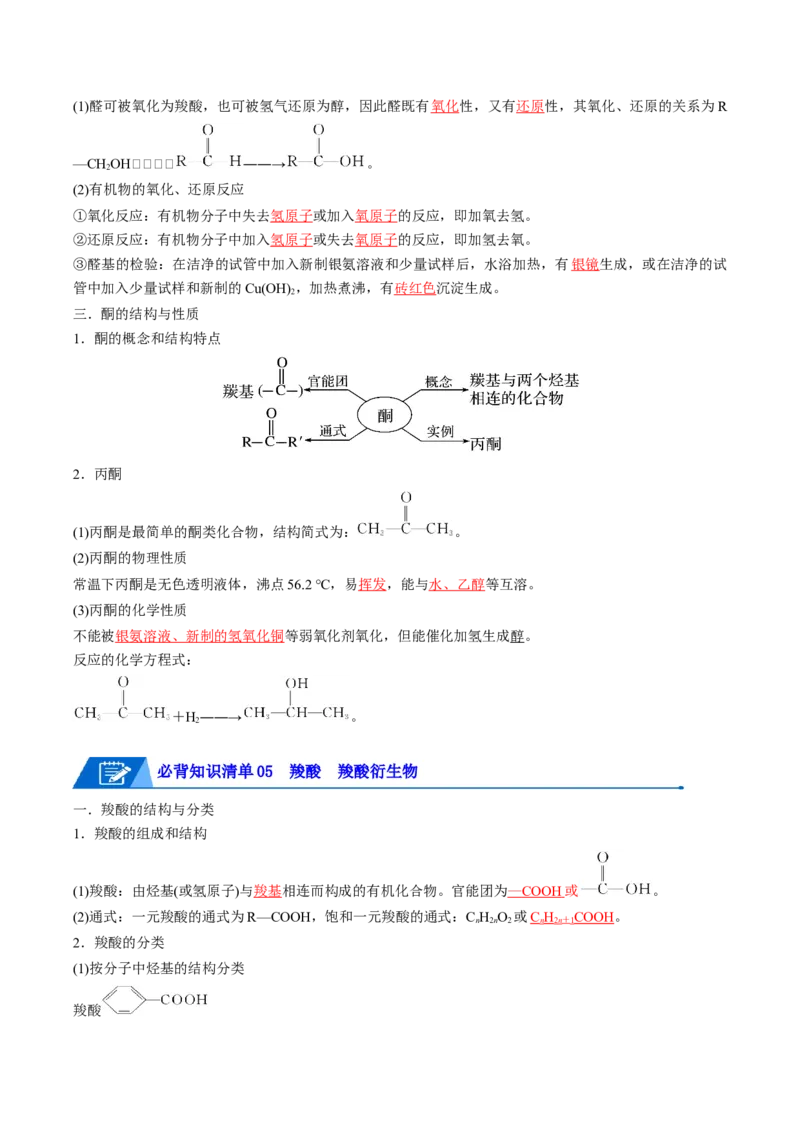
三.酮的结构与性质
1.酮的概念和结构特点
2.丙酮
(1)丙酮是最简单的酮类化合物,结构简式为: 。
(2)丙酮的物理性质
常温下丙酮是无色透明液体,沸点56.2 ℃,易挥发,能与水、乙醇等互溶。
(3)丙酮的化学性质
不能被银氨溶液、新制的氢氧化铜等弱氧化剂氧化,但能催化加氢生成醇。
反应的化学方程式:
+H――→ 。
2
必背知识清单05 羧酸 羧酸衍生物
一.羧酸的结构与分类
1.羧酸的组成和结构
(1)羧酸:由烃基(或氢原子)与羧基相连而构成的有机化合物。官能团为 — COOH 或 。
(2)通式:一元羧酸的通式为R—COOH,饱和一元羧酸的通式:C H O 或C H COOH。
n 2n 2 n 2n+1
2.羧酸的分类
(1)按分子中烃基的结构分类
羧酸(2)按分子中羧基的个数分类
羧酸
(3)按分子中烃基所含碳原子数多少分类
羧酸
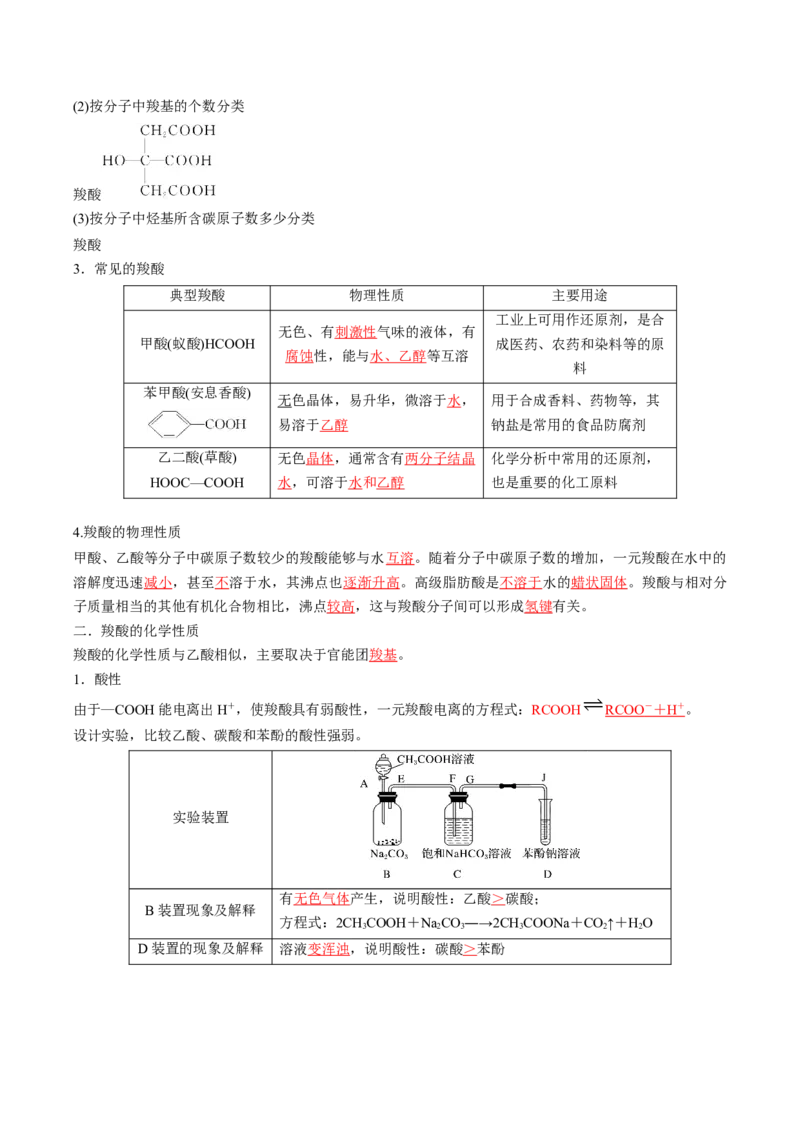
3.常见的羧酸
典型羧酸 物理性质 主要用途
工业上可用作还原剂,是合
无色、有刺激性气味的液体,有
甲酸(蚁酸)HCOOH 成医药、农药和染料等的原
腐蚀性,能与水、乙醇等互溶
料
苯甲酸(安息香酸)
无色晶体,易升华,微溶于水, 用于合成香料、药物等,其
易溶于乙醇 钠盐是常用的食品防腐剂
乙二酸(草酸) 无色晶体,通常含有两分子结晶 化学分析中常用的还原剂,
HOOC—COOH 水,可溶于水和乙醇 也是重要的化工原料
4.羧酸的物理性质
甲酸、乙酸等分子中碳原子数较少的羧酸能够与水互溶。随着分子中碳原子数的增加,一元羧酸在水中的
溶解度迅速减小,甚至不溶于水,其沸点也逐渐升高。高级脂肪酸是不溶于水的蜡状固体。羧酸与相对分
子质量相当的其他有机化合物相比,沸点较高,这与羧酸分子间可以形成氢键有关。
二.羧酸的化学性质
羧酸的化学性质与乙酸相似,主要取决于官能团羧基。
1.酸性
由于—COOH能电离出H+,使羧酸具有弱酸性,一元羧酸电离的方程式:RCOOH RCOO - + H + 。
设计实验,比较乙酸、碳酸和苯酚的酸性强弱。
实验装置
有无色气体产生,说明酸性:乙酸>碳酸;
B装置现象及解释
方程式:2CHCOOH+NaCO―→2CHCOONa+CO↑+HO
3 2 3 3 2 2
D装置的现象及解释 溶液变浑浊,说明酸性:碳酸>苯酚方程式: +CO+HO―→ +NaHCO
2 2 3
C装置的作用 除去B中挥发的乙酸
实验结论 酸性:乙酸>碳酸>苯酚
2.酯化反应
(1)概念
羧酸和醇在酸催化下生成酯和水的反应叫酯化反应,属于取代反应。
(2)反应规律
羧酸与醇发生酯化反应时,羧酸脱去羟基,醇脱去氢。如在浓硫酸催化作用下,醋酸与乙醇(CHCH18OH)
3 2
酯化反应的化学方程式为
必背知识清单06 羧酸衍生物
一.酯
1.酯的组成与结构
(1)酯是羧酸分子羧基中的—OH被—OR′取代后的产物,其结构可简写为 。
其中:①R和R′可以相同,也可以不同。
②R是烃基,也可以是H,但R′只能是烃基。
③羧酸酯的官能团是酯基。
(2)饱和一元羧酸C H COOH与饱和一元醇C H OH生成酯的结构简式为C H COOC H ,其组
n 2n+1 m 2m+1 n 2n+1 m 2m+1
成通式为C H O(n≥2)。
n 2n 2
(3)命名:根据生成酯的酸和醇命名为某酸某酯。
如:CHCOOCH CH 乙酸乙酯;HCOOCH CHCH 甲酸正丙酯。
3 2 3 2 2 3
2.酯的存在与物理性质
(1)存在:酯类广泛存在于自然界中,低级酯存在于各种水果和花草中。如苹果里含有戊酸戊酯,菠萝里含
有丁酸乙酯,香蕉里含有乙酸异戊酯等。
(2)物理性质
低级酯是具有芳香气味的液体,密度一般比水小,并难溶于水,易溶于乙醇和乙醚等有机溶剂中。
3.酯的化学性质
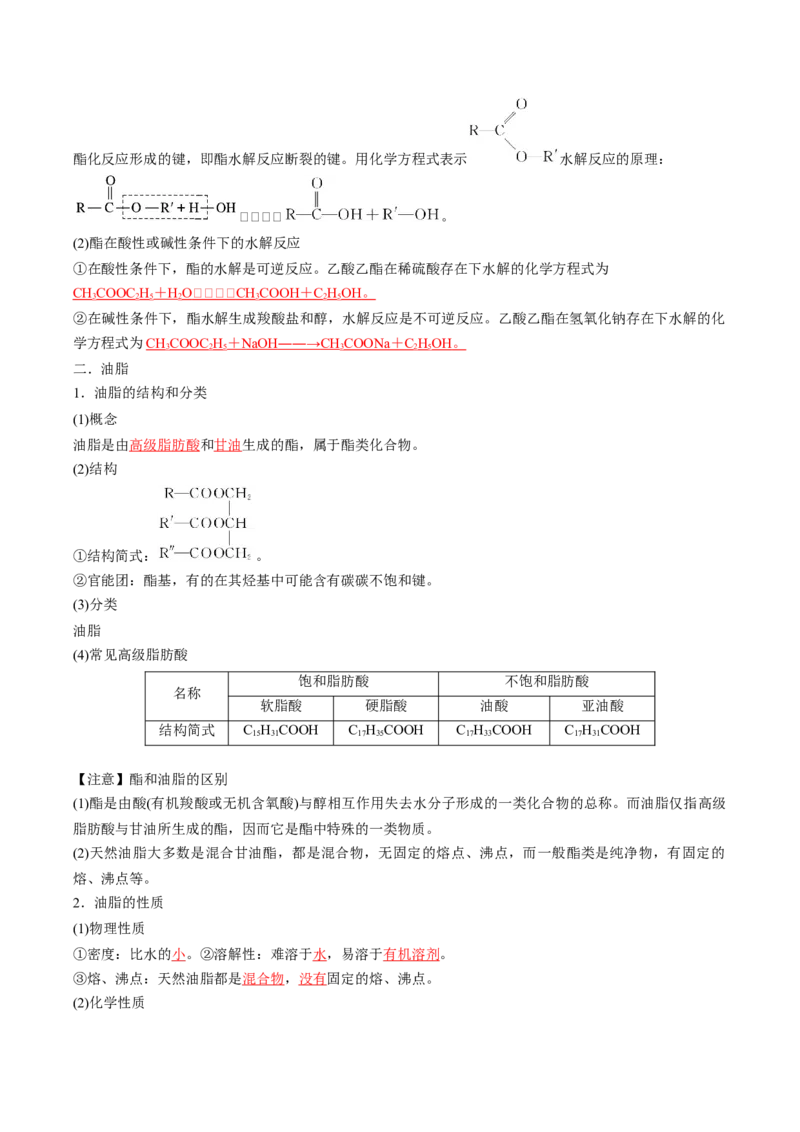
(1)酯的水解反应原理酯化反应形成的键,即酯水解反应断裂的键。用化学方程式表示 水解反应的原理:
。
(2)酯在酸性或碱性条件下的水解反应
①在酸性条件下,酯的水解是可逆反应。乙酸乙酯在稀硫酸存在下水解的化学方程式为
CHCOOC H + H O CH COOH + C H OH 。
3 2 5 2 3 2 5
②在碱性条件下,酯水解生成羧酸盐和醇,水解反应是不可逆反应。乙酸乙酯在氢氧化钠存在下水解的化
学方程式为CHCOOC H + NaOH ――→ CH COONa + C H OH 。
3 2 5 3 2 5
二.油脂
1.油脂的结构和分类
(1)概念
油脂是由高级脂肪酸和甘油生成的酯,属于酯类化合物。
(2)结构
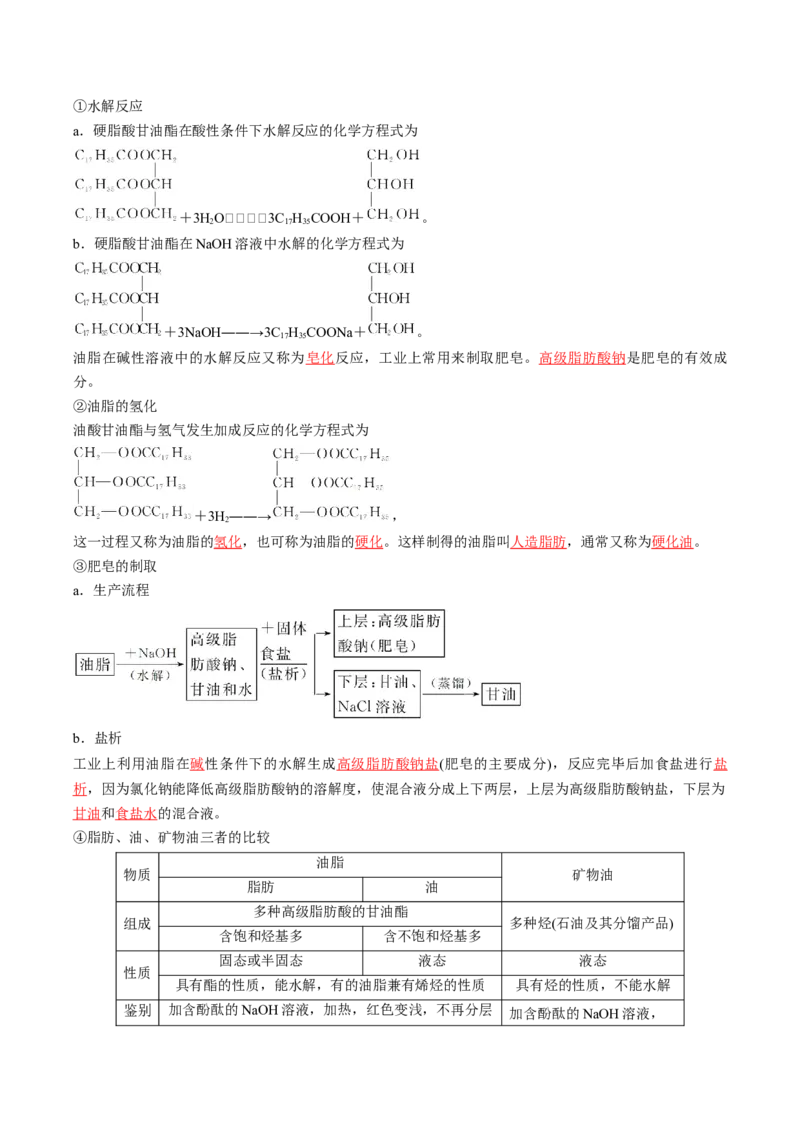
①结构简式: 。
②官能团:酯基,有的在其烃基中可能含有碳碳不饱和键。
(3)分类
油脂
(4)常见高级脂肪酸
饱和脂肪酸 不饱和脂肪酸
名称
软脂酸 硬脂酸 油酸 亚油酸
结构简式 C H COOH C H COOH C H COOH C H COOH
15 31 17 35 17 33 17 31
【注意】酯和油脂的区别
(1)酯是由酸(有机羧酸或无机含氧酸)与醇相互作用失去水分子形成的一类化合物的总称。而油脂仅指高级
脂肪酸与甘油所生成的酯,因而它是酯中特殊的一类物质。
(2)天然油脂大多数是混合甘油酯,都是混合物,无固定的熔点、沸点,而一般酯类是纯净物,有固定的
熔、沸点等。
2.油脂的性质
(1)物理性质
①密度:比水的小。②溶解性:难溶于水,易溶于有机溶剂。
③熔、沸点:天然油脂都是混合物,没有固定的熔、沸点。
(2)化学性质①水解反应
a.硬脂酸甘油酯在酸性条件下水解反应的化学方程式为
+3HO3C H COOH+ 。
2 17 35
b.硬脂酸甘油酯在NaOH溶液中水解的化学方程式为
+3NaOH――→3C H COONa+ 。
17 35
油脂在碱性溶液中的水解反应又称为皂化反应,工业上常用来制取肥皂。高级脂肪酸钠是肥皂的有效成
分。
②油脂的氢化
油酸甘油酯与氢气发生加成反应的化学方程式为
+3H――→ ,
2
这一过程又称为油脂的氢化,也可称为油脂的硬化。这样制得的油脂叫人造脂肪,通常又称为硬化油。
③肥皂的制取
a.生产流程
b.盐析
工业上利用油脂在碱性条件下的水解生成高级脂肪酸钠盐(肥皂的主要成分),反应完毕后加食盐进行盐
析,因为氯化钠能降低高级脂肪酸钠的溶解度,使混合液分成上下两层,上层为高级脂肪酸钠盐,下层为
甘油和食盐水的混合液。
④脂肪、油、矿物油三者的比较
油脂
物质 矿物油
脂肪 油
多种高级脂肪酸的甘油酯
组成 多种烃(石油及其分馏产品)
含饱和烃基多 含不饱和烃基多
固态或半固态 液态 液态
性质
具有酯的性质,能水解,有的油脂兼有烯烃的性质 具有烃的性质,不能水解
鉴别 加含酚酞的NaOH溶液,加热,红色变浅,不再分层 加含酚酞的NaOH溶液,加热,无变化
用途 营养素可食用,化工原料如制肥皂、甘油 燃料、化工原料
①植物油与裂化汽油均含碳碳双键,能使溴水和酸性KMnO 溶液褪色。
4
②区别油脂(酯)与矿物油(烃)的一般方法是加含酚酞的NaOH溶液,加热,红色变浅,最后不分层的为油脂
(酯),否则为矿物油(烃)。
三.酰胺
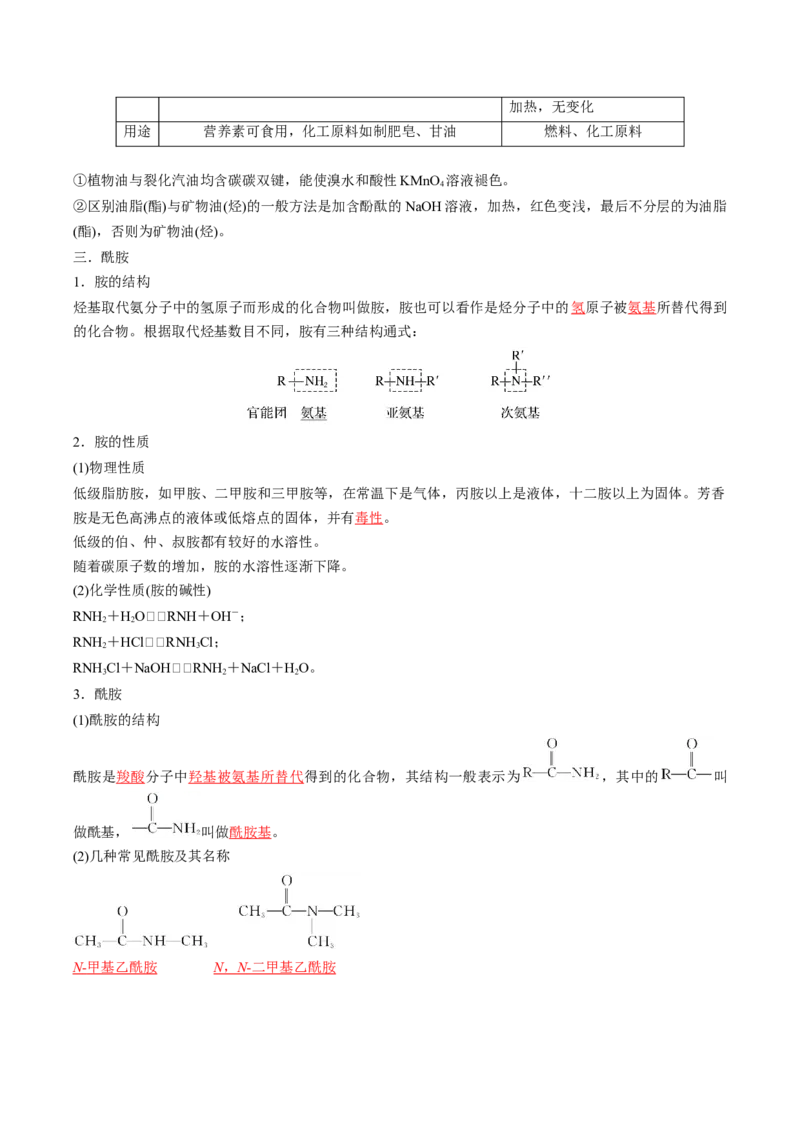
1.胺的结构
烃基取代氨分子中的氢原子而形成的化合物叫做胺,胺也可以看作是烃分子中的氢原子被氨基所替代得到
的化合物。根据取代烃基数目不同,胺有三种结构通式:
2.胺的性质
(1)物理性质
低级脂肪胺,如甲胺、二甲胺和三甲胺等,在常温下是气体,丙胺以上是液体,十二胺以上为固体。芳香
胺是无色高沸点的液体或低熔点的固体,并有毒性。
低级的伯、仲、叔胺都有较好的水溶性。
随着碳原子数的增加,胺的水溶性逐渐下降。
(2)化学性质(胺的碱性)
RNH +HORNH+OH-;
2 2
RNH +HClRNH Cl;
2 3
RNH Cl+NaOHRNH +NaCl+HO。
3 2 2
3.酰胺
(1)酰胺的结构
酰胺是羧酸分子中羟基被氨基所替代得到的化合物,其结构一般表示为 ,其中的 叫
做酰基, 叫做酰胺基。
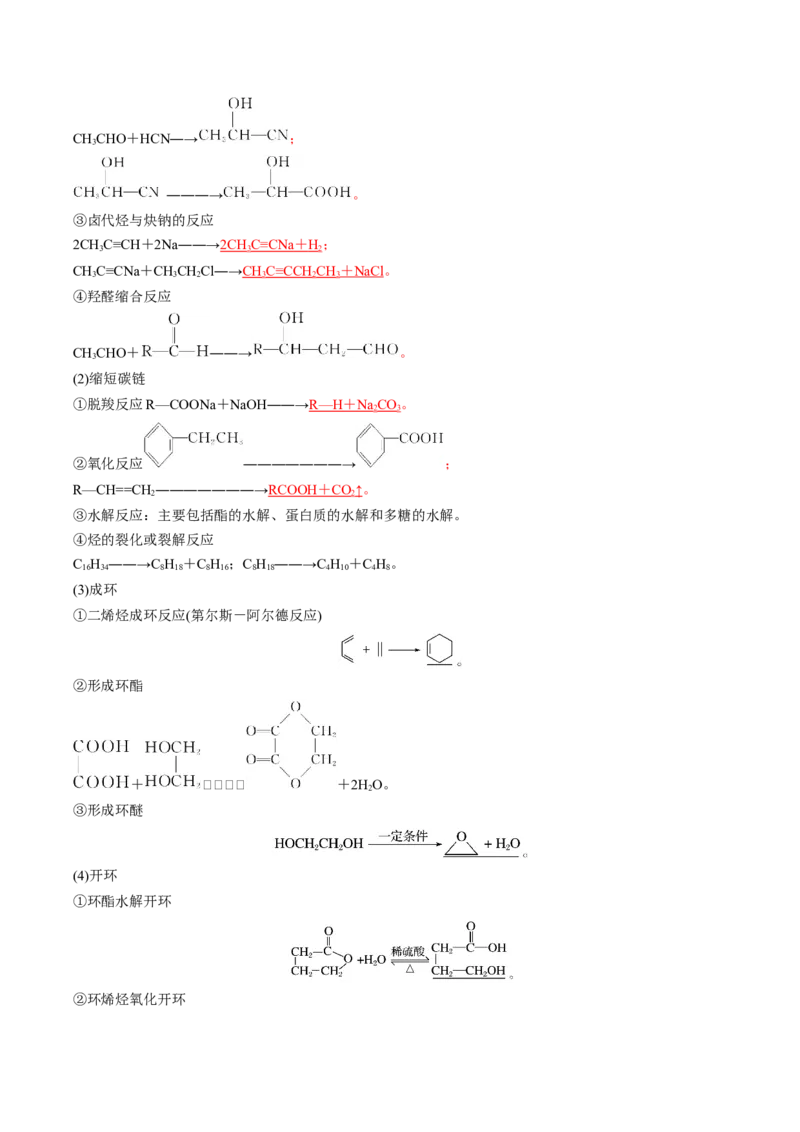
(2)几种常见酰胺及其名称
N - 甲基乙酰胺 N , N - 二甲基乙酰胺N - 甲基 - N - 乙基苯甲酰胺 N - 甲基苯甲酰胺
(3)酰胺的性质(水解反应)
酰胺在酸或碱存在并加热的条件下可以发生水解反应。如果水解时加入碱,生成的酸就会变成盐,同时有
氨气逸出。
RCONH +HO+HCl――→RCOOH+NH Cl;
2 2 4
RCONH +NaOH――→RCOONa+NH ↑。
2 3
必背知识清单07 有机合成
一.有机合成
1.有机合成的概念
有机合成指利用相对简单、易得的原料,通过有机化学反应来构建碳骨架和引入官能团,由此合成出具有
特定结构和性质的目标分子的过程方法。
2.有机合成的任务和过程
3.有机合成的原则
(1)起始原料要廉价、易得、低毒、低污染。
(2)尽量选择步骤最少的合成路线,使得反应过程中副反应少、产率高。
(3)符合“绿色化学”的要求,操作简单、条件温和、能耗低、易实现、原料利用率高、污染少,尽量实现
零排放。
(4)按照一定的反应顺序和规律引入官能团,不能臆造不存在的反应事实。
二.有机合成中的碳骨架的构建和官能团的引入
1.构建碳骨架
(1)增长碳链
①卤代烃与NaCN的反应
CHCHCl+NaCN―→CHCH CN( 丙腈 ) + NaCl ;
3 2 3 2
CHCHCN―――→CHCHCOOH。
3 2 3 2
②醛、酮与氢氰酸的加成反应CHCHO+HCN―→ ;
3
―――→ 。
③卤代烃与炔钠的反应
2CHC≡CH+2Na――→2CH C≡CNa + H ;
3 3 2
CHC≡CNa+CHCHCl―→CHC≡CCH CH + NaC l。
3 3 2 3 2 3
④羟醛缩合反应
CHCHO+ ――→ 。
3
(2)缩短碳链
①脱羧反应R—COONa+NaOH――→ R—H + Na CO。
2 3
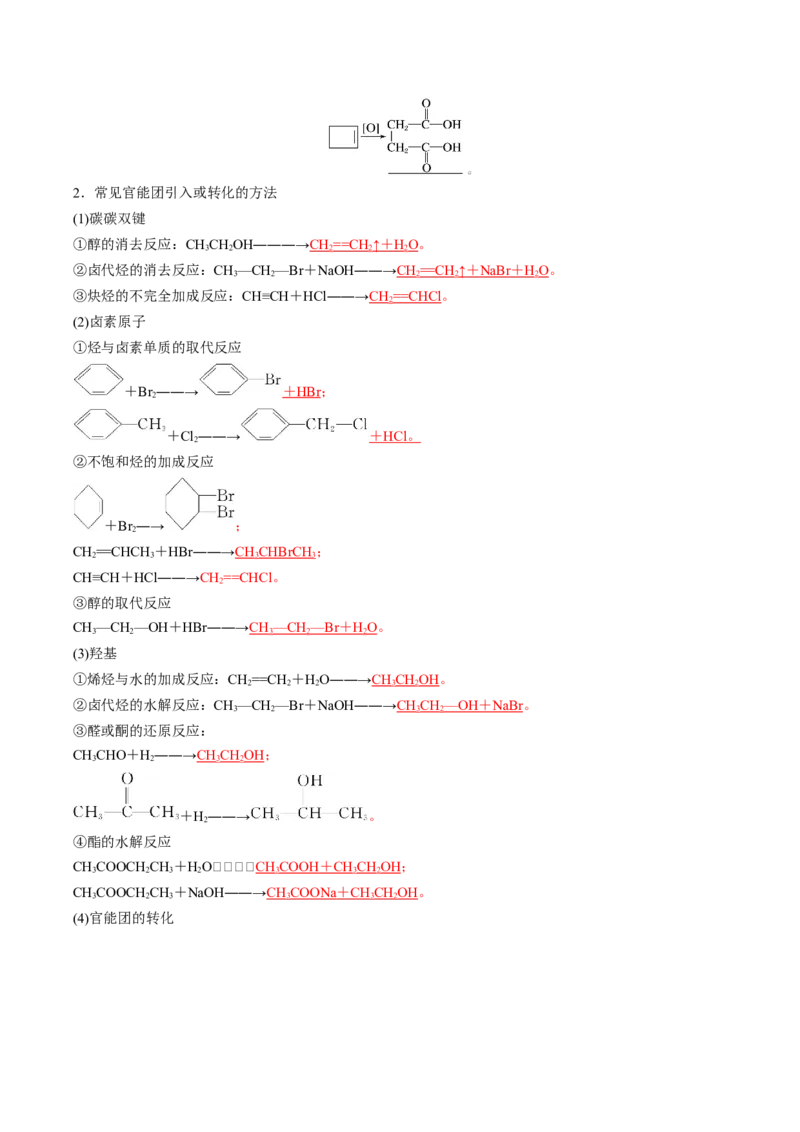
②氧化反应 ―――――――→ ;
R—CH==CH ―――――――→ RCOOH + CO ↑。
2 2
③水解反应:主要包括酯的水解、蛋白质的水解和多糖的水解。
④烃的裂化或裂解反应
C H ――→C H +C H ;C H ――→C H +C H。
16 34 8 18 8 16 8 18 4 10 4 8
(3)成环
①二烯烃成环反应(第尔斯-阿尔德反应)
②形成环酯
+ +2HO。
2
③形成环醚
(4)开环
①环酯水解开环
②环烯烃氧化开环2.常见官能团引入或转化的方法
(1)碳碳双键
①醇的消去反应:CHCHOH―――→CH = =CH ↑ + H O。
3 2 2 2 2
②卤代烃的消去反应:CH—CH—Br+NaOH――→CH == CH ↑ + NaBr + H O。
3 2 2 2 2
③炔烃的不完全加成反应:CH≡CH+HCl――→CH = =CHCl 。
2
(2)卤素原子
①烃与卤素单质的取代反应
+Br ――→ + HB r;
2
+Cl――→ + HC l 。
2
②不饱和烃的加成反应
+Br ―→ ;
2
CH==CHCH +HBr――→CHCHBrCH ;
2 3 3 3
CH≡CH+HCl――→CH==CHCl。
2
③醇的取代反应
CH—CH—OH+HBr――→CH—CH —Br + H O。
3 2 3 2 2
(3)羟基
①烯烃与水的加成反应:CH==CH +HO――→CHCHOH。
2 2 2 3 2
②卤代烃的水解反应:CH—CH—Br+NaOH――→CHCH —OH + NaBr 。
3 2 3 2
③醛或酮的还原反应:
CHCHO+H――→CHCHOH;
3 2 3 2
+H――→ 。
2
④酯的水解反应
CHCOOCH CH+HOCH COOH + CH CHOH;
3 2 3 2 3 3 2
CHCOOCH CH+NaOH――→CH COONa + CH CHOH。
3 2 3 3 3 2
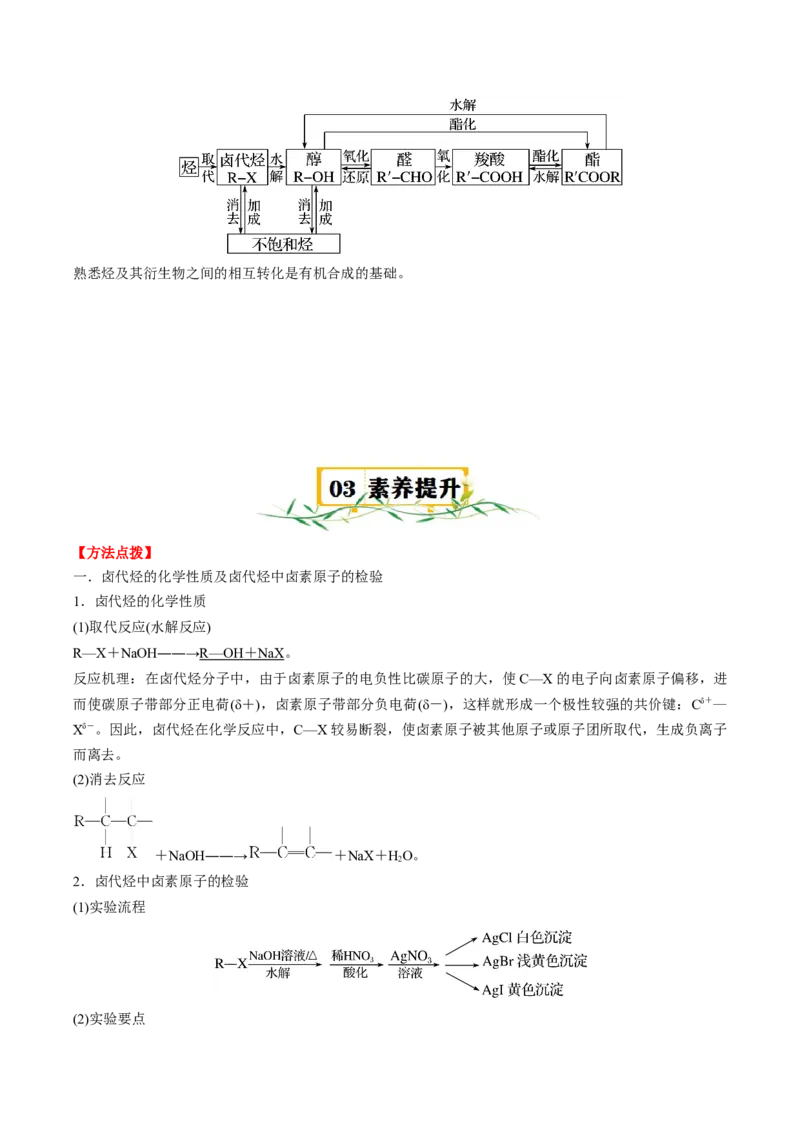
(4)官能团的转化熟悉烃及其衍生物之间的相互转化是有机合成的基础。
【方法点拨】
一.卤代烃的化学性质及卤代烃中卤素原子的检验
1.卤代烃的化学性质
(1)取代反应(水解反应)
R—X+NaOH――→ R—OH + NaX 。
反应机理:在卤代烃分子中,由于卤素原子的电负性比碳原子的大,使C—X的电子向卤素原子偏移,进
而使碳原子带部分正电荷(δ+),卤素原子带部分负电荷(δ-),这样就形成一个极性较强的共价键:Cδ+—
Xδ-。因此,卤代烃在化学反应中,C—X较易断裂,使卤素原子被其他原子或原子团所取代,生成负离子
而离去。
(2)消去反应
+NaOH――→ +NaX+HO。
2
2.卤代烃中卤素原子的检验
(1)实验流程
(2)实验要点①通过水解反应或消去反应将卤素原子转化为卤素离子。
②排除其他离子对卤素离子检验的干扰,卤素原子转化为卤素离子后必须加入稀硝酸中和过量的碱。
【典例1】为检验1-溴丁烷中的溴元素,下列实验操作正确的顺序是
①加入硝酸银溶液②加热煮沸③取少量1-溴丁烷④加入足量稀硝酸酸化⑤加入氢氧化钠溶液⑥冷却
A.③②⑤①④⑥ B.③⑤②①④⑥
C.③⑤②⑥④① D.③④②⑥①⑤
【答案】C
【解析】
先取少量1-溴丁烷,加入氢氧化钠溶液,然后加热进行水解,溶液冷却后,加入硝酸中和过量的氢氧化
钠,再加入硝酸银观察是否有沉淀,故正确顺序为:③⑤②⑥④①;
故选C。
二.消去反应——乙烯的实验室制法
(1)实验装置
(2)实验步骤
①将浓硫酸与乙醇按体积比约3∶1混合,即将15 mL浓硫酸缓缓加入到盛有5 mL 95%乙醇的烧杯中混合均
匀,冷却后再倒入长颈圆底烧瓶中,并加入碎瓷片防止暴沸;
②加热混合溶液,迅速升温到170 ℃,将生成的气体分别通入酸性KMnO 溶液和溴的四氯化碳溶液中,观
4
察现象。
(3)实验现象
酸性KMnO 溶液、溴的四氯化碳溶液褪色。
4
(4)实验结论
乙醇在浓硫酸作用下,加热到170 ℃,发生了消去反应,生成乙烯。
分子中 b 、 d 键断裂,化学方程式为
CHCHOH―――→CH==CH ↑+HO。
3 2 2 2 2
【典例2】实验室可用加热乙醇和浓硫酸混合物至170℃时反应制取乙烯,实验室制取乙烯( )并进行
有关性质检验时,下列装置能达到相应实验目的的是A.制备 B.除去 中的 C.收集 D.吸收 尾气
【答案】B
【解析】实验室利用乙醇的消去反应制备乙烯,制备原理为CHCHOH CH=CH ↑+H O,由
3 2 2 2 2
于浓硫酸具有脱水性,可使部分乙醇脱水碳化,然后发生C+2H SO (浓) CO↑+2SO↑+2H O,即制得的乙
2 4 2 2 2
烯中混有CO、SO 气体。
2 2
A.乙醇在170℃发生消去反应产生乙烯,温度计要插入反应液,A错误;
B.SO 是酸性氧化物,能与NaOH溶液反应,可用NaOH溶液吸收SO ,B正确;
2 2
C.乙烯的相对分子质量为28,与空气平均相对分子质量29相近,不能用排空气法收集,应用排水法收
集,C错误;
D.乙烯难溶于水,不能用水吸收乙烯尾气,D错误;
选B。
三.苯、苯酚与Br 反应的比较
2
类别 苯 苯酚
溴的状态 液溴 饱和溴水
条件 催化剂 无催化剂
取代
产物
反应
特点 苯酚与溴的取代反应比苯易进行
原因 酚羟基对苯环的影响使苯环上的邻、对位氢原子变得活泼,易被取代
脂肪醇、芳香醇和酚的比较
类别 脂肪醇 芳香醇 酚
实例 CHCHOH
3 2
官能团 醇羟基(—OH) 醇羟基(—OH) 酚羟基(—OH)—OH与苯环侧链上
结构特点 —OH与链烃基相连 —OH与苯环直接相连
的碳原子相连
(1)与钠反应;(2)取代反应;(3)部分能发生 (1)弱酸性;(2)取代反应;(3)
主要化学
消去反应;(4)氧化反应;(5)酯化反应;(6) 显色反应;(4)加成反应;(5)与
性质
部分能发生加成反应 钠反应;(6)氧化反应
灼热的铜丝插入醇中,有刺激性气味物质
特性 遇FeCl 溶液发生显色反应
3
(醛或酮)生成
【典例3】绿原酸 是金银花的抗菌、抗病毒有效药理成分之一,其结构如图所示。下列说法正确的是
A.M可发生酯化、加聚、水解、氧化反应
B.M属于烃类化合物
C.M中有3种不同的官能团
D.足量的M与 溶液完全反应,可得到
【答案】A
【解析】绿原酸中含有羧基和羟基可发生酯化反应,含有碳碳双键可发生加聚反应,含有酯基可发生水解
反应,燃烧可发生氧化反应
A. 由分析,绿原酸中含有羧基和羟基、碳碳双键、酯基,M可发生酯化、加聚、水解、氧化反应,故A
正确;
B. M含有C、H、O,属于烃的衍生物,故B错误;
C. M中含有羧基和羟基、碳碳双键、酯基,有4种不同的官能团,故C错误;
D. 足量的M与 溶液完全反应,可得到标准状况下 ,故D错误;
故选A。
四.“形形色色”的酯化反应
(1)一元羧酸与二元醇或二元羧酸与一元醇的酯化反应
如:2CHCOOH+HOCH CHOHCHCOOCH CHOOCCH + 2H O。
3 2 2 3 2 2 3 2
(2)二元羧酸与二元醇的酯化反应
①形成环状酯
+ +2HO。
2
②形成高分子化合物——聚酯nHOOC—COOH+nHOCH CHOH +(2n-1)H O。
2 2 2
(3)含有羧基(—COOH)和羟基(—OH)有机物的酯化反应,如乳酸( )
①两分子酯化:
+ +2HO。
2
②羟基酸分子内脱水生成酯
+HO。
2
③羟基酸自身聚合形成高分子化合物——聚酯
+ ( n - 1)H O。
2
五.有机合成路线的设计
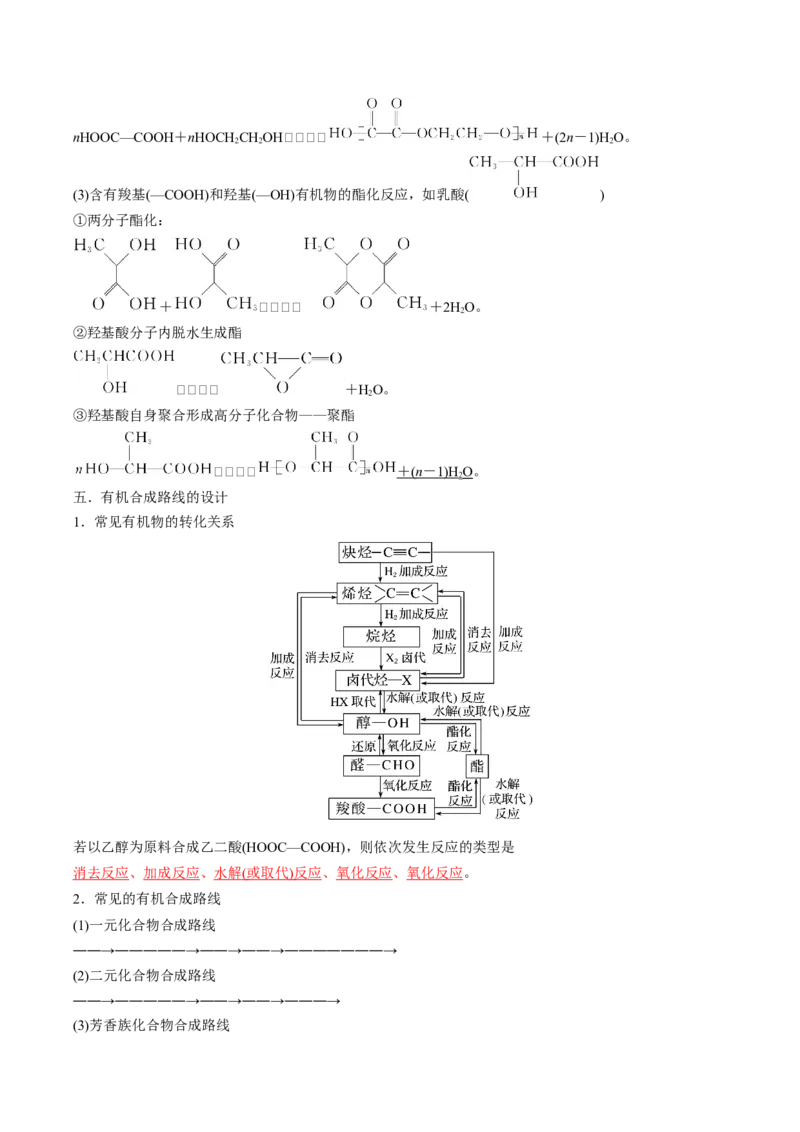
1.常见有机物的转化关系
若以乙醇为原料合成乙二酸(HOOC—COOH),则依次发生反应的类型是
消去反应、加成反应、 水解 ( 或取代 ) 反应 、氧化反应、氧化反应。
2.常见的有机合成路线
(1)一元化合物合成路线
――→―――――→――→――→―――――――→
(2)二元化合物合成路线
――→―――――→――→――→―――→
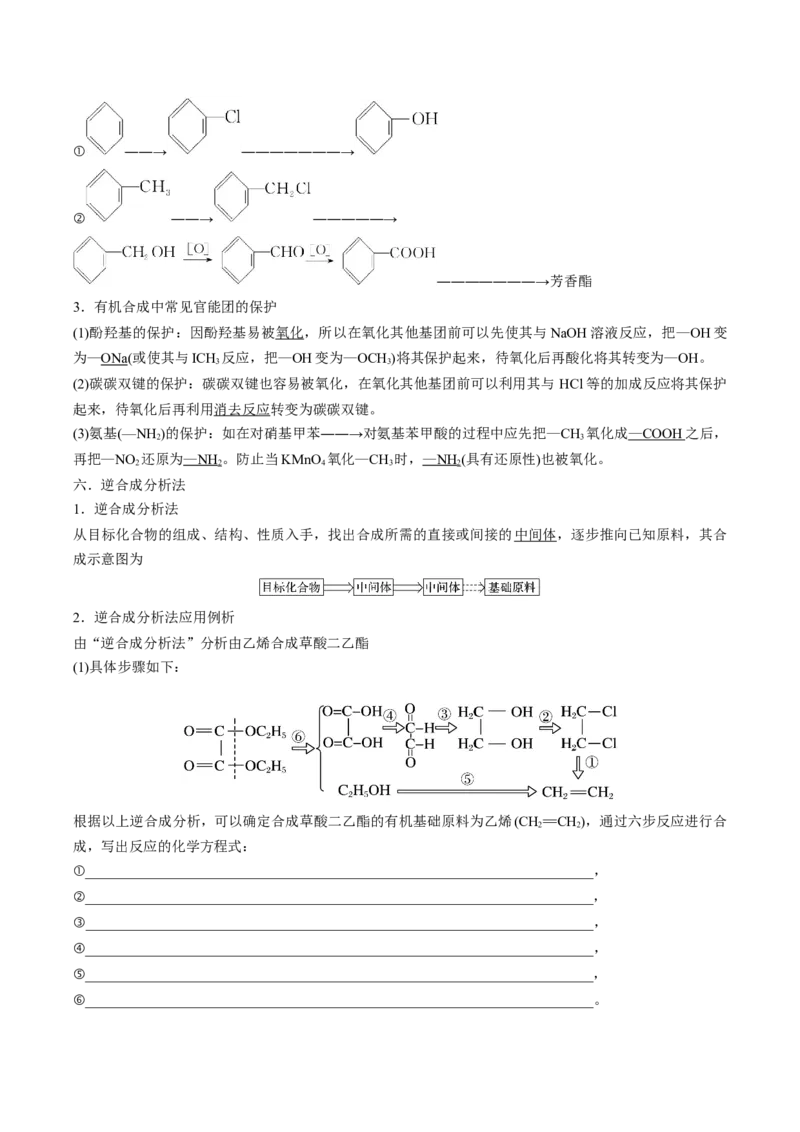
(3)芳香族化合物合成路线① ――→ ―――――――→
② ――→ ―――――→
―――――――→芳香酯
3.有机合成中常见官能团的保护
(1)酚羟基的保护:因酚羟基易被氧化,所以在氧化其他基团前可以先使其与NaOH溶液反应,把—OH变
为—ONa(或使其与ICH 反应,把—OH变为—OCH )将其保护起来,待氧化后再酸化将其转变为—OH。
3 3
(2)碳碳双键的保护:碳碳双键也容易被氧化,在氧化其他基团前可以利用其与 HCl等的加成反应将其保护
起来,待氧化后再利用消去反应转变为碳碳双键。
(3)氨基(—NH )的保护:如在对硝基甲苯――→对氨基苯甲酸的过程中应先把—CH 氧化成 — COOH 之后,
2 3
再把—NO 还原为 — NH 。防止当KMnO 氧化—CH 时, — NH (具有还原性)也被氧化。
2 2 4 3 2
六.逆合成分析法
1.逆合成分析法
从目标化合物的组成、结构、性质入手,找出合成所需的直接或间接的中间体,逐步推向已知原料,其合
成示意图为
2.逆合成分析法应用例析
由“逆合成分析法”分析由乙烯合成草酸二乙酯
(1)具体步骤如下:
根据以上逆合成分析,可以确定合成草酸二乙酯的有机基础原料为乙烯(CH==CH),通过六步反应进行合
2 2
成,写出反应的化学方程式:
①________________________________________________________________________,
②________________________________________________________________________,
③________________________________________________________________________,
④________________________________________________________________________,
⑤________________________________________________________________________,
⑥________________________________________________________________________。答案 ①CH==CH+Cl――→
2 2 2
② +2NaOH――→ +2NaCl
③
④
⑤CH==CH +HO――→CHCHOH
2 2 2 3 2
⑥ +2CHCHOH
3 2
+2HO
2
(2)根据以上逆合成分析,合成步骤如下: