文档内容
第三章 铁 金属材料
第一节 铁及其化合物
铁及其化合物,是高中阶段学习的非常典型的一种变价金属元素系列,这一部分内容和氧
化还原理论联系密切,又和好多的实验物质制备,工业产品生产相关联,所以在实验题和
化学工艺流程题中经常见到铁及其化合物的身影,为了好好掌握,还是先看看价类二维图
吧!一、 铁及其化合物的颜色
铁粉是黑色的;铁块是银白色的
Fe2+—浅绿色
Fe O—黑色晶体
3 4
Fe(OH) —白色沉淀
2
Fe3+—黄色
Fe(OH) —红褐色沉淀
3
Fe(SCN) —血红色溶液
3
FeO—黑色粉末
Fe O—红棕色粉末
2 3
FeS—黑色固体
这部分内容有时候作为基础题考察记忆颜色的准确性,更多的时候是作为一些推断题的突
破口。
对点练习1
(2020·浙江高一月考)下列关于Na、Fe及其化合物的说法不正确的是
A.Na着火时不能使用泡沫灭火器灭火
B.NaO在空气中久置变为NaCO
2 2 3
C.Fe O 常用作油漆、涂料的红色颜料
2 3
D.铁粉与水蒸气反应生成黑色的氧化亚铁
二、铁与水蒸气反应的实验探究
常温下,铁与水不反应,只有在高温条件下,Fe才会与水蒸气反应。实验时只要注意
以下细节,就能顺利完成。
a、棉花最好是一整块的,揉捏到合适大小后伸入试管底部。如果只有多块小棉花,则
必须沿试管的纵向,用较大的包裹较小的,然后再塞入。不要把小块棉花简单堆积,因热
水沸腾时会使外面的棉花冲出,一旦接触到高温铁粉,一方面使水突然剧烈沸腾,另一方
面降低了铁粉的温度,不利于反应。
b、铁粉的用量要较多,铺满中部试管为宜,略有鼓起,最好较为集中,因火焰的加热
面积有限(可观察直接加热区域与两端铁粉变化的区别)。
c、先对准铁粉加热。开始加热时估计因消耗氧气,出现受热反而倒吸的现象。解决办
法是,先让肥皂液接触一下导管口,然后让导管离开页面,才开始加热。好处是,可以看到那一小环肥皂液在导管中的上升和下降,当气压缩小,肥皂液上升,正在倒吸。一旦开
始下降,说明铁粉温度足够,开始膨胀或产生气体。这时,再把导管伸入肥皂液,若产生
气泡较慢,再多用一个酒精灯加热棉花。这时加热棉花才有意义,大量水蒸气经过前面已
加热的铁粉才会加速反应。若一开始就加热棉花,由于铁粉温度不够,反而使铁粉吸水变
湿,不利反应。关注棉花的情况,随时停止对棉花的加热,加热过久,棉花焦化,容易使
试管破裂。当产生较多气泡时,用燃着的木条点燃气泡,将会有明显的火焰。
d、实验的结束:先移开肥皂液,再停止加热,以防倒吸。
对点练习2
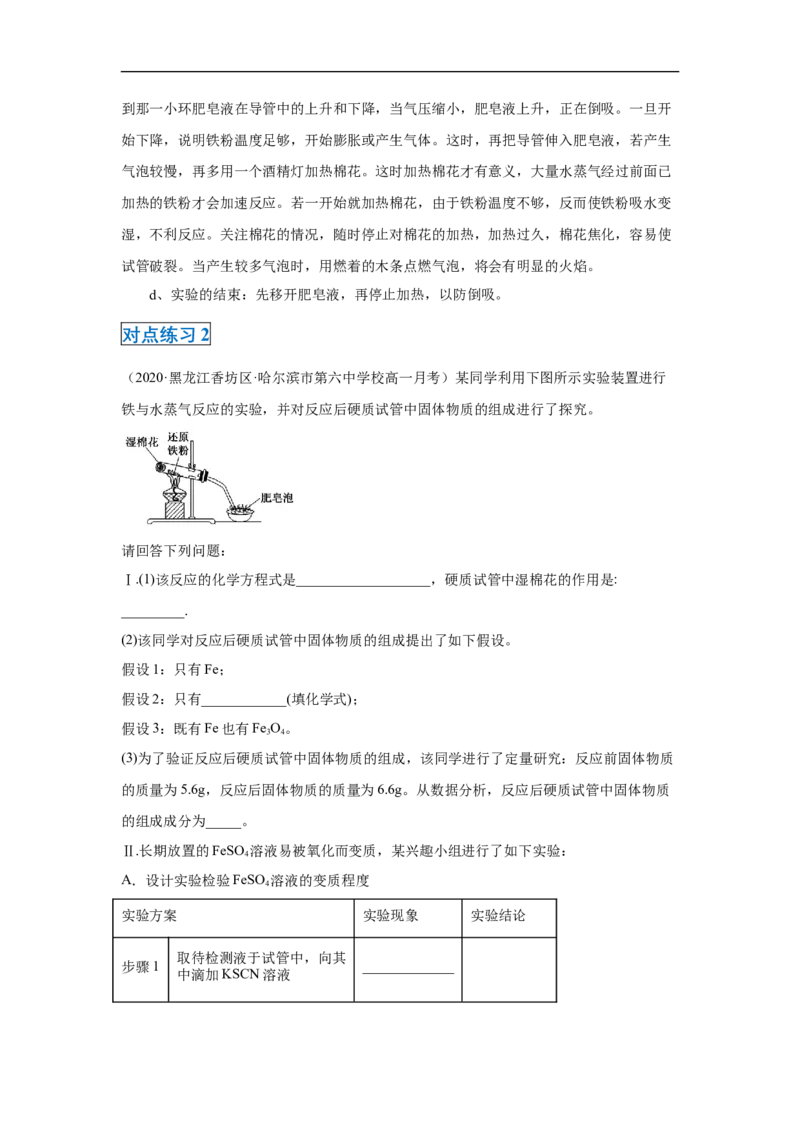
(2020·黑龙江香坊区·哈尔滨市第六中学校高一月考)某同学利用下图所示实验装置进行
铁与水蒸气反应的实验,并对反应后硬质试管中固体物质的组成进行了探究。
请回答下列问题:
Ⅰ.(1)该反应的化学方程式是___________________,硬质试管中湿棉花的作用是:
_________.
(2)该同学对反应后硬质试管中固体物质的组成提出了如下假设。
假设1:只有Fe;
假设2:只有____________(填化学式);
假设3:既有Fe也有Fe O。
3 4
(3)为了验证反应后硬质试管中固体物质的组成,该同学进行了定量研究:反应前固体物质
的质量为5.6g,反应后固体物质的质量为6.6g。从数据分析,反应后硬质试管中固体物质
的组成成分为_____。
Ⅱ.长期放置的FeSO 溶液易被氧化而变质,某兴趣小组进行了如下实验:
4
A.设计实验检验FeSO 溶液的变质程度
4
实验方案 实验现象 实验结论
取待检测液于试管中,向其
步骤1 _____________
中滴加KSCN溶液取待检测液于试管中,向其 FeSO 溶液
步骤2 ____________ 4
中滴加K[Fe(SCN) ]溶液 部分变质
3 6
①将上述方案补充完整
②步骤2涉及的离子反应方程式是______________。
③若要使变质的FeSO 复原,方法是________________。(写离子反应方程式)
4
三、铁的还原性
铁是变价金属,与强氧化剂反应生成三价铁,与弱氧化剂反应生成二价铁。
(1)铁与弱氧化剂
如:H+、Cu2+、S、I 反应时,被氧化为+2价。
2
(2)铁与HO(g)、O 反应的氧化产物为Fe O。
2 2 3 4
(3)铁与Cl、Br 等反应时,被氧化为+3价。
2 2
对点练习3
下列反应中,铁只能生成高价化合物的是
A.过量的铁与稀HNO 反应 B.铁粉与硫蒸气反应
3
C.铁粉与氯气反应 D.红热的铁粉与水蒸气反应
四、 铁的氧化物
(1)铁的氧化物中Fe的常见化合价只有+2价和+3价,Fe O 可以看成由FeO和Fe O
3 4 2 3
按物质的量之比1∶1组合而成的复杂氧化物,通常也可写成FeO·Fe O 的形式。
2 3
(2)FeO、Fe O 属于碱性氧化物,Fe O 不属于碱性氧化物。
2 3 3 4
(3)Fe O 与盐酸反应可看作Fe O、FeO分别与盐酸反应,然后把两个反应式相加。
3 4 2 3
(4)FeO、Fe O 遇氧化性酸(如HNO)发生氧化还原反应,+2价的铁均被氧化成+3价。
3 4 3
对点练习4
(2020·浙江高一期中)下列有关铁的氧化物的叙述中正确的是( )
A.铁的氧化物 FeO、Fe O、Fe O 都可由碱受热分解制得
2 3 3 4
B.铁的氧化物中 Fe O、Fe O 都有磁性
2 3 3 4
C.FeO 不稳定,在空气里受热,能迅速氧化成 Fe O
3 4
D.铁的氧化物 Fe O、Fe O 都只有氧化性
2 3 3 4
五、Fe(OH) 制备时的注意事项
2
a.原理 Fe2++2OH-===Fe(OH)2↓由于Fe(OH)2、Fe2+易被空气中的O2氧化,导致无法得到Fe(OH)2白色沉淀,故该实验
的关键之处为排出空气、隔绝空气。
b.排空、隔空常见具体措施
(1)将配制溶液的蒸馏水煮沸,驱除溶液中的氧气。
(2)将盛有NaOH溶液的胶头滴管尖端插入试管的亚铁盐溶液底部,并慢慢挤出NaOH溶液。
(3)在亚铁盐溶液上面充入保护气,如H2、N2、稀有气体等。
(4)在亚铁盐溶液上面加保护层,如苯、植物油等。
对点练习5
用下面两种方法可以制得白色 沉淀。
方法一:用 溶液与不含 的蒸馏水配制的 溶液反应制备 。
(1)除去蒸馏水中溶解的 常采用_____________________的方法。
(2)生成白色 沉淀的操作是用长滴管吸取不含 的 溶液,插入 溶
液液面以下,再挤出 溶液。这样操作的理由是______________________。
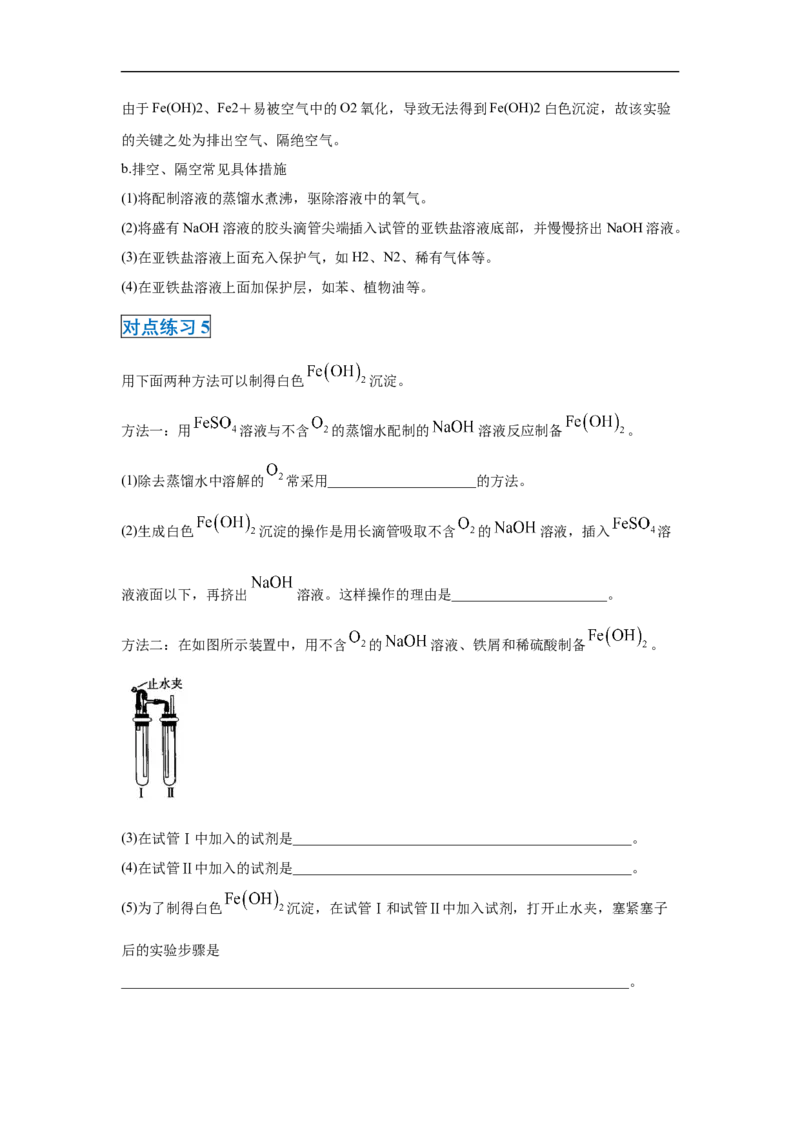
方法二:在如图所示装置中,用不含 的 溶液、铁屑和稀硫酸制备 。
(3)在试管Ⅰ中加入的试剂是________________________________________________。
(4)在试管Ⅱ中加入的试剂是________________________________________________。
(5)为了制得白色 沉淀,在试管Ⅰ和试管Ⅱ中加入试剂,打开止水夹,塞紧塞子
后的实验步骤是
________________________________________________________________________。(6)这样生成的 沉淀能较长时间保持白色,其理由是
_____________________________________________________________________。
六、检验Fe2+的注意事项
(1)只含Fe2+的溶液
检验Fe2+加入试剂的顺序:
待测液――→不变色――→ 红色(含Fe2+,不含Fe3+)。
①加KSCN溶液前,不能加氧化性物质[如HO、NO(H+)等],防止Fe2+被氧化。
2 2
②氧化剂不能选用酸性KMnO 溶液,原因有:酸性KMnO 溶液本身显紫红色,对
4 4
Fe(SCN) 红色有干扰;酸性KMnO 溶液能氧化KSCN,溶液不变红色,不能证明不含Fe2
3 4
+。
(2)同时含有Fe2+和Fe3+的溶液
Fe2+对检验Fe3+无干扰,可以滴加KSCN溶液检验Fe3+;
Fe3+对检验Fe2+有干扰,不能加KSCN溶液检验Fe2+,通常向溶液中滴加适量酸性
KMnO 溶液,溶液紫红色褪去说明含有Fe2+(当然如果含有氯离子这个方法就不行了)。
4
对点练习6
为了检验某氯化亚铁溶液是否变质,可向溶液中加入( )
A.氢氧化钠溶液 B.铁片
C.硫氰酸钾溶液 D.酸性KMnO 溶液
4
七、 Fe2+、Fe3+、Fe之间的相互转化关系
(1)Fe只具有还原性。可被弱氧化剂(H+、S等)氧化成Fe2+,被强氧化剂(Cl 等)氧化成
2
Fe3+。
(2)Fe2+既有氧化性又有还原性。可被强氧化剂[Cl 、KMnO (H+)等]氧化为Fe3+;可被
2 4
还原剂(Al、Zn、CO、C等)还原为Fe。
(3)Fe3+只具有氧化性,可被弱还原剂(Fe、Cu等)还原为Fe2+,被强还原剂(Al、Zn、
CO等)还原为Fe。
对点练习7(2020·黑龙江尖山区·双鸭山一中高一月考)下图为铁及其化合物的“价-类” 二维图。
(1)填写二维图缺失的类别①__________和化学式②__________。
(2)某同学利用以下试剂研究FeCl 性质,进行了如下预测:
3
①Cl ②Fe③NaOH④HSO ⑤AgNO
2 2 4 3
从物质类别上看,FeCl 属于__________,可能与__________发生反应(填序号);从化合
3
价角度看,Fe3+具有__________性,可能与__________发生反应(填序号)。
(3)某工厂用FeCl 溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:
3
Cu+2FeCl ==CuCl +2FeCl
3 2 2
①用双线桥表示电子转移。__________
②写出该反应的离子方程式__________。
本节跟踪练习
1.下列关于铁的氧化物说法不正确的是( )
A.铁的氧化物通常状况下都是有色固体
B.四氧化三铁是一种复杂的铁的氧化物,它与盐酸反应后的溶液中同时存在Fe2+和Fe3+
C.氧化铁是铁锈的主要成分,因此氧化铁俗称为铁锈
D.工业上常使用铁的氧化物做原料冶炼铁
2.(2019·广东湛江市·高一期末)将下列四种化合物溶于稀盐酸,滴加硫氰化钾溶液,没
有颜色变化,再加氯水即呈现红色的是( )
A.FeO B.Fe O C.Fe O D.Fe (SO )
2 3 3 4 2 4 3
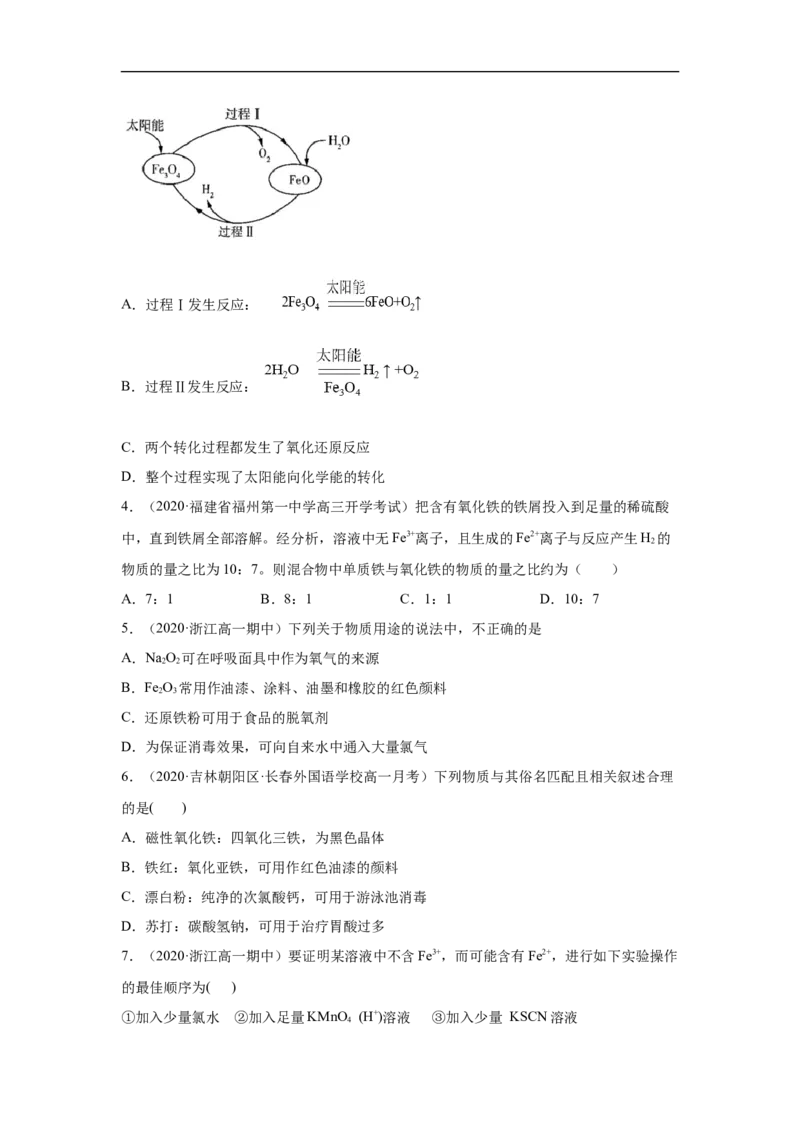
3.(2020·全国高一课时练习)纳米级 可用于以太阳能为热源分解水制 ,过程如
图所示。下列说法错误的是( )A.过程Ⅰ发生反应:
B.过程Ⅱ发生反应:
C.两个转化过程都发生了氧化还原反应
D.整个过程实现了太阳能向化学能的转化
4.(2020·福建省福州第一中学高三开学考试)把含有氧化铁的铁屑投入到足量的稀硫酸
中,直到铁屑全部溶解。经分析,溶液中无Fe3+离子,且生成的Fe2+离子与反应产生H 的
2
物质的量之比为10:7。则混合物中单质铁与氧化铁的物质的量之比约为( )
A.7:1 B.8:1 C.1:1 D.10:7
5.(2020·浙江高一期中)下列关于物质用途的说法中,不正确的是
A.NaO 可在呼吸面具中作为氧气的来源
2 2
B.Fe O 常用作油漆、涂料、油墨和橡胶的红色颜料
2 3
C.还原铁粉可用于食品的脱氧剂
D.为保证消毒效果,可向自来水中通入大量氯气
6.(2020·吉林朝阳区·长春外国语学校高一月考)下列物质与其俗名匹配且相关叙述合理
的是( )
A.磁性氧化铁:四氧化三铁,为黑色晶体
B.铁红:氧化亚铁,可用作红色油漆的颜料
C.漂白粉:纯净的次氯酸钙,可用于游泳池消毒
D.苏打:碳酸氢钠,可用于治疗胃酸过多
7.(2020·浙江高一期中)要证明某溶液中不含Fe3+,而可能含有Fe2+,进行如下实验操作
的最佳顺序为( )
①加入少量氯水 ②加入足量KMnO (H+)溶液 ③加入少量 KSCN溶液
4A.①③ B.③② C.③① D.①②③
8.(2020·宁波市北仑中学高一期中)下列实验操作和现象、结论或目的均正确的是
选项 操作和现象 结论或目的
A 将NaOH浓溶液滴加到饱和的FeCl 溶液中 制备Fe(OH) 胶体
3 3
CO还原Fe O 得到的黑色固体加入盐酸溶解后
B 3 4 黑色固体中可能有Fe O
再加入KSCN溶液,溶液不显红色 3 4
取少量FeCl 试样加水溶解,滴加高锰酸钾,紫
C 2 该FeCl 试样已经变质
红色褪去 2
向某溶液中通入Cl,然后再加入KSCN溶液变
D 2 原溶液中含有Fe2+
红色
A.A B.B C.C D.D
9.(2020·浙江高一月考)下列说法正确的是( )
A.新制氯水放在棕色广口试剂瓶中
B.溧白粉能长期放置于敞口烧杯中
C.配制FeCl 溶液时,要加入少量铁粉
2
D.可用氯气除去Fe (SO ) 溶液中少量的Fe2+
2 4 3
10.(2020·湖南省平江县第一中学高三月考)硫酸亚铁是一种重要的化工原料,可以制备
一系列物质(如图所示)。下列说法错误的是( )
A.碱式硫酸铁水解能产生Fe(OH) 胶体,可用做净水剂
3
B.为防止NH HCO 分解,生产FeCO 需在较低温度下进行
4 3 3
C.可用KSCN溶液检验(NH )Fe(SO ) 是否被氧化
4 2 4 2
D.该温度下,(NH )Fe(SO ) 在水中的溶解度比FeSO 的大
4 2 4 2 4
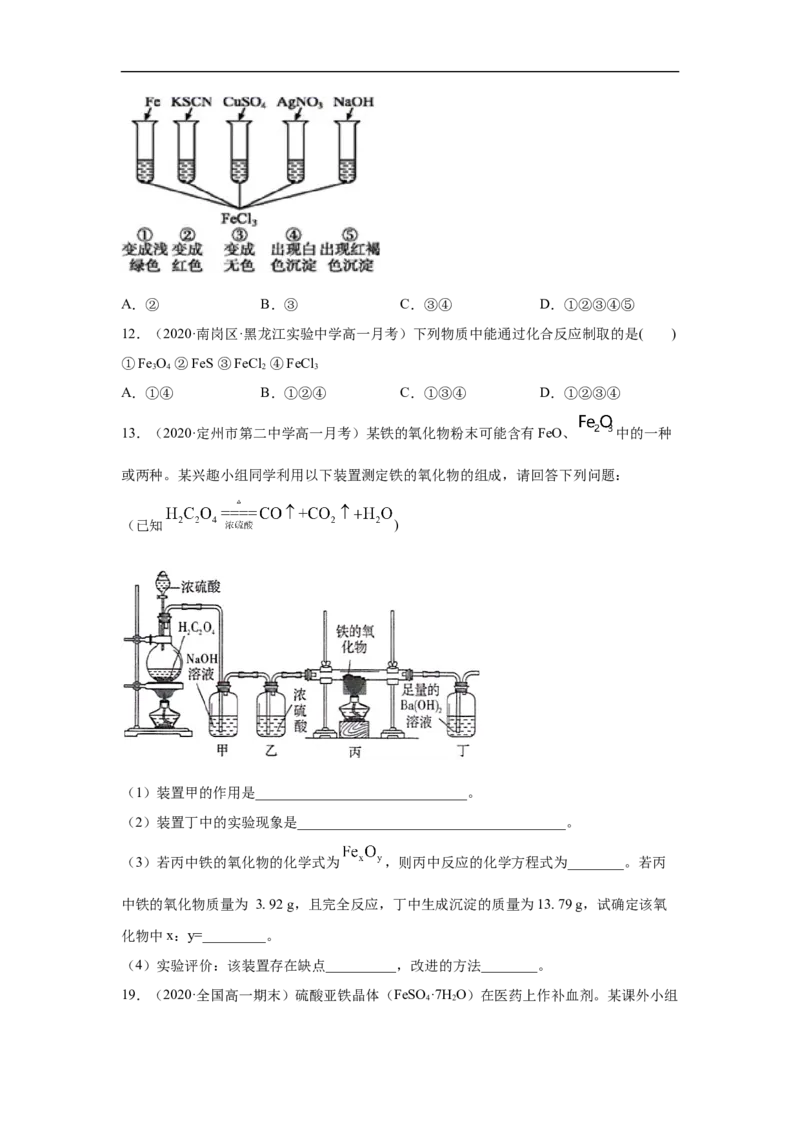
11.(2020·全国高一课时练习)为了验证Fe3+的性质,某化学兴趣小组设计了如图所示的
一组实验,其中实验方案设计错误的是( )A.② B.③ C.③④ D.①②③④⑤
12.(2020·南岗区·黑龙江实验中学高一月考)下列物质中能通过化合反应制取的是( )
①Fe O ②FeS③FeCl ④FeCl
3 4 2 3
A.①④ B.①②④ C.①③④ D.①②③④
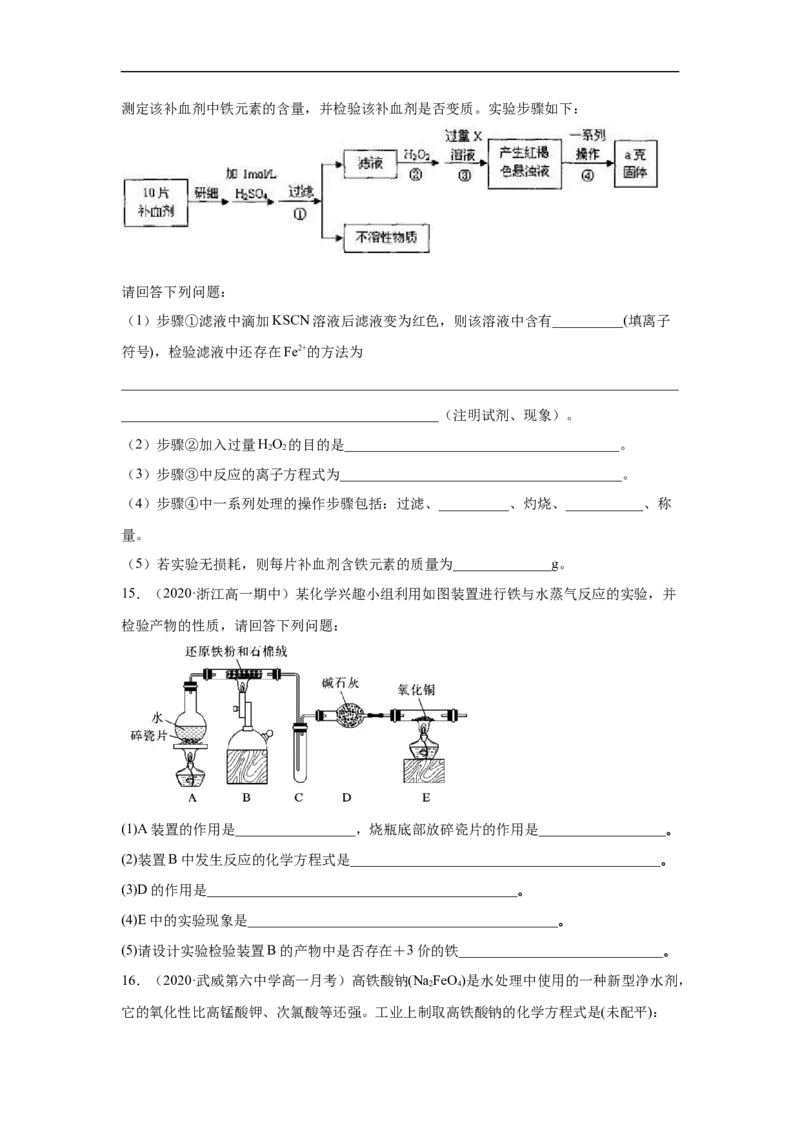
13.(2020·定州市第二中学高一月考)某铁的氧化物粉末可能含有FeO、 中的一种
或两种。某兴趣小组同学利用以下装置测定铁的氧化物的组成,请回答下列问题:
(已知 )
(1)装置甲的作用是______________________________。
(2)装置丁中的实验现象是______________________________________。
(3)若丙中铁的氧化物的化学式为 ,则丙中反应的化学方程式为________。若丙
中铁的氧化物质量为 3. 92 g,且完全反应,丁中生成沉淀的质量为13. 79 g,试确定该氧
化物中x:y=_________。
(4)实验评价:该装置存在缺点__________,改进的方法________。
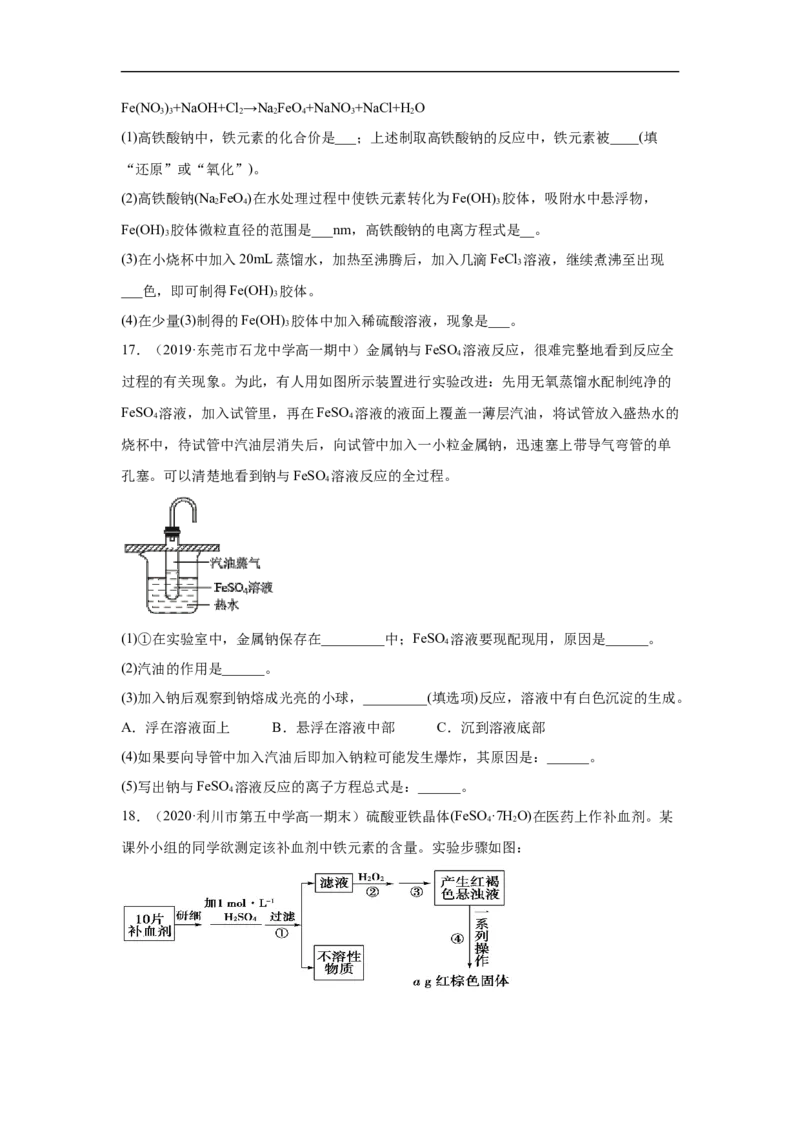
19.(2020·全国高一期末)硫酸亚铁晶体(FeSO ·7H O)在医药上作补血剂。某课外小组
4 2测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
请回答下列问题:
(1)步骤①滤液中滴加KSCN溶液后滤液变为红色,则该溶液中含有__________(填离子
符号),检验滤液中还存在Fe2+的方法为
_______________________________________________________________________________
_____________________________________________(注明试剂、现象)。
(2)步骤②加入过量HO 的目的是_______________________________________。
2 2
(3)步骤③中反应的离子方程式为________________________________________。
(4)步骤④中一系列处理的操作步骤包括:过滤、__________、灼烧、___________、称
量。
(5)若实验无损耗,则每片补血剂含铁元素的质量为______________g。
15.(2020·浙江高一期中)某化学兴趣小组利用如图装置进行铁与水蒸气反应的实验,并
检验产物的性质,请回答下列问题:
(1)A装置的作用是_________________,烧瓶底部放碎瓷片的作用是__________________。
(2)装置B中发生反应的化学方程式是____________________________________________。
(3)D的作用是____________________________________________。
(4)E中的实验现象是____________________________________________。
(5)请设计实验检验装置B的产物中是否存在+3价的铁_____________________________。
16.(2020·武威第六中学高一月考)高铁酸钠(Na FeO)是水处理中使用的一种新型净水剂,
2 4
它的氧化性比高锰酸钾、次氯酸等还强。工业上制取高铁酸钠的化学方程式是(未配平):Fe(NO )+NaOH+Cl →NaFeO+NaNO +NaCl+HO
3 3 2 2 4 3 2
(1)高铁酸钠中,铁元素的化合价是___;上述制取高铁酸钠的反应中,铁元素被____(填
“还原”或“氧化”)。
(2)高铁酸钠(Na FeO)在水处理过程中使铁元素转化为Fe(OH) 胶体,吸附水中悬浮物,
2 4 3
Fe(OH) 胶体微粒直径的范围是___nm,高铁酸钠的电离方程式是__。
3
(3)在小烧杯中加入20mL蒸馏水,加热至沸腾后,加入几滴FeCl 溶液,继续煮沸至出现
3
___色,即可制得Fe(OH) 胶体。
3
(4)在少量(3)制得的Fe(OH) 胶体中加入稀硫酸溶液,现象是___。
3
17.(2019·东莞市石龙中学高一期中)金属钠与FeSO 溶液反应,很难完整地看到反应全
4
过程的有关现象。为此,有人用如图所示装置进行实验改进:先用无氧蒸馏水配制纯净的
FeSO 溶液,加入试管里,再在FeSO 溶液的液面上覆盖一薄层汽油,将试管放入盛热水的
4 4
烧杯中,待试管中汽油层消失后,向试管中加入一小粒金属钠,迅速塞上带导气弯管的单
孔塞。可以清楚地看到钠与FeSO 溶液反应的全过程。
4
(1)①在实验室中,金属钠保存在_________中;FeSO 溶液要现配现用,原因是______。
4
(2)汽油的作用是______。
(3)加入钠后观察到钠熔成光亮的小球,_________(填选项)反应,溶液中有白色沉淀的生成。
A.浮在溶液面上 B.悬浮在溶液中部 C.沉到溶液底部
(4)如果要向导管中加入汽油后即加入钠粒可能发生爆炸,其原因是:______。
(5)写出钠与FeSO 溶液反应的离子方程总式是:______。
4
18.(2020·利川市第五中学高一期末)硫酸亚铁晶体(FeSO ·7H O)在医药上作补血剂。某
4 2
课外小组的同学欲测定该补血剂中铁元素的含量。实验步骤如图:请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是取样,先滴加KSCN溶液,再滴加___,该过程的现
象为____。
(2)步骤②加入过量HO 的目的是__________。
2 2
(3)步骤②中反应的离子方程式是___________。
(4)步骤④中一系列操作步骤:过滤、________、灼烧、________、称量。
(5)若实验中铁无损耗,则每片补血剂中含铁元素的质量为________g。(含a的表达式)