文档内容
《化学反应与能量》检测题
一、单选题
1.工业上可采用CO和H 合成甲醇,发生的反应为CO(g)+2H (g) CH OH(g) ΔH<0,若该
2 2 3
反应在绝热、恒容的密闭容器中进行,下列示意图正确且能说明反应在进行到t 时刻达到平
1
衡状态的是( )
A. B. C. D.
2.在地壳内SiO 和HF存在以下平衡:SiO (s)+4HF(g) SiF (g)+2H O(g),△H= +148.9
2 2 4 2
kJ。如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,( )
A.2v(正、HF)=v(逆、H O) B.v(H O)=2v(SiF )
2 2 4
C.SiO 的质量保持不变 D.反应物不再转化为生成物
2
3.下列能够使反应Cu+2H O=Cu(OH) +H ↑发生的是( )
2 2 2
A.用铜片作电极电解H SO 溶液 B.铜锌合金在潮湿空气中形成原电池被腐蚀
2 4
C.用铜片作电极电解NaCl溶液 D.铜片与浓硫酸加热条件下反应
4.MgCO 和CaCO 的能量关系如图所示(M=Ca、Mg):
3 3
下列说法正确的是
A.△H (CaCO )>△H (MgCO )>0
1 3 1 3
B.△H (MgCO )>△H (CaCO )>0
2 3 2 3
C.△H (CaCO )-△H (MgCO )=△H (CaO)-△H (MgO)
1 3 1 3 3 3
D.对于MgCO 和CaCO ,△H +△H >△H
3 3 1 2 3
5.下列关于原电池的叙述不正确的是( )
A.发生氧化反应的为负极,而正极为电子流入的一极
B.钢铁酸性条件下,易发生析氢腐蚀,在干燥空气里不易腐蚀
C.海水电池中,正极反应式为:O +4e-+2H O=4OH-
2 2
D.金属腐蚀普遍属于化学腐蚀,其本质是M-ne-=Mn+
6.将V mL 0.1mol·L-1的Fe (SO ) 溶液与2mL 0.1mol·L-1KI溶液混合,待充分反应后,下
1 2 4 3
列方法可证明该反应具有一定限度的是( )
A.若V <1,加入淀粉 B.若V ≤1,加入KSCN溶液
1 1C.若V ≥1,加入AgNO 溶液 D.加入Ba(NO ) 溶液
1 3 3 2
7.一种新型的乙醇电池(DEFC)是用磺酸类质子溶剂作电解质,在 200℃左右时供电( 如
下 图 所 示 ), 比 甲 醇 电 池 效 率 高 出 32 倍 , 且 比 较 安 全 。 电 池 总
反 应 为C H OH+3O ==2CO +3H O。则下列说法正确的是( )
2 5 2 2 2
A.a 极为电池的正极
B.电池正极的电极反应:O + 4H+ + 4e- = 2H O
2 2
C.电池工作时电子由 b 极沿导线经灯泡再到 a 极
D.溶液中 H+ 向 a 电极移动
8.2SO (g)+O (g) 2SO (g) △H=-198kJ/mol,在V O 存在时,该反应机理为:
2 2 3 2 5
V O +SO →2VO +SO (快); 4VO +O →2V O (慢),下列说法正确的是( )
2 5 2 2 3 2 2 2 5
A.反应速率主要取决于V O 的质量 B.VO 是该反应的催化剂
2 5 2
C.该反应逆反应的活化能大于198kJ/mol D.升高温度,该反应的△H增大
9.固态或气态碘分别与氢气反应的热化学方程式如下:
①
②
下列判断不正确的是( )
A.①中的 为固态,②中的 为气态
B.①的反应物总能量比②的反应物总能量高
C.反应①的产物与反应②的产物热稳定性相同
D.1mol 固态碘完全升华会吸热35.96kJ
10.下列各组反应(表内物质均为反应物)刚开始时,放出H 的速率最大的是 ( )
2
编号 金属(粉末状) 物质的量 酸的浓度 酸的体积 反应温度
A Fe 0.1mol 4mol/L盐酸 10mL 70℃
B Mg 0.1mol 4mol/L盐酸 10mL 40℃
C Mg 0.1mol 7mol/L硝酸 10mL 70℃
D Mg 0.1mol 4mol/L盐酸 10mL 70℃A.A B.B C.C D.D
11.下列图象能正确地表达可逆反应3A(g)+B(g) ⇌2C(g)(ΔH<0)的是 ( )
A. B.
C. D.
12.H O 溶液发生分解反应:2H O =O ↑+2H O,在其他条件都相同的情况下,下列反应温度
2 2 2 2 2 2
中氧气生成速率最大的是
A.80℃ B.60℃ C.40℃ D.20℃
二、实验题
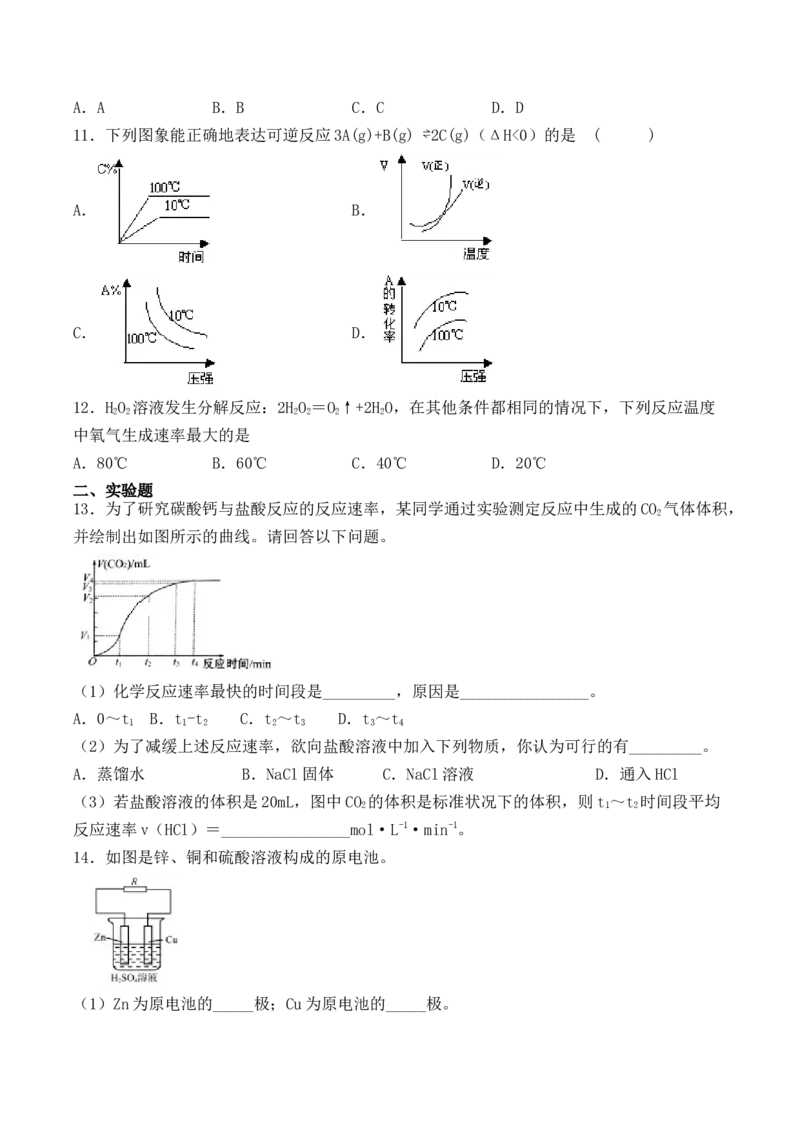
13.为了研究碳酸钙与盐酸反应的反应速率,某同学通过实验测定反应中生成的CO 气体体积,
2
并绘制出如图所示的曲线。请回答以下问题。
(1)化学反应速率最快的时间段是_________,原因是________________。
A.0~t B.t -t C.t ~t D.t ~t
1 1 2 2 3 3 4
(2)为了减缓上述反应速率,欲向盐酸溶液中加入下列物质,你认为可行的有_________。
A.蒸馏水 B.NaCl固体 C.NaCl溶液 D.通入HCl
(3)若盐酸溶液的体积是20mL,图中CO 的体积是标准状况下的体积,则t ~t 时间段平均
2 1 2
反应速率v(HCl)=________________mol·L-1·min-1。
14.如图是锌、铜和硫酸溶液构成的原电池。
(1)Zn为原电池的_____极;Cu为原电池的_____极。(2)该原电池中电子的流向为_____→R→_____。
(3)电极反应式:正极_____。负极_____。总方程式为:_____。
(4)反应一段时间后,可观察到的现象为_____。
三、推断题
15.X、Y、Z、W、Q是原子序数依次增大的短周期主族元素,X与Y位于不同周期,X与W位
于同一主族;原子最外层电子数之比N(Y):N(Q)=3:4;Z的原子序数等于Y、W、Q三种
元素原子的最外层电子数之和。请回答下列问题:
(1)Y元素在周期表中的位置是______________;QX 的电子式为_____________。
4
(2)一种名为“PowerTrekk”的新型充电器是以化合物W Q和X Z为原料设计的,这两种化
2 2
合物相遇会反应生成W QZ 和气体X ,利用气体X 组成原电池提供能量。
2 3 2 2
①写出W Q和X Z反应的化学方程式:______________。
2 2
②以稀硫酸为电解质溶液,向两极分别通入气体X 和Z 可形成原电池,其中通入气体X 的一
2 2 2
极是_______(填“正极”或“负极”)。
③若外电路有3mol电子转移,则理论上需要W Q的质量为_________。
2
16.某学生为了探究Zn与硫酸反应过程中的速率变化,在100mL稀硫酸中加入足量的Zn粒,
用排水集气法收集反应放出的H ,实验记录如下(累计值):
2
时间(min) 1 2 3 4 5
氢气体积(mL)(标况下) 50 120 232 290 310
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大________,原因是
_________。
(2)哪一时间段的反应速率最小_________,原因是____________。
(3)该同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速
率。
①硫酸铜溶液可以加快氢气生成速率的原因是____________。
②当加入的CuSO 溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降
4
的主要原因____________。
(4)要加快上述实验中气体产生的速率,还可采取的措施有________(答两种)。
17.某小组按图1所示的装置探究铁的吸氧腐蚀。(1)图2是图1所示装置的示意图,在图2的小括号内填写正极材料的化学式_________;在
方括号内用箭头表示出电子流动的方向___________。
(2)正极反应式为_____________________,负极反应式为__________________。
(3)按图1装置实验,约8 min时才看到导管中液柱上升,下列措施可以更快更清晰地观察到
液柱上升的是________。
a.用纯氧气代替具支试管内的空气
b.将食盐水浸泡过的铁钉表面撒上铁粉和碳粉的混合物
c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水
四、计算题
18.一定条件下,将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应:3A(g)
+B(g) mC(g)+2D(g),经过5 min后,反应达到平衡。此时测得,D的浓度为0.5
mol/L,c(A)∶c(B)=1∶3,C的反应速率是0.1 mol·L-1·min-1.求:
①m的值为多少?_____________
②A在5 min末的浓度。__________
③B的平衡转化率。___________
④该反应的平衡常数。___________
19.一定温度下,定容密闭容器中0.4mol/LN ,1mol/LH 进行反应:N (g)+ 3H (g)
2 2 2 2
2NH (g),10min反应达到平衡,此时测得N 浓度为0.2mol/L。
3 2
(1)10min内,用H 浓度变化来表示的反应速率为___,平衡时NH 的物质的量浓度为____;
2 3
(2)能判断该反应达到化学平衡状态的依据是____
A.容器中密度不随时间变化而变化 B.容器中各物质的浓度保持不变
C.N 和NH 的消耗速率之比为2∶1 D.N 消耗速率与H 生成速率之比为3:1
2 3 2 2
(3)平衡时N 和H 的转化率之比为____;该反应的平衡常数表达式为K=____,该温度下反
2 2
应的平衡常数是___。
参考答案
1.C2.C3.C4.D5.D6.B7.B8.C9.C10.D11.D 12.A
13.B 反应放热 AC (V -V )/[224x(t -t )]
2 1 2 1
14.负 正 Zn Cu 2H++2e-=H ↑ Zn-2e-═Zn2+ 2H++Zn=H ↑+Zn2+ 锌逐
2 2
渐溶解,铜电极上有气泡产生
15.第二周期第ⅢA族 负极 37g
16.2~3min 反应放热,加快反应速率 4~5min 硫酸的浓度减小,反应速率减慢
Zn置换出Cu,形成原电池,加快反应速率 置换出的铜太多,覆盖在锌的表面,减小了锌与稀硫酸的接触面积,使反应速率慢 升高反应的温度;适当提高硫酸的浓度;将锌粒换
成锌粉
17.C O +2H O+e-=4OH- Fe-2e-=Fe abc
2 2
18.m=2 0.25 mol·L-1 25%
19.0.06mol/( L·min) 0.4mol/L B 5:6 12.5(L/mol)2