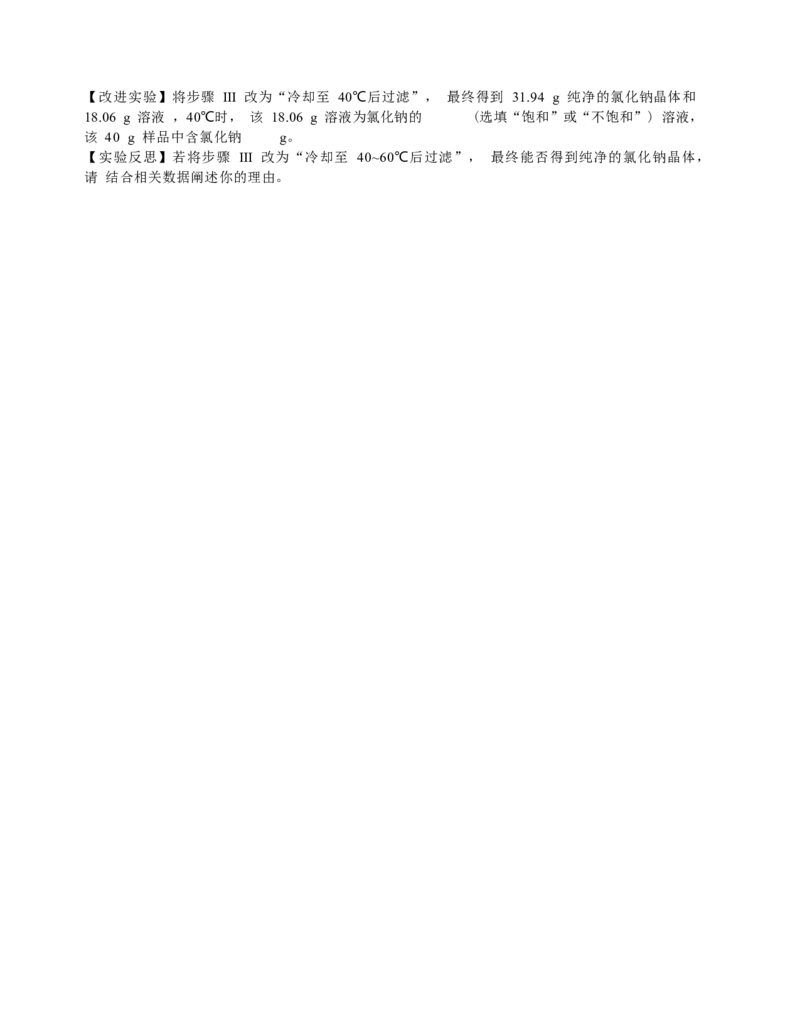文档内容
专题05 溶液与溶解度曲线
目录
【题型一】 溶液
【题型二】 溶解度曲线
题型一 溶液
一、单选题
1.(2023·上海宝山·统考二模)下列饮品属于溶液的是( )
A.可乐 B.牛奶 C.果粒橙 D.豆浆
2.(2023·上海宝山·统考二模)生活中物质的pH大于7的是
A.苏打水 B.食盐水 C.雪碧 D.食醋
3.(2023·上海松江·统考二模)在水中能形成溶液的是
A.泥沙 B.植物油 C.食盐 D.粉笔灰
4.(2023·上海浦东新区·统考二模)放入水中形成乳浊液的是
A.酒精 B.食盐 C.豆油 D.蔗糖
5.(2023·上海闵行·统考二模)加入水中能形成蓝色溶液的是
A.粉笔灰 B.食用油 C.硫酸铜 D.氯化钠
6.(2023·上海静安·统考二模)下列物质中,属于溶液的是
A.冰水 B.豆浆 C.糖水 D.牛奶
7(2023·上海静安·统考二模).一些饮品的 pH 范围如下,其中呈碱性的是
A.柠檬汁(2.0~3.0) B.咖啡(4.5~5.5)
C.西瓜汁(5.2~6.2) D.苏打水(7.7~9.0)
8.(2023·上海虹口·统考二模).放入水中能形成溶液的是( )
A.氧化铜 B.大理石 C.氢氧化铁 D.硝酸银
9. (2023·上海黄埔·统考二模)能在水中形成溶液的物质是
A. 花生油 B. 葡萄糖 C. 面粉 D. 碳酸钙10. (2023·上海黄埔·统考二模)某溶液呈棕黄色,该溶液可能是
A. 氯化铁溶液 B. 硫酸铜溶液 C. 石蕊溶液 D. 氯化钠溶液
11.(不定向) (2023·上海黄埔·统考二模) 通过以下方法,能配制得到100g、20%的氯化钠溶液的是
A. 将20g氯化钠与80mL水混合,充分搅拌
B. 将80g、25%的氯化钠溶液与20mL水充分混合
C. 将10g氯化钠加入至90g、20%的氯化钠溶液,充分搅拌
D. 将10g氯化钠加入至200g、5%的氯化钠溶液,充分搅拌后取出一半质量的溶液
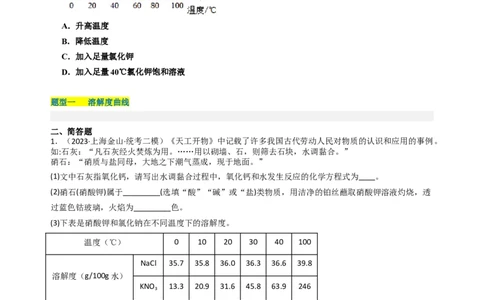
12(不定向)(2023·上海崇明·统考二模)现有t ℃时等质量的甲、乙、丙三种物质(不含结晶水)的饱和溶
2
液,将其均降温到t ℃,对所得溶液的描述正确的是
1
A.溶质质量分数:乙>甲=丙
B.溶液质量:乙>甲>丙
C.溶剂质量:丙>乙>甲
D.溶解度:乙>甲=丙
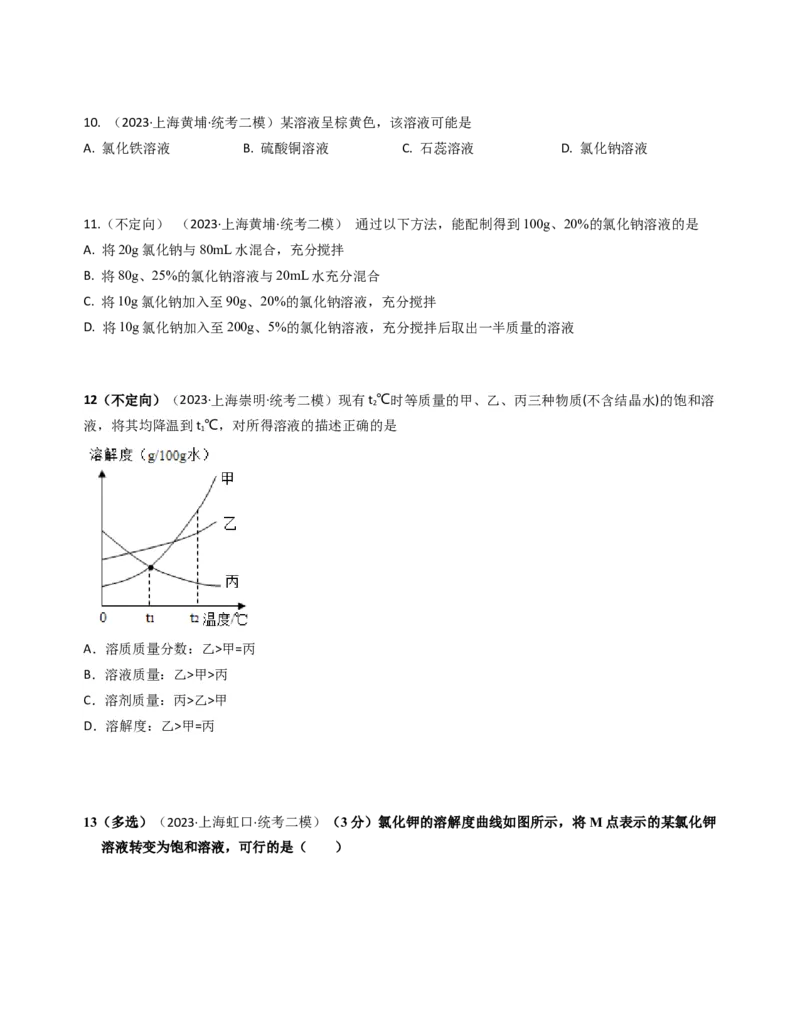
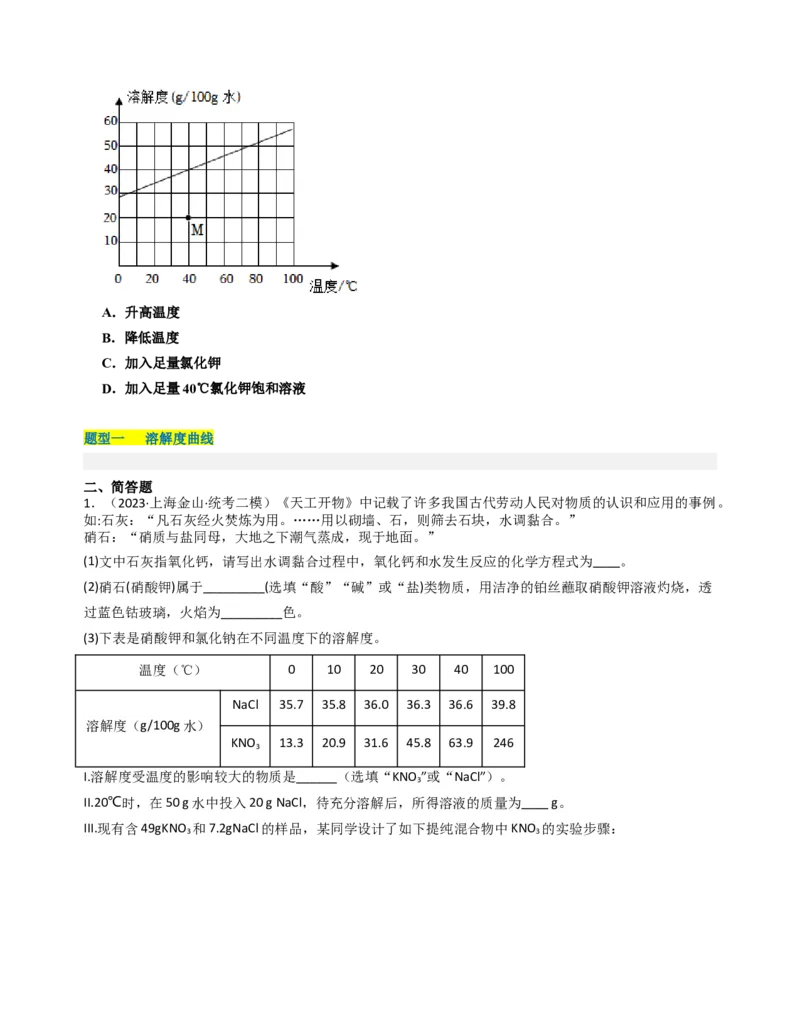
13(多选)(2023·上海虹口·统考二模)(3分)氯化钾的溶解度曲线如图所示,将M点表示的某氯化钾
溶液转变为饱和溶液,可行的是( )A.升高温度
B.降低温度
C.加入足量氯化钾
D.加入足量40℃氯化钾饱和溶液
题型一 溶解度曲线
二、简答题
1.(2023·上海金山·统考二模)《天工开物》中记载了许多我国古代劳动人民对物质的认识和应用的事例。
如:石灰:“凡石灰经火焚炼为用。……用以砌墙、石,则筛去石块,水调黏合。”
硝石:“硝质与盐同母,大地之下潮气蒸成,现于地面。”
(1)文中石灰指氧化钙,请写出水调黏合过程中,氧化钙和水发生反应的化学方程式为____。
(2)硝石(硝酸钾)属于_________(选填“酸”“碱”或“盐)类物质,用洁净的铂丝蘸取硝酸钾溶液灼烧,透
过蓝色钴玻璃,火焰为_________色。
(3)下表是硝酸钾和氯化钠在不同温度下的溶解度。
温度(℃) 0 10 20 30 40 100
NaCl 35.7 35.8 36.0 36.3 36.6 39.8
溶解度(g/100g水)
KNO 13.3 20.9 31.6 45.8 63.9 246
3
I.溶解度受温度的影响较大的物质是______(选填“KNO ”或“NaCl”)。
3
II.20℃时,在50 g水中投入20 g NaCl,待充分溶解后,所得溶液的质量为____ g。
III.现有含49gKNO 和7.2gNaCl的样品,某同学设计了如下提纯混合物中KNO 的实验步骤:
3 3i.滤液B中,KNO _______(选填“达到”或“未达到”)饱和状态。
3
ii.上述过程中采用的结晶方法是_______。
iii.步骤Ⅱ中蒸发ag水适宜的量为多少并结合相关数据说明理由。_____________
2.(2023·上海崇明·统考二模).某兴趣小组对某氯化钠样品(可能含有硝酸钾)进行实验探究。
(1)为检验氯化钠样品中是否含有硝酸钾,甲同学取少量样品进行焰色反应,透过蓝色的钴玻璃片观察,火
焰呈___________色,证明样品中含有硝酸钾。
(2)为测定样品中氯化钠的含量,乙同学称取一定质量的样品溶于足量的水,再进行如下实验。
I.加入硝酸银溶液后反应的化学方程式为___________。
II.为确定一定量样品中氯化钠的含量,还需进行的实验操作为___________。
(3)下表是硝酸钾和氯化钠的部分溶解度数据。
温度(℃) 0 20 40 60 80
氯化钠 35.7 36.0 36.6 37.3 38.4
溶解度(g/100g水)
硝酸钾 13.3 31.6 63.9 110 169
I.40℃时,氯化钠的溶解度为___________。
II.80℃时,200g硝酸钾加到100g水中,充分溶解并恢复至原温度,所得溶液中溶质的质量分数是
___________(用相应的数据列式表示,不用计算)。
III.某样品中含38.9g氯化钠、9.8g硝酸钾。20℃时,在该样品中加入110g水,充分溶解后,蒸发浓缩;
当蒸发至剩余水量为10g时,至60℃时过滤,用数据分析此过程中析出晶体的组成情况___________。
3.(2023·上海嘉定·统考二模)KCl有着广泛的用途。
(1)农业生产中KCl可用作_____(选填“钾”“氮”或“磷”)肥。
(2)对KCl溶液进行焰色反应,透过蓝色钴玻璃片,火焰呈_____色。
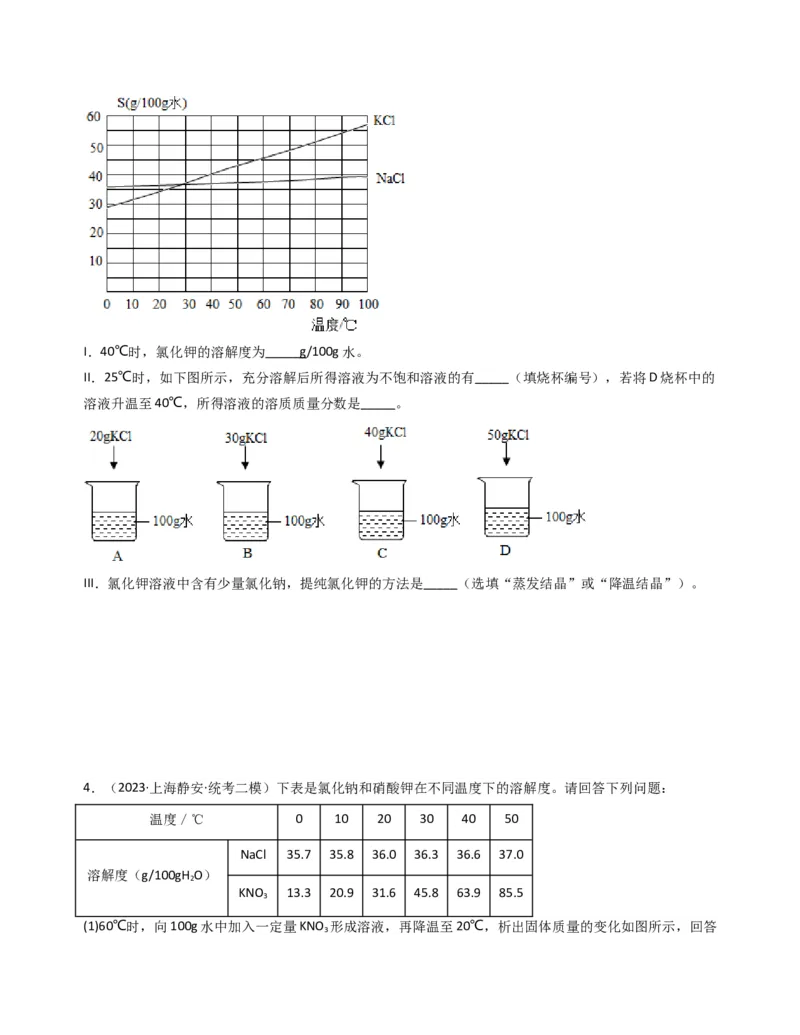
(3)海水中含有氯化钠和氯化钾等物质。根据下图的溶解度曲线回答问题。I.40℃时,氯化钾的溶解度为_____g/100g水。
II.25℃时,如下图所示,充分溶解后所得溶液为不饱和溶液的有_____(填烧杯编号),若将D烧杯中的
溶液升温至40℃,所得溶液的溶质质量分数是_____。
III.氯化钾溶液中含有少量氯化钠,提纯氯化钾的方法是_____(选填“蒸发结晶”或“降温结晶”)。
4.(2023·上海静安·统考二模)下表是氯化钠和硝酸钾在不同温度下的溶解度。请回答下列问题:
温度/℃ 0 10 20 30 40 50
NaCl 35.7 35.8 36.0 36.3 36.6 37.0
溶解度(g/100gH O)
2
KNO 13.3 20.9 31.6 45.8 63.9 85.5
3
(1)60℃时,向100g水中加入一定量KNO 形成溶液,再降温至20℃,析出固体质量的变化如图所示,回答
3下列问题。
1.20℃时KNO 溶解度为______g/100g水,该温度下,20gKNO 溶解在50g水中,所得溶液的质量为
3 3
______g。
II.60℃时加入的KNO 质量为______g,此时所得溶液为______(填“饱和”或“不饱和”)。
3
III.降温过程中,下列说法正确的是______。
A.时间0至t 过程中,溶液中溶质质量分数不变
1
B.时间t 时,溶液为20℃时KNO 溶解度的饱和溶液
1 3
C.时间t 至t 过程中,硝酸钾的溶解度逐渐变小
1 2
(2)50℃时,将80.0g一定质量分数的氯化钠溶液恒温蒸发,溶液的质量随蒸发水的质量变化关系如图所示,
则a点溶液中溶质的质量为______g。
(3)除去硝酸钾中含有的少量氯化钠,采用的方法是______。
5.(2023·上海闵行·统考二模)氯化钠和硝酸钾在不同温度时的溶解度见下表:
温度(℃) 20 30 40 60 80 100
氯化钠 36.0 36.3 36.6 37.3 38.4 39.8
溶解度(g/100g水)
硝酸钾 31.6 45.8 63.9 110 169 246
(1)40℃时,氯化钠的溶解度是_______g。
(2)两物质中溶解度受温度影响较大的是_______。
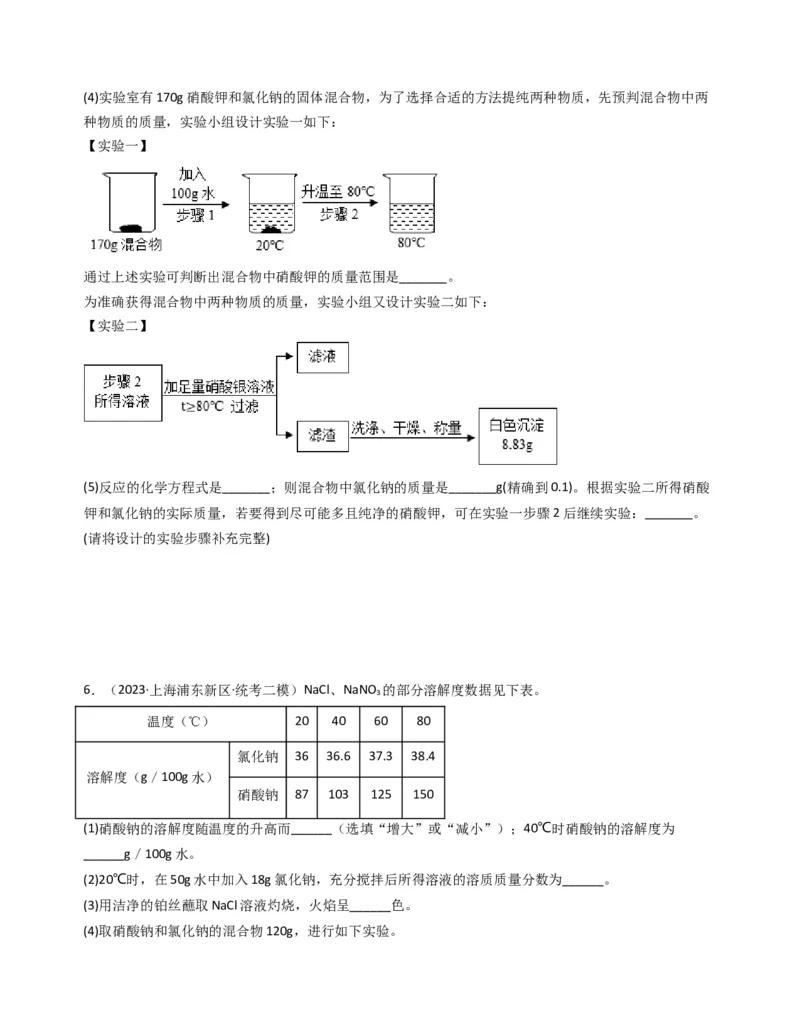
(3)60℃时,100g硝酸钾饱和溶液中溶质与溶剂的质量比是_______。(4)实验室有170g硝酸钾和氯化钠的固体混合物,为了选择合适的方法提纯两种物质,先预判混合物中两
种物质的质量,实验小组设计实验一如下:
【实验一】
通过上述实验可判断出混合物中硝酸钾的质量范围是_______。
为准确获得混合物中两种物质的质量,实验小组又设计实验二如下:
【实验二】
(5)反应的化学方程式是_______;则混合物中氯化钠的质量是_______g(精确到0.1)。根据实验二所得硝酸
钾和氯化钠的实际质量,若要得到尽可能多且纯净的硝酸钾,可在实验一步骤2后继续实验:_______。
(请将设计的实验步骤补充完整)
6.(2023·上海浦东新区·统考二模)NaCl、NaNO 的部分溶解度数据见下表。
3
温度(℃) 20 40 60 80
氯化钠 36 36.6 37.3 38.4
溶解度(g/100g水)
硝酸钠 87 103 125 150
(1)硝酸钠的溶解度随温度的升高而______(选填“增大”或“减小”);40℃时硝酸钠的溶解度为
______g/100g水。
(2)20℃时,在50g水中加入18g氯化钠,充分搅拌后所得溶液的溶质质量分数为______。
(3)用洁净的铂丝蘸取NaCl溶液灼烧,火焰呈______色。
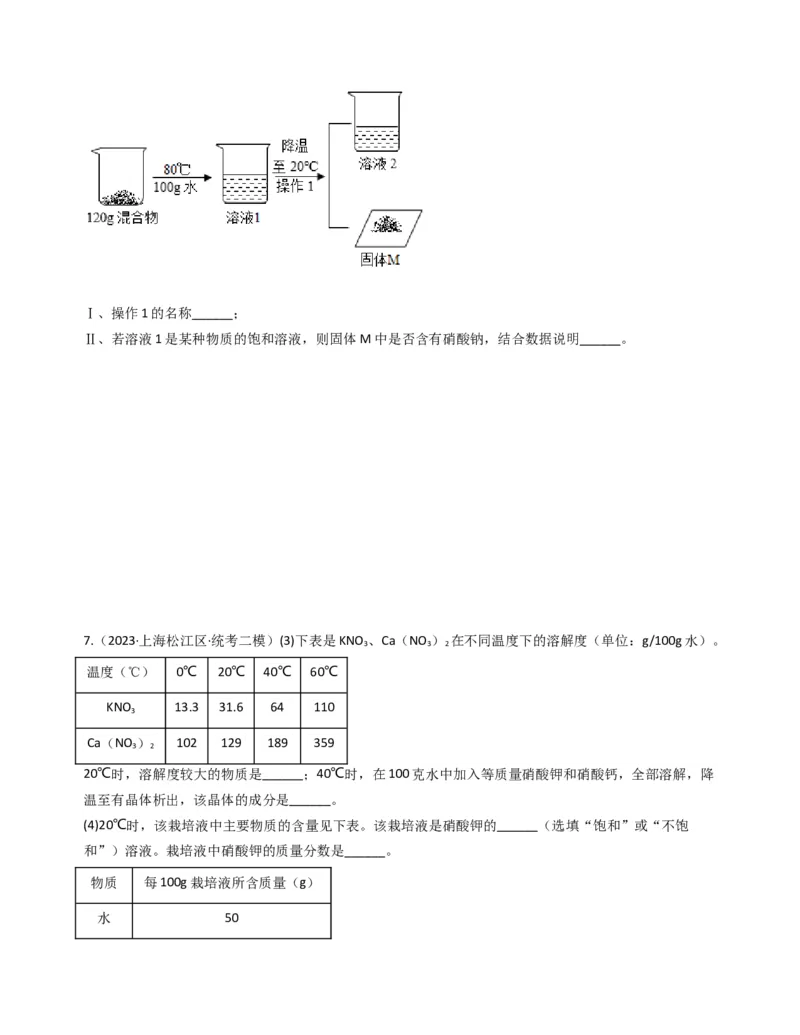
(4)取硝酸钠和氯化钠的混合物120g,进行如下实验。Ⅰ、操作1的名称______;
Ⅱ、若溶液1是某种物质的饱和溶液,则固体M中是否含有硝酸钠,结合数据说明______。
7.(2023·上海松江区·统考二模)(3)下表是KNO 、Ca(NO ) 在不同温度下的溶解度(单位:g/100g水)。
3 3 2
温度(℃) 0℃ 20℃ 40℃ 60℃
KNO 13.3 31.6 64 110
3
Ca(NO ) 102 129 189 359
3 2
20℃时,溶解度较大的物质是______;40℃时,在100克水中加入等质量硝酸钾和硝酸钙,全部溶解,降
温至有晶体析出,该晶体的成分是______。
(4)20℃时,该栽培液中主要物质的含量见下表。该栽培液是硝酸钾的______(选填“饱和”或“不饱
和”)溶液。栽培液中硝酸钾的质量分数是______。
物质 每100g栽培液所含质量(g)
水 50硝酸钾 10
硝酸钙 30
8(2023·上海徐汇区·统考二模)在NaCl中添加一定量的KCl可制成“低钠盐”供某些疾病的患者食用。
(1)用洁净的铂丝蘸取NaCl溶液灼烧,火焰呈__________色。
(2)NaCl和KCl的溶解度数据如下表示所示。80℃时,KCl的溶解度为__________g/100g水。若KCl中混有少
量NaCl,可依次通过溶解、蒸发浓缩、__________,过滤等操作提纯KCl。
溶解度(g/100g水)
温度(℃) 0 20 60 80
NaCl 35.7 36 37.3 38.4
KCl 28 34.2 45.8 51.3
(3)有一包由NaCl和KCl混合成的样品,称取50g该样品进行如下实验(忽略物质的损耗)①溶液B中NaCl的质量为_________g。
②溶液A中KCl__________(选填“达到”或“未达到”)饱和状态。
③该样品中KCl的质量分数为__________。
④另有一包由NaCl和KCl混合成的样品,其中KCl的质量分数介于30%~40%之间,称取50g该样品,重
复上述实验中步骤i和步骤ii,能否测出KCl的质量分数?为什么?__________。
9.(2023·上海杨浦区·统考二模)下表是KNO 、NaC1在不同温度下的溶解度(单位:g)
3
温度(℃) 0 10 20 40 50 60 70 80 90 100
KNO 13.3 20.9 32 64 85.5 110 138 169 202 246
3
NaCl 35.7 35.8 36 36.6 37 37.3 37.8 38.4 39 39.8
(1)60℃时,50g水中溶解32g硝酸钾形成不饱和溶液,欲使该溶液恰好达到饱和,可以恒温蒸发水的质量
______g(精确到1g);当其它条件不变时,也可以降温到_____℃恰好饱和。
(2)KNO 溶液中含有少量NaCl时,可通过_____方法提纯。析出的晶体和剩余溶液描述正确的是______(填
3
写编号)。
A.剩余溶液一定是当时KNO 的饱和溶液
3
B.剩余溶液一定是当时NaCl的不饱和溶液C.上述方法无法将两者完全分离
D.析出的晶体中一定不含有NaCl
(3)t℃时,将一定量KNO 的不饱和溶液平均分为三份,分别恒温蒸发出水的质量为5g、10g、15g,析出
3
KNO 晶体的质量依次为ag、bg、cg,则a、b、c三者的关系为_____。
3
A.c=a+b B.c=2b-a C.c=a+2b D.c=2a-b
10(2023·上海黄埔区·统考二模) 氯化钾在工业、农业等方面有着重要的作用。
(1)验证性质
取氯化钾溶液进行焰色反应,透过蓝色钴玻璃片,火焰呈______色;在氯化钾溶液中滴加硝酸银溶液,反
应的化学方程式是______。
(2)粗制氯化钾
氯化钾、氯化钠部分溶解度数据(g/100g水)
氯化钾、氯化钠部分溶解度数据(g/100g水)
温度(℃) 20 40 80 100
氯化钾 34.2 40.1 51.3 56.3
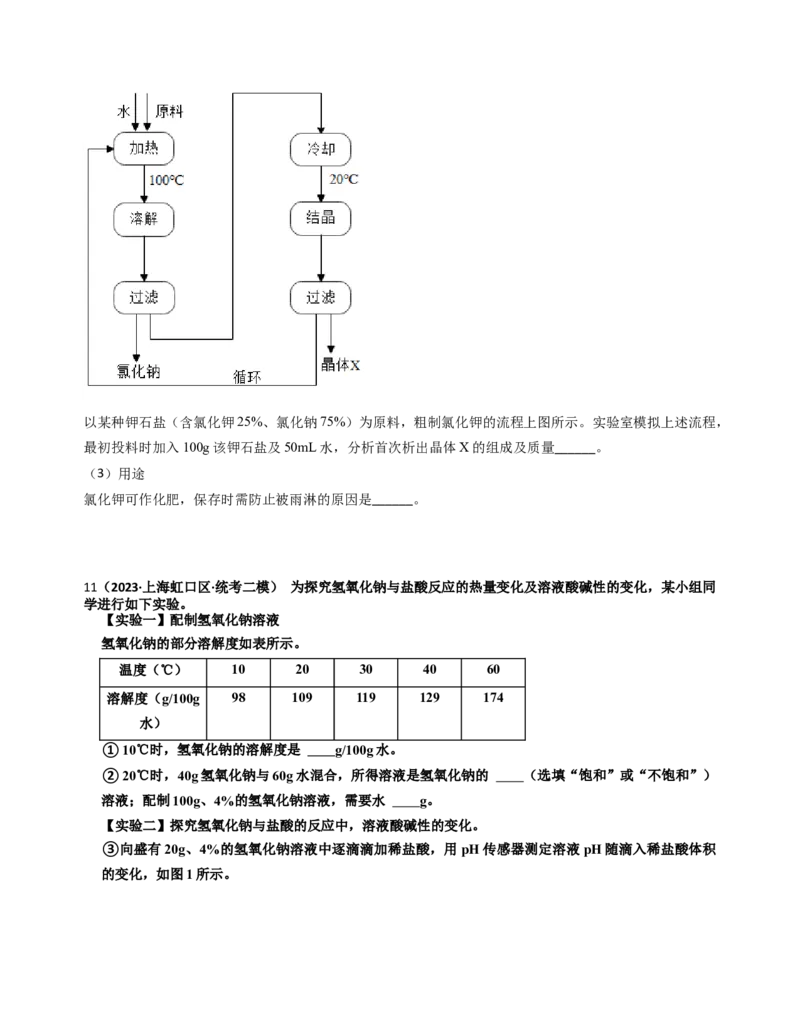
氯化钠 35.9 36.4 38.0 39.2以某种钾石盐(含氯化钾25%、氯化钠75%)为原料,粗制氯化钾的流程上图所示。实验室模拟上述流程,
最初投料时加入100g该钾石盐及50mL水,分析首次析出晶体X的组成及质量______。
(3)用途
氯化钾可作化肥,保存时需防止被雨淋的原因是______。
11(2023·上海虹口区·统考二模) 为探究氢氧化钠与盐酸反应的热量变化及溶液酸碱性的变化,某小组同
学进行如下实验。
【实验一】配制氢氧化钠溶液
氢氧化钠的部分溶解度如表所示。
温度(℃) 10 20 30 40 60
溶解度(g/100g 98 109 119 129 174
水)
①10℃时,氢氧化钠的溶解度是 g/100g水。
②20℃时,40g氢氧化钠与60g水混合,所得溶液是氢氧化钠的 (选填“饱和”或“不饱和”)
溶液;配制100g、4%的氢氧化钠溶液,需要水 g。
【实验二】探究氢氧化钠与盐酸的反应中,溶液酸碱性的变化。
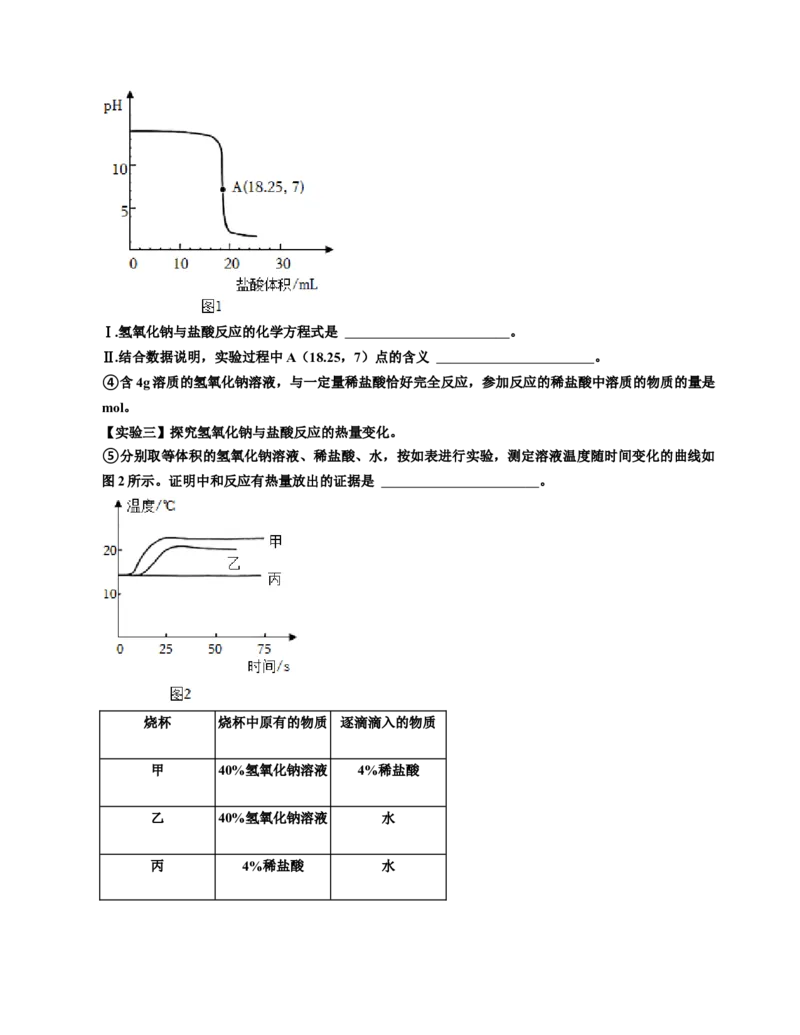
③向盛有20g、4%的氢氧化钠溶液中逐滴滴加稀盐酸,用pH传感器测定溶液pH随滴入稀盐酸体积
的变化,如图1所示。Ⅰ.氢氧化钠与盐酸反应的化学方程式是 。
Ⅱ.结合数据说明,实验过程中A(18.25,7)点的含义 。
④含4g溶质的氢氧化钠溶液,与一定量稀盐酸恰好完全反应,参加反应的稀盐酸中溶质的物质的量是
mol。
【实验三】探究氢氧化钠与盐酸反应的热量变化。
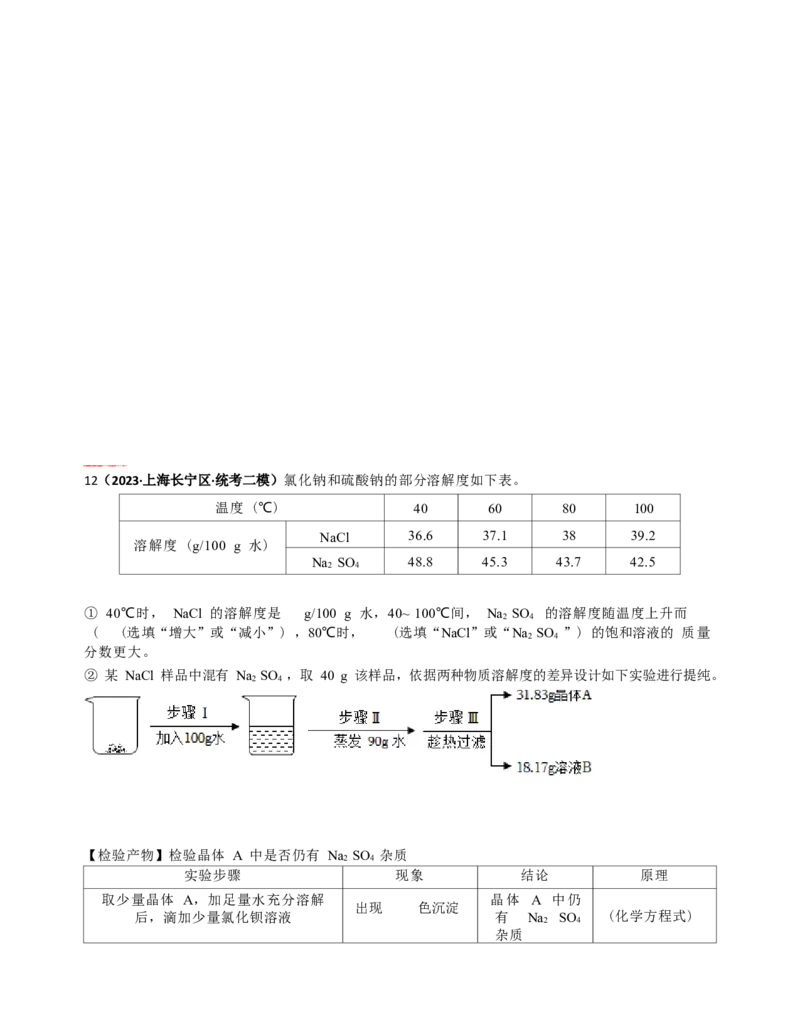
⑤分别取等体积的氢氧化钠溶液、稀盐酸、水,按如表进行实验,测定溶液温度随时间变化的曲线如
图2所示。证明中和反应有热量放出的证据是 。
烧杯 烧杯中原有的物质 逐滴滴入的物质
甲 40%氢氧化钠溶液 4%稀盐酸
乙 40%氢氧化钠溶液 水
丙 4%稀盐酸 水声明:试题解析著作权属所有,未经书面同意,不得复制发布日期:2023/5/16 14:35:06;用户:天空之城;邮箱:2230668592@qq.com;学号:20667957
12(2023·上海长宁区·统考二模)氯化钠和硫酸钠的部分溶解度如下表。
温度 (℃) 40 60 80 100
NaCl 36.6 37.1 38 39.2
溶解度 (g/100 g 水)
Na SO 48.8 45.3 43.7 42.5
2 4
① 40℃时, NaCl 的溶解度是 g/100 g 水,40~ 100℃间, Na SO 的溶解度随温度上升而
2 4
( (选填“增大”或“减小”) ,80℃时, (选填“NaCl”或“Na SO ”) 的饱和溶液的 质量
2 4
分数更大。
② 某 NaCl 样品中混有 Na SO ,取 40 g 该样品,依据两种物质溶解度的差异设计如下实验进行提纯。
2 4
【检验产物】检验晶体 A 中是否仍有 Na SO 杂质
2 4
实验步骤 现象 结论 原理
取少量晶体 A,加足量水充分溶解 晶体 A 中仍
出现 色沉淀
后,滴加少量氯化钡溶液 有 Na SO (化学方程式)
2 4
杂质【改进实验】将步骤 III 改为“冷却至 40℃后过滤”, 最终得到 31.94 g 纯净的氯化钠晶体和
18.06 g 溶液 ,40℃时, 该 18.06 g 溶液为氯化钠的 (选填“饱和”或“不饱和”) 溶液,
该 40 g 样品中含氯化钠 g。
【实验反思】若将步骤 III 改为“冷却至 40~60℃后过滤”, 最终能否得到纯净的氯化钠晶体,
请 结合相关数据阐述你的理由。