文档内容
专题05 溶液与溶解度曲线
目录
【题型一】 溶液
【题型二】 溶解度曲线
题型一 溶液
一、单选题
1.(2023·上海宝山·统考二模)下列饮品属于溶液的是( )
A.可乐 B.牛奶 C.果粒橙 D.豆浆
【答案】A
【分析】溶液是均一的、稳定的混合物。根据溶液的特征进行分析。
【详解】A、可乐是均一的、稳定的混合物,是溶液,符合题意;
B、牛奶是小液滴分散形成不均一、不稳定的混合物,不是溶液,不符合题意;
C、果粒橙有不溶性果肉成分,不是均一的、稳定的混合物,不是溶液,不符合题意;
D、豆浆不是均一的稳定的混合物,不是溶液,不符合题意。
故选A。
2.(2023·上海宝山·统考二模)生活中物质的pH大于7的是
A.苏打水 B.食盐水 C.雪碧 D.食醋
【答案】A
【详解】A、苏打水含有碳酸钠,显碱性,pH>7;
B、食盐水显中性,pH=7;
C、雪碧中含有碳酸,显酸性,pH<7;
D、食醋中含有醋酸,显酸性,pH<7;
答案:A。
3.(2023·上海松江·统考二模)在水中能形成溶液的是
A.泥沙 B.植物油 C.食盐 D.粉笔灰
【答案】C
【详解】A、泥沙不溶于水,不能和水形成均一、稳定的混合物,即不能够形成溶液,错误;
B、植物油不溶于水,不能和水形成均一、稳定的混合物,即不能够形成溶液,形成的是乳浊液,错误;
C、食盐可溶于水形成均一、稳定的混合物,属于溶液,正确;
D、粉笔灰不溶于水,不能和水形成均一、稳定的混合物,即不能够形成溶液,形成的是悬浊液,错误。
故选C。4.(2023·上海浦东新区·统考二模)放入水中形成乳浊液的是
A.酒精 B.食盐 C.豆油 D.蔗糖
【答案】C
【详解】A、酒精易溶于水,形成均一、稳定的混合物,属于溶液,不符合题意;
B、食盐易溶于水,形成均一、稳定的混合物,属于溶液,不符合题意;
C、豆油不溶于水,把豆油放到水里是液滴分散到液体中形成的混合物,属于乳浊液,符合题意;
D、蔗糖易溶于水,形成均一、稳定的混合物,属于溶液,不符合题意。
故选C。
5.(2023·上海闵行·统考二模)加入水中能形成蓝色溶液的是
A.粉笔灰 B.食用油 C.硫酸铜 D.氯化钠
【答案】C
【详解】A、粉笔灰不溶于水,与水混合生成的是悬浊液,不符合题意;
B、食用油不溶于水,与水混合形成的是乳浊液,不符合题意;
C、硫酸铜溶于水形成的是蓝色溶液,符合题意;
D、氯化钠溶于水形成的是无色溶液,不符合题意;
故选C。
6.(2023·上海静安·统考二模)下列物质中,属于溶液的是
A.冰水 B.豆浆 C.糖水 D.牛奶
【答案】C
【详解】A、冰水由一种物质组成,属于纯净物,溶液必须是混合物,故错误;
B、豆浆不均一、不稳定属于悬浊液,故错误;
C、糖水是均一、稳定的混合物,属于溶液,故正确;
D、牛奶属于乳浊液,不均一、不稳定,故错误。
故选C。
7(2023·上海静安·统考二模).一些饮品的 pH 范围如下,其中呈碱性的是
A.柠檬汁(2.0~3.0) B.咖啡(4.5~5.5)
C.西瓜汁(5.2~6.2) D.苏打水(7.7~9.0)
【答案】D
【详解】A、柠檬汁:2.0~3.0,pH<7,呈酸性,故选项不符合题意;
B、咖啡:4.5~5.5,pH<7,呈酸性,故选项不符合题意;
C、西瓜汁:5.2~6.2,pH<7,呈酸性,故选项不符合题意;
D、苏打水:7.7~9.0,pH>7,呈碱性,故选项符合题意。
故选D。【点睛】酸性溶液pH小于7,中性溶液pH等于7,碱性溶液pH大于7。
8.(2023·上海虹口·统考二模).放入水中能形成溶液的是( )
A.氧化铜 B.大理石 C.氢氧化铁 D.硝酸银
【答案】D
【解答】解:A、氧化铜不溶于水,与水混合形成不均一、不稳定的悬浊液,故A错;
B、大理石不溶于水,与水混合形成不均一、不稳定的悬浊液,故B错;
C、氢氧化铁不溶于水,与水混合形成不均一、不稳定的悬浊液,故C错;
D、硝酸银易溶于水,形成均一、稳定的混合物,属于溶液,故D正确。
故选:D。
9. (2023·上海黄埔·统考二模)能在水中形成溶液的物质是
A. 花生油 B. 葡萄糖 C. 面粉 D. 碳酸钙
【答案】B
【解析】
【详解】A、花生油不溶于水,无法形成溶液;
B、葡萄糖溶于水,形成均一稳定的混合物,能形成溶液;
C、面粉不溶于水,无法形成溶液;
D、碳酸钙不溶于水,无法形成溶液;
故选B。
10. (2023·上海黄埔·统考二模)某溶液呈棕黄色,该溶液可能是
A. 氯化铁溶液 B. 硫酸铜溶液 C. 石蕊溶液 D. 氯化钠溶液
【答案】A
【解析】
【详解】A.含Fe3+的盐溶液呈棕黄色,某溶液呈棕黄色,该溶液可能是氯化铁溶液,故A正确;
B.硫酸铜溶液呈蓝色,故B错误;
C.石蕊溶液呈紫色,故C错误;
D.氯化钠溶液为无色溶液,故D错误。
故选:A。
11. (不定向)(2023·上海黄埔·统考二模) 通过以下方法,能配制得到100g、20%的氯化钠溶液的是
A. 将20g氯化钠与80mL水混合,充分搅拌
B. 将80g、25%的氯化钠溶液与20mL水充分混合
C. 将10g氯化钠加入至90g、20%的氯化钠溶液,充分搅拌
D. 将10g氯化钠加入至200g、5%的氯化钠溶液,充分搅拌后取出一半质量的溶液【答案】AB
【解析】
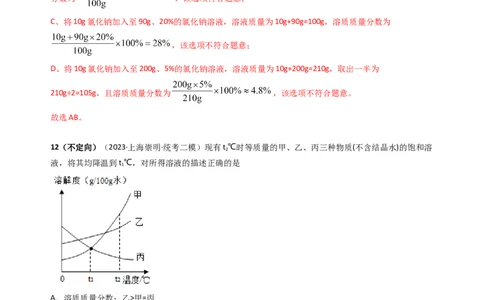
【详解】A、80mL水的质量为80mL×1g/cm3=80g,则将20g氯化钠与80mL水混合,所得溶液质量为
100g,质量分数为 ,该选项符合题意;
B、稀释前后溶质质量不变,将80g、25%的氯化钠溶液与20mL水充分混合,所得溶液质量为100g,质量
分数为 ,该选项符合题意;
C、将10g氯化钠加入至90g、20%的氯化钠溶液,溶液质量为10g+90g=100g,溶质质量分数为
,该选项不符合题意;
D、将10g氯化钠加入至200g、5%的氯化钠溶液,溶液质量为10g+200g=210g,取出一半为
210g÷2=105g,且溶质质量分数为 ,该选项不符合题意。
故选AB。
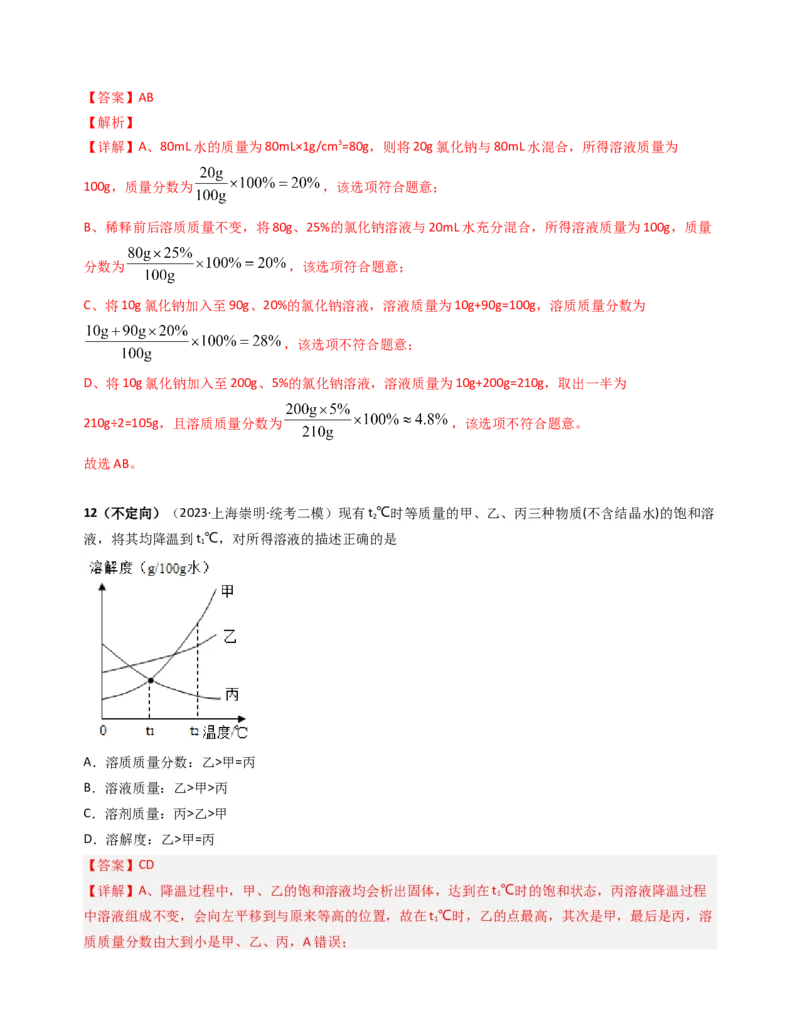
12(不定向)(2023·上海崇明·统考二模)现有t ℃时等质量的甲、乙、丙三种物质(不含结晶水)的饱和溶
2
液,将其均降温到t ℃,对所得溶液的描述正确的是
1
A.溶质质量分数:乙>甲=丙
B.溶液质量:乙>甲>丙
C.溶剂质量:丙>乙>甲
D.溶解度:乙>甲=丙
【答案】CD
【详解】A、降温过程中,甲、乙的饱和溶液均会析出固体,达到在t ℃时的饱和状态,丙溶液降温过程
1
中溶液组成不变,会向左平移到与原来等高的位置,故在t ℃时,乙的点最高,其次是甲,最后是丙,溶
1
质质量分数由大到小是甲、乙、丙,A错误;B、原三种溶液质量相等,丙未析出固体,甲析出固体较多,乙析出固体较少,溶液质量由大到小是丙、
乙、甲,B错误;
C、溶剂的质量在降温过程中不变,三种等质量的溶液在t ℃时溶质质量分数最大的溶剂质量最小,溶剂
2
最小的是甲,其次是乙,最多的是丙,溶剂质量由大到小的顺序是丙>乙>甲,C正确;
D、溶解度大小与物质是否达到饱和状态无关,图中可知,t ℃时溶解度由大到小的顺序是乙>甲=丙,D正
1
确。
故选:CD。
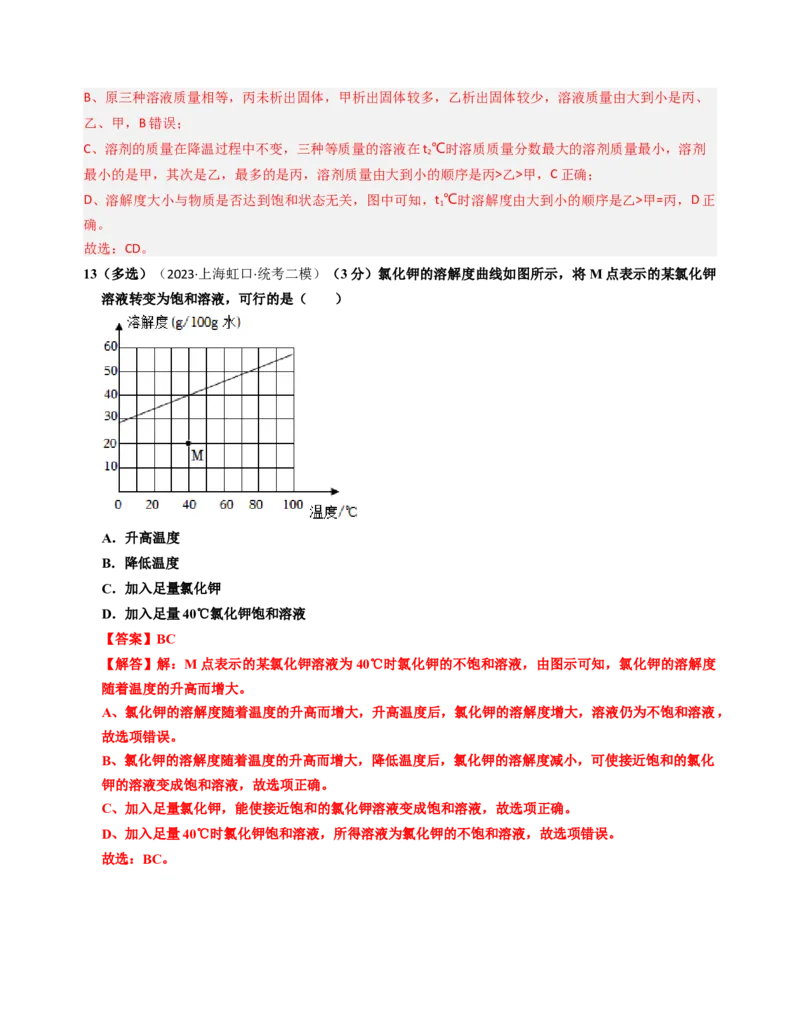
13(多选)(2023·上海虹口·统考二模)(3分)氯化钾的溶解度曲线如图所示,将M点表示的某氯化钾
溶液转变为饱和溶液,可行的是( )
A.升高温度
B.降低温度
C.加入足量氯化钾
D.加入足量40℃氯化钾饱和溶液
【答案】BC
【解答】解:M点表示的某氯化钾溶液为40℃时氯化钾的不饱和溶液,由图示可知,氯化钾的溶解度
随着温度的升高而增大。
A、氯化钾的溶解度随着温度的升高而增大,升高温度后,氯化钾的溶解度增大,溶液仍为不饱和溶液,
故选项错误。
B、氯化钾的溶解度随着温度的升高而增大,降低温度后,氯化钾的溶解度减小,可使接近饱和的氯化
钾的溶液变成饱和溶液,故选项正确。
C、加入足量氯化钾,能使接近饱和的氯化钾溶液变成饱和溶液,故选项正确。
D、加入足量40℃时氯化钾饱和溶液,所得溶液为氯化钾的不饱和溶液,故选项错误。
故选:BC。题型一 溶解度曲线
二、简答题
1.(2023·上海金山·统考二模)《天工开物》中记载了许多我国古代劳动人民对物质的认识和应用的事例。
如:石灰:“凡石灰经火焚炼为用。……用以砌墙、石,则筛去石块,水调黏合。”
硝石:“硝质与盐同母,大地之下潮气蒸成,现于地面。”
(1)文中石灰指氧化钙,请写出水调黏合过程中,氧化钙和水发生反应的化学方程式为____。
(2)硝石(硝酸钾)属于_________(选填“酸”“碱”或“盐)类物质,用洁净的铂丝蘸取硝酸钾溶液灼烧,透
过蓝色钴玻璃,火焰为_________色。
(3)下表是硝酸钾和氯化钠在不同温度下的溶解度。
温度(℃) 0 10 20 30 40 100
NaCl 35.7 35.8 36.0 36.3 36.6 39.8
溶解度(g/100g水)
KNO 13.3 20.9 31.6 45.8 63.9 246
3
I.溶解度受温度的影响较大的物质是______(选填“KNO ”或“NaCl”)。
3
II.20℃时,在50 g水中投入20 g NaCl,待充分溶解后,所得溶液的质量为____ g。
III.现有含49gKNO 和7.2gNaCl的样品,某同学设计了如下提纯混合物中KNO 的实验步骤:
3 3
i.滤液B中,KNO _______(选填“达到”或“未达到”)饱和状态。
3
ii.上述过程中采用的结晶方法是_______。
iii.步骤Ⅱ中蒸发ag水适宜的量为多少并结合相关数据说明理由。_____________
【答案】(1)CaO + H O = Ca(OH)
2 2
(2) 盐 紫
(3) KNO 68 达到 冷却结晶 蒸发80g水,因为20℃时,7.2g氯化钠在20g水中恰
3
好全溶,确保氯化钠全部溶解且降温到20℃时不析出,同时得到最多量的硝酸钾
【详解】(1)氧化钙和水发生反应生成氢氧化钙,化学方程式为CaO + H O = Ca(OH) ;
2 2
(2)硝酸钾由硝酸根离子和钾离子构成,属于盐;钾离子的焰色反应火焰颜色是紫色;
(3)I、从表中看出,硝酸钾的溶解度随温度的升高变化更大,故填KNO ;
3
II、20℃时,氯化钠溶解度为36.0g,50g水可溶解18.0g氯化钠,故所得溶液的质量为50g+18.0g=68g;III i、步骤三后得到硝酸钾固体和滤液,故滤液B中硝酸钾是饱和的;
ii、图中是先采用高温水溶解更多质量的硝酸钾,再冷却,使得硝酸钾溶解度下降、结晶出固体,采用的
结晶方法是冷却结晶;
iii、因为20℃时,7.2g氯化钠在20g水中恰好全部溶解,为确保氯化钠全部溶解且降温到20℃时不析出,
同时得到最多量的硝酸钾,可采用蒸发80g水。
2.(2023·上海崇明·统考二模).某兴趣小组对某氯化钠样品(可能含有硝酸钾)进行实验探究。
(1)为检验氯化钠样品中是否含有硝酸钾,甲同学取少量样品进行焰色反应,透过蓝色的钴玻璃片观察,火
焰呈___________色,证明样品中含有硝酸钾。
(2)为测定样品中氯化钠的含量,乙同学称取一定质量的样品溶于足量的水,再进行如下实验。
I.加入硝酸银溶液后反应的化学方程式为___________。
II.为确定一定量样品中氯化钠的含量,还需进行的实验操作为___________。
(3)下表是硝酸钾和氯化钠的部分溶解度数据。
温度(℃) 0 20 40 60 80
氯化钠 35.7 36.0 36.6 37.3 38.4
溶解度(g/100g水)
硝酸钾 13.3 31.6 63.9 110 169
I.40℃时,氯化钠的溶解度为___________。
II.80℃时,200g硝酸钾加到100g水中,充分溶解并恢复至原温度,所得溶液中溶质的质量分数是
___________(用相应的数据列式表示,不用计算)。
III.某样品中含38.9g氯化钠、9.8g硝酸钾。20℃时,在该样品中加入110g水,充分溶解后,蒸发浓缩;
当蒸发至剩余水量为10g时,至60℃时过滤,用数据分析此过程中析出晶体的组成情况___________。
【答案】(1)紫
(2) AgNO +NaCl=AgCl↓+NaNO 称量固体a
3 3
(3) 36.6g 60℃时10g水中最多溶解KNO 11g,大于9.8g,所以没有硝酸
3
钾析出。60℃时10g水中最多溶解NaC13.73g,9.8g,因此析出的晶体是NaCl,质量为
38.9g。-3.73g=35.17g
【详解】(1)钾离子的焰色呈紫色,所以用铂丝蘸取少量溶液进行焰色反应,透过蓝色钻玻璃观察到火焰呈紫色,说明含钾离子。故样品中含有硝酸钾。
(2)I.加入硝酸银溶液后,氯化钠会与硝酸银发生化学反应:AgNO +NaCl=AgCl↓+NaNO ;
3 3
II.想要确定样品中氯化钠的含量,就需要知道最终溶液中生成了多少克固体a。通过固体a的质量进行计
算,求出氯化钠的质量,最终求出样品中氯化钠的含量.
(3)Ⅰ.由表可知40℃时氯化钠的溶解度为36.6g;
II.因为80℃时硝酸钾的溶解度为169g,所以质量分数为
III.60℃时10g水中最多溶解KNO 11g,大于9.8g,所以没有硝酸钾析出。60℃时10g水中最多溶解NaC1
3
3.73g,小于9.8g,因此析出的晶体是NaCl,质量为38.9g-3.73g=35.17g
3.(2023·上海嘉定·统考二模)KCl有着广泛的用途。
(1)农业生产中KCl可用作_____(选填“钾”“氮”或“磷”)肥。
(2)对KCl溶液进行焰色反应,透过蓝色钴玻璃片,火焰呈_____色。
(3)海水中含有氯化钠和氯化钾等物质。根据下图的溶解度曲线回答问题。
I.40℃时,氯化钾的溶解度为_____g/100g水。
II.25℃时,如下图所示,充分溶解后所得溶液为不饱和溶液的有_____(填烧杯编号),若将D烧杯中的
溶液升温至40℃,所得溶液的溶质质量分数是_____。
III.氯化钾溶液中含有少量氯化钠,提纯氯化钾的方法是_____(选填“蒸发结晶”或“降温结晶”)。【答案】(1)钾
(2)紫
(3) 40 AB 28.6% 降温结晶
【详解】(1)氯化钾中含有钾元素,含有钾元素的肥料称为钾肥;
(2)氯化钾中含有钾元素,透过蓝色钴玻璃片,焰色反应时火焰是紫色;
(3)①由图可知,40℃时,氯化钾的溶解度为40g/100g水;
②由图可知,25℃时,氯化钾的溶解度大于30g/100g水,小于40g/100g水,四个烧杯中分别加入100g水
和不同质量的氯化钾,充分溶解后,AB烧杯中加入氯化钾的质量小于等于30g,则为不饱和溶液,CD烧
杯中加入氯化钾的质量大于等于40g,则为饱和溶液;
③若将D烧杯中的溶液升温至40℃,由图可知40℃时氯化钾的溶解度为40g/100g水,D烧杯中加入50g
氯化钾,最多可溶解40g,所得溶液的溶质质量分数是 ;
④由图可知氯化钠和氯化钾的溶解度都随温度升高而增大,氯化钾的溶解度随温度变化比氯化钠的溶解度
随温度变化大,故可以使用降温结晶的方法提纯氯化钾。
4.(2023·上海静安·统考二模)下表是氯化钠和硝酸钾在不同温度下的溶解度。请回答下列问题:
温度/℃ 0 10 20 30 40 50
NaCl 35.7 35.8 36.0 36.3 36.6 37.0
溶解度(g/100gH O)
2
KNO 13.3 20.9 31.6 45.8 63.9 85.5
3
(1)60℃时,向100g水中加入一定量KNO 形成溶液,再降温至20℃,析出固体质量的变化如图所示,回答
3
下列问题。
1.20℃时KNO 溶解度为______g/100g水,该温度下,20gKNO 溶解在50g水中,所得溶液的质量为
3 3
______g。II.60℃时加入的KNO 质量为______g,此时所得溶液为______(填“饱和”或“不饱和”)。
3
III.降温过程中,下列说法正确的是______。
A.时间0至t 过程中,溶液中溶质质量分数不变
1
B.时间t 时,溶液为20℃时KNO 溶解度的饱和溶液
1 3
C.时间t 至t 过程中,硝酸钾的溶解度逐渐变小
1 2
(2)50℃时,将80.0g一定质量分数的氯化钠溶液恒温蒸发,溶液的质量随蒸发水的质量变化关系如图所示,
则a点溶液中溶质的质量为______g。
(3)除去硝酸钾中含有的少量氯化钠,采用的方法是______。
【答案】(1) 31.6 65.8 41.6 不饱和 AC
(2)18.5
(3)降温结晶
【详解】(1)Ⅰ、由表中数据可知,20℃时,KNO 溶解度为31.6g/100g水;
3
该温度下,50g水中最多可溶解硝酸钾的质量为 ,则将20gKNO 溶解在50g水中,所得
3
溶液的质量为15.8g+50g=65.8g。
Ⅱ、由于降温至20℃时,析出10g固体,而20℃时,KNO 溶解度为31.6g,则说明加入的硝酸钾的质量为
3
31.6g+10g=41.6g;
由于降温一段时间后才有固体析出,则说明所得溶液为不饱和溶液。
Ⅲ、A、时间0至t 过程中,没有固体析出,则溶液中的溶质质量不变,则溶液中溶质质量分数不变,该
1
选项说法正确;
B、t 之后,溶液中有固体析出,则说明该溶液为KNO 溶液的饱和溶液,但温度不是20℃,该选项说法不
1 3
正确;
C、时间t 至t 过程中,由于析出固体越来越多,则说明硝酸钾的溶解度逐渐变小,该选项说法正确。
1 2
故选AC。
(2)由于a点后,随着水的蒸发,溶液质量减少变多,则说明a点之前没有固体析出,则a点时溶液质量为80g-11.5g=68.5g,而50℃时,氯化钠的溶解度为37g,则68.5g饱和溶液中溶质质量为
。
(3)硝酸钾和氯化钠的溶解度均随温度升高而增大,且硝酸钾溶解度受温度影响比较大,氯化钠溶解度
受温度影响较小,则除去硝酸钾中含有的少量氯化钠,可采用降温结晶的方法。
5.(2023·上海闵行·统考二模)氯化钠和硝酸钾在不同温度时的溶解度见下表:
温度(℃) 20 30 40 60 80 100
氯化钠 36.0 36.3 36.6 37.3 38.4 39.8
溶解度(g/100g水)
硝酸钾 31.6 45.8 63.9 110 169 246
(1)40℃时,氯化钠的溶解度是_______g。
(2)两物质中溶解度受温度影响较大的是_______。
(3)60℃时,100g硝酸钾饱和溶液中溶质与溶剂的质量比是_______。
(4)实验室有170g硝酸钾和氯化钠的固体混合物,为了选择合适的方法提纯两种物质,先预判混合物中两
种物质的质量,实验小组设计实验一如下:
【实验一】
通过上述实验可判断出混合物中硝酸钾的质量范围是_______。
为准确获得混合物中两种物质的质量,实验小组又设计实验二如下:
【实验二】
(5)反应的化学方程式是_______;则混合物中氯化钠的质量是_______g(精确到0.1)。根据实验二所得硝酸
钾和氯化钠的实际质量,若要得到尽可能多且纯净的硝酸钾,可在实验一步骤2后继续实验:_______。
(请将设计的实验步骤补充完整)
【答案】(1)36.6(2)硝酸钾
(3)11:10
(4)131.6g≤m≤169g
(5) 设混合物中氯化钠的质量为x
答:混合物中氯化钠的质量为3.6g; 蒸发90g水,再降温至20℃,过滤,将所得固体洗涤干燥
【详解】(1)由表格数据可知,40℃时,氯化钠的溶解度是36.6g/100g水;
(2)由表格数据可知,硝酸钾的溶解度受温度影响较大;
(3)60℃时,硝酸钾的溶解度为110g,100g硝酸钾饱和溶液中溶质与溶剂的质量比应为11:10;
(4)80℃时,烧杯中没有固物质剩余,此时硝酸钾的溶解度为169g,所以混合物中硝酸钾的质量最大为
169g,80℃时,氯化钠的溶解度为38.4g,所以混合物中硝酸钾的质量最小为170g-38.4g=131.6g,因此混
合物中硝酸钾的质量范围是131.6g≤m≤169g;
(5)硝酸银和氯化钠反应生成氯化银和硝酸钠,反应的化学方程式为:AgNO +NaCl=AgCl↓+NaNO ,混
3 3
合物中氯化钠的质量见解析;根据实验二所得硝酸钾和氯化钠的实际质量,若要得到尽可能多且纯净的硝
酸钾,混合物中氯化钠3.6g,只需要20℃的10g水就可以完全溶解,可在实验一步骤2后继续实验:蒸发
90g水,再降温至20℃,过滤,将所得固体洗涤干燥。
6.(2023·上海浦东新区·统考二模)NaCl、NaNO 的部分溶解度数据见下表。
3
温度(℃) 20 40 60 80
氯化钠 36 36.6 37.3 38.4
溶解度(g/100g水)
硝酸钠 87 103 125 150
(1)硝酸钠的溶解度随温度的升高而______(选填“增大”或“减小”);40℃时硝酸钠的溶解度为
______g/100g水。
(2)20℃时,在50g水中加入18g氯化钠,充分搅拌后所得溶液的溶质质量分数为______。
(3)用洁净的铂丝蘸取NaCl溶液灼烧,火焰呈______色。
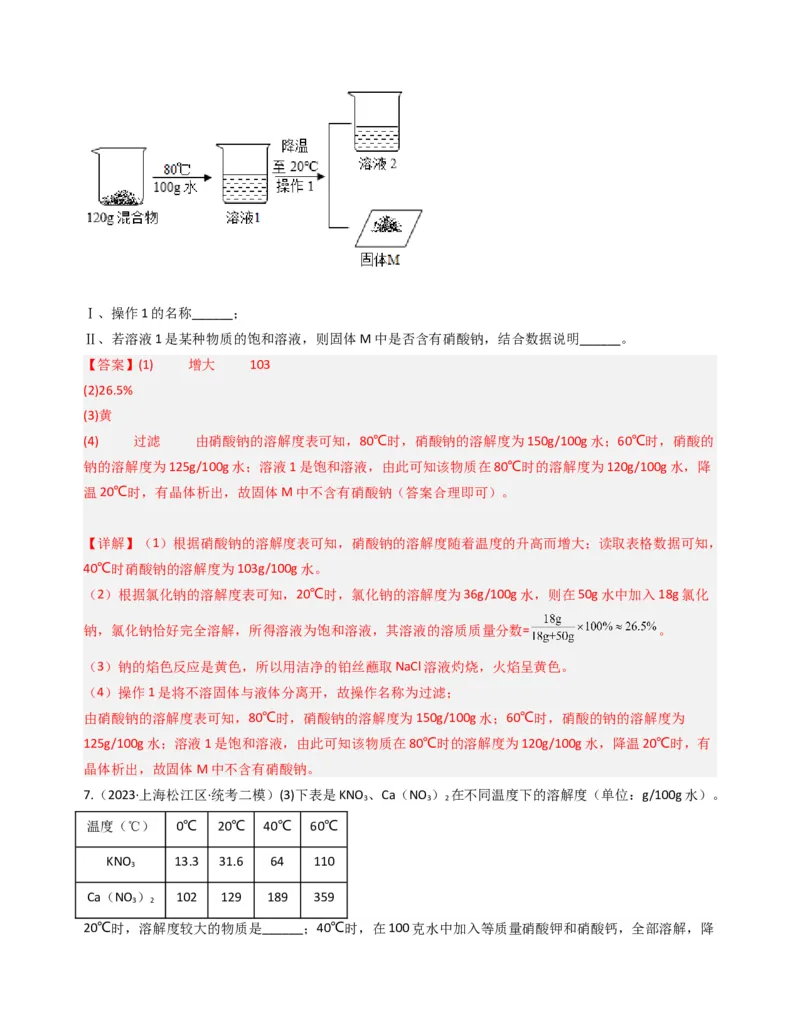
(4)取硝酸钠和氯化钠的混合物120g,进行如下实验。Ⅰ、操作1的名称______;
Ⅱ、若溶液1是某种物质的饱和溶液,则固体M中是否含有硝酸钠,结合数据说明______。
【答案】(1) 增大 103
(2)26.5%
(3)黄
(4) 过滤 由硝酸钠的溶解度表可知,80℃时,硝酸钠的溶解度为150g/100g水;60℃时,硝酸的
钠的溶解度为125g/100g水;溶液1是饱和溶液,由此可知该物质在80℃时的溶解度为120g/100g水,降
温20℃时,有晶体析出,故固体M中不含有硝酸钠(答案合理即可)。
【详解】(1)根据硝酸钠的溶解度表可知,硝酸钠的溶解度随着温度的升高而增大;读取表格数据可知,
40℃时硝酸钠的溶解度为103g/100g水。
(2)根据氯化钠的溶解度表可知,20℃时,氯化钠的溶解度为36g/100g水,则在50g水中加入18g氯化
钠,氯化钠恰好完全溶解,所得溶液为饱和溶液,其溶液的溶质质量分数= 。
(3)钠的焰色反应是黄色,所以用洁净的铂丝蘸取NaCl溶液灼烧,火焰呈黄色。
(4)操作1是将不溶固体与液体分离开,故操作名称为过滤;
由硝酸钠的溶解度表可知,80℃时,硝酸钠的溶解度为150g/100g水;60℃时,硝酸的钠的溶解度为
125g/100g水;溶液1是饱和溶液,由此可知该物质在80℃时的溶解度为120g/100g水,降温20℃时,有
晶体析出,故固体M中不含有硝酸钠。
7.(2023·上海松江区·统考二模)(3)下表是KNO 、Ca(NO ) 在不同温度下的溶解度(单位:g/100g水)。
3 3 2
温度(℃) 0℃ 20℃ 40℃ 60℃
KNO 13.3 31.6 64 110
3
Ca(NO ) 102 129 189 359
3 2
20℃时,溶解度较大的物质是______;40℃时,在100克水中加入等质量硝酸钾和硝酸钙,全部溶解,降温至有晶体析出,该晶体的成分是______。
(4)20℃时,该栽培液中主要物质的含量见下表。该栽培液是硝酸钾的______(选填“饱和”或“不饱
和”)溶液。栽培液中硝酸钾的质量分数是______。
物质 每100g栽培液所含质量(g)
水 50
硝酸钾 10
硝酸钙 30
【答案】
(3) 硝酸钙/Ca(NO ) 硝酸钾/KNO
3 2 3
(4) 不饱和 10%
【详解】(3)根据表格数据可知20℃硝酸钙的溶解度较大;
假设40℃时,在100克水中加入64g硝酸钾和硝酸钙,则可以全部溶解,得到硝酸钾的饱和溶液,硝酸钙
的不饱和溶液,两物质的溶解度均随温度的降低而降低,则降温后硝酸钾的溶液变为过饱和溶液立即会有
晶体析出,而硝酸钙的溶液还是不饱和溶液,则没有晶体析出;
(4)20℃时,硝酸钾的溶解度为31.6g,则饱和溶液的溶质质量分数= ,根据表
格数据可知100g水中含有10g硝酸钾,则硝酸钾的溶质质量分数为 ,10%<31.6%,则
得到的为硝酸钾的不饱和溶液;
根据上述分析可知硝酸钾的溶质质量分数为10%。
8(2023·上海徐汇区·统考二模)在NaCl中添加一定量的KCl可制成“低钠盐”供某些疾病的患者食用。
(1)用洁净的铂丝蘸取NaCl溶液灼烧,火焰呈__________色。
(2)NaCl和KCl的溶解度数据如下表示所示。80℃时,KCl的溶解度为__________g/100g水。若KCl中混有少
量NaCl,可依次通过溶解、蒸发浓缩、__________,过滤等操作提纯KCl。
溶解度(g/100g水)
温度(℃) 0 20 60 80
NaCl 35.7 36 37.3 38.4
KCl 28 34.2 45.8 51.3
(3)有一包由NaCl和KCl混合成的样品,称取50g该样品进行如下实验(忽略物质的损耗)①溶液B中NaCl的质量为_________g。
②溶液A中KCl__________(选填“达到”或“未达到”)饱和状态。
③该样品中KCl的质量分数为__________。
④另有一包由NaCl和KCl混合成的样品,其中KCl的质量分数介于30%~40%之间,称取50g该样品,重
复上述实验中步骤i和步骤ii,能否测出KCl的质量分数?为什么?__________。
【答案】(1)黄
(2) 51.3 降温结晶
(3) 36 未达到 26% 不能,20℃时样品会完全溶解,无法确定其中氯化钠和氯化钾的质
量
【详解】(1)焰色反应为元素的性质,钠元素的焰色反应火焰呈黄色。
(2)据表格数据可知,80℃时,KCl的溶解度为51.3g/100g水。
据表格数据可知,NaCl溶解度受温度变化影响不大,KCl溶解度受温度变化影响很大,所以若KCl中混有
少量NaCl,可依次通过溶解、蒸发浓缩、降温结晶,过滤等操作提纯KCl。
(3)①据图可知,析出1g氯化钠,说明溶液B是氯化钠的饱和溶液,20℃时100g水溶解氯化钠36g达到
饱和,所以溶液B中NaCl的质量为36g。即50g该样品中含有氯化钠37g,氯化钾13g。
②由①知道,80℃时100g水溶解氯化钾13g,而80℃时氯化钾的溶解度为51.3g,即溶液A中KCl未达到
饱和状态。
③该样品中KCl的质量分数= 。
④当样品中KCl的质量分数=30%时,即氯化钾质量=50g×30%=15g时,氯化钠质量=50g-15g=35g<36g,由
于氯化钠在20℃时的溶解度是36g,即20℃时样品会完全溶解,无法确定其中氯化钠和氯化钾的质量,所
以KCl的质量分数介于30%~40%之间,称取50g该样品,重复上述实验中步骤i和步骤ii,不能测出KCl
的质量分数。
9.(2023·上海杨浦区·统考二模)下表是KNO 、NaC1在不同温度下的溶解度(单位:g)
3
温度(℃) 0 10 20 40 50 60 70 80 90 100
KNO 13.3 20.9 32 64 85.5 110 138 169 202 246
3NaCl 35.7 35.8 36 36.6 37 37.3 37.8 38.4 39 39.8
(1)60℃时,50g水中溶解32g硝酸钾形成不饱和溶液,欲使该溶液恰好达到饱和,可以恒温蒸发水的质量
______g(精确到1g);当其它条件不变时,也可以降温到_____℃恰好饱和。
(2)KNO 溶液中含有少量NaCl时,可通过_____方法提纯。析出的晶体和剩余溶液描述正确的是______(填
3
写编号)。
A.剩余溶液一定是当时KNO 的饱和溶液
3
B.剩余溶液一定是当时NaCl的不饱和溶液
C.上述方法无法将两者完全分离
D.析出的晶体中一定不含有NaCl
(3)t℃时,将一定量KNO 的不饱和溶液平均分为三份,分别恒温蒸发出水的质量为5g、10g、15g,析出
3
KNO 晶体的质量依次为ag、bg、cg,则a、b、c三者的关系为_____。
3
A.c=a+b B.c=2b-a C.c=a+2b D.c=2a-b
【答案】(1) 20.9 40
(2) 降温结晶 AC
(3)B
【详解】(1)60℃时,硝酸钾的溶解度为110g,所以32g硝酸钾形成饱和溶液只需水的职位为:
,则需要恒温蒸发的水的质量为: ,故填:20.9g;
②当其他条件不变时,50g水中溶解32g硝酸钾能达到饱和,说明溶解度应该小于等于64g,对照表格发
现,40℃时硝酸钾的溶解度恰好为64g,故填:40℃;
(2)因为硝酸钾的溶解度随温度的升高而升高,氯化钠的溶解度随温度变化很小,所以当KNO 溶液中含
3
有少量NaCl时,可通过降温结晶的方法提纯,故填:降温结晶;
②A.饱和溶液是指在一定温度下,不能再溶解这种溶质的溶液,既然有晶体析出,剩余的溶液一定是硝
酸钾的饱和溶液;
B.但不一定是氯化钠的饱和溶液;
C.该方法不能将两物质完全分离,析出的晶体中可能含有氯化钠;
故选AC;
(3)硝酸钾的不饱和溶液蒸发5g水时析出晶体为a g,蒸发10 g水时析出晶体为b g,可知硝酸钾饱和溶
液蒸发5 g水时析出晶体为(b-a)g,那么硝酸
钾饱和溶液蒸发10 g水时析出晶体为2(b-a)g,又根据蒸发15g水时析出晶体为cg,得出硝酸钾饱和溶液蒸发10 g水时析出晶体为(c一a) g,列式为 ,得 ,故选B。
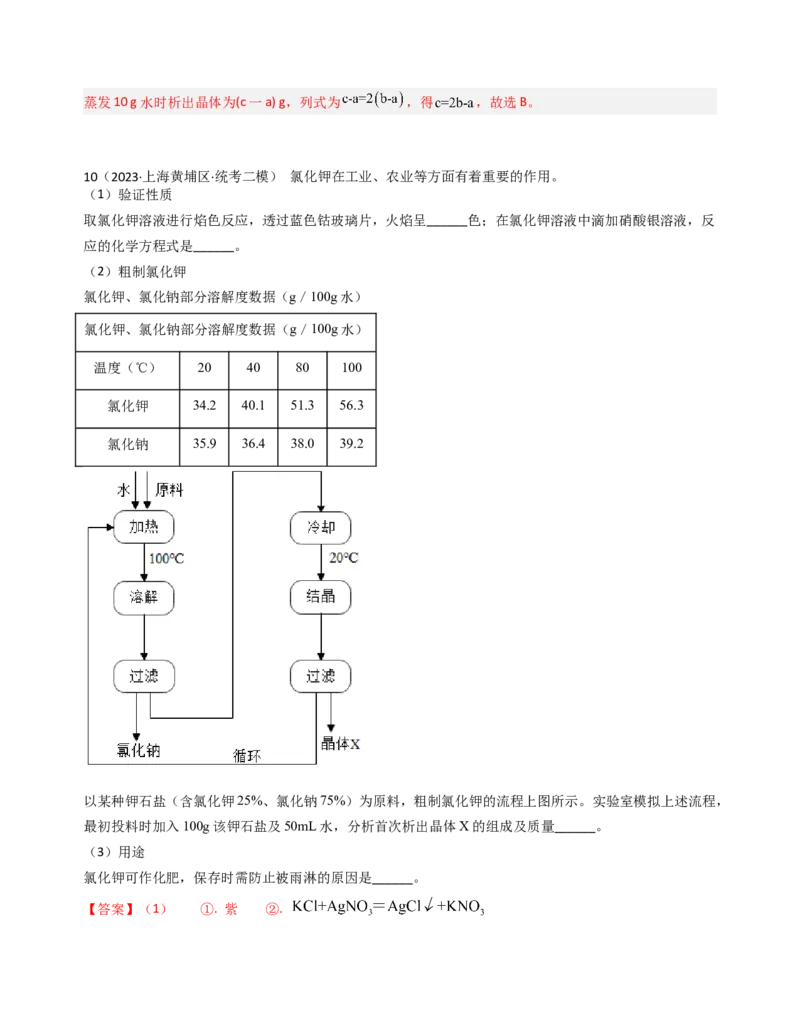
10(2023·上海黄埔区·统考二模) 氯化钾在工业、农业等方面有着重要的作用。
(1)验证性质
取氯化钾溶液进行焰色反应,透过蓝色钴玻璃片,火焰呈______色;在氯化钾溶液中滴加硝酸银溶液,反
应的化学方程式是______。
(2)粗制氯化钾
氯化钾、氯化钠部分溶解度数据(g/100g水)
氯化钾、氯化钠部分溶解度数据(g/100g水)
温度(℃) 20 40 80 100
氯化钾 34.2 40.1 51.3 56.3
氯化钠 35.9 36.4 38.0 39.2
以某种钾石盐(含氯化钾25%、氯化钠75%)为原料,粗制氯化钾的流程上图所示。实验室模拟上述流程,
最初投料时加入100g该钾石盐及50mL水,分析首次析出晶体X的组成及质量______。
(3)用途
氯化钾可作化肥,保存时需防止被雨淋的原因是______。
【答案】(1) ①. 紫 ②.(2)氯化钾7.9g,氯化钠1.65g
(3)KCl的溶解度比较大,雨淋能使大量的KCl溶解流失
【解析】
【小问1详解】
取氯化钾溶液进行焰色反应,透过蓝色钴玻璃片,火焰呈紫色,因为钾离子的颜色反应是紫色;
氯化钾和硝酸银反应生成硝酸钾和氯化银沉淀,反应的方程式为 ;
【小问2详解】
该钾石盐含氯化钾25%、氯化钠75%,故100g钾石盐中含有氯化钾 ,含有氯化钠
;
分析流程图:100℃时,氯化钾的溶解度为56.3g,氯化钠的溶解度为39.2g,故50mL水中最多溶解氯化钾
28.15g,最多溶解氯化钠19.6g,由于 ,氯化钾完全溶解,而 ,氯化钠有晶体
析出,析出氯化钠的质量为 ;此时溶液中只溶解25g的氯化钾和19.6g的氯化钠;
冷却至20℃后,氯化钾的溶解度为34.2g,氯化钠的溶解度为35.9g,故50mL水中此时最多溶解氯化钾
17.1g,最多溶解氯化钠17.95g,由于 ,故氯化钾、氯化钠均有晶体析出,析
出质量为 ;
故首次析出晶体X为氯化钾7.9g,氯化钠1.65g;
【小问3详解】
分析溶解度表格可知,KCl的溶解度比较大,雨淋能使大量的KCl溶解流失,故保存时需防止被雨淋。
11(2023·上海虹口区·统考二模) 为探究氢氧化钠与盐酸反应的热量变化及溶液酸碱性的变化,某小组同
学进行如下实验。
【实验一】配制氢氧化钠溶液
氢氧化钠的部分溶解度如表所示。
温度(℃) 10 20 30 40 60
溶解度(g/100g 98 109 119 129 174
水)
①10℃时,氢氧化钠的溶解度是 g/100g水。
②20℃时,40g氢氧化钠与60g水混合,所得溶液是氢氧化钠的 (选填“饱和”或“不饱和”)
溶液;配制100g、4%的氢氧化钠溶液,需要水 g。
【实验二】探究氢氧化钠与盐酸的反应中,溶液酸碱性的变化。
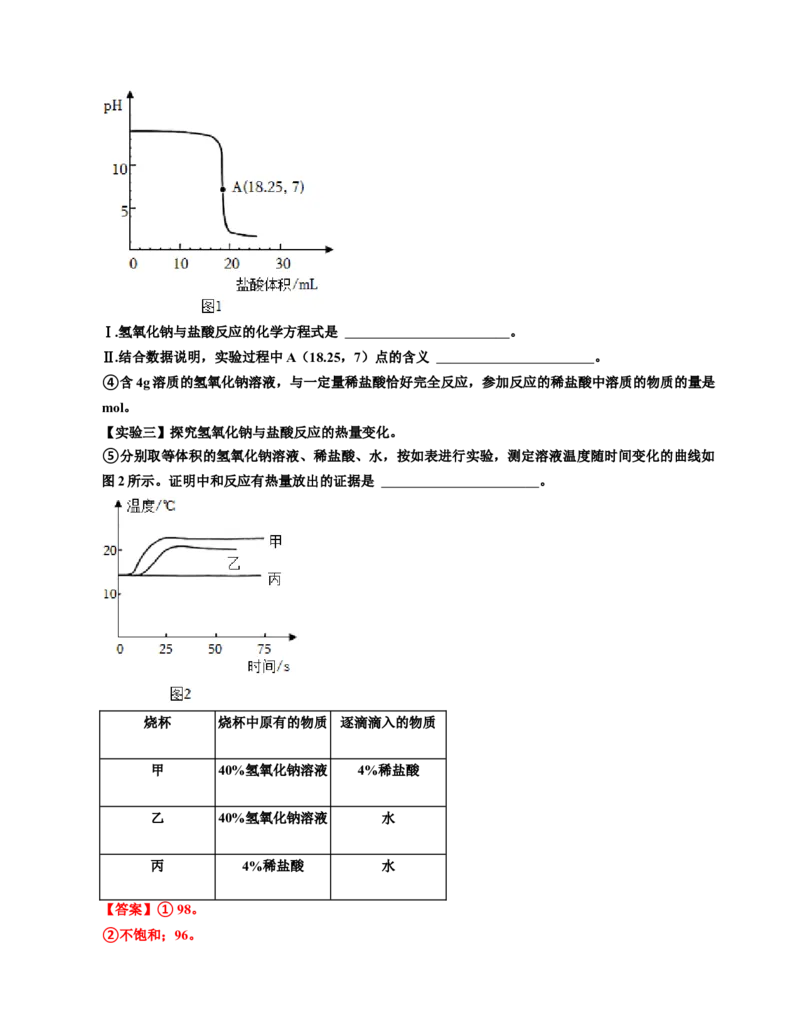
③向盛有20g、4%的氢氧化钠溶液中逐滴滴加稀盐酸,用pH传感器测定溶液pH随滴入稀盐酸体积
的变化,如图1所示。Ⅰ.氢氧化钠与盐酸反应的化学方程式是 。
Ⅱ.结合数据说明,实验过程中A(18.25,7)点的含义 。
④含4g溶质的氢氧化钠溶液,与一定量稀盐酸恰好完全反应,参加反应的稀盐酸中溶质的物质的量是
mol。
【实验三】探究氢氧化钠与盐酸反应的热量变化。
⑤分别取等体积的氢氧化钠溶液、稀盐酸、水,按如表进行实验,测定溶液温度随时间变化的曲线如
图2所示。证明中和反应有热量放出的证据是 。
烧杯 烧杯中原有的物质 逐滴滴入的物质
甲 40%氢氧化钠溶液 4%稀盐酸
乙 40%氢氧化钠溶液 水
丙 4%稀盐酸 水
【答案】①98。
②不饱和;96。NaOH+HCl═NaCl+H O。
2
Ⅱ.加入18.25mL稀盐酸时恰好完全反应。
④0.1。
⑤丙中温度无明显变化,甲比乙放热多。
【解答】解:①10℃时,氢氧化钠的溶解度是98g/100g水。
故答案为:98。
②20℃时氢氧化钠溶解度是109g,40g氢氧化钠与60g水混合,所得溶液是氢氧化钠的不饱和溶液;
配制100g、4%的氢氧化钠溶液,需要水100g﹣100g×4%=96g。
故答案为:不饱和;96。
③Ⅰ.氢氧化钠与盐酸反应的化学方程式是NaOH+HCl═NaCl+H O。
2
故答案为:NaOH+HCl═NaCl+H O。
2
Ⅱ.实验过程中A(18.25,7)点的含义是加入18.25mL稀盐酸时恰好完全反应。
故答案为:加入18.25mL稀盐酸时恰好完全反应。
④含4g溶质的氢氧化钠溶液(氢氧化钠物质的量是0.1mol),与一定量稀盐酸恰好完全反应,氢氧化
钠和氯化氢物质的量之比是1:1,参加反应的稀盐酸中溶质的物质的量是0.1mol。
故答案为:0.1。
⑤证明中和反应有热量放出的证据是丙中温度无明显变化,甲比乙放热多。
故答案为:丙中温度无明显变化,甲比乙放热多。
声明:试题解析著作权属所有,未经书面同意,不得复制发布日期:2023/5/16 14:35:06;用户:天空之城;邮箱:2230668592@qq.com;学号:20667957
12(2023·上海长宁区·统考二模)氯化钠和硫酸钠的部分溶解度如下表。
温度 (℃) 40 60 80 100
NaCl 36.6 37.1 38 39.2
溶解度 (g/100 g 水)
Na SO 48.8 45.3 43.7 42.5
2 4
① 40℃时, NaCl 的溶解度是 g/100 g 水,40~ 100℃间, Na SO 的溶解度随温度上升而
2 4
( 2 1 ) (选填“增大”或“减小”) ,80℃时, ( 2 2 ) (选填“NaCl”或“Na SO ”) 的饱和溶液
2 4
的 质量分数更大。
② 某 NaCl 样品中混有 Na SO ,取 40 g 该样品,依据两种物质溶解度的差异设计如下实验进行提纯。
2 4【检验产物】检验晶体 A 中是否仍有 Na SO 杂质
2 4
实验步骤 现象 结论 原理
取少量晶体 A,加足量水充分溶解 晶体 A 中仍 ( 2 4 )
出现 ( 2 3 ) 色沉淀
后,滴加少量氯化钡溶液 有 Na SO (化学方程式)
2 4
杂质
【改进实验】将步骤 III 改为“冷却至 40℃后过滤”, 最终得到 31.94 g 纯净的氯化钠晶体和
18.06 g 溶液 ,40℃时, 该 18.06 g 溶液为氯化钠的 ( 2 5 ) (选填“饱和”或“不饱和”) 溶液,
该 40 g 样品中含氯化钠 ( 2 6 ) g。
【实验反思】若将步骤 III 改为“冷却至 40~60℃后过滤”, 最终能否得到纯净的氯化钠晶体,
请 结合相关数据阐述你的理由。 ( 2 7 )【答案】①36.6;减小;Na SO ;
2 4
②白;Na SO +BaCl =BaSO ↓+2NaCl;
2 4 2 4
【改进实验】饱和;35.6;
【实验反思】能得到纯净的氯化钠晶体,理由是根据40~60℃时硫酸钠的溶解度可知,40~60℃时10g
水中最少要溶解4.53g硫酸钠才能达到饱和,而40g样品中只有4.4g硫酸钠,在该温度下不会从溶液中
析出。
【解答】解:①根据氯化钠和硫酸钠的部分溶解度表可知,40℃时,NaCl的溶解度是36.6g/100g水,
40~100℃间,Na SO 的溶解度随温度上升而减小,80℃时氯化钠的溶解度为38g/100g水,硫酸钠的溶
2 4
解度为43.7g/100g水,故80℃时,Na SO 的饱和溶液的质量分数更大;
2 4
②晶体A中仍有Na SO 杂质,硫酸钠与氯化钡溶液反应会生成白色沉淀硫酸钡,故可观察到有白色沉
2 4
淀产生,发生的化学方程式为Na SO +BaCl =BaSO ↓+2NaCl;
2 4 2 4
【改进实验】饱和溶液析出晶体后,仍是该温度下的饱和溶液,故将步骤Ⅲ改为“冷却至 40℃后过
滤”,最终得到31.94g纯净的氯化钠晶体和18.06g溶液,40℃时,该18.06g溶液为氯化钠的饱和溶液,
40℃时,氯化钠的溶解度为36.6g/100g水,则40℃时,10g水中最多溶解3.66g氯化钠,则18.06g溶液
中有氯化钠3.66g,故该40g样品中含氯化钠为31.94g+3.66g=35.6g;
【实验反思】根据40~60℃时硫酸钠的溶解度可知,40~60℃时10g水中最少要溶解4.53g硫酸钠才能
达到饱和,而40g样品中只有4.4g硫酸钠,在该温度下不会从溶液中析出,故若将步骤Ⅲ改为“冷却至
40~60℃后过滤”,最终能得到纯净的氯化钠晶体,理由是根据 40~60℃时硫酸钠的溶解度可知,40
~60℃时10g水中最少要溶解4.53g硫酸钠才能达到饱和,而40g样品中只有4.4g硫酸钠,在该温度下
不会从溶液中析出。
故答案为:①36.6;减小;Na SO ;
2 4
②白;Na SO +BaCl =BaSO ↓+2NaCl;
2 4 2 4
【改进实验】饱和;35.6;
【实验反思】能得到纯净的氯化钠晶体,理由是根据40~60℃时硫酸钠的溶解度可知,40~60℃时10g
水中最少要溶解4.53g硫酸钠才能达到饱和,而40g样品中只有4.4g硫酸钠,在该温度下不会从溶液中
析出。