文档内容
姓名 座位号
(在此卷上答题无效)
绝密 ★ 启用前
化 学
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号框涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号框。回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将答题卡交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Cl-35.5 Fe-56
一、选择题:本题共 14 小题,每题 3 分,共 42 分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
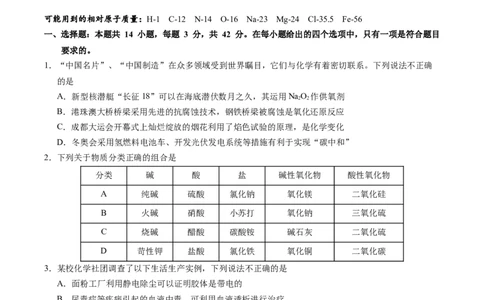
1.“中国名片”、“中国制造”在众多领域受到世界瞩目,它们与化学有着密切联系。下列说法不正确
的是
A.新型核潜艇“长征18”可以在海底潜伏数月之久,其运用NaO 作供氧剂
2 2
B.港珠澳大桥桥梁采用先进的抗腐蚀技术,钢铁桥梁被腐蚀是氧化还原反应
C.成都大运会开幕式上灿烂绽放的烟花利用了焰色试验的原理,是化学变化
D.冬奥会采用氢燃料电池车、开发光伏发电系统等措施有利于实现“碳中和”
2.下列关于物质分类正确的组合是
分类 碱 酸 盐 碱性氧化物 酸性氧化物
A 纯碱 硫酸 氯化钠 氧化镁 二氧化硅
B 火碱 硝酸 小苏打 氧化钠 三氧化硫
C 烧碱 醋酸 碳酸铵 碱石灰 二氧化硫
D 苛性钾 盐酸 氯化铁 氧化铜 二氧化碳
3.某校化学社团调查了以下生活生产实例,下列说法不正确的是
A.面粉工厂利用静电除尘可以证明胶体是带电的
B.尿毒症等疾病引起的血液中毒,可利用血液透析进行治疗
C.阳光穿透清晨的树林时形成的光柱,是胶体的丁达尔效应的体现
D.长江三角洲形成的主要原因是胶体的聚沉
4.N 表示阿伏加德罗常数的值,下列说法正确的是
A
A.7.1gCl 与足量铁在加热条件下完全反应时转移的电子数为0.3N
2 A
B.100mL 1mol/LKClO 溶液中含有的Cl- 数为0.1N
3 A
C.常温常压下,46gNO 和NO 的混合气体中氧原子总数为2N
2 2 4 A
D.标准状况下,5.6LCO和N 的混合气体中含有的原子总数为N
2 A
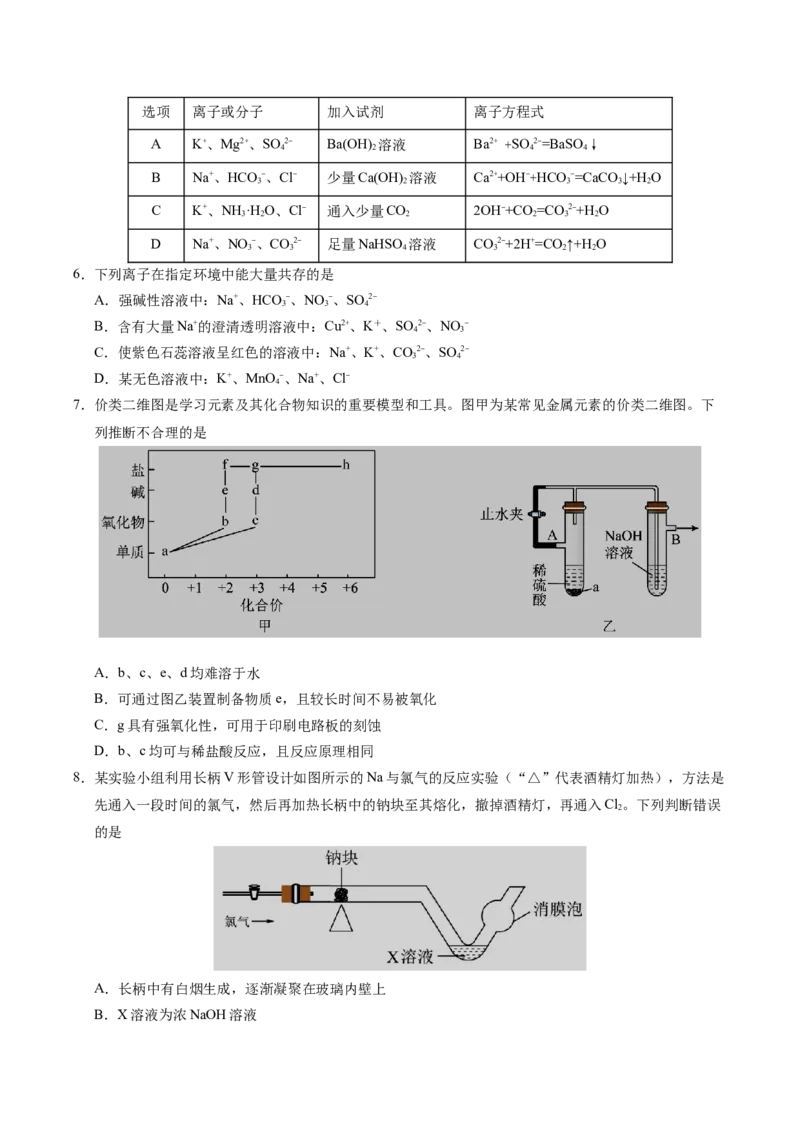
5.下列各组离子或分子能大量共存,加入相应试剂后发生反应的离子方程式书写正确的是选项 离子或分子 加入试剂 离子方程式
A K+、Mg2+、SO 2- Ba(OH) 溶液 Ba2+ +SO 2-=BaSO ↓
4 2 4 4
B Na+、HCO -、Cl- 少量Ca(OH) 溶液 Ca2++OH-+HCO -=CaCO ↓+H O
3 2 3 3 2
C K+、NH ·H O、Cl- 通入少量CO 2OH-+CO =CO 2-+H O
3 2 2 2 3 2
D Na+、NO -、CO2- 足量NaHSO 溶液 CO2-+2H+=CO ↑+H O
3 3 4 3 2 2
6.下列离子在指定环境中能大量共存的是
A.强碱性溶液中:Na+、HCO -、NO -、SO 2-
3 3 4
B.含有大量Na+的澄清透明溶液中:Cu2+、K+、SO 2-、NO -
4 3
C.使紫色石蕊溶液呈红色的溶液中:Na+、K+、CO2-、SO 2-
3 4
D.某无色溶液中:K+、MnO -、Na+、Cl-
4
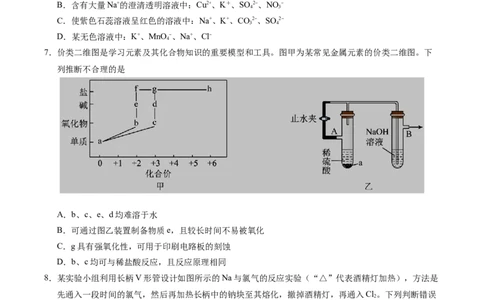
7.价类二维图是学习元素及其化合物知识的重要模型和工具。图甲为某常见金属元素的价类二维图。下
列推断不合理的是
A.b、c、e、d均难溶于水
B.可通过图乙装置制备物质e,且较长时间不易被氧化
C.g具有强氧化性,可用于印刷电路板的刻蚀
D.b、c均可与稀盐酸反应,且反应原理相同
8.某实验小组利用长柄V形管设计如图所示的Na与氯气的反应实验(“△”代表酒精灯加热),方法是
先通入一段时间的氯气,然后再加热长柄中的钠块至其熔化,撤掉酒精灯,再通入Cl。下列判断错误
2
的是
A.长柄中有白烟生成,逐渐凝聚在玻璃内壁上
B.X溶液为浓NaOH溶液C.V形管的“消膜泡”的作用主要是用来消除泡沫
D.钠在氯气中燃烧的火焰为黄色
9.下列物质转化(“→”表示一种物质转化为另一种物质)中,每次转化只通过一步反应,不可能全部
实现的是
A.HO→O→CO→HCO
2 2 2 2 2 3
B.CaCO →CaO→Ca(OH)→NaOH
3 2
C.NaOH→NaCl→Na CO→NaNO
2 3 3
D.Mg→MgCl →Mg(OH)→Mg(NO )
2 2 3 2
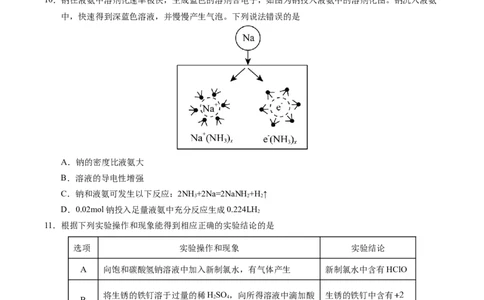
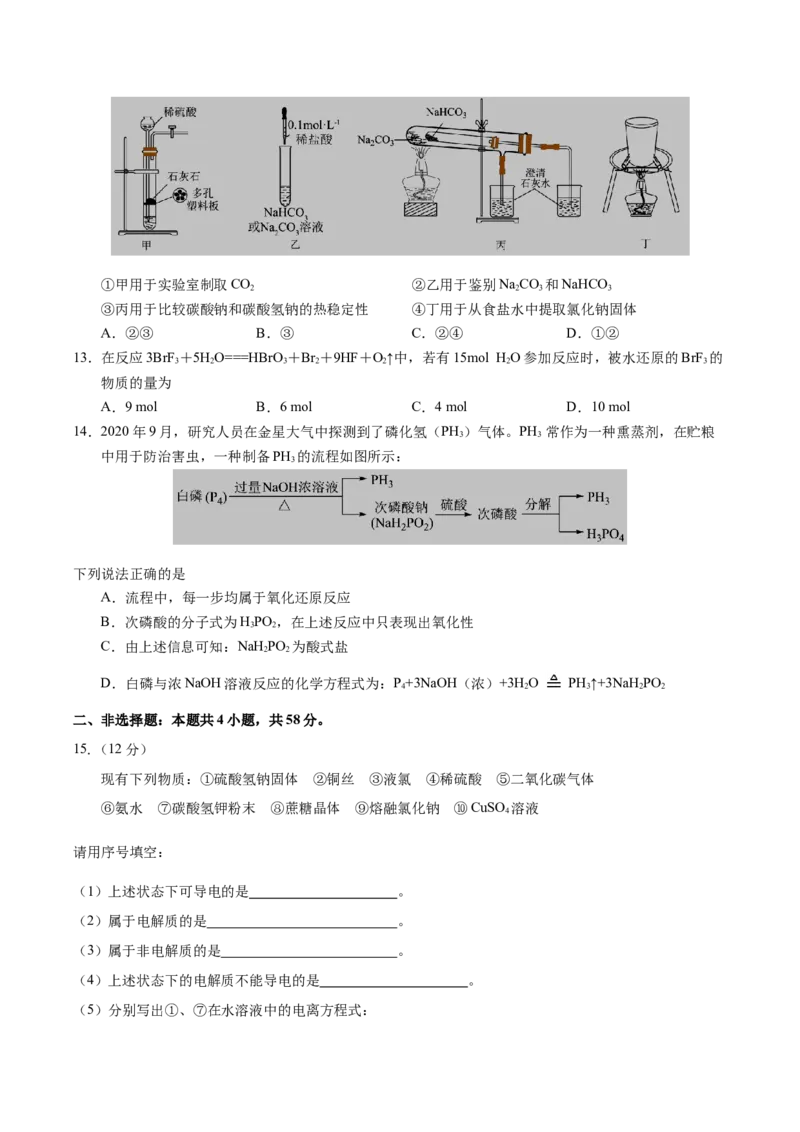
10.钠在液氨中溶剂化速率极快,生成蓝色的溶剂合电子,如图为钠投入液氨中的溶剂化图。钠沉入液氨
中,快速得到深蓝色溶液,并慢慢产生气泡。下列说法错误的是
A.钠的密度比液氨大
B.溶液的导电性增强
C.钠和液氨可发生以下反应:2NH +2Na=2NaNH+H ↑
3 2 2
D.0.02mol钠投入足量液氨中充分反应生成0.224LH
2
11.根据下列实验操作和现象能得到相应正确的实验结论的是
选项 实验操作和现象 实验结论
A 向饱和碳酸氢钠溶液中加入新制氯水,有气体产生 新制氯水中含有HClO
将生锈的铁钉溶于过量的稀HSO ,向所得溶液中滴加酸 生锈的铁钉中含有
B 2 4
性KMnO 溶液,振荡,红色褪去 价的铁
4
C 用铂丝蘸取某溶液进行焰色试验,火焰呈黄色 该溶液为NaCl溶液
D 向淀粉-KI溶液中加入FeCl 溶液,溶液变蓝 氧化性:I < Fe3+
3 2
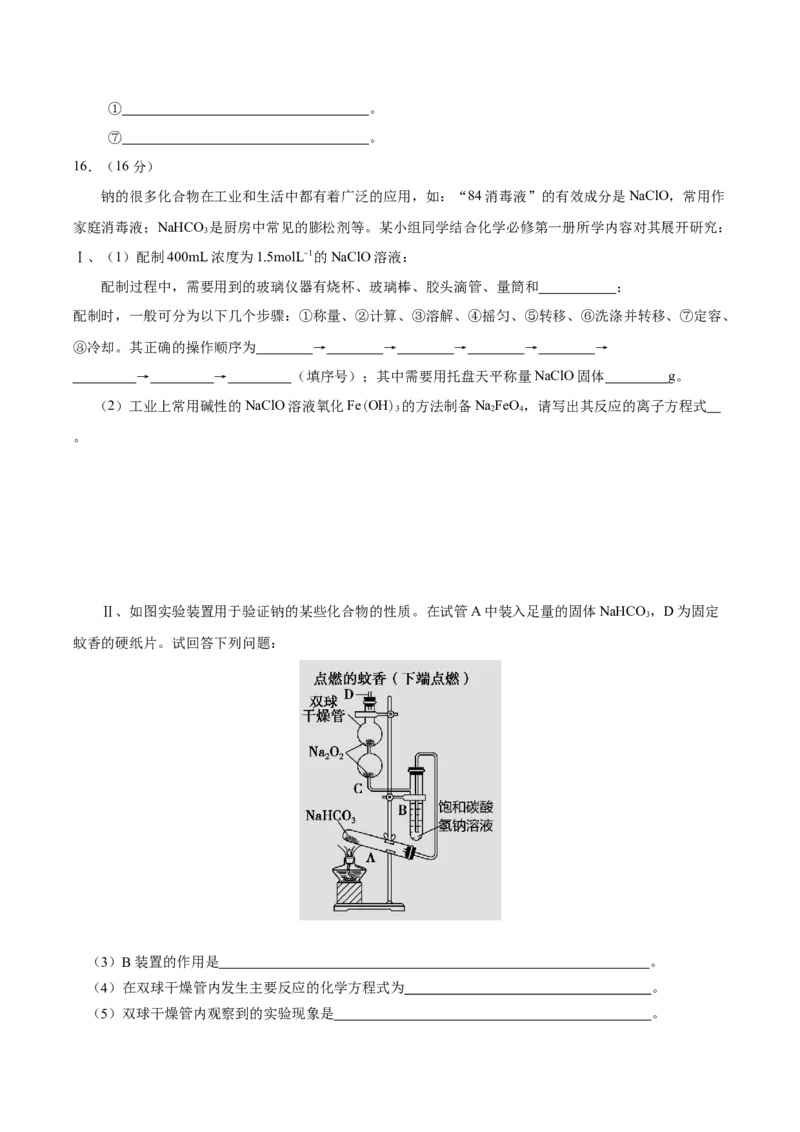
12.用下列装置进行相应实验,能达到实验目的是①甲用于实验室制取CO ②乙用于鉴别NaCO 和NaHCO
2 2 3 3
③丙用于比较碳酸钠和碳酸氢钠的热稳定性 ④丁用于从食盐水中提取氯化钠固体
A.②③ B.③ C.②④ D.①②
13.在反应3BrF+5HO===HBrO +Br +9HF+O↑中,若有15mol HO参加反应时,被水还原的BrF 的
3 2 3 2 2 2 3
物质的量为
A.9 mol B.6 mol C.4 mol D.10 mol
14.2020年9月,研究人员在金星大气中探测到了磷化氢(PH )气体。PH 常作为一种熏蒸剂,在贮粮
3 3
中用于防治害虫,一种制备PH 的流程如图所示:
3
下列说法正确的是
A.流程中,每一步均属于氧化还原反应
B.次磷酸的分子式为HPO ,在上述反应中只表现出氧化性
3 2
C.由上述信息可知:NaH PO 为酸式盐
2 2
D.白磷与浓NaOH溶液反应的化学方程式为:P+3NaOH(浓)+3H O PH ↑+3NaHPO
4 2 3 2 2
二、非选择题:本题共4小题,共58分。
15.(12分)
现有下列物质:①硫酸氢钠固体 ②铜丝 ③液氯 ④稀硫酸 ⑤二氧化碳气体
⑥氨水 ⑦碳酸氢钾粉末 ⑧蔗糖晶体 ⑨熔融氯化钠 ⑩CuSO 溶液
4
请用序号填空:
(1)上述状态下可导电的是 。
(2)属于电解质的是 。
(3)属于非电解质的是 。
(4)上述状态下的电解质不能导电的是 。
(5)分别写出①、⑦在水溶液中的电离方程式:① 。
⑦ 。
16.(16分)
钠的很多化合物在工业和生活中都有着广泛的应用,如:“84消毒液”的有效成分是NaClO,常用作
家庭消毒液;NaHCO 是厨房中常见的膨松剂等。某小组同学结合化学必修第一册所学内容对其展开研究:
3
Ⅰ、(1)配制400mL浓度为1.5molL-1的NaClO溶液:
配制过程中,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒和 ;
配制时,一般可分为以下几个步骤:①称量、②计算、③溶解、④摇匀、⑤转移、⑥洗涤并转移、⑦定容、
⑧冷却。其正确的操作顺序为 → → → → →
→ → (填序号);其中需要用托盘天平称量NaClO固体 g。
(2)工业上常用碱性的NaClO溶液氧化Fe(OH) 的方法制备NaFeO,请写出其反应的离子方程式
3 2 4
。
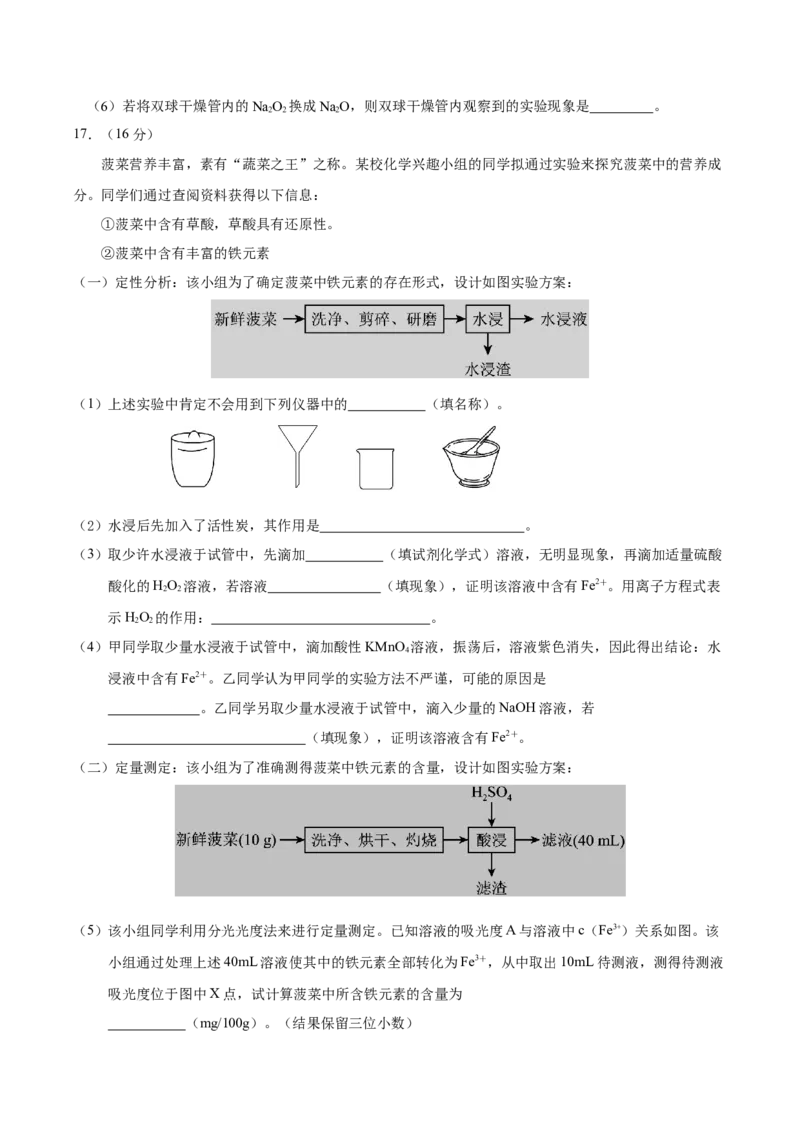
Ⅱ、如图实验装置用于验证钠的某些化合物的性质。在试管A中装入足量的固体NaHCO ,D为固定
3
蚊香的硬纸片。试回答下列问题:
(3)B装置的作用是 。
(4)在双球干燥管内发生主要反应的化学方程式为 。
(5)双球干燥管内观察到的实验现象是 。(6)若将双球干燥管内的NaO 换成NaO,则双球干燥管内观察到的实验现象是 。
2 2 2
17.(16分)
菠菜营养丰富,素有“蔬菜之王”之称。某校化学兴趣小组的同学拟通过实验来探究菠菜中的营养成
分。同学们通过查阅资料获得以下信息:
①菠菜中含有草酸,草酸具有还原性。
②菠菜中含有丰富的铁元素
(一)定性分析:该小组为了确定菠菜中铁元素的存在形式,设计如图实验方案:
(1)上述实验中肯定不会用到下列仪器中的 (填名称)。
(2)水浸后先加入了活性炭,其作用是 。
(3)取少许水浸液于试管中,先滴加 (填试剂化学式)溶液,无明显现象,再滴加适量硫酸
酸化的HO 溶液,若溶液 (填现象),证明该溶液中含有Fe2+。用离子方程式表
2 2
示HO 的作用: 。
2 2
(4)甲同学取少量水浸液于试管中,滴加酸性KMnO 溶液,振荡后,溶液紫色消失,因此得出结论:水
4
浸液中含有Fe2+。乙同学认为甲同学的实验方法不严谨,可能的原因是
。乙同学另取少量水浸液于试管中,滴入少量的NaOH溶液,若
(填现象),证明该溶液含有Fe2+。
(二)定量测定:该小组为了准确测得菠菜中铁元素的含量,设计如图实验方案:
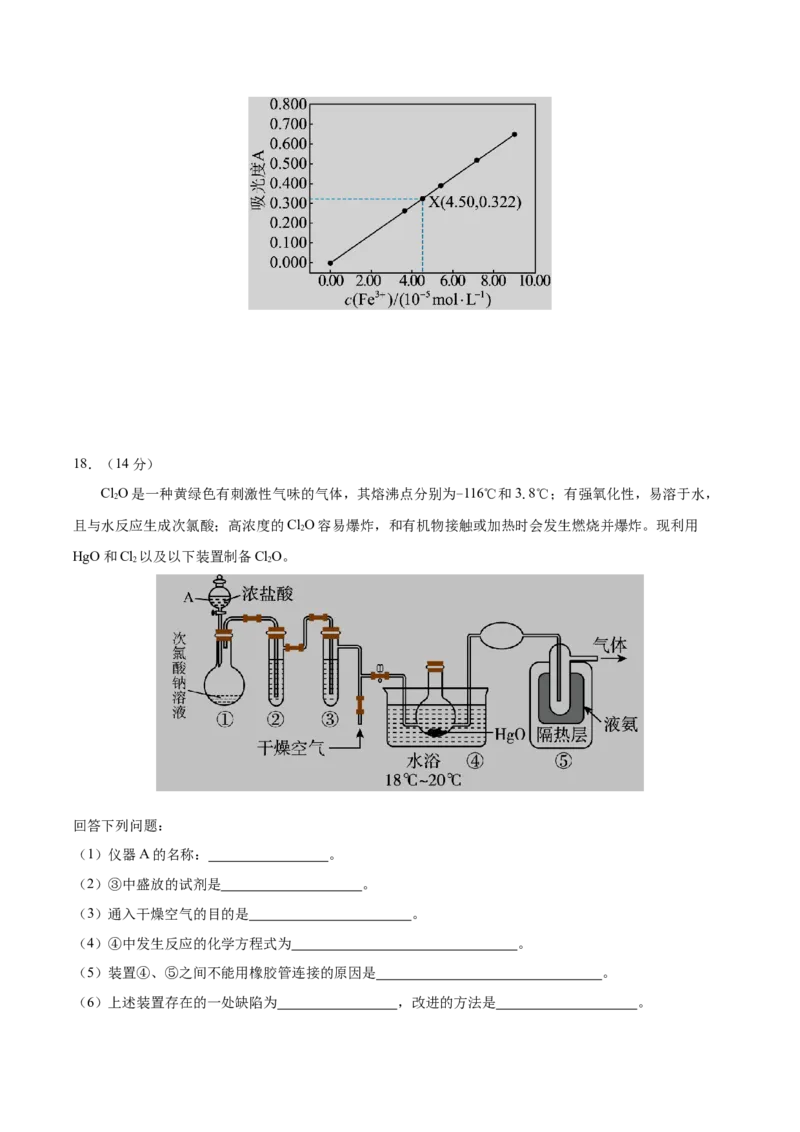
(5)该小组同学利用分光光度法来进行定量测定。已知溶液的吸光度A与溶液中c(Fe3+)关系如图。该
小组通过处理上述40mL溶液使其中的铁元素全部转化为Fe3+,从中取出10mL待测液,测得待测液
吸光度位于图中X点,试计算菠菜中所含铁元素的含量为
(mg/100g)。(结果保留三位小数)18.(14分)
ClO是一种黄绿色有刺激性气味的气体,其熔沸点分别为-116℃和3.8℃;有强氧化性,易溶于水,
2
且与水反应生成次氯酸;高浓度的ClO容易爆炸,和有机物接触或加热时会发生燃烧并爆炸。现利用
2
HgO和Cl 以及以下装置制备ClO。
2 2
回答下列问题:
(1)仪器A的名称: 。
(2)③中盛放的试剂是 。
(3)通入干燥空气的目的是 。
(4)④中发生反应的化学方程式为 。
(5)装置④、⑤之间不能用橡胶管连接的原因是 。
(6)上述装置存在的一处缺陷为 ,改进的方法是 。