文档内容
化学部分
相对原子质量:H-1
一、选择题(1~14每题均只有1个正确选项,15~17每题均有1~2个正确选项)
1. 我国科学家在嫦娥五号月壤中发现嫦娥石,属于陨磷钠镁钙石族。这里的“钙”指的是
A. 元素 B. 原子 C. 单质 D. 金属
【答案】A
【解析】
【详解】物质是由元素组成的,陨磷钠镁钙石族中的“钙”指的是钙元素,与具体形态无关。故选A。
2. 钙的元素符号是
A. C B. CA C. Ca D. Ga
【答案】C
【解析】
【详解】书写元素符号注意“一大二小”,钙的元素符号是Ca。故选C。
3. SO 中硫元素的化合价是
2
A. +1 B. +2 C. +3 D. +4
【答案】D
【解析】
【详解】SO 中氧元素化合价为-2价,设硫元素化合价为x,根据化合物中正负化合价代数为0,则有x+
2
(-2)×2=0,得x=+4价,故选D。
4. 含有原子团的物质是
A. Cu B. CuO C. CuCl D. Cu(OH)
2 2
【答案】D
【解析】
【详解】A、Cu中只含有铜元素一种元素,不含原子团,故选项错误;
B、CuO中只含有铜元素和氧元素,不含原子团,故选项错误;
C、CuCl 中只含有铜元素和氯元素,不含原子团,故选项错误;
2
D、Cu(OH) 中含有氢氧根,含有原子团,故选项正确。
2
故选D。
5. 属于空气污染物的是
A. N B. Ne C. CO D. SO
2 2 2
【答案】D
【解析】
第1页/共13页
学科网(北京)股份有限公司【详解】空气中各成分的体积分数分别是:氮气大约占78%、氧气大约占21%、稀有气体大约占0.94%、
二氧化碳大约占0.03%、水蒸气和其它气体和杂质大约占0.03%;目前计入空气质量评价的主要污染物为:
二氧化硫、一氧化碳、二氧化氮、可吸入颗粒物(粒径小于等于10微米的颗粒物,称PM )、细颗粒物
10
(粒径小于等于2.5微米的颗粒物,称PM )和臭氧等。N、 Ne、 CO 是空气的成分,二氧化硫属于空
2.5 2 2
气污染物。
故选D。
6. 属于稀有气体的是
A. H B. He C. O D. CO
2 2 2
【答案】B
【解析】
【详解】A、H 的名称是氢气,不属于稀有气体,故错误;
2
B、He的名称是氦气,是稀有气体之一,故正确;
C、O 的名称是氧气,不属于稀有气体,故错误;
2
D、CO 的名称是二氧化碳,不属于稀有气体,故错误。
2
故选B。
7. 在水的净化过程中,可用作消毒剂的是
A. 明矾 B. 液氯 C. 活性炭 D. 食盐
【答案】B
【解析】
【详解】A、明矾溶于水具有吸附凝聚沉淀的作用,不具有杀菌的作用,故错误;
B、液氯具有杀菌作用,常用于自来水消毒,故正确;
C、活性炭具有吸附性,恩能够吸附色素和异味,不具有杀菌的作用,故错误;
D、食盐可以消毒,但不能用于自来水消毒,故错误。
故选B。
8. 与石墨互为同素异形体的是
A. 木炭 B. 金刚石 C. 大理石 D. 煤炭
【答案】B
【解析】
【详解】同素异形体是同种元素形成的不同单质,与石墨互为同素异形体的是金刚石。
故选B。
9. 属于水的化学性质是
A. 可与酒精互溶 B. 密度大于酒精
C. 放入生石灰,产生大量热 D. 能吸收大量热量
第2页/共13页
学科网(北京)股份有限公司【答案】C
【解析】
【详解】A、水与酒精可以以任意比例混合,属于物质的溶解性,不需要通过化学变化表现出来,属于物
理性质;
B、密度大于酒精,不需要通过化学变化表现出来,属于物理性质;
C、生石灰和水反应生成氢氧化钙,产生大量热,需要通过化学变化表现出来,属于化学性质;
D、能吸收大量热量,不需要通过化学变化表现出来,属于物理性质。
故选C。
10. 粗盐提纯的操作中,正确的是
A. 漏斗下端尖嘴处紧靠烧杯内壁 B. 玻璃棒轻抵单层滤纸处
C. 漏斗内液面要低于漏斗边缘 D. 先放置蒸发皿,再调整铁圈高度
【答案】A
【解析】
【详解】A、过滤液体时,注意“一贴、二低、三靠”的原则,漏斗下端的尖嘴口紧靠烧杯内壁,故选项说
法正确;
B、过滤液体时,注意“一贴、二低、三靠”的原则,玻璃棒末端靠在漏斗内三层滤纸处,故选项说法错误;
C、过滤液体时,注意“一贴、二低、三靠”的原则,过滤时液面要低于滤纸边缘,故选项说法错误;
D、搭建蒸发装置时,一般按照从下到上的顺序进行,先放置酒精灯,再固定铁圈位置,并放上蒸发皿,
故选项说法错误。
故选A。
11. 将二氧化碳通入滴有紫色石蕊试液的试管中,再充分加热,溶液的颜色会
A. 先变红后变紫 B. 先褪色后变红 C. 先变红后褪色 D. 先变蓝后变紫
【答案】A
【解析】
【详解】紫色石蕊试液颜色为紫色,将二氧化碳通入滴有紫色石蕊试液的试管中,二氧化碳与水反应生成
碳酸,碳酸显酸性,可使紫色石蕊试液变红,碳酸不稳定,加热生成二氧化碳和水,二氧化碳气体逸出,
溶液变为紫色,故选:A。
12. 乙炔在氧气中燃烧可达360℃,常用于气焊和气割。使用氧气的目的是
A. 减少二氧化碳排放量 B. 供应足量的助燃剂,使乙炔充分燃烧
C. 降低乙炔的着火点 D. 减小乙炔分子间间隙
【答案】B
【解析】
【详解】A、乙炔在氧气中燃烧生成水和二氧化碳,不能减少二氧化碳排放量,选项错误;
第3页/共13页
学科网(北京)股份有限公司B、氧气具有助燃性,使用氧气可供应足量的助燃剂,使乙炔充分燃烧,选项正确;
C、物质着火点与物质本身有关,与氧气无关,选项错误;
D、分子间间隙与温度,压强等有关,与是否使用氧气无关,选项错误。
故选B。
13. “酒精温度计遇热,酒精液柱上升”的微观解释正确的是
A. 酒精分子有规则运动 B. 酒精分子体积变大
C. 酒精分子质量变小 D. 酒精分子间间隙变大
【答案】D
【解析】
【详解】A、酒精分子做无规则运动,故A错误;
B、该变化是物理变化,酒精分子体积不变,故B错误;
C、该变化是物理变化,酒精分子质量不变,故C错误;
D、酒精温度计遇热,酒精液柱上升,是由于温度升高,酒精分子间间隔变大,酒精液体体积增大,故D
正确。
故选:D。
14. 分别用三角形表示氧化物、方形表示化合物、圆形表示混合物,能正确描述这三类物质关系的图是
A. B. C. D.
【答案】C
【解析】
【详解】物质分为纯净物和混合物,纯净物分为单质和化合物,化合物分为氧化物等,观察图中关系,只
有C项正确。故选C。
15. 对氧气的认识正确的是
A. 空气中氧气的质量分数约为 B. 空气中氧气的体积分数约为
C. 木炭在空气中燃烧比在氧气中燃烧更旺 D. 铁丝在空气中剧烈燃烧
【答案】B
【解析】
【详解】A、空气中氧气的体积分数约为 ,故说法错误;
B、空气中氧气的体积分数约为 ,故说法正确;
C、木炭在氧气中比在空气中燃烧更旺,发出白光,并放出热量,故说法错误;
第4页/共13页
学科网(北京)股份有限公司D、铁丝在空气中只能烧至发红,不会产生火星,故说法错误。
故选B。
16. 一定能增大二氧化碳在水中溶解度的操作是
A. 升温 B. 加压 C. 降温加压 D. 升温加压
【答案】C
【解析】
【详解】气体的溶解度主要受温度和压强的影响,气体的溶解度随温度的升高而减小,随着压强的增大而
增大,因此一定能增大二氧化碳在水中溶解度的操作是降温加压。
故选C。
的
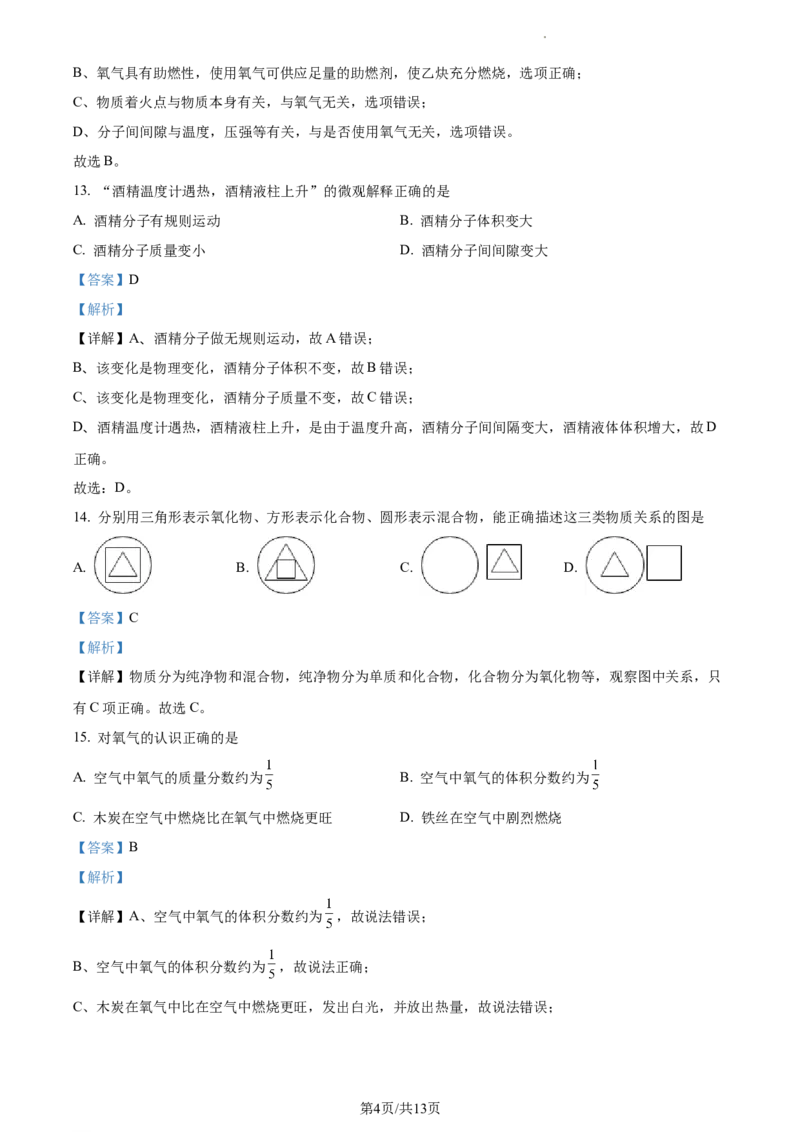
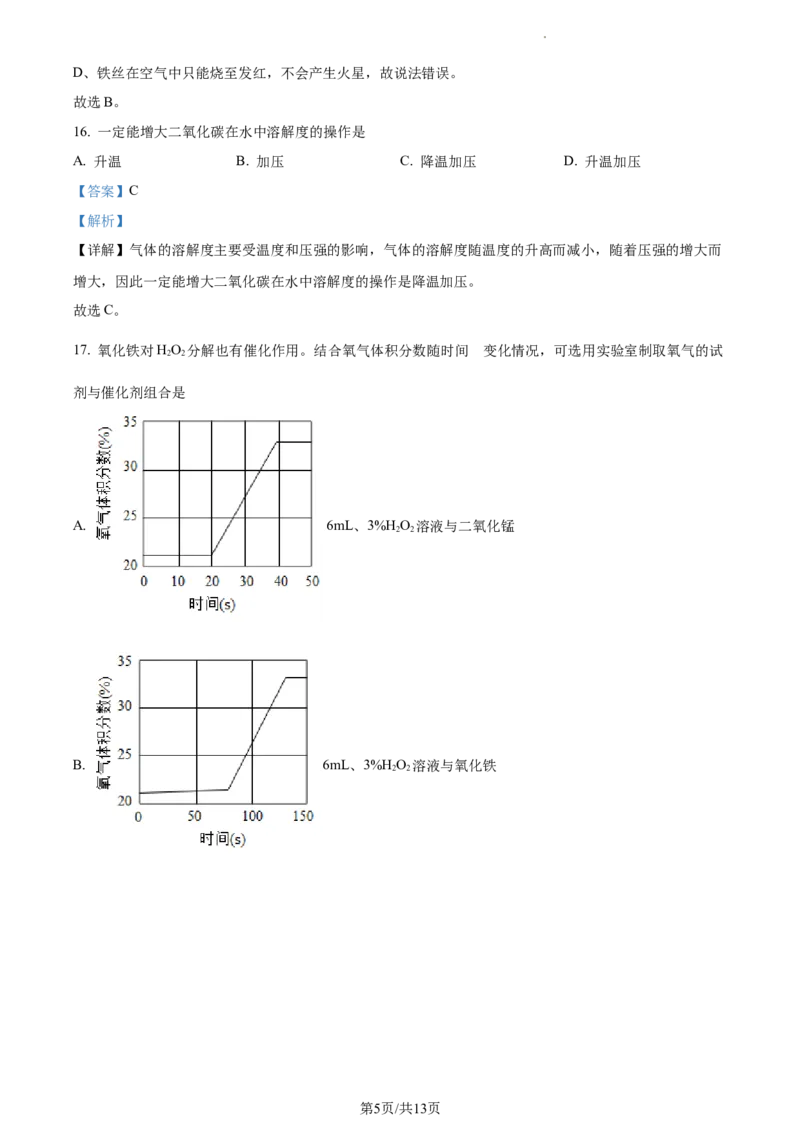
17. 氧化铁对HO 分解也有催化作用。结合氧气体积分数随时间 变化情况,可选用实验室制取氧气的试
2 2
剂与催化剂组合是
A. 6mL、3%H O 溶液与二氧化锰
2 2
B. 6mL、3%H O 溶液与氧化铁
2 2
第5页/共13页
学科网(北京)股份有限公司C. 3mL、6%H O 溶液与二氧化锰
2 2
D. 3mL、6%H O 溶液与氧化铁
2 2
【答案】AD
【解析】
【详解】A、6mL、3%H O 溶液与二氧化锰在大约20秒时产生氧气,速率适中,可用于实验室制取氧气;
2 2
B、6mL、3%H O 溶液与氧化铁在大约80秒时产生氧气,速率太慢,不可用于实验室制取氧气;
2 2
C、3mL、6%H O 溶液与二氧化锰在大约3秒时产生氧气,速率太快,不可用于实验室制取氧气;
2 2
D、3mL、6%H O 溶液与氧化铁在大约20几秒时产生氧气,速率适中,可用于实验室制取氧气。
2 2
故选AD。
六、简答题(共30分)
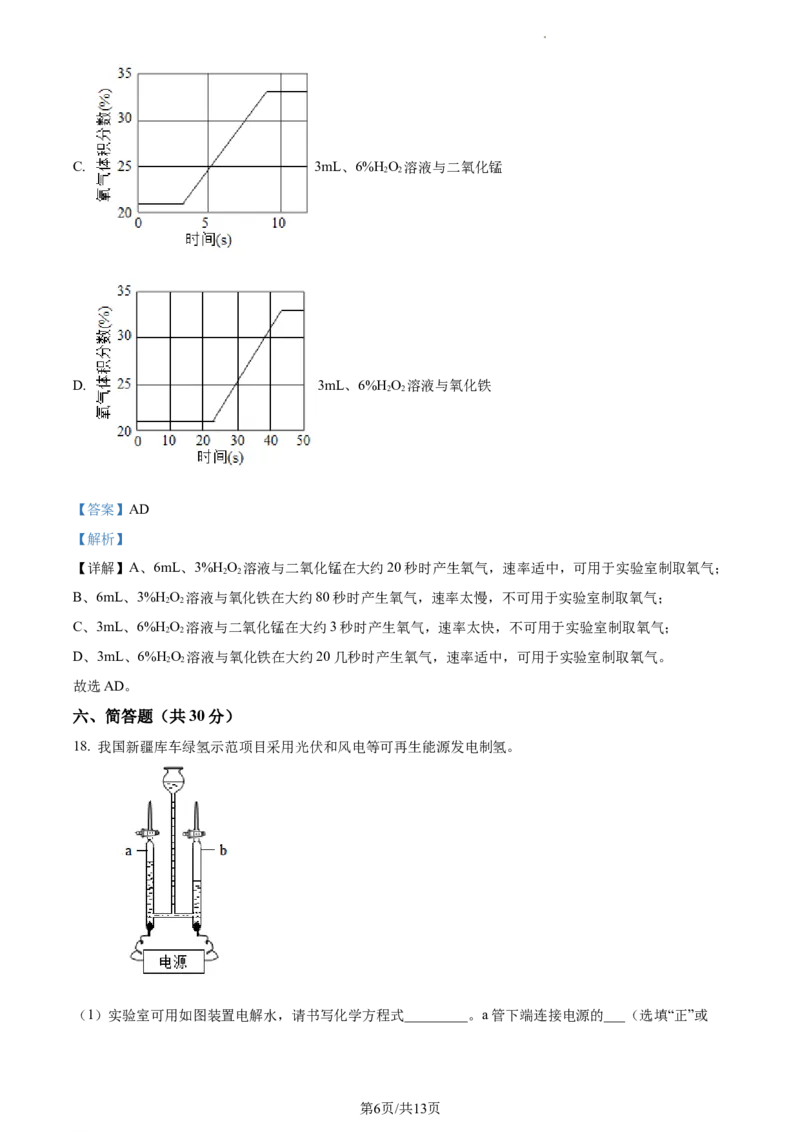
18. 我国新疆库车绿氢示范项目采用光伏和风电等可再生能源发电制氢。
(1)实验室可用如图装置电解水,请书写化学方程式_________。a管下端连接电源的___(选填“正”或
第6页/共13页
学科网(北京)股份有限公司“负”)极,生成氢气与氧气的体积比为________;
(2)生成的氢气可与氧气通过氢燃料电池,将化学能直接转换成电能。1mol H 中约含有________个氢分
2
子,H 的摩尔质量为________;
2
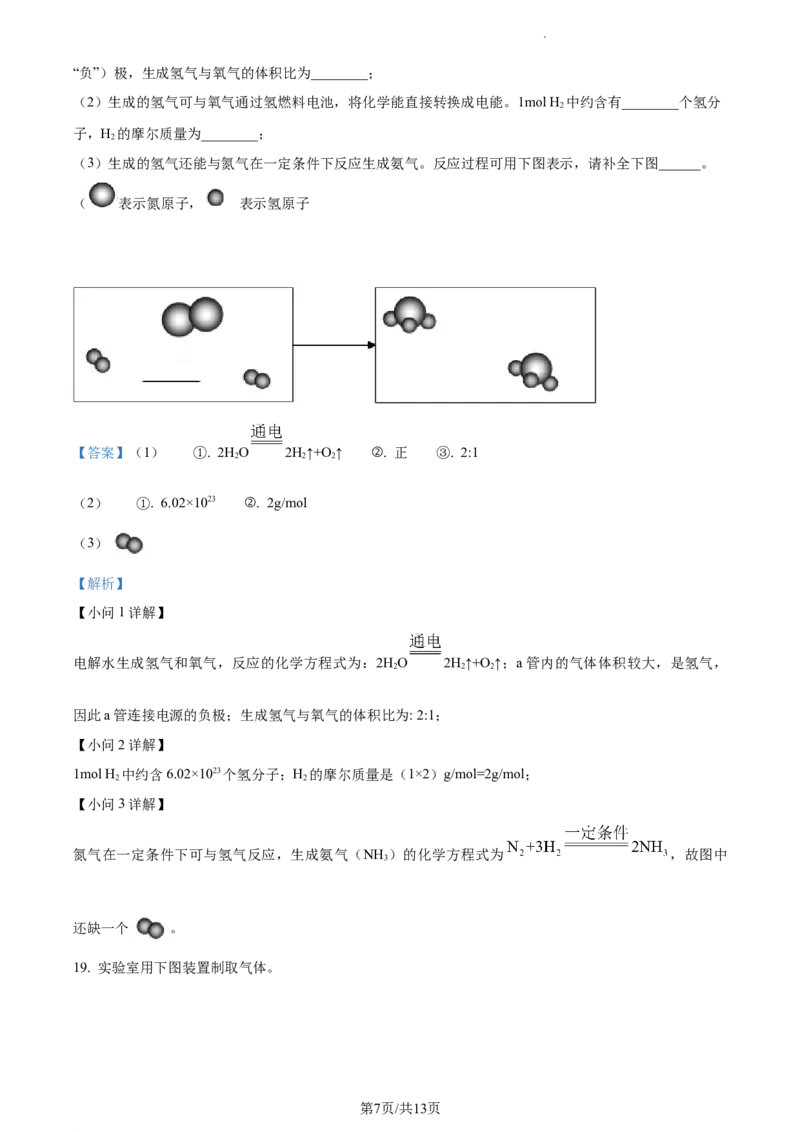
(3)生成的氢气还能与氮气在一定条件下反应生成氨气。反应过程可用下图表示,请补全下图______。
( 表示氮原子, 表示氢原子
【答案】(1) ①. 2HO 2H↑+O ↑ ②. 正 ③. 2:1
2 2 2
(2) ①. 6.02×1023 ②. 2g/mol
(3)
【解析】
【小问1详解】
电解水生成氢气和氧气,反应的化学方程式为:2HO 2H↑+O ↑;a管内的气体体积较大,是氢气,
2 2 2
因此a管连接电源的负极;生成氢气与氧气的体积比为: 2:1;
【小问2详解】
1mol H 中约含6.02×1023个氢分子;H 的摩尔质量是(1×2)g/mol=2g/mol;
2 2
【小问3详解】
氮气在一定条件下可与氢气反应,生成氨气(NH )的化学方程式为 ,故图中
3
还缺一个 。
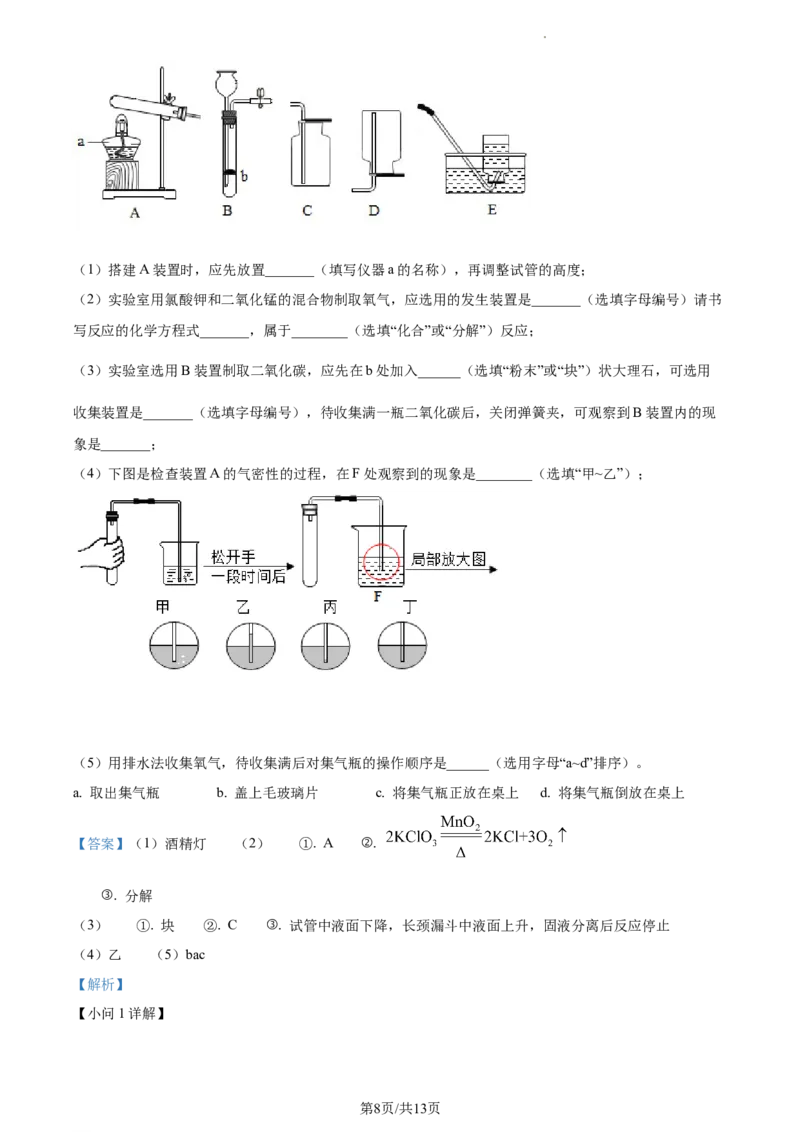
19. 实验室用下图装置制取气体。
第7页/共13页
学科网(北京)股份有限公司(1)搭建A装置时,应先放置_______(填写仪器a的名称),再调整试管的高度;
(2)实验室用氯酸钾和二氧化锰的混合物制取氧气,应选用的发生装置是_______(选填字母编号)请书
写反应的化学方程式_______,属于________(选填“化合”或“分解”)反应;
的
(3)实验室选用B装置制取二氧化碳,应先在b处加入______(选填“粉末”或“块”)状大理石,可选用
收集装置是_______(选填字母编号),待收集满一瓶二氧化碳后,关闭弹簧夹,可观察到B装置内的现
象是_______;
(4)下图是检查装置A的气密性的过程,在F处观察到的现象是________(选填“甲~乙”);
(5)用排水法收集氧气,待收集满后对集气瓶的操作顺序是______(选用字母“a~d”排序)。
a. 取出集气瓶 b. 盖上毛玻璃片 c. 将集气瓶正放在桌上 d. 将集气瓶倒放在桌上
【答案】(1)酒精灯 (2) ①. A ②.
③. 分解
(3) ①. 块 ②. C ③. 试管中液面下降,长颈漏斗中液面上升,固液分离后反应停止
(4)乙 (5)bac
【解析】
【小问1详解】
第8页/共13页
学科网(北京)股份有限公司组装仪器时,正确的组装顺序为从下到上,从左到右,故搭建A装置时,应先放置酒精灯,再调整试管的
高度;
【小问2详解】
实验室用氯酸钾和二氧化锰制取氧气,属于固体加热反应,发生装置可选A;
氯酸钾在二氧化锰 的催化下受热分解生成氯化钾和氧气,该反应的化学方程式为:
;
该反应符合“一变多”的特点,属于分解反应;
【小问3详解】
实验室通常用石灰石(或大理石)与稀盐酸反应制取二氧化碳,选用B装置制取二氧化碳,B装置适用于
块状固体和液体的反应,应将块状大理石置于b处;
二氧化碳溶于水,密度比空气大,可用向上排空气法收集,收集装置可选C;
待收集满一瓶二氧化碳后,关闭弹簧夹,装置内压强增大,将液体压入长颈漏斗中,固液分离,反应停止,
故现象是:试管中液面下降,长颈漏斗中液面上升,固液分离后反应停止;
【小问4详解】
检查装置A的气密性:将导管置于水中,用手紧握试管,试管内气体受热膨胀逸出,松开手后,试管内温
度降低,压强减小,故导管内液面上升,故观察到的现象是:乙;
【小问5详解】
用排水法收集氧气,待收集满后对集气瓶的操作顺序是:在水下盖上玻璃片,将集气瓶取出,氧气的密度
比空气大,故将集气瓶正放在桌面上,故顺序是:bac。
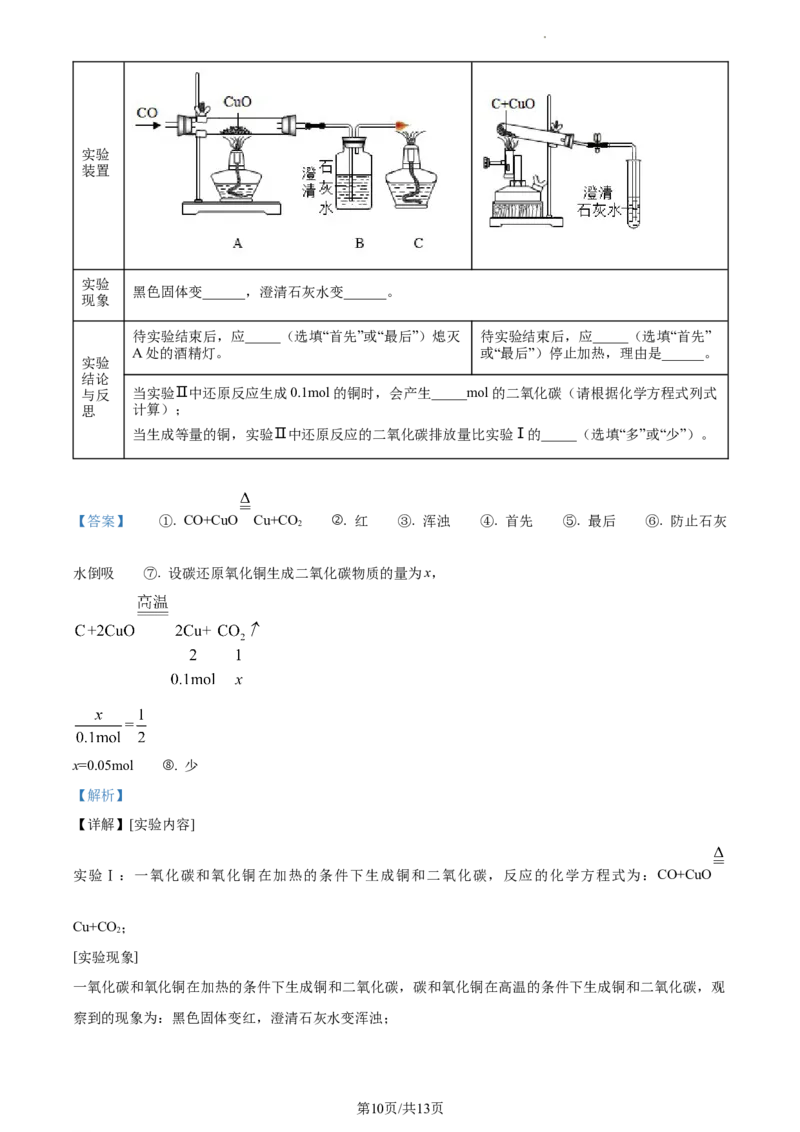
20. 对比分析是有效的学习方法。
实验
实验Ⅰ:一氧化碳还原氧化铜 实验Ⅱ:木炭还原氧化铜
内容
反应
_______(请书写化学方程式) C+2CuO 2Cu+CO ↑
原理 2
第9页/共13页
学科网(北京)股份有限公司实验
装置
实验
黑色固体变______,澄清石灰水变______。
现象
待实验结束后,应_____(选填“首先”或“最后”)熄灭 待实验结束后,应_____(选填“首先”
A处的酒精灯。 或“最后”)停止加热,理由是______。
实验
结论
与反 当实验Ⅱ中还原反应生成0.1mol的铜时,会产生_____mol的二氧化碳(请根据化学方程式列式
思 计算);
当生成等量的铜,实验Ⅱ中还原反应的二氧化碳排放量比实验Ⅰ的_____(选填“多”或“少”)。
【答案】 ①. CO+CuO Cu+CO ②. 红 ③. 浑浊 ④. 首先 ⑤. 最后 ⑥. 防止石灰
2
水倒吸 ⑦. 设碳还原氧化铜生成二氧化碳物质的量为x,
x=0.05mol ⑧. 少
【解析】
【详解】[实验内容]
实验Ⅰ:一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳,反应的化学方程式为:CO+CuO
Cu+CO ;
2
[实验现象]
一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳,碳和氧化铜在高温的条件下生成铜和二氧化碳,观
察到的现象为:黑色固体变红,澄清石灰水变浑浊;
第10页/共13页
学科网(北京)股份有限公司[实验结论与反思]
实验Ⅰ:防止高温下铜又被进入的空气氧化,实验结束后,应先停止加热玻璃管,继续通入CO直至冷却
至室温;
实验Ⅱ:若先撤酒精灯试管中的气体冷却使试管内的气体压强小于外界大气压,右边试管中的澄清石灰水
会倒流入试管,试管比较热遇到冷的液体会炸裂;
见答案;
根据反应关系 、 可知,实验Ⅱ中还原反应的二氧化碳
排放量比实验Ⅰ的少。
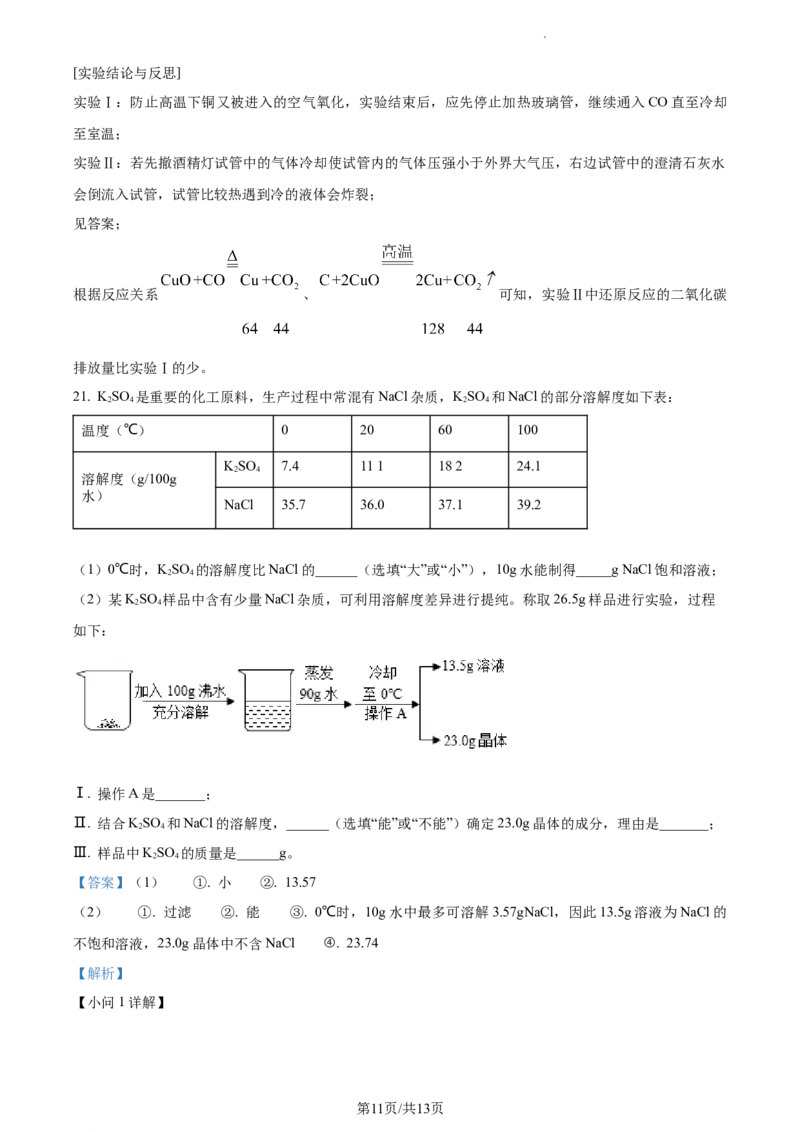
21. KSO 是重要的化工原料,生产过程中常混有NaCl杂质,KSO 和NaCl的部分溶解度如下表:
2 4 2 4
温度(℃) 0 20 60 100
. .
KSO 7.4 111 182 24.1
2 4
溶解度(g/100g
水)
NaCl 35.7 36.0 37.1 39.2
(1)0℃时,KSO 的溶解度比NaCl的______(选填“大”或“小”),10g水能制得_____g NaCl饱和溶液;
2 4
(2)某KSO 样品中含有少量NaCl杂质,可利用溶解度差异进行提纯。称取26.5g样品进行实验,过程
2 4
如下:
Ⅰ. 操作A是_______;
Ⅱ. 结合KSO 和NaCl的溶解度,______(选填“能”或“不能”)确定23.0g晶体的成分,理由是_______;
2 4
Ⅲ. 样品中KSO 的质量是______g。
2 4
【答案】(1) ①. 小 ②. 13.57
(2) ①. 过滤 ②. 能 ③. 0℃时,10g水中最多可溶解3.57gNaCl,因此13.5g溶液为NaCl的
不饱和溶液,23.0g晶体中不含NaCl ④. 23.74
【解析】
【小问1详解】
第11页/共13页
学科网(北京)股份有限公司根据表格中数据可知,0℃时,KSO 的溶解度比NaCl的小;10g水能制得 NaCl饱和溶液质量=
2 4
;
【小问2详解】
Ⅰ. 根据流程图可知,操作A能将晶体(固体)和溶液(液体)分离了,是过滤;
Ⅱ. 结合KSO 和NaCl的溶解度,能确定23.0g晶体的成分,理由是0℃时,10g水中最多可溶解
2 4
3.57gNaCl,因此13.5g溶液为NaCl的不饱和溶液,23.0g晶体中不含NaCl;
Ⅲ.根据硫酸钾的溶解度可知,0℃时,10g水中最多可溶解0.74gK SO ,样品中KSO 的质量
2 4 2 4
=23g+0.74g=23.74g。
第12页/共13页
学科网(北京)股份有限公司第13页/共13页
学科网(北京)股份有限公司