文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
华东师大二附中 2022 学年第二学期期中考试卷
高二 化学
(考试时间:60分钟卷面满分:100分)
可能用到的原子量:H 1 C 12 O 16
一、选择题(每题只有一个答案,本题共 40分)
1. 下列说法正确的是
A. 油脂的皂化反应属于加成反应
B. 多次盐析和溶解可以分离提纯蛋白质
C. 在酒化酶的作用下葡萄糖水解为乙醇和二氧化碳
D. 乙酸、汽油、纤维素均能和氢氧化钠溶液反应
2. 为了除去MgCl 酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种试剂,过滤后,再向滤液中加入适
2
量的盐酸,这种试剂是
A. NaOH B. Na CO C. NH •H O D. MgCO
2 3 3 2 3
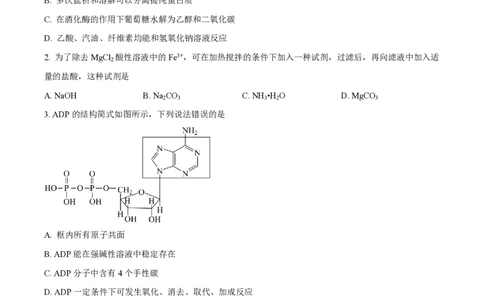
3. ADP的结构简式如图所示,下列说法错误的是
A. 框内所有原子共面
B. ADP能在强碱性溶液中稳定存在
C. ADP分子中含有4个手性碳
D. ADP一定条件下可发生氧化、消去、取代、加成反应
4. 下列实验能达到实验目的的是
第 1 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 制作简单的燃料电池 B. 证明苯环使羟基活化
C. 制备并收集NO D. 检验溴乙烷的水解产物Br-
2
5. 2021年诺贝尔化学奖颁给了“在不对称催化方面”做出贡献的两位科学家。脯氨酸(结构如图)可参与诱导不
对称催化反应,下列关于肺氨酸的说法错误的是
A. 既可以与酸反应,又可以与碱反应 B. 饱和碳原子上的一氯代物有3种
C. 分子间可以发生缩聚反应 D. 与 互为同分异构体
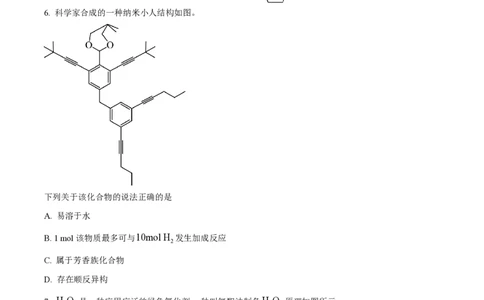
6. 科学家合成的一种纳米小人结构如图。
下列关于该化合物的说法正确的是
A. 易溶于水
B. 1 mol该物质最多可与10mol H 发生加成反应
2
C. 属于芳香族化合物
D. 存在顺反异构
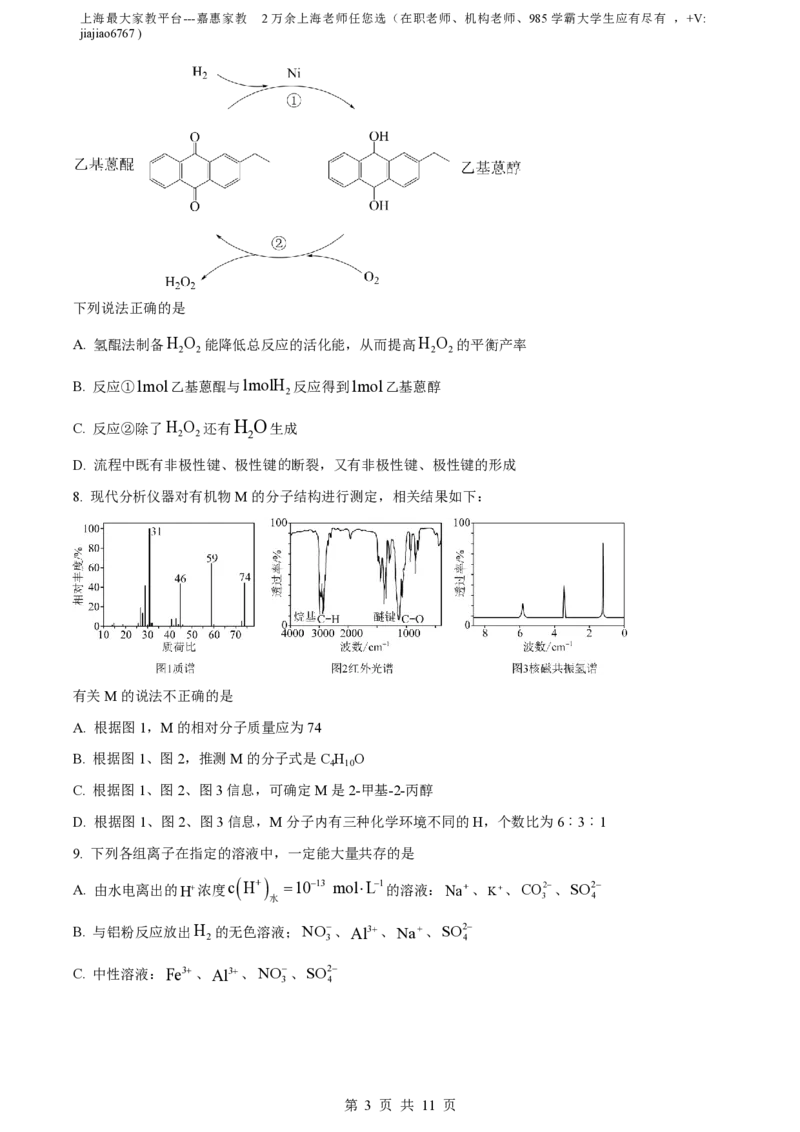
7. H O 是一种应用广泛的绿色氧化剂.一种叫氢醌法制备H O 原理如图所示:
2 2 2 2
第 2 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
下列说法正确的是
A. 氢醌法制备H O 能降低总反应的活化能,从而提高H O 的平衡产率
2 2 2 2
B. 反应①1mol乙基蒽醌与1molH 反应得到1mol乙基蒽醇
2
C. 反应②除了H O 还有H O生成
2 2 2
D. 流程中既有非极性键、极性键的断裂,又有非极性键、极性键的形成
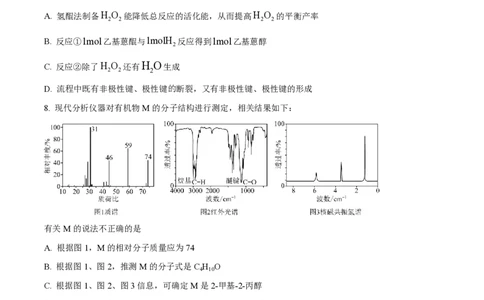
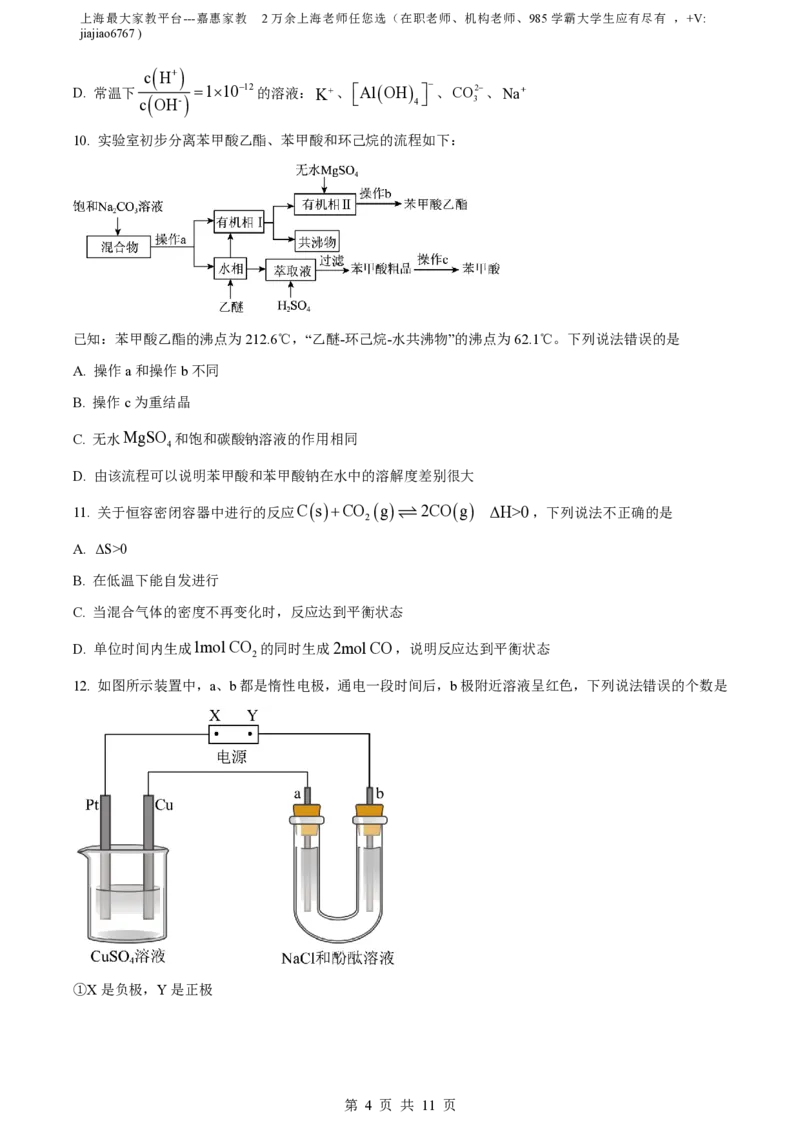
8. 现代分析仪器对有机物M的分子结构进行测定,相关结果如下:
有关M的说法不正确的是
A. 根据图1,M的相对分子质量应为74
B. 根据图1、图2,推测M的分子式是C H O
4 10
C. 根据图1、图2、图3信息,可确定M是2-甲基-2-丙醇
D. 根据图1、图2、图3信息,M分子内有三种化学环境不同的H,个数比为6︰3︰1
9. 下列各组离子在指定的溶液中,一定能大量共存的是
A. 由水电离出的H浓度c H+ 1013 molL1 的溶液:Na+、K+、CO2、SO2
水 3 4
B. 与铝粉反应放出H 的无色溶液;NO、Al3、Na、SO2
2 3 4
C. 中性溶液:Fe3、Al3、NO、SO2
3 4
第 3 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
c
H+
D. 常温下 11012的溶液:K、AlOH 、CO2、Na+
c OH- 4 3
10. 实验室初步分离苯甲酸乙酯、苯甲酸和环己烷的流程如下:
已知:苯甲酸乙酯的沸点为212.6℃,“乙醚-环己烷-水共沸物”的沸点为62.1℃。下列说法错误的是
A. 操作a和操作b不同
B. 操作c为重结晶
C. 无水MgSO 和饱和碳酸钠溶液的作用相同
4
D. 由该流程可以说明苯甲酸和苯甲酸钠在水中的溶解度差别很大
11.
关于恒容密闭容器中进行的反应CsCO
2
g
2COg
ΔH>0,下列说法不正确的是
A. ΔS>0
B. 在低温下能自发进行
C. 当混合气体的密度不再变化时,反应达到平衡状态
D. 单位时间内生成1mol CO 的同时生成2mol CO,说明反应达到平衡状态
2
12. 如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,下列说法错误的个数是
①X是负极,Y是正极
第 4 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
②若用右侧装置(电解液改为CuSO 溶液)在钥匙上镀铜,则将钥匙放在b处
4
③CuSO 溶液的酸性先增强,当铜电极有气泡产生时,此后一段时间酸性会继续增强
4
④若用右侧装置(电解液改为CuSO 溶液)精炼粗铜时,则将粗铜放在b处
4
A. 1个 B. 2个 C. 3个 D. 4个
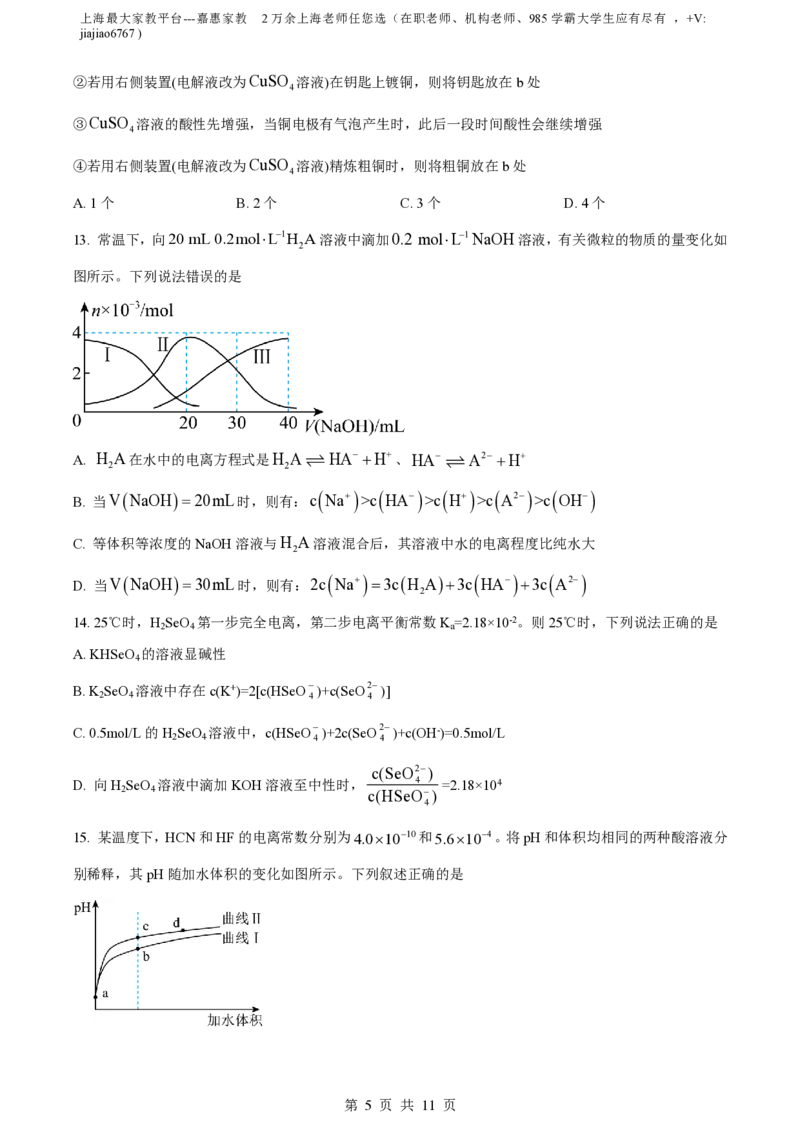
13. 常温下,向20 mL 0.2molL1H A溶液中滴加0.2 molL1NaOH溶液,有关微粒的物质的量变化如
2
图所示。下列说法错误的是
A. H 2 A在水中的电离方程式是H 2 A HA H、HA A2 H
B. 当VNaOH20mL时,则有:c Na >c HA >c H >c A2 >c OH
C. 等体积等浓度的NaOH溶液与H A溶液混合后,其溶液中水的电离程度比纯水大
2
D. 当VNaOH30mL时,则有:2c Na 3cH A3c HA 3c A2
2
14. 25℃时,H SeO 第一步完全电离,第二步电离平衡常数K =2.18×10-2。则25℃时,下列说法正确的是
2 4 a
A. KHSeO 的溶液显碱性
4
B. K SeO 溶液中存在c(K+)=2[c(HSeO)+c(SeO2)]
2 4 4 4
C. 0.5mol/L的H SeO 溶液中,c(HSeO)+2c(SeO2)+c(OH-)=0.5mol/L
2 4 4 4
c(SeO2)
D. 向H SeO 溶液中滴加KOH溶液至中性时, 4 =2.18×104
2 4 c(HSeO)
4
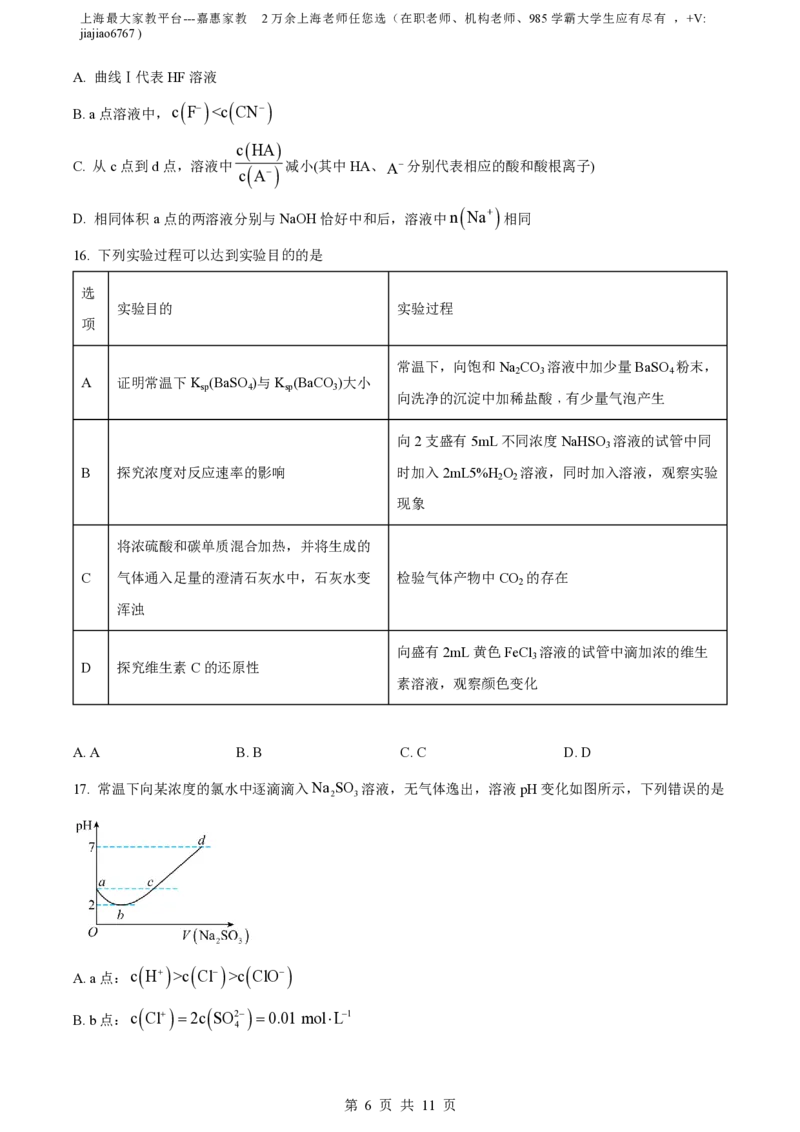
15. 某温度下,HCN和HF的电离常数分别为4.01010和5.6104。将pH和体积均相同的两种酸溶液分
别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
第 5 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 曲线Ⅰ代表HF溶液
B. a点溶液中,c
F
c
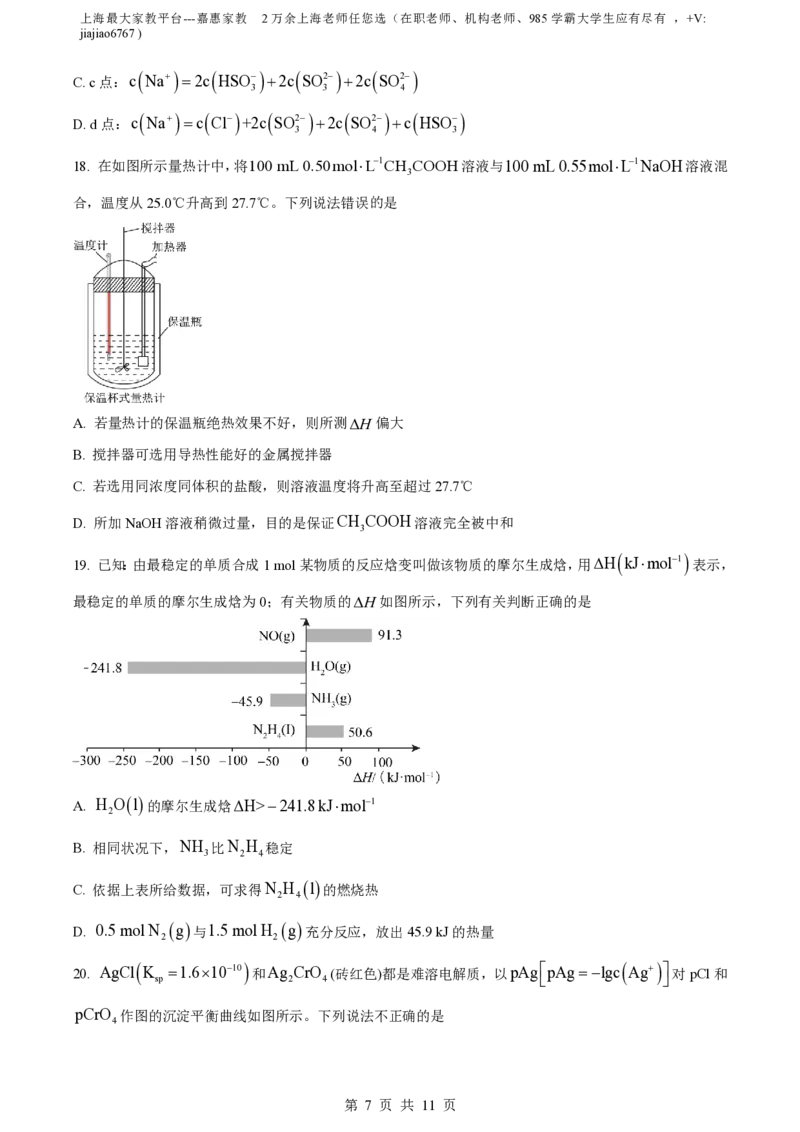
Cl
>c
ClO
B. b点:c Cl 2c SO2 0.01 molL1
4
第 6 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
C. c点:c
Na
2c
HSO
2c
SO2
2c
SO2
3 3 4
D. d点:c
Na
c
Cl
+2c
SO2
2c
SO2
c
HSO
3 4 3
18. 在如图所示量热计中,将100 mL 0.50molL1CH COOH溶液与100 mL 0.55molL1NaOH溶液混
3
合,温度从25.0℃升高到27.7℃。下列说法错误的是
A. 若量热计的保温瓶绝热效果不好,则所测H 偏大
B. 搅拌器可选用导热性能好的金属搅拌器
C. 若选用同浓度同体积的盐酸,则溶液温度将升高至超过27.7℃
D. 所加NaOH溶液稍微过量,目的是保证CH COOH溶液完全被中和
3
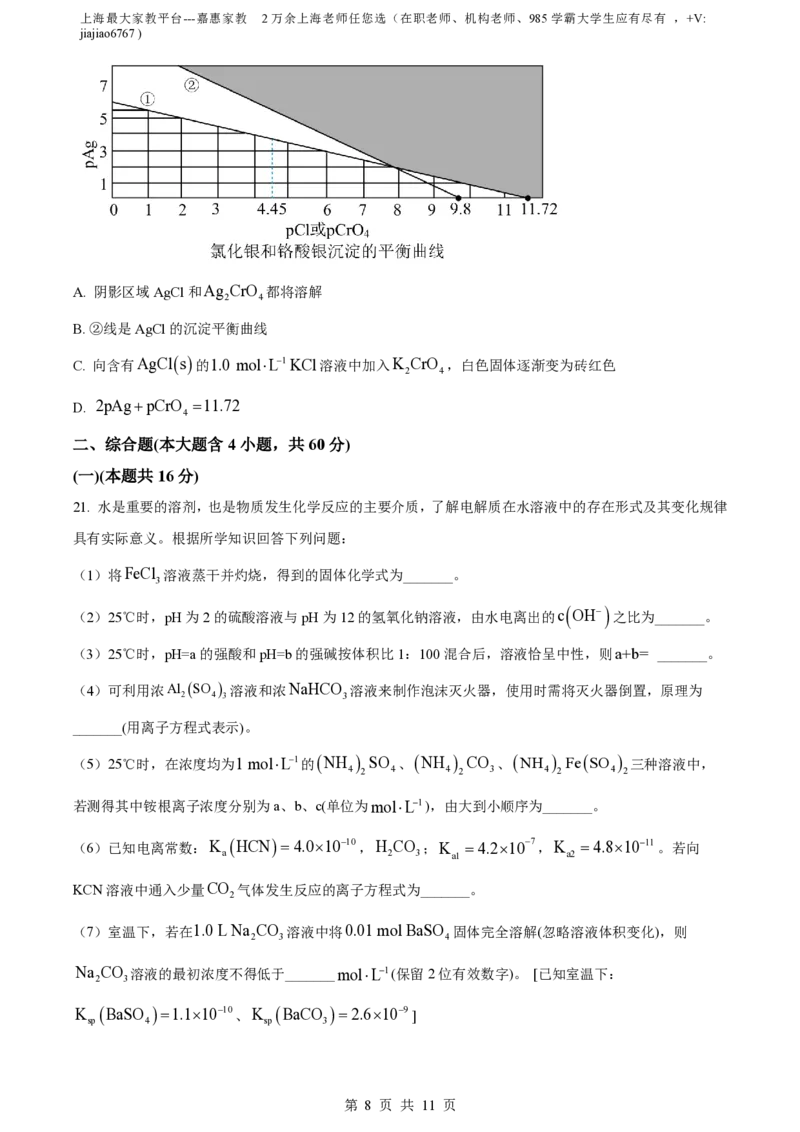
19. 已知:由最稳定的单质合成1 mol某物质的反应焓变叫做该物质的摩尔生成焓,用ΔH
kJmol1
表示,
最稳定的单质的摩尔生成焓为0;有关物质的H 如图所示,下列有关判断正确的是
A. H Ol 的摩尔生成焓ΔH>241.8kJmol1
2
B. 相同状况下,NH 比N H 稳定
3 2 4
C. 依据上表所给数据,可求得N H l 的燃烧热
2 4
D. 0.5 mol N g 与1.5 mol H g 充分反应,放出45.9 kJ的热量
2 2
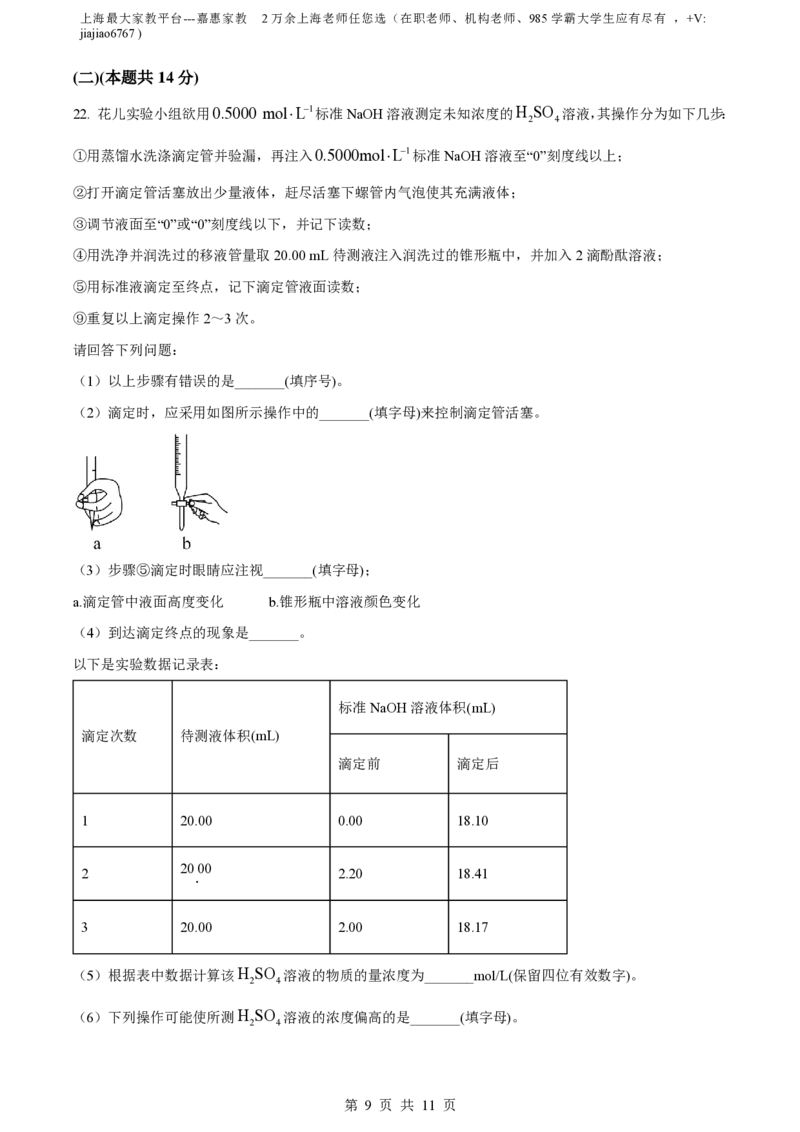
20. AgCl K 1.61010 和Ag CrO (砖红色)都是难溶电解质,以pAgpAg lgc Ag对pCl和
sp 2 4
pCrO 作图的沉淀平衡曲线如图所示。下列说法不正确的是
4
第 7 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 阴影区域AgCl和Ag CrO 都将溶解
2 4
B. ②线是AgCl的沉淀平衡曲线
C. 向含有AgCls 的1.0 molL1KCl溶液中加入K CrO ,白色固体逐渐变为砖红色
2 4
D. 2pAgpCrO 11.72
4
二、综合题(本大题含 4小题,共 60分)
(一)(本题共 16分)
21. 水是重要的溶剂,也是物质发生化学反应的主要介质,了解电解质在水溶液中的存在形式及其变化规律
具有实际意义。根据所学知识回答下列问题:
(1)将FeCl 溶液蒸干并灼烧,得到的固体化学式为_______。
3
(2)25℃时,pH为2的硫酸溶液与pH为12的氢氧化钠溶液,由水电离出的c
OH
之比为_______。
(3)25℃时,pH=a的强酸和pH=b的强碱按体积比1:100混合后,溶液恰呈中性,则a+b= _______。
(4)可利用浓Al SO 溶液和浓NaHCO 溶液来制作泡沫灭火器,使用时需将灭火器倒置,原理为
2 4 3 3
_______(用离子方程式表示)。
(5)25℃时,在浓度均为1 molL1的 NH SO 、 NH CO 、 NH FeSO 三种溶液中,
4 2 4 4 2 3 4 2 4 2
若测得其中铵根离子浓度分别为a、b、c(单位为molL1),由大到小顺序为_______。
(6)已知电离常数:K HCN4.01010,H CO ;K 4.210 7,K 4.81011。若向
a 2 3 a1 a2
KCN溶液中通入少量CO 气体发生反应的离子方程式为_______。
2
(7)室温下,若在1.0 L Na CO 溶液中将0.01 mol BaSO 固体完全溶解(忽略溶液体积变化),则
2 3 4
Na CO 溶液的最初浓度不得低于_______molL1(保留2位有效数字)。 [已知室温下:
2 3
K BaSO 1.11010、K BaCO 2.6109 ]
sp 4 sp 3
第 8 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(二)(本题共 14分)
22. 花儿实验小组欲用0.5000 molL1标准NaOH溶液测定未知浓度的H SO 溶液,其操作分为如下几步:
2 4
①用蒸馏水洗涤滴定管并验漏,再注入0.5000molL1标准NaOH溶液至“0”刻度线以上;
②打开滴定管活塞放出少量液体,赶尽活塞下螺管内气泡使其充满液体;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④用洗净并润洗过的移液管量取20.00 mL待测液注入润洗过的锥形瓶中,并加入2滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数;
⑨重复以上滴定操作2~3次。
请回答下列问题:
(1)以上步骤有错误的是_______(填序号)。
(2)滴定时,应采用如图所示操作中的_______(填字母)来控制滴定管活塞。
(3)步骤⑤滴定时眼睛应注视_______(填字母);
a.滴定管中液面高度变化 b.锥形瓶中溶液颜色变化
(4)到达滴定终点的现象是_______。
以下是实验数据记录表:
标准NaOH溶液体积(mL)
滴定次数 待测液体积(mL)
滴定前 滴定后
1 20.00 0.00 18.10
2000
2 . 2.20 18.41
3 20.00 2.00 18.17
(5)根据表中数据计算该H SO 溶液的物质的量浓度为_______mol/L(保留四位有效数字)。
2 4
(6)下列操作可能使所测H SO 溶液的浓度偏高的是_______(填字母)。
2 4
第 9 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A、锥形瓶装液前,留有少量蒸馏水
B、滴定管盛装标准液前未润洗
C、滴定前滴定管尖嘴有气泡,滴定结束无气泡
D、滴定过程中刚变色就立即停止滴定
E、接近滴定终点时滴定速度过快
F、滴定前平视读数,滴定后仰视读数
(三)(本题共 13分)
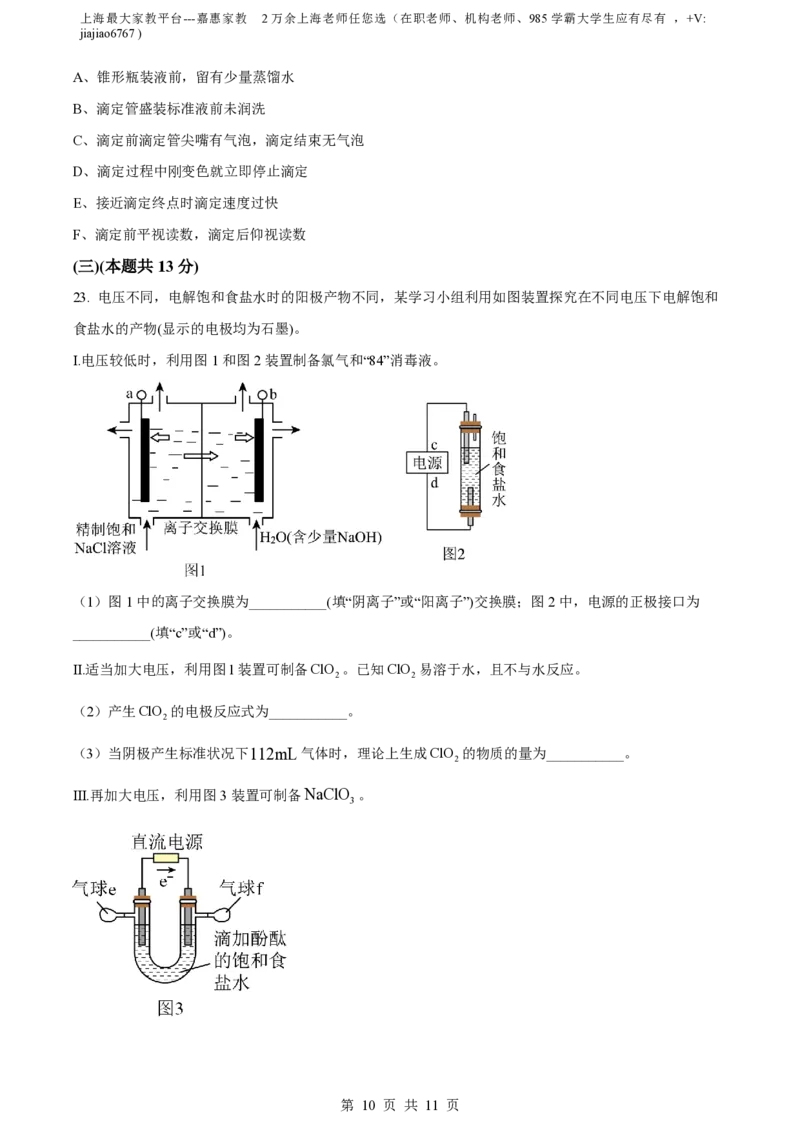
23. 电压不同,电解饱和食盐水时的阳极产物不同,某学习小组利用如图装置探究在不同电压下电解饱和
食盐水的产物(显示的电极均为石墨)。
Ⅰ.电压较低时,利用图1和图2装置制备氯气和“84”消毒液。
(1)图1中的离子交换膜为___________(填“阴离子”或“阳离子”)交换膜;图2中,电源的正极接口为
___________(填“c”或“d”)。
Ⅱ.适当加大电压,利用图l装置可制备ClO 。已知ClO 易溶于水,且不与水反应。
2 2
(2)产生ClO 的电极反应式为___________。
2
(3)当阴极产生标准状况下112mL气体时,理论上生成ClO 的物质的量为___________。
2
Ⅲ.再加大电压,利用图3装置可制备NaClO 。
3
第 10 页 共 11 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(4)该装置中反应的离子方程式为___________;观察到的实验现象为___________。
(四)(本题共 17分)
24. Sharpless教授发现,在亚铜的催化下,末端炔烃可以高区域选择性地与叠氮化合物发生高效的Click(点
击)反应,Sharpless教授也因此获得了2022年诺贝尔化学奖。科学家以乙烯和1,3-丁二烯等为原料,经过
多步转化和Click反应合成化合物G,合成路线如下(Ph—表示苯基,部分反应条件已简化):
Click反应示例:
请回答下列问题:
(1)乙烯和1,3-丁二烯生成A的反应类型是_______。
(2)A的化学名称为_______。
(3)A→C的化学方程式为_______。
(4)D为环醚,其结构简式为_______。
(5)G的结构简式为_______。
(6)乙烯和1,3-丁二烯生成 的反应称为Diels-Alder反应,是有机化学合成反应中碳碳键形成
的重要手段之一、两分子环戊二烯也可以发生Diels-Alder反应生成二聚环戊二烯(分子式为C H ),二聚
10 12
环戊二烯的结构简式为_______。
(7)在B的同分异构体中,画出同时满足下列条件的化合物的结构简式_______。
a.有四个碳原子在一条直线上 b.不含环状结构
c.含有硝基和溴原子 d.含有手性碳
第 11 页 共 11 页