文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
复旦大学附属中学 2022 学年第一学期
高二年级化学期中考试试卷
(本试卷满分 100分,考试时间 60分钟,共 32题)
可能用到的相对原子质量:H-1 C-12 O-16 S-32 Cl-35.5 Cu-64
一、选择题(每题只右 1个正确答案,每题 2分,共 20分)
1. 下列化学用语表达正确的是
A. 既可以表示CH 分子,又可以表示CCl 分子 B. 乙基共有16个电子
4 4
C. 四氯化碳的电子式为 D. 正丁烷的球棍模型:
2. 判断电解质强弱的合理依据是
A. 溶液的导电能力 B. 水溶性大小
C. 一定浓度时的电离程度 D. 与酸或碱反应时消耗酸或碱的量
3. 下列说法正确的是
A. 洗涤油污常用热的Na CO 溶液,这是利用了盐类水解的原理
2 3
B. 用加热的方法就可以除去KCl溶液中的Fe3+
C. 配制FeSO 溶液时,将FeSO 固体溶于稀盐酸中,然后稀释至所需浓度
4 4
D. 将AlCl 溶液和Na SO 溶液分别加热蒸干、灼烧后,所得固体为Al O 和Na SO
3 2 3 2 3 2 3
4. 甲、乙两种有机物的球棍模型如下,有关二者的描述中正确的是
A. 甲、乙为同一物质 B. 甲、乙互为同系物
C. 甲、乙分子的一氯取代物的数目相同 D. 甲、乙分子中含有的共价键数目不同
5. 室温下,将等质量的固体Mg(OH) 置于等体积的下列液体中,均有固体剩余,其中剩余固体最少的是
2
A. 在纯水中 B. 在0.1molL-1的MgCl 溶液中
2
第 1 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
C. 在0.1molL-1的NH H O中 D. 在0.1molL-1的NH Cl溶液中
3 2 4
c
H+
6. 要使0.1molL-1的醋酸溶液中 的值增大,可以采取的措施是
cCH COOH
3
①加少量烧碱固体 ②升高温度 ③加少量冰醋酸 ④加水 ⑤加少量醋酸钠固体
A. ①② B. ②③④ C. ③④⑤ D. ②④
7. 下图是室温下的BaCO
K
=2.610-9
和BaSO
K
=1.110-10
在水中的沉淀溶解平衡曲线,下列
3 sp 4 sp
说法错误的是
A. 位于上面的那条曲线是BaCO B. c点加入Na SO 后可变到a点
3 2 4
C. a点加入Na SO 后可变到b点 D. d点的沉淀溶解状态:v >v
2 4 溶解 沉淀
8. 常温下,下列各组离子在指定溶液中一定能大量共存的是
A. K w / H+ =0.1的溶液:K+、NH 3 H 2 O、SO2 4 -、NO 3 -
B. 能使甲基橙变红色的溶液:Na+、NH+、MnO-、HCO-
4 4 3
C. H+ OH- =110-24 的溶液:Al3+、Fe3+、Cl-、SO2-
水 水 4
D. 和Al反应放出H 的溶液:Mg2+、Cu2+、NO-、SO2-
2 3 4
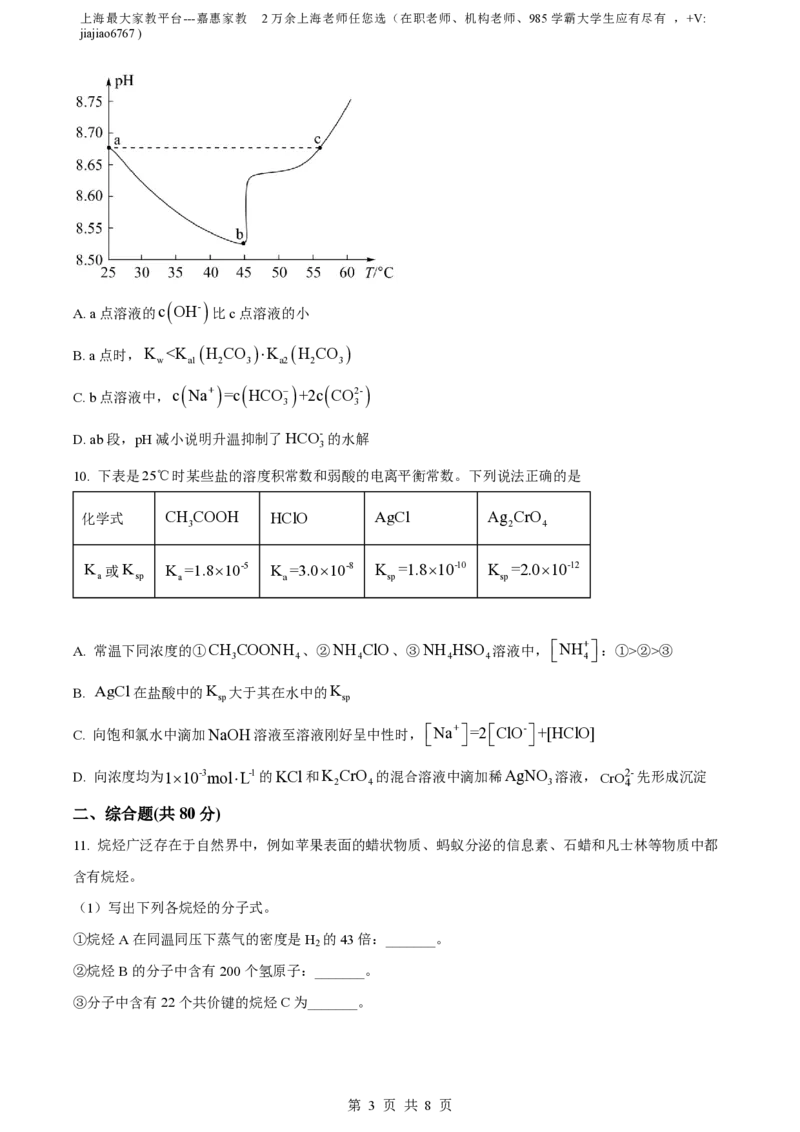
9. 如图为某实验测得0.1molL-1NaHCO 溶液在升温过程中(不考虑水挥发)的pH变化曲线。下列说法正
3
确的是
第 2 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. a点溶液的c
OH-
比c点溶液的小
B. a点时,K ②>③
B. AgCl在盐酸中的K 大于其在水中的K
sp sp
C. 向饱和氯水中滴加NaOH溶液至溶液刚好呈中性时, Na+ =2 ClO- +[HClO]
D. 向浓度均为110-3molL-1的KCl和K CrO 的混合溶液中滴加稀AgNO 溶液,CrO 2-先形成沉淀
2 4 3 4
二、综合题(共 80分)
11. 烷烃广泛存在于自然界中,例如苹果表面的蜡状物质、蚂蚁分泌的信息素、石蜡和凡士林等物质中都
含有烷烃。
(1)写出下列各烷烃的分子式。
①烷烃A在同温同压下蒸气的密度是H 的43倍:_______。
2
②烷烃B的分子中含有200个氢原子:_______。
③分子中含有22个共价键的烷烃C为_______。
第 3 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
④0.1mol烷烃D完全燃烧,消耗标准状况下的O 11.2L_______。
2
(2)下列关于烷烃的叙述中正确的是_______。
A. 都是易燃物,燃烧产物一定为二氧化碳和水 B. 在光照条件下,能使溴水褪色
C. 烷烃的卤代反应很难得到纯净的产物 D. 能使酸性KMnO 溶液褪色
4
(3)把下列物质的沸点按由高到低的顺序排列_______。(填入编号)
①CH CH CH ② CH C ③2,3,4三甲基戊烷 ④CH CHCH CH CH
3 2 3 3 3 4 3 2 2 2 3
(4)用系统命名法命名下面的烃A:_______;A的一氯代物有_______种。
(5)某烷烃的相对分子质量为114,与氯气发生取代反应所得的一氯代物只有一种。写出该取代反应的化
学方程式。(注意有机物要写结构简式)_______。
(6)某烷烃的系统命名为□,□-二乙基庚烷,写出所有符合的结构简式:_______。
12. 葡萄酒中SO 最大使用量为0.25gL-1。取500mL葡萄酒,通过适当的方法使共所含SO 全部逸出并
2 2
用H O 将其全部氧化为H SO ,这样得到100mL溶液,然后用0.0900molL-1NaOH标准溶液进行滴
2 2 2 4
定。
(1)若用50mL滴定管进行实验,当滴定管中液面在刻度“10”处,则管内液体的体积_______。
A 10mL B. 40mL C. <10mL D. >40mL
.
(2)上述滴定实验中,可选择_______为指示剂,如何判断反应到达滴定终点:_______。若锥形瓶用待
测液润洗,则测量结果比实际值_______(填“偏高”“偏低”或“无影响”)。
具体操作步骤包括:
A.移取20.00mL待测硫酸溶液注入洁净的锥形瓶中,并加入2~3滴指示剂;
B.用标准NaOH溶液润洗滴定管2~3次;
C.调节滴定管使尖嘴处充满溶液,并使液面至“0”或“0”以下刻度,记下读数;
D.取标准NaOH溶液注入滴定管至刻度“0”以上2~3cm处;
E.检漏,并用蒸馏水洗涤滴定管;
F.把锥形瓶放在滴定管下面,用标准NaOH溶液滴定至终点并记下读数。
第 4 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
实验 消耗NaOH溶液的体积/mL 待测酸的体积/mL
1 22.62 20.00
2 22.72 20.00
3 25.80 20.00
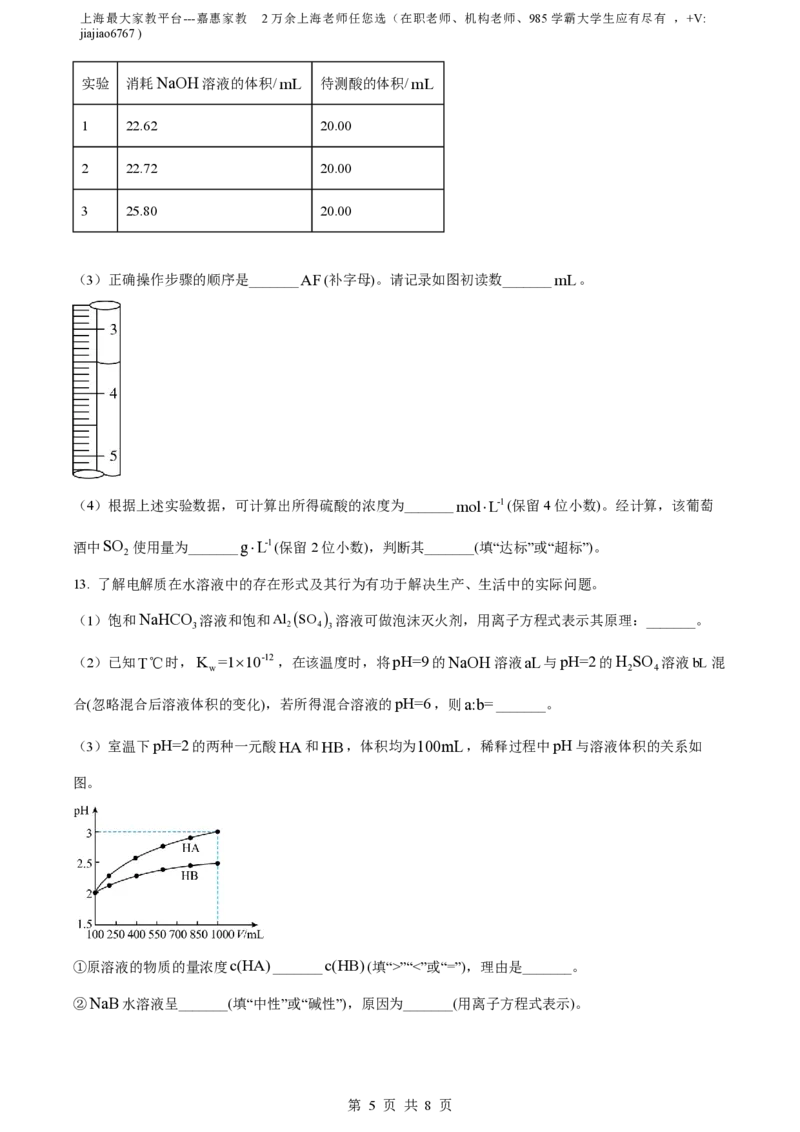
(3)正确操作步骤的顺序是_______AF(补字母)。请记录如图初读数_______mL。
(4)根据上述实验数据,可计算出所得硫酸的浓度为_______molL-1(保留4位小数)。经计算,该葡萄
酒中SO 使用量为_______gL-1(保留2位小数),判断其_______(填“达标”或“超标”)。
2
13. 了解电解质在水溶液中的存在形式及其行为有功于解决生产、生活中的实际问题。
(1)饱和NaHCO 溶液和饱和Al SO 溶液可做泡沫灭火剂,用离子方程式表示其原理:_______。
3 2 4 3
(2)已知T℃时,K =110-12,在该温度时,将pH=9的NaOH溶液aL与pH=2的H SO 溶液bL混
w 2 4
合(忽略混合后溶液体积的变化),若所得混合溶液的pH=6,则a:b=_______。
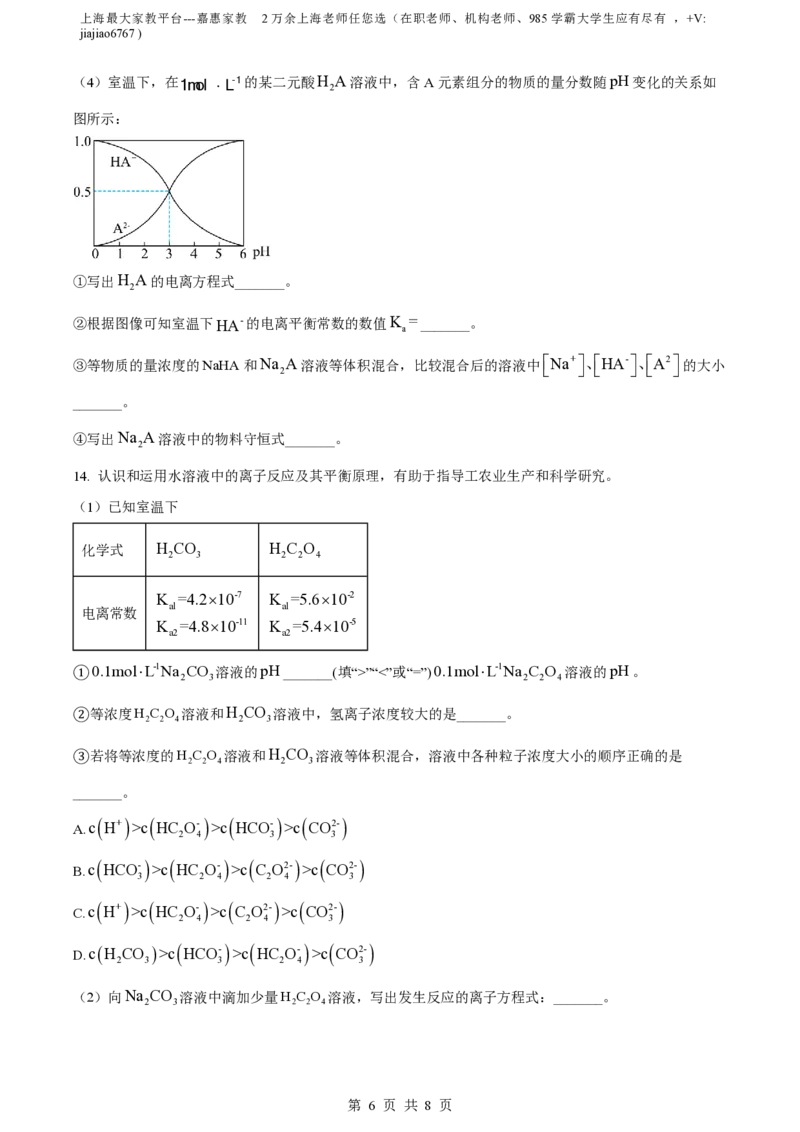
(3)室温下pH=2的两种一元酸HA和HB,体积均为100mL,稀释过程中pH与溶液体积的关系如
图。
①原溶液的物质的量浓度c(HA)_______c(HB)(填“>”“<”或“=”),理由是_______。
②NaB水溶液呈_______(填“中性”或“碱性”),原因为_______(用离子方程式表示)。
第 5 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(4)室温下,在1mol L-1的某二元酸H A溶液中,含A元素组分的物质的量分数随pH变化的关系如
2
图所示:
①写出H A的电离方程式_______。
2
②根据图像可知室温下HA-的电离平衡常数的数值K =_______。
a
③等物质的量浓度的NaHA和Na
2
A溶液等体积混合,比较混合后的溶液中
Na+
、
HA-
、
A2
的大小
_______。
④写出Na A溶液中的物料守恒式_______。
2
14. 认识和运用水溶液中的离子反应及其平衡原理,有助于指导工农业生产和科学研究。
(1)已知室温下
化学式 H CO H C O
2 3 2 2 4
K =4.210-7 K =5.610-2
al al
电离常数
K =4.810-11 K =5.410-5
a2 a2
①0.1molL-1Na CO 溶液的pH_______(填“>”“<”或“=”)0.1molL-1Na C O 溶液的pH。
2 3 2 2 4
②等浓度H C O 溶液和H CO 溶液中,氢离子浓度较大的是_______。
2 2 4 2 3
③若将等浓度的H C O 溶液和H CO 溶液等体积混合,溶液中各种粒子浓度大小的顺序正确的是
2 2 4 2 3
_______。
A.c H+ >c HC O- >c HCO- >c CO2-
2 4 3 3
B.c HCO- >c HC O- >c C O2- >c CO2-
3 2 4 2 4 3
C.c H+ >c HC O- >c C O2- >c CO2-
2 4 2 4 3
D.cH CO >c HCO- >c HC O- >c CO2-
2 3 3 2 4 3
(2)向Na CO 溶液中滴加少量H C O 溶液,写出发生反应的离子方程式:_______。
2 3 2 2 4
第 6 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(3)SO 会对环境和人体健康带来极大的危害,工业上采取多种方法减少SO 的排放。
2 2
方法1(双碱法):用NaOH溶液吸收SO ,并用CaO使NaOH再生
2
NaOH溶液 ⅰ.S O 2Na SO 溶液
ⅱ.C aO 2 3
①写出过程i的离子方程式:_______
②CaO在水中存在如下转化:
CaO(s)+H O(l)Ca(OH) (s)Ca2+(aq)+2OH-(aq)
2 2
从平衡移动的角度,简述过程ⅱ中NaOH再生的原理:_______。
(4)方法2:用亚硫酸盐(X)吸收烟气中的SO ,会生成酸式盐
HSO
2 3
①已知NaHSO 溶液呈酸性,比较Na+以及溶液中各种含硫元素微粒的浓度大小关系_______。
3
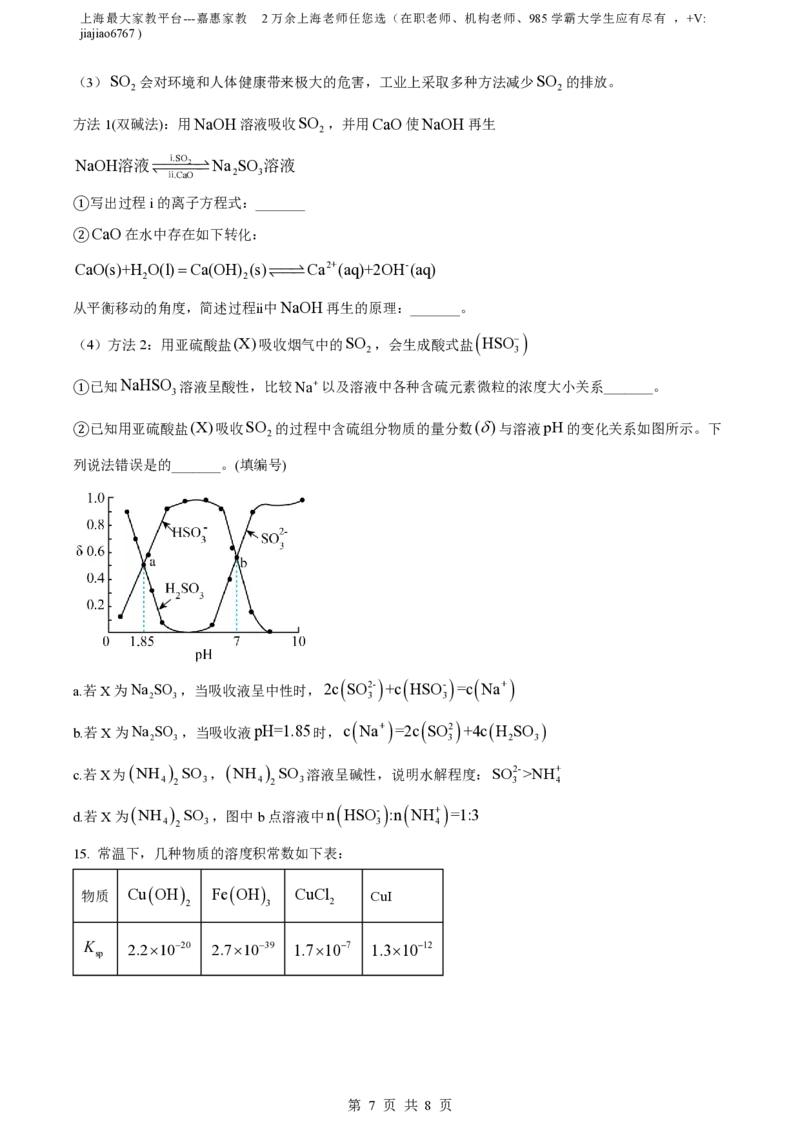
②已知用亚硫酸盐(X)吸收SO 的过程中含硫组分物质的量分数()与溶液pH的变化关系如图所示。下
2
列说法错误是的_______。(填编号)
a.若X为Na SO ,当吸收液呈中性时,2c
SO2-
+c
HSO-
=c
Na+
2 3 3 3
b.若X为Na SO ,当吸收液pH=1.85时,c Na+ =2c SO2 +4cH SO
2 3 3 2 3
c.若X为 NH SO , NH SO 溶液呈碱性,说明水解程度:SO2->NH+
4 2 3 4 2 3 3 4
d.若X为 NH SO ,图中b点溶液中n HSO- :n NH+ =1:3
4 2 3 3 4
15. 常温下,几种物质的溶度积常数如下表:
物质 CuOH FeOH CuCl CuI
2 3 2
K 2.21020 2.71039 1.7107 1.31012
sp
第 7 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(1)某酸性CuCl 溶液中含少量的FeCl ,为制得纯净CuCl 溶液,宜加入_______调至溶液pH=4,使
2 3 2
Fe3转化为FeOH 沉淀,此时溶液中c Fe3+ =_______。
3
(2)过滤后,将所得滤液经过_______、_______、过滤等操作,可得到CuCl 2H O晶体。
2 2
(3)由CuCl 2H O晶体得到纯的无水CuCl ,需要进行的操作是_______。
2 2 2
(4)某学习小组用“间接碘量法”测定含有CuCl 2H O晶体的试样(不含能与I发生反应的氧化性杂质)
2 2
的纯度,过程如下:取0.800g试样溶于水,加入过量KI固体。充分反应,生成白色沉淀(CuI)。用
0.1000ml/LNa S O 标准溶液滴定,达到滴定终点时,消耗Na S O 标准溶液40.00mL。(已知:
2 2 3 2 2 3
I 2S O2 S O2 2I)
2 2 3 4 6
①可选用_______作指示剂,滴定终点的现象是_______。
②CuCl 溶液与KI反应的离子方程式为_______。
2
③该试样中CuCl 2H O的质量分数为_______。
2 2
第 8 页 共 8 页