文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
复旦大学附属中学 2022 学年第二学期
高二年级化学期中等级性考试试卷
(本卷共五道大题,时间 60分钟,满分 100分)
注:单项选择指只有一个正确选项;不定项选择指可能有 1个或 2个正确选项。
本卷可能用到的相对原子质量:H-1,C-12,O-16,K-39,Ca-40
一、(共 22分)
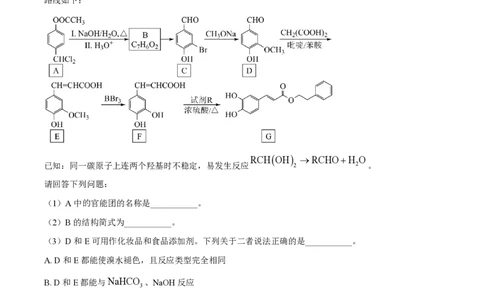
1. 咖啡酸苯乙酯G是蜂胶的主要活性组分之一,是一种NF-KB抑制剂,以芳香族化合物A为原料制备的
路线如下:
RCHOH RCHOH O
已知:同一碳原子上连两个羟基时不稳定,易发生反应 2 2 。
请回答下列问题:
(1)A中的官能团的名称是___________。
(2)B的结构简式为___________。
(3)D和E可用作化妆品和食品添加剂。下列关于二者说法正确的是___________。
A. D和E都能使溴水褪色,且反应类型完全相同
B. D和E都能与NaHCO 、NaOH反应
3
C. 通常情况下,D和E都能发生取代、加成、消去反应
D. 可用银氨溶液或新制氢氧化铜鉴别D和E
(4)F中最多有___________个原子共平面。
A. 16 B. 18 C. 20 D. 21
(5)F→G的反应除有机产物外仅有水生成,该反应类型是___________,试剂R的分子式为
___________。
(6)写出G在碱性条件下水解的方程式:___________,1mol G最多可以与___________mol H 反应,
2
第 1 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
最多可以消耗___________mol浓溴水中的Br 。
2
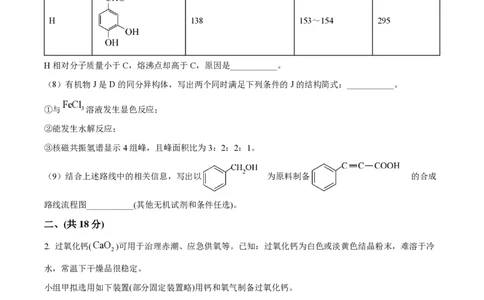
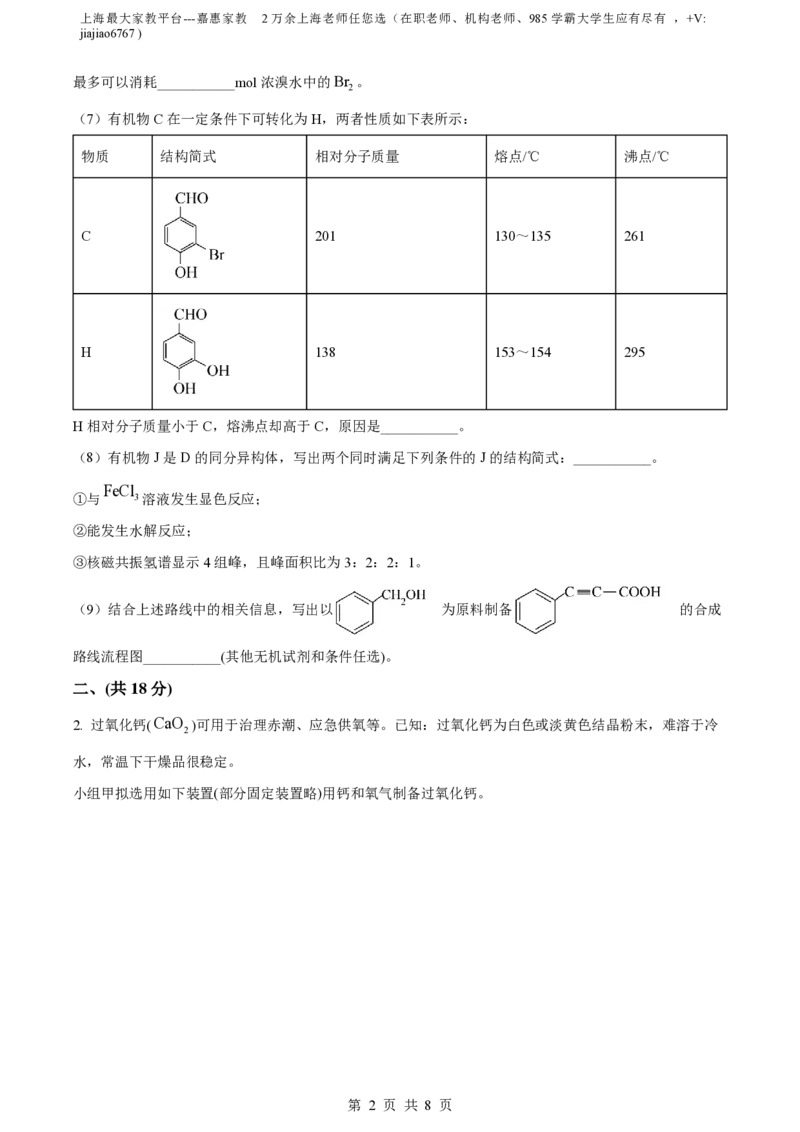
(7)有机物C在一定条件下可转化为H,两者性质如下表所示:
物质 结构简式 相对分子质量 熔点/℃ 沸点/℃
C 201 130~135 261
H 138 153~154 295
H相对分子质量小于C,熔沸点却高于C,原因是___________。
(8)有机物J是D的同分异构体,写出两个同时满足下列条件的J的结构简式:___________。
FeCl
①与 3溶液发生显色反应;
②能发生水解反应;
③核磁共振氢谱显示4组峰,且峰面积比为3:2:2:1。
(9)结合上述路线中的相关信息,写出以 为原料制备 的合成
路线流程图___________(其他无机试剂和条件任选)。
二、(共 18分)
2. 过氧化钙(CaO )可用于治理赤潮、应急供氧等。已知:过氧化钙为白色或淡黄色结晶粉末,难溶于冷
2
水,常温下干燥品很稳定。
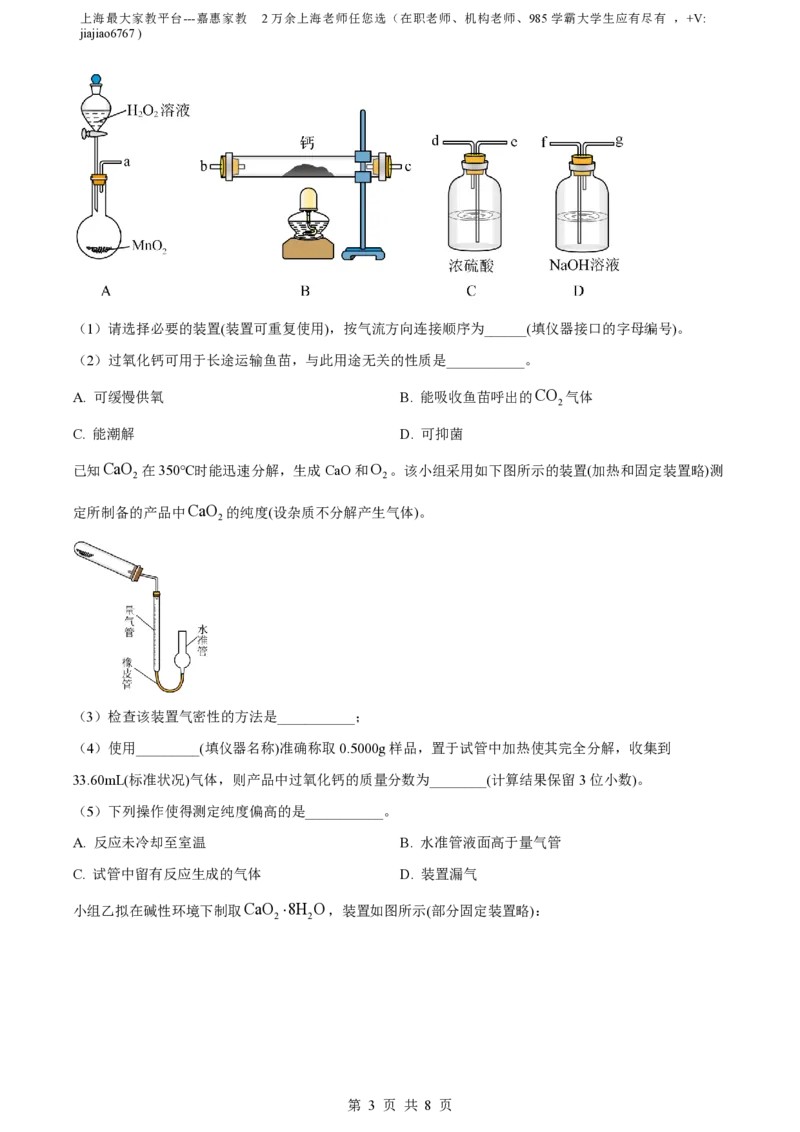
小组甲拟选用如下装置(部分固定装置略)用钙和氧气制备过氧化钙。
第 2 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(1)请选择必要的装置(装置可重复使用),按气流方向连接顺序为______(填仪器接口的字母编号)。
(2)过氧化钙可用于长途运输鱼苗,与此用途无关的性质是___________。
A. 可缓慢供氧 B. 能吸收鱼苗呼出的CO 气体
2
C. 能潮解 D. 可抑菌
已知CaO 在350℃时能迅速分解,生成CaO和O 。该小组采用如下图所示的装置(加热和固定装置略)测
2 2
定所制备的产品中CaO 的纯度(设杂质不分解产生气体)。
2
(3)检查该装置气密性的方法是___________;
(4)使用_________(填仪器名称)准确称取0.5000g样品,置于试管中加热使其完全分解,收集到
33.60mL(标准状况)气体,则产品中过氧化钙的质量分数为________(计算结果保留3位小数)。
(5)下列操作使得测定纯度偏高的是___________。
A. 反应未冷却至室温 B. 水准管液面高于量气管
C. 试管中留有反应生成的气体 D. 装置漏气
小组乙拟在碱性环境下制取CaO 8H O,装置如图所示(部分固定装置略):
2 2
第 3 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(6)上图的装置B中制取CaO 8H O的离子方程式为___________;采用冰水浴控制温度,其可能原因
2 2
是___________、___________。长颈漏斗的作用___________。
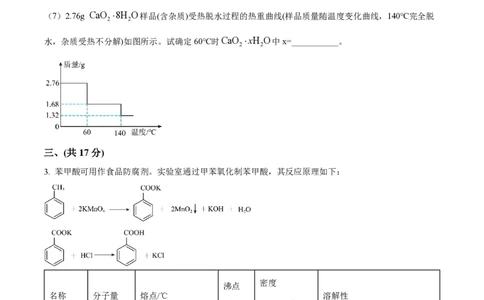
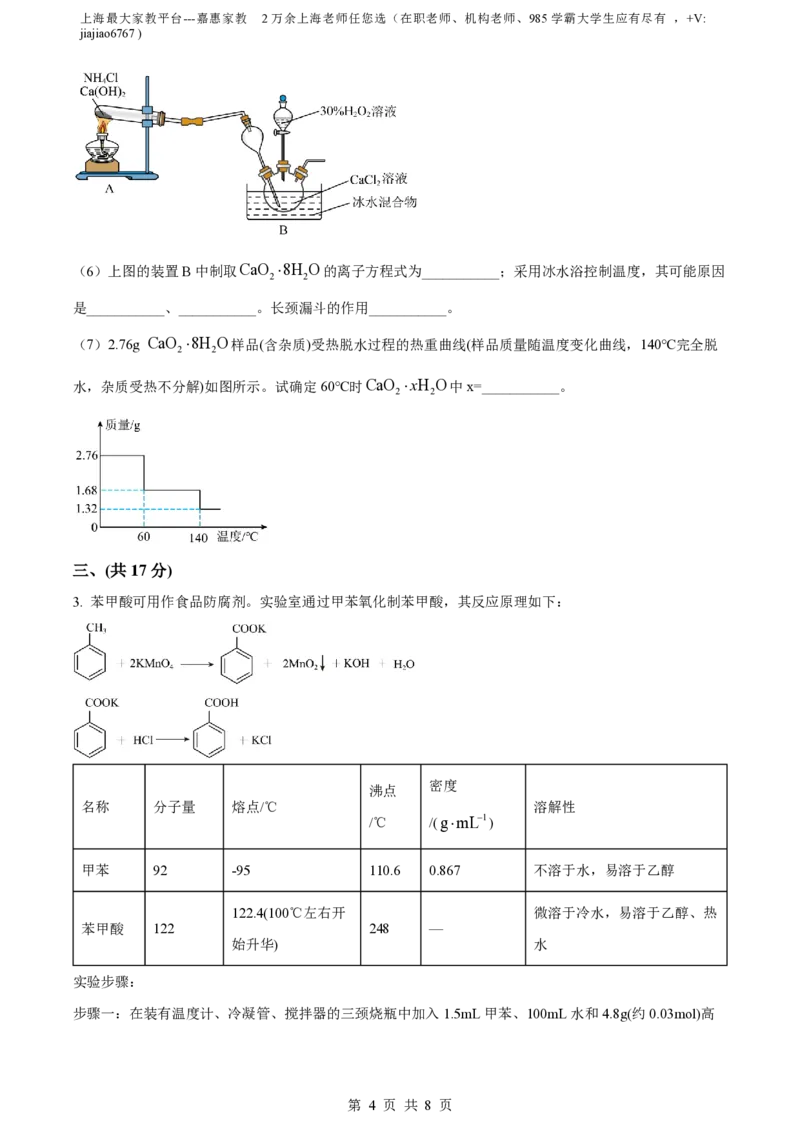
(7)2.76g CaO 8H O样品(含杂质)受热脱水过程的热重曲线(样品质量随温度变化曲线,140℃完全脱
2 2
水,杂质受热不分解)如图所示。试确定60℃时CaO xH O中x=___________。
2 2
三、(共 17分)
3. 苯甲酸可用作食品防腐剂。实验室通过甲苯氧化制苯甲酸,其反应原理如下:
密度
沸点
名称 分子量 熔点/℃ 溶解性
/℃ /(gmL1)
甲苯 92 -95 110.6 0.867 不溶于水,易溶于乙醇
122.4(100℃左右开 微溶于冷水,易溶于乙醇、热
苯甲酸 122 248 —
始升华) 水
实验步骤:
步骤一:在装有温度计、冷凝管、搅拌器的三颈烧瓶中加入1.5mL甲苯、100mL水和4.8g(约0.03mol)高
第 4 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
锰酸钾,慢慢开启搅拌器,并加热回流至回流液不再出现油珠。
步骤二:停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和亚硫酸氢钠溶液,并将反应
混合物趁热过滤,用少量热水洗涤滤渣。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲
酸析出完全。
步骤三:将析出的苯甲酸过滤,洗涤,干燥,称量,粗产品为1.0g。
步骤四:纯度测定:称取0.122g粗产品,配成乙醇溶液,于100mL容量瓶中定容,每次移取25.00mL溶
液,用0.0100molL1的KOH标准溶液滴定,三次滴定平均消耗21.50mL的KOH标准溶液。
回答下列问题:
(1)根据上述实验药品的用量,三颈烧瓶的最适宜规格为___________。
A. 100mL B. 250mL C. 500mL D. 1000mL
(2)冷凝管的水应从___________口进(填“a”或“b”),当回流液不再出现油珠即可判断反应已完成,其判断
理由是___________。
(3)步骤二中加入适量饱和亚硫酸氢钠溶液的目的是___________;“用少量热水洗涤滤渣”一步中滤渣的
主要成分是___________。
(4)步骤三中洗涤苯甲酸晶体时应选择___________。
A. 热水 B. 冷水 C. 乙醇 D. 甲苯
(5)步骤三中干燥苯甲酸晶体时,若温度过高,可能出现的结果是___________。
(6)本实验制备的苯甲酸的纯度为___________(计算结果保留2位小数,下同);据此计算苯甲酸的产率
为___________。
(7)下列操作可能导致苯甲酸纯度测定结果偏高的是___________。
A. 定容时仰视刻度线 B. 滴定管未用标准溶液润洗
C. 锥形瓶未用待测溶液润洗 D. 滴定前尖嘴处有气泡,滴定后气泡消失
(8)若要得到纯度更高的苯甲酸,可通过___________的方法提纯。
四、(共 18分)
4. 电池种类丰富,发展飞速,应用广泛,为我们的生产和生活带来了非常大的便利。
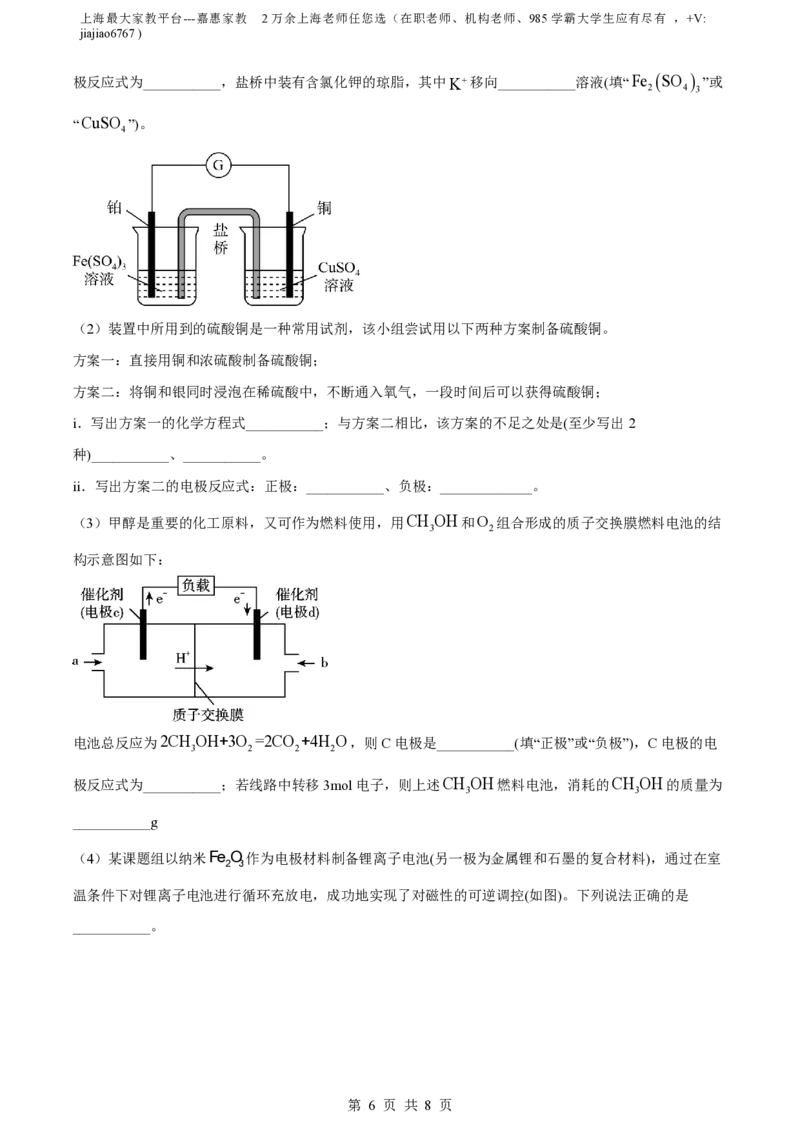
(1)某兴趣小组设计了如图所示的原电池装置,该电池的负极为___________(填“铂”或“铜”),正极的电
第 5 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
极反应式为___________,盐桥中装有含氯化钾的琼脂,其中K移向___________溶液(填“Fe SO ”或
2 4 3
“CuSO ”)。
4
(2)装置中所用到的硫酸铜是一种常用试剂,该小组尝试用以下两种方案制备硫酸铜。
方案一:直接用铜和浓硫酸制备硫酸铜;
方案二:将铜和银同时浸泡在稀硫酸中,不断通入氧气,一段时间后可以获得硫酸铜;
i.写出方案一的化学方程式___________;与方案二相比,该方案的不足之处是(至少写出2
种)___________、___________。
ii.写出方案二的电极反应式:正极:___________、负极:_____________。
(3)甲醇是重要的化工原料,又可作为燃料使用,用CH OH和O 组合形成的质子交换膜燃料电池的结
3 2
构示意图如下:
电池总反应为2CH OH+3O =2CO +4H O,则C电极是___________(填“正极”或“负极”),C电极的电
3 2 2 2
极反应式为___________;若线路中转移3mol电子,则上述CH OH燃料电池,消耗的CH OH的质量为
3 3
___________g
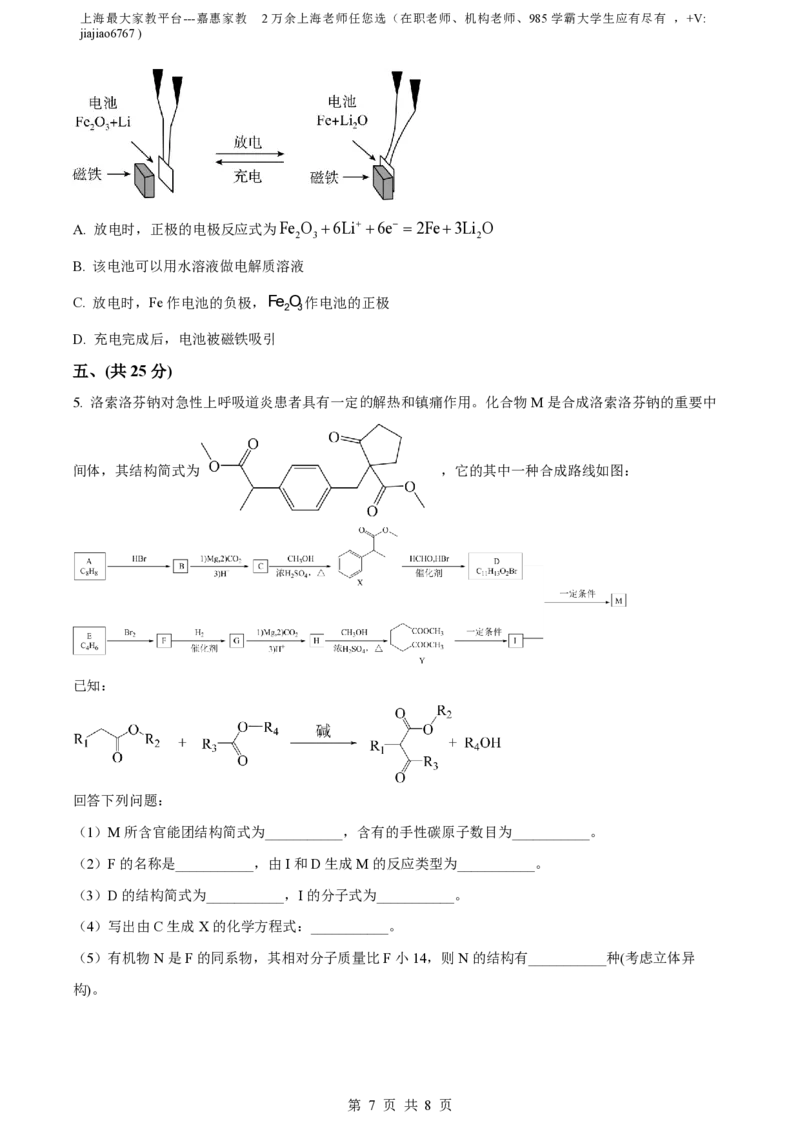
(4)某课题组以纳米Fe O作为电极材料制备锂离子电池(另一极为金属锂和石墨的复合材料),通过在室
2 3
温条件下对锂离子电池进行循环充放电,成功地实现了对磁性的可逆调控(如图)。下列说法正确的是
___________。
第 6 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 放电时,正极的电极反应式为Fe O 6Li 6e 2Fe3Li O
2 3 2
B. 该电池可以用水溶液做电解质溶液
C. 放电时,Fe作电池的负极,Fe O作电池的正极
2 3
D. 充电完成后,电池被磁铁吸引
五、(共 25分)
5. 洛索洛芬钠对急性上呼吸道炎患者具有一定的解热和镇痛作用。化合物M是合成洛索洛芬钠的重要中
间体,其结构简式为 ,它的其中一种合成路线如图:
已知:
回答下列问题:
(1)M所含官能团结构简式为___________,含有的手性碳原子数目为___________。
(2)F的名称是___________,由I和D生成M的反应类型为___________。
(3)D的结构简式为___________,I的分子式为___________。
(4)写出由C生成X的化学方程式:___________。
(5)有机物N是F的同系物,其相对分子质量比F小14,则N的结构有___________种(考虑立体异
构)。
第 7 页 共 8 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
一定条件
(6)已知:RCOOR′+R″OH RCOOR″+R′OH,写出H和乙二醇在一定条件下生成高聚物的化学
方程式:________________。
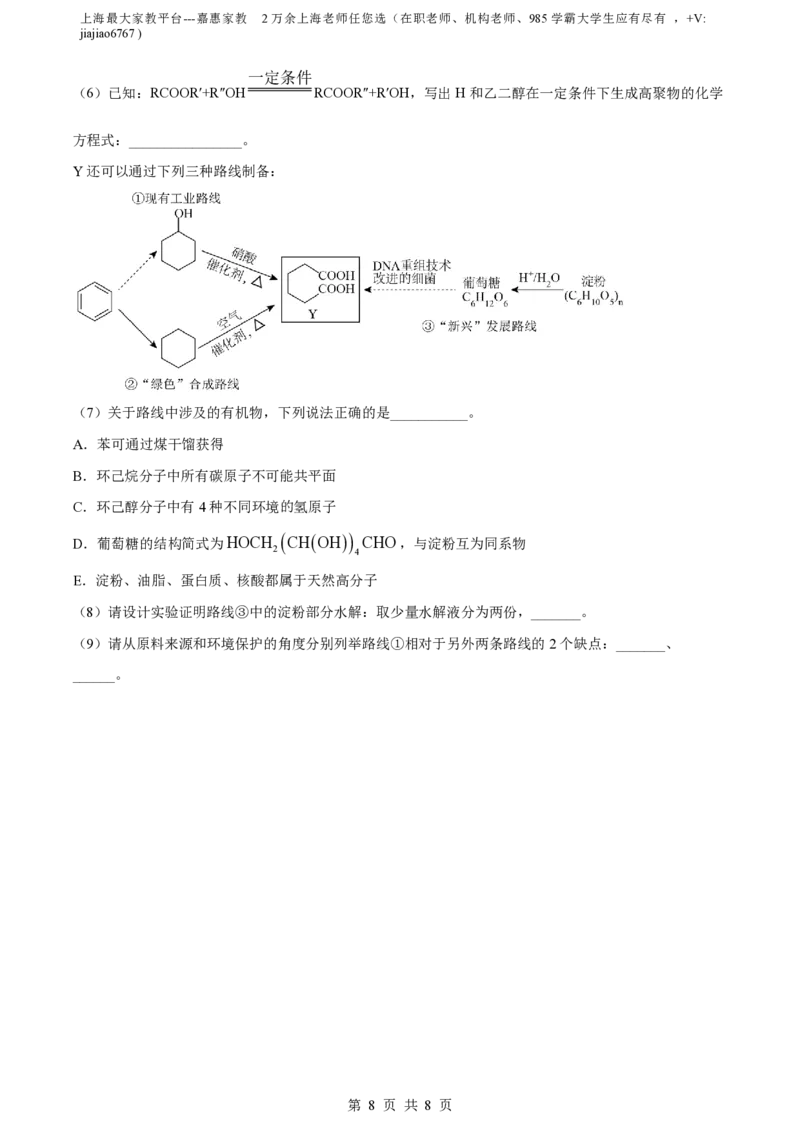
Y还可以通过下列三种路线制备:
(7)关于路线中涉及的有机物,下列说法正确的是___________。
A.苯可通过煤干馏获得
B.环己烷分子中所有碳原子不可能共平面
C.环己醇分子中有4种不同环境的氢原子
D.葡萄糖的结构简式为HOCH
CHOH
CHO,与淀粉互为同系物
2 4
E.淀粉、油脂、蛋白质、核酸都属于天然高分子
(8)请设计实验证明路线③中的淀粉部分水解:取少量水解液分为两份,_______。
(9)请从原料来源和环境保护的角度分别列举路线①相对于另外两条路线的2个缺点:_______、
______。
第 8 页 共 8 页