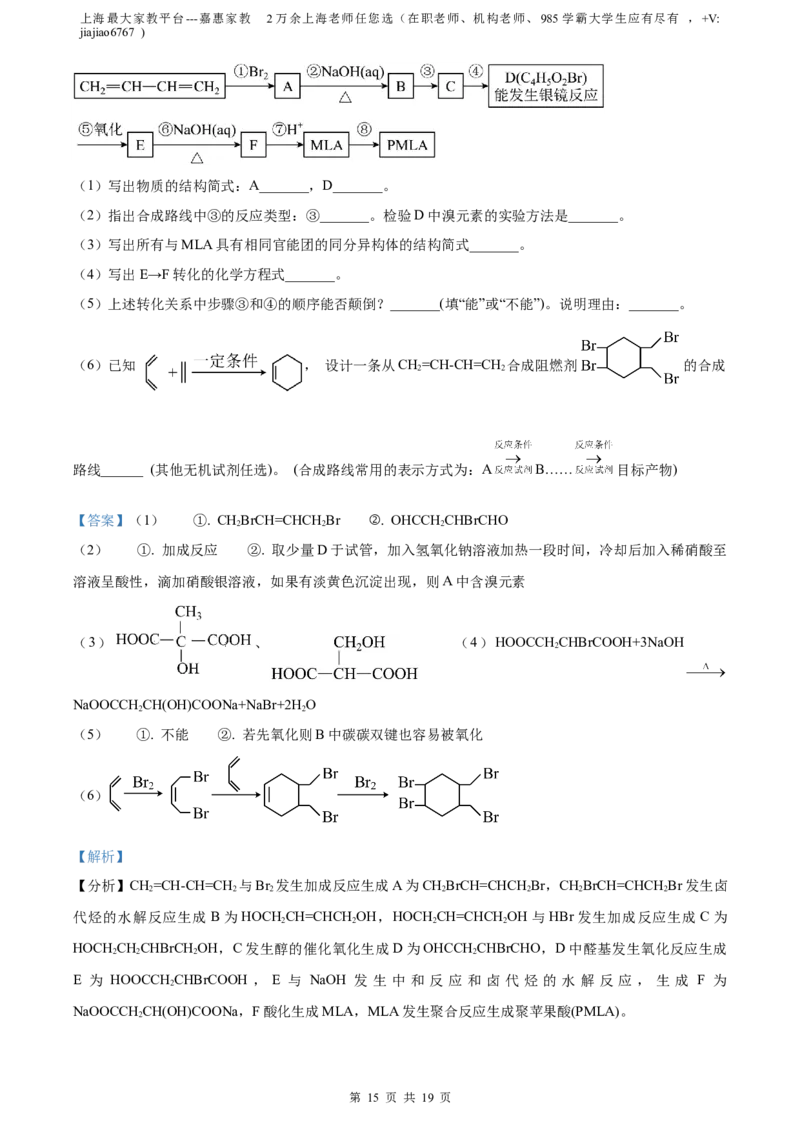
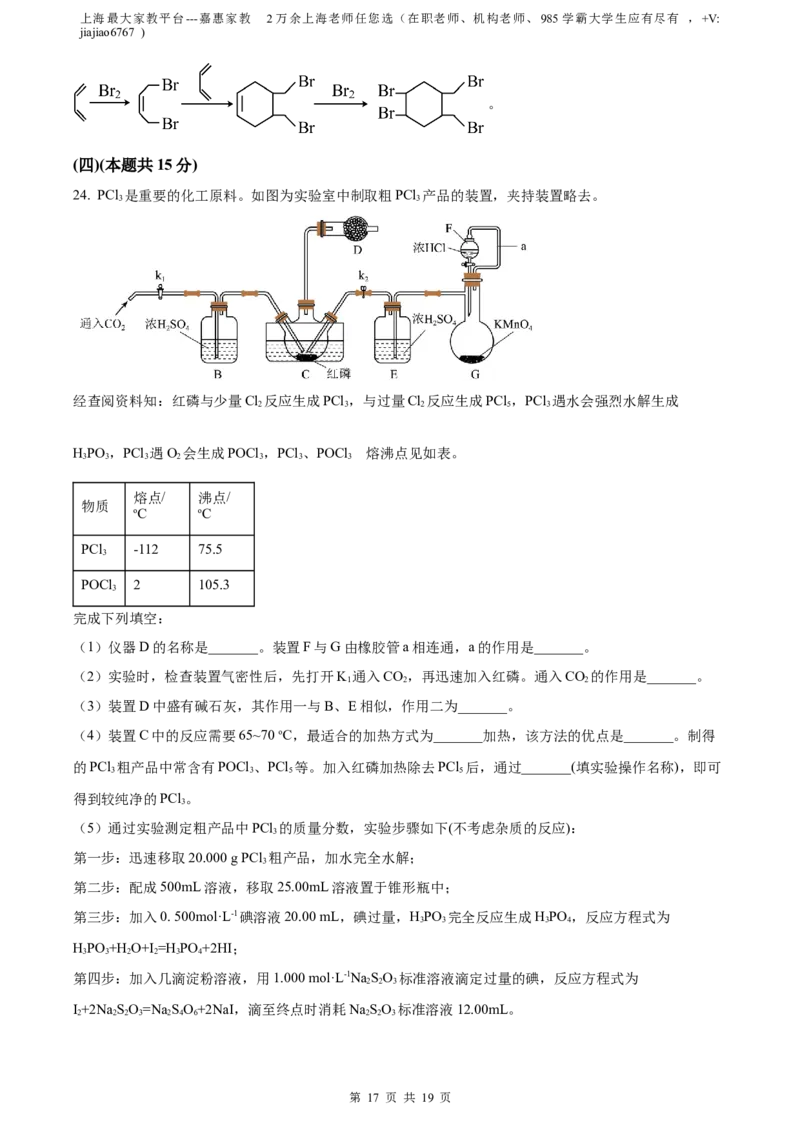
文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
松江区 2022 学年度第二学期等级考质量监控试卷
高三化学
(满分100分,完卷时间60分钟)
考生注意:
1.本考试分设试卷和答题纸。试卷包括两部分,第一部分为选择题,第二部分为综合题。
2.答题前,务必在答题纸上填写学校、班级、姓名、考号。作答必须涂或写在答题纸上,在
试卷上作答一律不得分。第一部分的作答必须涂在答题纸上相应的区域,第二部分的作答必
须写在答题纸上与试题号对应的位置。
相对原子质量:H-1 C-12 N-14 O-16 Na-23 P-31 Cl-35.5
一、选择题(本题共40分,每小题2分,每小题只有一个正确答案)
1. 2023年2月,我国海关在对进境邮件进行查验时,查获违法红珊瑚制品。珊瑚显红色,源于在海底长期
积淀某种元素的氧化物,该元素是
A. C B. Si C. Fe D. Na
【答案】C
【解析】
【详解】A.C的氧化物中无红色物质,A错误;
B.Si的氧化物中无红色物质,B错误;
C.Fe的氧化物中,Fe O 为红色,C正确;
2 3
D.Na的氧化物中无红色物质,D错误;
故答案选C。
2. “碳中和”是指CO 的排放总量和减少总量相当。下列措施中能促进“碳中和”最直接有效的是
2
A. 研发催化剂将CO 还原为甲醇 B. 大规模开采可燃冰作为新能源
2
C. 安装脱硫设备减少煤燃烧污染 D. 将重质油裂解为轻质油作为燃料
【答案】A
【解析】
【详解】A.研发催化剂将CO 还原为甲醇,降低CO 排放,能促进“碳中和”,故选A;
2 2
B.可燃冰燃烧生成二氧化碳,大规模开采可燃冰作为新能源,不能降低二氧化碳排放,故不选B;
C.安装脱硫设备减少煤燃烧污染,降低二氧化硫排放,不能降低二氧化碳排放,故不选C;
D.将重质油裂解为轻质油作为燃料,不能降低二氧化碳排放,故不选D;
选A。
3. 春季是流感、诺如病毒等疾病的高发期,需要对重点场所做好定期清洁消毒。下列物质中,不是消毒剂
第 1 页 共 19 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
的是
A. 漂粉精 B. 洁厕灵 C. 碘酒 D. 臭氧
【答案】B
【解析】
【详解】A.漂粉精中含有次氯酸钙,次氯酸钙能与CO、HO反应生成HClO具有消毒作用,漂粉精为消
2 2
毒剂,A错误;
B.洁厕灵的主要成分为较高浓度的盐酸,不具备消毒作用,不是消毒剂,B正确;
C.碘酒中碘单质具有氧化性,能杀菌消毒,碘酒是消毒剂,C错误;
D.臭氧具有强氧化性,能杀菌消毒,臭氧是消毒剂,D错误;
故答案选B。
4. 下列物质中,分子的空间结构为直线型的是
A. 乙烯 B. 甲烷 C. 氨 D. 二氧化碳
【答案】D
【解析】
【详解】A.乙烯空间构型为平面型,A错误;
B.甲烷的空间构型为正四面体结构,B错误;
C.氨的空间构型的三角锥形,C错误;
D.二氧化碳为直线型分子,D正确;
故选D。
5. 科学家们创造出了最轻的镁同位素18Mg,18Mg与24Mg具有
A. 不同电子数 B. 不同物理性质
C. 不同核电荷数 D. 不同化学性质
【答案】B
【解析】
【详解】A.18Mg和24Mg都具有12个电子,A错误;
B.18Mg和24Mg相对原子质量不同,物理性质不同,B正确;
C.18Mg和24Mg核电荷数均为12,C错误;
D.18Mg和24Mg最外层电子数均为2,两者化学性质相同,D错误;
故答案选B。
6. 在FeSO 、CuSO 、Al (SO ) 的混合溶液中通入适量HS,产生的沉淀物是
4 4 2 4 3 2
A. Al(OH) B. Al S C. CuS D. FeS
3 2 3
【答案】C
【解析】
第 2 页 共 19 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【详解】FeSO 、CuSO 、Al (SO ) 的混合溶液中通入适量HS,生成最难溶的CuS沉淀;
4 4 2 4 3 2
故答案选C。
7. 在合成氨和接触法制硫酸的工业生产中,下列说法错误的是
A. 均采用高压条件 B. 均选择较高温度
C. 均进行循环操作 D. 均使用合适催化剂
【答案】A
【解析】
【详解】A.接触法制硫酸的过程中,不需要采用高压条件,A错误;
B.合成氨和接触法制硫酸的工业生产中均需要较高的温度,B正确;
C.合成氨和接触法制硫酸的工业生产中均涉及到可逆反应,都需要进行循环操作,C正确;
D.合成氨和接触法制硫酸 的工业生产中均需要使用合适的催化剂,D正确;
故答案选A。
8. 一定条件下,存在“一种物质过量,另一种物质仍不能完全反应”情况的是
A. 一氧化氮与过量氧气 B. 氯化铝溶液与过量稀氨水
C. 铁片与过量浓硝酸 D. 澄清石灰水与过量二氧化碳
【答案】C
【解析】
【详解】A.一氧化氮和氧气反应生成二氧化氮,此反应不是可逆反应,氧气过量的情况下一氧化氮完全
反应,A错误;
B.氯化铝与氨水反应生成氢氧化铝和氯化铵,此反应不是可逆反应,氨水过量的情况下,氯化铝完全反
应,B错误;
C.常温下铁片在浓硝酸中发生钝化,浓硝酸过量的情况下,铁片仍不能完全反应,C正确;
D.澄清石灰水与过量二氧化碳反应生成碳酸氢钙,该反应不是可逆反应,二氧化碳过量的情况下,澄清
石灰水完全反应,D错误;
故答案选C。
9. 海水提溴与海带提碘,共同点是
A. 浓缩方法 B. 采用热空气吹出
C. 四氯化碳萃取 D. 氧化剂可选择氯水
【答案】D
【解析】
【详解】A.海水提溴和海带提碘的浓缩方法不同,A错误;
B.海水提溴过程中涉及热空气吹出,海带提碘不涉及热空气吹出,B错误;
第 3 页 共 19 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
C.海水提溴过程中未使用四氯化碳萃取,C错误;
D.海水提溴和海带提碘中,氧化剂都可选择氯气,Cl 与I-、Br-反应生成I 和Br ,D正确;
2 2 2
故答案选D。
10. 下列各组物质的转化关系不能全部通过一步反应完成的是
A. Na→NaOH→Na CO→NaCl B. Fe→FeCl →Fe(OH) →Fe O
2 3 3 3 2 3
C. Al→Al O→Al(OH) →AlCl D. Mg→MgCl →Mg(OH) →MgSO
2 3 3 3 2 2 4
【答案】C
【解析】
【详解】A.Na与水反应生成NaOH,NaOH与CO 反应生成NaCO,NaCO 与盐酸反应生成NaCl,以
2 2 3 2 3
上转化关系均能通过一步反应完成,A正确;
B.Fe与Cl 反应生成FeCl ,FeCl 与NaOH反应生成Fe(OH) ,Fe(OH) 加热分解生成Fe O ,以上转化关
2 3 3 3 3 2 3
系均能通过一步反应完成,B正确;
C.Al与氧气反应生成Al O,Al O 无法通过一步反应生成Al(OH) ,C错误;
2 3 2 3 3
D.Mg与Cl 反应生成MgCl ,MgCl 与NaOH反应生成Mg(OH) ,Mg(OH) 与HSO 反应生成MgSO ,以
2 2 2 2 2 2 4 4
上转化关系均能通过一步反应完成,D正确;
故答案选C。
11. 下列各组溶液中的反应,无论反应物量的多少,都只能用同一个离子方程式来表示的是
A. FeBr 与C1 B. Ca(HCO ) 与Ca(OH)
2 2 3 2 2
C. HCl与NaCO D. Ba(OH) 与NaHSO
2 3 2 4
【答案】B
【解析】
【详解】A.还原性强弱:Fe2+>Br-。Cl 与FeBr 物质的量之比小于等于1,产生FeBr 和FeCl ;Cl 与
2 2 3 3 2
FeBr 物质的量之比在1至1.5之间,有FeCl 和Br 、FeBr 。若Cl 与FeBr 物质的量之比大于等于1.5有
2 3 2 3 2 2
FeCl 和Br ,A项不符合题意;
3 2
B.该组无论量均产生水和CaCO ,可用一个方程式表达,B项符合题意;
3
C.若盐酸少量产生的是NaHCO ,而若盐酸足量产生的是CO 和HO,C项不符合题意;
3 2 2
D.若Ba(OH) 少量产生BaSO、HO、NaSO ;若Ba(OH) 足量产生BaSO、HO、NaOH,两反应不能用
2 4 2 2 4 2 4 2
同一离子方程式表达,D项不符合题意;
故选B。
12. 侯氏制碱法制造纯碱同时副产氯化铵。在母液处理上,有关说法错误的是
A. 水浴加热,有利于NH Cl更多地析出
4
B. 加入食盐,增大Cl-的浓度,使NH Cl更多地析出
4
第 4 页 共 19 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
的
C. 通入氨气,增大NH + 浓度,使NH Cl更多地析出
4 4
D. 通入氨气,使NaHCO 转化为NaCO,提高析出的NH Cl纯度
3 2 3 4
【答案】A
【解析】
【详解】A.从母液中获得NH Cl晶体,采用的时降温结晶的方法,故A说法错误;
4
B.加入食盐,增加c(Cl-),使NH Cl更多析出,故B说法正确;
4
C.通入NH ,NH +HO=NH ·H O,NH ·H O NH +OH-,c(NH )增大,使NH Cl更多地析出,
3 3 2 3 2 3 2 4
故C说法正确;
D.通入氨气,NH ·H O与NaHCO 反应生成NaCO ,溶解度小的转化成溶解度大的,c(NH )增大,提高
3 2 3 2 3
析出NH Cl的纯度,故D说法正确。
4
故选A。
13. 下列装置用于实验室中制取干燥氨气的实验,其中能达到实验目的的是
A. 用装置甲制备氨气 B. 用装置乙除去氨气中的少量水
C. 用装置丙收集氨气 D. 用装置丁吸收多余的氨气
【答案】A
【解析】
【详解】A.浓氨水遇碱石灰放出氨气,实验室可以用装置甲制备氨气,故选A;
B.浓硫酸和氨气反应生成硫酸铵,浓硫酸能吸收氨气,不能用浓硫酸干燥氨气,故不选B;
C.体系密闭,若用装置丙收集氨气,空气无法排除,故不选C;
D.氨气极易溶于水,漏斗口浸没在水中,若用装置丁吸收多余的氨气,引起倒吸,故不选D;
选A。
14. 断肠草中分离出来的2种毒素的结构简式如下,有关推断正确的是
第 5 页 共 19 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 互为同系物 B. 均能与氢氧化钠溶液反应
C. 互为同分异构体 D. 1mol均能与6molH 加成
2
【答案】B
【解析】
【详解】A.根据图示可知,分子组成上①比②多一个CHO,两者不是同系物,A错误;
2
B.①和②中都含有酯基,均能与氢氧化钠溶液反应,B正确;
C.①和②分子式不同,不是同分异构体,C错误;
D.①和②中酯基不能与氢气发生加成反应,1mol两种物质均能与5molH 加成,D错误;
2
故答案选B。
15. 可降解塑料PCL的合成路线如下:
下列说法错误的是
A. B的分子式为C H O B. C→D发生的是氧化反应
6 12
C. D→PCL发生的是缩聚反应 D. D与PCL的水解产物相同
【答案】C
【解析】
【分析】A与氢气发生加成反应生成B为 ,B发生醇的催化氧化生成C,C与过氧乙酸反应生成
D,D一定条件下反应生成PCL,根据PCL的结构简式和D的分子式可知,D为 。
【详解】A.根据分析可知,B的分子式为C H O,A正确;
6 12
B.C到D的过程为加氧的过程,发生氧化反应,B正确;
第 6 页 共 19 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
C.D为 ,D一定条件下反应生成PCL并未脱水缩合,发生的不是缩聚反应,C错误;
D.D与PCL水解的产物均为HOCH CHCHCHCHCOOH,D正确;
2 2 2 2 2
故答案选C。
16. 有一澄清透明的溶液,可能含有大量的 、 、 、 、 、 、 中的几种,
向该溶液中滴入 溶液一定体积后才产生沉淀。下列判断正确的是
A. 溶液中可能含有 B. 溶液中一定不含
C. 溶液中可能含有 D. 溶液中一定不含
【答案】D
【解析】
【分析】向该溶液中滴入 溶液一定体积后才产生沉淀,溶液中一定含有 ,因为
与 反应, ,所以溶液中一定不含 , 与 反应生成 ,
一定不存在,溶液中一定含有阴离子为 , 在酸性条件下有强氧化性, 一定不存在,
加入 产生沉淀, 和 可能都存在,或者存在其中之一。
【详解】A.根据以上分析,该溶液中 一定不存在,A错误;
B.加入 产生沉淀, 和 可能都存在,或者存在其中之一,B错误;
C.根据以上分析,溶液中一定含有 ,C错误;
D.溶液中含有 ,一定不含 ,D正确;
故选D。
17. 将表面发黑(黑色物质为Ag S)的银器浸入盛有食盐水的铝制容器中(如图),一段时间后黑色褪去。有关
2
说法正确的是
第 7 页 共 19 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. 该处理过程中电能转化为化学能
B. 铝质容器为阳极,其质量变轻
C. Ag S溶解于食盐水生成了AgCl
2
D. 银器为正极,Ag S被还原为单质银
2
【答案】D
【解析】
【分析】将表面发黑的银器浸入盛有食盐水的铝制容器中,形成原电池装置,铝做负极失电子,Ag S做正
2
极得电子生成Ag。
【详解】A.该处理过程利用了原电池的原理,化学能转化为电能,A错误;
B.铝质容器为负极,铝失电子转化为铝离子,质量变轻,B错误;
C.Ag S做正极得电子转化为Ag从而使银器表面黑色褪去,不是因为其溶解于食盐水中生成了AgCl,C
2
错误;
D.银器为正极,Ag S得电子被还原为Ag单质,D正确;
2
故答案选D。
18. 下列化学反应,相应的离子方程式一定正确的是
A. 向 溶液中加入少量 溶液:
B. 溶液与一定量氯气反应,转移电子数为6.02×1023时:
C. 将2.24L(标准状况)CO 通入500mL 0.3 mol·L-1 溶液中:
2
D. 向 溶液通入少量SO :
2
【答案】C
【解析】
【详解】A.Fe3+结合OH-能力更强,先产生Fe(OH) ,A项错误;
3
B.计算得FeBr 物质的量为1mol。还原性强弱:Fe2+>Br-,转移6.02×1023电子时只有Fe2+被氧化即2Fe2+
2
+Cl=2Cl-+2Fe3+,B项错误;
2
第 8 页 共 19 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
C.CO 和NaOH物质的量之比为0.1:0.15=2:3,反应同时产生 和 ,该离子方程式正确,C项
2
正确;
D.HClO为强氧化性能将SO 氧化为 ,该反应表达错误,D项错误;
2
故选C。
19. 工业上以铜阳极泥(主要成分是 )为原料提取碲(第五周期VIA族),涉及反应:
① ②
以下说法正确的是
A. 中 元素的化合价是 价
B. 氧化性强弱顺序为:
C. 反应②中氧化剂是SO ,氧化产物是HSO
2 2 4
D. 每制备 理论上共转移12mol电子
【答案】D
【解析】
【详解】A.碲为第五周期VIA族,最低负化合价为 价,根据化合价 正的负化合价为0, 中
元素的化合价是 价,A错误;
B.已知反应: ,氧化剂的氧化性强于氧化产物,所
以氧化性: ,在反应 中, 为氧化剂, 为还原
剂,所以氧化性 ,所以氧化性: ,B错误;
C.根据化合价的升降, ,硫元素的化合价升高,被氧化, 为还原剂, 为氧化
产物,C错误;
D.制备 ,反应①消耗 ,转移 ,反应② ,转移 ,
第 9 页 共 19 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
共转移 ,D正确;
故选D。
20. 常温下,向1LpH=10的NaOH溶液中持续通入CO,通入的CO 体积(V)与溶液中水电离出的OH-
2 2
离子浓度的关系如图所示。下列叙述不正确的是( )
A. a点溶液中:水电离出的c(H+)=1×10-10mol·L-1
B. b点溶液中:c(H+)=1×10-7mol·L-1
C. c点溶液中:c(Na+)>c(CO 2-)>c(HCO-)
3 3
D. d点溶液中:c(Na+)=2c(CO 2-)+c(HCO-)
3 3
【答案】B
【解析】
【详解】A. a点溶液为1LpH=10的NaOH溶液,溶液中氢离子浓度为1×10-10mol·L-1,就是水电离出的,
故正确;
B. b点溶液为氢氧化钠和碳酸钠,水电离的氢氧根离子浓度为1×10-7mol·L-1,但溶液中还有氢氧化钠电
离出的氢氧根离子,所以根据水的离子积常数计算,溶液中的c(H+)不为1×10-7mol·L-1,故错误;
C. c点溶液中水电离出的氢氧根离子浓度最大,说明溶液为碳酸钠,根据碳酸根水解分析,溶液中离子浓
度关系为:c(Na+)>c(CO 2-)>c(HCO-),故正确;
3 3
D. d点溶液为碳酸氢钠和碳酸的混合液,此时溶液呈中性,电荷守恒为c(Na+) +c(H+)=2c(CO 2-)+c(HCO-)+
3 3
c(OH-),c(OH-)= c(H+)=1×10-7mol·L-1,则:c(Na+)=2c(CO 2-)+c(HCO-),故正确。
3 3
故选B。
【点睛】掌握溶液中的水电离程度的变化,氢氧化钠抑制水的电离,碳酸钠存在水解,促进水的电离,所
以向氢氧化钠溶液中通入二氧化碳,水的电离程度逐渐增大,当全为碳酸钠时,水的电离程度最大,然后
碳酸钠反应生成碳酸氢钠,水的电离程度又逐渐减小。分清溶液中的氢离子和水电离的氢离子的关系。
二、综合题(共60分)
(一)(本题15分)
21. HO (过氧化氢) 应用领域非常广泛。
2 2
第 10 页 共 19 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
已知:2HO(l) 2HO(l)+O(g)+Q(Q>0)
2 2 2 2
HO(aq) H+(aq)+HO (aq) ,K(25oC)=2.24×10-12
2 2
完成下列填空:
(1)氧原子最外层成对电子和未成对电子数目之比为_______。
(2)HO 的电子式为_______。对HO 分子结构,有以下两种推测:
2 2 2 2
要确定HO 分子结构,需要测定HO 分子中的_______。(选填序号)
2 2 2 2
a. H—O键长 b. O—O键长 c. H—O—O键角 d. H—O、O—O键能
(3)HO 分解反应的平衡常数表达式K=_______。不同温度下HO 分解反应的平衡常数
2 2 2 2
K(25oC)_______K(40oC) (选填“>”“<”或“=”)。标准状况下,某5mL HO 溶液60s内产生氧气22.4mL(溶液体
2 2
积变化忽略不计)。则0~60s v(H O)= _______。
2 2
(4)25oC,pH(H O) _______pH(H O) (选填“>”“<”或“=”)。研究表明,HO 溶液中HO 浓度越大,HO
2 2 2 2 2 2 2
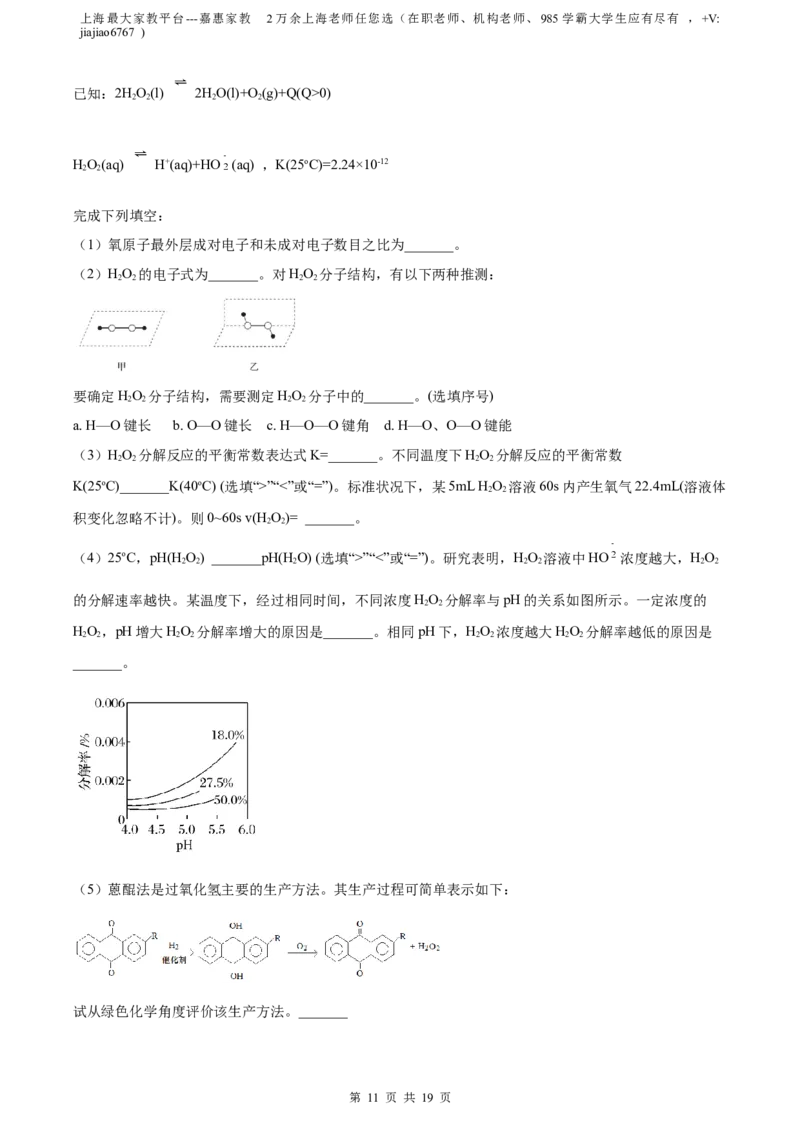
的分解速率越快。某温度下,经过相同时间,不同浓度HO 分解率与pH的关系如图所示。一定浓度的
2 2
HO,pH增大HO 分解率增大的原因是_______。相同pH下,HO 浓度越大HO 分解率越低的原因是
2 2 2 2 2 2 2 2
_______。
(5)蒽醌法是过氧化氢主要的生产方法。其生产过程可简单表示如下:
试从绿色化学角度评价该生产方法。_______
第 11 页 共 19 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【答案】(1)2:1 (2) ①. ②. c
(3) ①. c(O) ②. > ③. 0.4mol·L-1·min-1(或0.0067mol·L-1·s-1)
2
(4) ①. < ②. pH升高,HO 的浓度增加,HO 分解速率加快 ③. HO 浓度越高,电离程度
2 2 2 2
越低,分解率越小
(5)该法生产原子利用率是100%,符合“绿色化学工艺”
【解析】
【小问1详解】
O原子的核外电子排布式为1s22s22p4,最外层成对电子数为4个,未成对电子数为2个,成对电子数和未
成对电子数之比为2:1。
【小问2详解】
HO 的电子式为 ,对于HO 的分子结构有图示两种推测,这两种结构的不同之处在于H-O-O的
2 2 2 2
键角不同,因此需要测定HO 分子内H-O-O键角,故答案选c。
2 2
【小问3详解】
HO 分解反应为2HO(l) 2HO(l)+O(g),平衡常数表达式K= c(O )。已知HO 的分解反应为放热反应,
2 2 2 2 2 2 2 2 2
升高温度化学平衡逆向移动,则平衡常数K(25℃)>K(40℃)。5mLH O 溶液60s内生成氧气22.4mL即
2 2
1×10-3mol,则参与反应的HO 有2×10-3mol,v(H O)= 。
2 2 2 2
【小问4详解】
25℃时,HO 电离生成H+和 的平衡常数K=2.24×10-12>1×10-14,同温度下过氧化氢电离程度大于水,
2 2
故25℃时pH(H O)” “<”或“=”)。理由是_______。
2
(5)已知I + AsO +2OH- 2I-+AsO +HO。为验证该反应具有可逆性,将等物质的量浓度的碘水与
2 2
NaAsO 溶液按体积比为V:V 的比例混合(另加入适量的碱)。当V_______V (填“>”或“<”) 时,只需加
3 3 1 2 1 2
入_______ (填试剂名称)就可以确定该反应具有可逆性。上述反应显示:AsO 能在碱性溶液中被I 氧化成
2
AsO ,而HAsO 又能在酸性溶液中被I-还原成HAsO ,这表明_______。
3 4 3 3
【答案】(1)6Zn+As O+12HCl=6ZnCl +2AsH ↑+3H O
2 3 2 3 2
(2)2:1 (3)SO
2
(4) ①. HAsO +OH-=H AsO +H O ②. > ③. NaHAsO 溶液呈碱性,HAsO 水解程度大于
3 3 2 2 2 3
其电离程度
(5) ①. < ②. 淀粉溶液 ③. 溶液的酸碱性影响物质的氧化还原性
第 13 页 共 19 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
【解析】
【小问1详解】
As O 与Zn、HCl反应生成AsH 、ZnCl 和HO,化学方程式为6Zn+As O+12HCl=6ZnCl +2AsH ↑+3H O。
2 3 3 2 2 2 3 2 3 2
【小问2详解】
As S 和SnCl 在盐酸中反应生成As S、SnCl 和HS,化学方程式为
2 3 2 4 4 4 2
2As S+2SnCl +4HCl=As S+2SnCl +2H S↑,该反应As S 中As得电子化合价降低,As S 为还原产物,
2 3 2 4 4 4 2 2 3 4 4
SnCl 中Sn失电子化合价升高,SnCl 为氧化产物,则氧化产物和还原产物的物质的量之比为2:1。
2 4
【小问3详解】
As S 与O 反应生成As O 和物质a,1molAs S 参与反应时,转移28mol电子,1molAs S 转化为As O 时
4 4 2 2 3 4 4 4 4 2 3
As转移4mol电子,则剩余24mol电子为S失电子所转移,1mol AsS 含有4molS,S化合价为-2价,则产
4 4
物中S为+4价,因此物质a为SO 。
2
【小问4详解】
pH=11时, 的量最多,其余物质相对较少,则此过程的离子反应为HAsO +OH-=H AsO +H O。
3 3 2 2
从图中可知,溶液中溶质为NaHAsO 时溶液呈碱性,说明 的水解程度大于电离程度,故
2 3
NaHAsO 溶液中c( )>c( )。
2 3
【小问5详解】
为验证该反应具有可逆性,将等物质的量浓度的碘水和NaAsO 溶液按体积比V:V 的比例混合,只要确
3 3 1 2
保NaAsO 过量,再用淀粉溶液检验混合物中是否存在I 即可验证该反应是否具有可逆性,如不可逆,则
3 3 2
加入淀粉溶液后,混合液不变蓝。因此V