文档内容
上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
上海师范大学附属中学 2022 学年度第一学期期中教学质量自主调研
高一年级化学
(考试时间:60分钟 满分:100分)
一、选择题(本大题共 30题,每题 2分,满分 60 分)
1. 溶液、胶体和浊液这三种分散系的本质区别是
A. 能否发生丁达尔效应
B. 是否均一、透明、稳定
C 能否透过滤纸或半透膜
.
D. 分散质粒子直径的大小
2. 微纳米材料研究所研发的纳米量级碳酸钙直径约为30nm,已取得重大突破。下列有关说法正确的是
A. 纳米量级碳酸钙是一种胶体
B 若将纳米量级碳酸钙均匀分散到蒸馏水中,会产生丁达尔效应
.
C. 若将纳米量级碳酸钙均匀分散到蒸馏水中,不能透过滤纸
D. 若将纳米量级碳酸钙加入稀盐酸中,不会有二氧化碳产生
3. 下列物质中与0.3molH O含有相同氢原子数的是
2
A. 0.3molHNO B. 0.1molH PO C. 0.2molCH D. 3.612×1023个HCl分子
3 3 4 4
4. 下列溶液中物质的量浓度为1 mol·L-1的是
A. 将1 mol CuSO ·5H O溶解在1 L水中
4 2
B. 将22.4 L HCl气体溶于水配成1 L溶液
C. 将1 L 10 mol·L-1的浓盐酸加入9 L水中
D. 将10 g NaOH溶解在少量水中,再加蒸馏水直到溶液体积为250 mL
5. “S、T、P”是指
A. 20℃,1大气压 B. 273K,101.3KPa
C. 293K,1大气压 D. 0℃,101.3Pa
6. 用N 表示阿伏伽德罗常数的数值,则下列说法中正确的是
A
A. 44g CO 所含的原子数为N
2 A
B. 常温常压下,11.2L氧气所含的原子数为N
A
C. 常温常压下,N 个氢分子的质量为1g
A
第 1 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
D. 常温常压下,32g O 的原子数为2N
3 A
7. 对于同温同压下等质量的NO和NO ,下列叙述正确的是
2
A. 分子数之比为1:1 B. 体积之比为15:23
C. 所含原子数之比为46:45 D. 密度之比为23:15
8. 25℃、101kPa条件下,相同体积的两个密闭容器甲和乙,甲中充满O ,乙中充满O 和O 的混合气
2 2 3
体。下列说法错误的是
A. 两容器中气体的质量不相同 B. 两容器中气体的分子数目相同
C. 两容器中气体的氧原子数目不相同 D. 两容器中气体的密度相同
9. N 表示阿伏伽德罗常数,如果40 g 某气体中所含有的分子数为2N ,则25 g该气体在标况下的体积是
A A
A. 22.4 L B. 28 L C. 33.6 L D. 40 L
10. 瓦斯中甲烷与氧气的体积比为1:2时极易爆炸,此时甲烷与氧气的质量比为
A. 1:1 B. 1:2 C. 1:3 D. 1:4
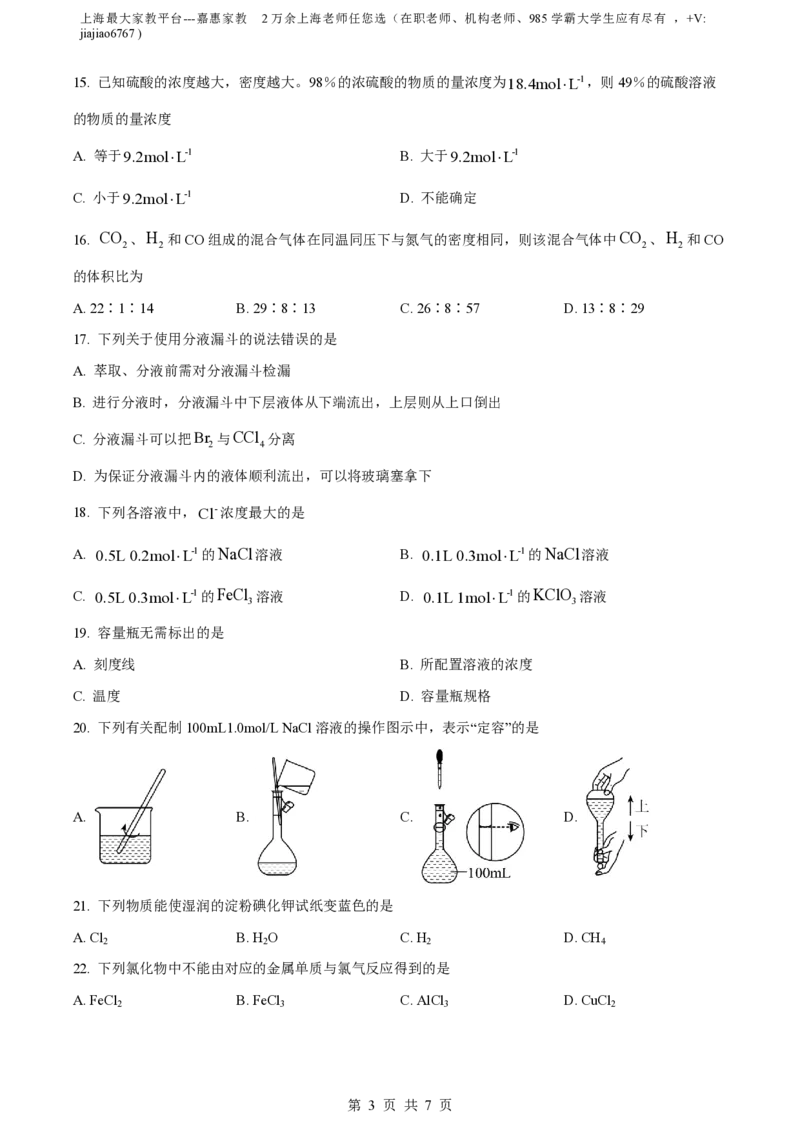
11. 用重结晶法提纯苯甲酸的实验中,需要用到的仪器是
A. B. C. D.
12. 有些化学仪器加热时需要放在石棉网上,但也有一些仪器可以直接在酒精灯上加热,下列各组仪器中
可以用酒精灯直接加热的一组是
A. 试管、蒸发皿、坩埚 B. 试管、烧杯、蒸馏烧瓶
C. 试管、平底烧瓶、坩埚 D. 蒸发皿、圆底烧瓶
13. 下列实验操作中错误的是
A. 蒸馏时,应使温度计水银球的中端靠近蒸馏烧瓶的支管口下沿处
B. 蒸发时,应使混合物中的大部分固体析出后停止加热
C. 过滤时,应使滤纸的边缘略低于漏斗的边沿
D. 萃取时,选择萃取剂的密度不一定比原溶剂大
14. 下列括号中的分离方法运用得当的是
A. 植物油和自来水(蒸馏) B. 水溶液中的食盐和碘(分液)
C. 自来水中的杂质(萃取) D. CaCO 和CaCl (溶解、过滤、蒸发)
3 2
第 2 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
15. 已知硫酸的浓度越大,密度越大。98%的浓硫酸的物质的量浓度为18.4molL-1,则49%的硫酸溶液
的物质的量浓度
A. 等于9.2molL-1 B. 大于9.2molL-1
C. 小于9.2molL-1 D. 不能确定
16. CO 、H 和CO组成的混合气体在同温同压下与氮气的密度相同,则该混合气体中CO 、H 和CO
2 2 2 2
的体积比为
A. 22∶1∶14 B. 29∶8∶13 C. 26∶8∶57 D. 13∶8∶29
17. 下列关于使用分液漏斗的说法错误的是
A. 萃取、分液前需对分液漏斗检漏
B. 进行分液时,分液漏斗中下层液体从下端流出,上层则从上口倒出
C. 分液漏斗可以把Br 与CCl 分离
2 4
D. 为保证分液漏斗内的液体顺利流出,可以将玻璃塞拿下
18. 下列各溶液中,Cl-浓度最大的是
A. 0.5L 0.2molL-1的NaCl溶液 B. 0.1L 0.3molL-1的NaCl溶液
C. 0.5L 0.3molL-1的FeCl 溶液 D. 0.1L 1molL-1的KClO 溶液
3 3
19. 容量瓶无需标出的是
A. 刻度线 B. 所配置溶液的浓度
C. 温度 D. 容量瓶规格
20. 下列有关配制100mL1.0mol/L NaCl溶液的操作图示中,表示“定容”的是
A. B. C. D.
21. 下列物质能使湿润的淀粉碘化钾试纸变蓝色的是
A. Cl B. H O C. H D. CH
2 2 2 4
22. 下列氯化物中不能由对应的金属单质与氯气反应得到的是
A. FeCl B. FeCl C. AlCl D. CuCl
2 3 3 2
第 3 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
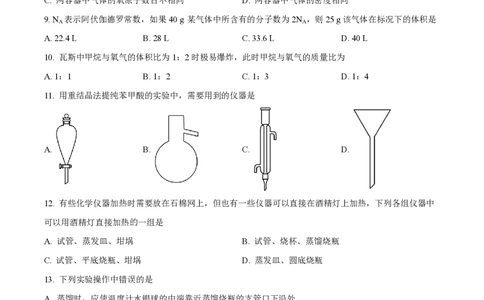
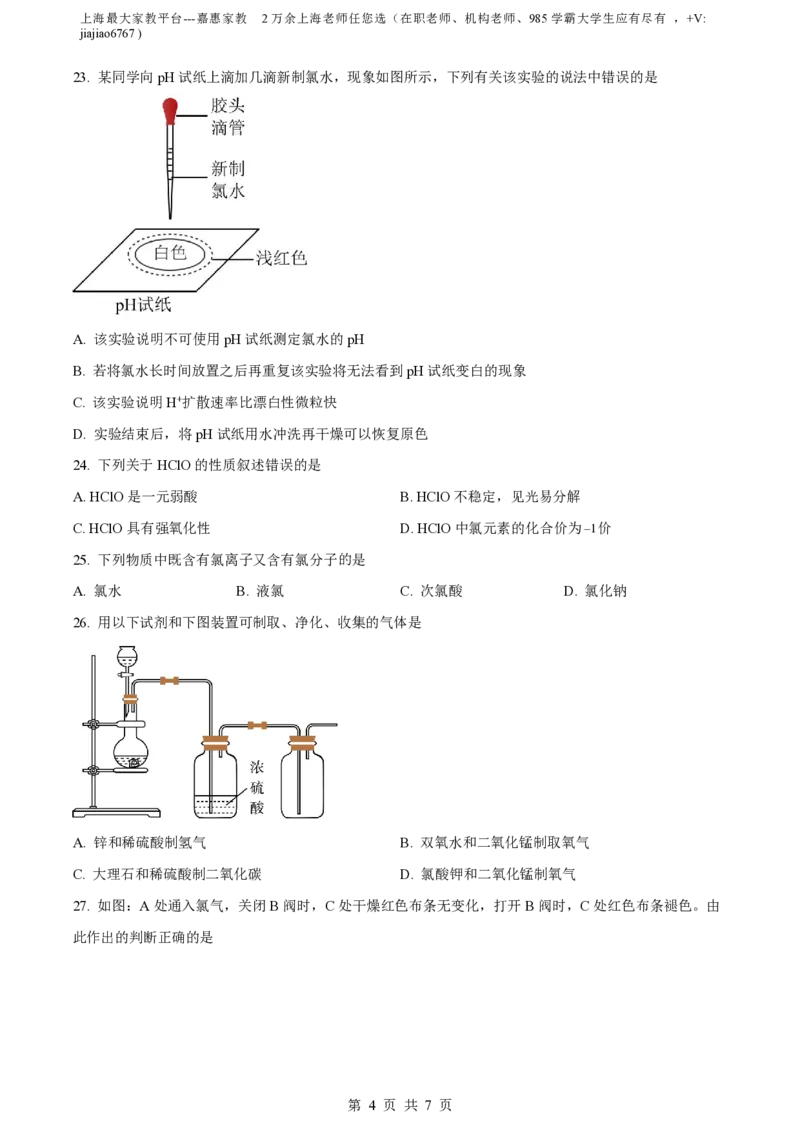
23. 某同学向pH试纸上滴加几滴新制氯水,现象如图所示,下列有关该实验的说法中错误的是
A. 该实验说明不可使用pH试纸测定氯水的pH
B. 若将氯水长时间放置之后再重复该实验将无法看到pH试纸变白的现象
C. 该实验说明H+扩散速率比漂白性微粒快
D. 实验结束后,将pH试纸用水冲洗再干燥可以恢复原色
24. 下列关于HClO的性质叙述错误的是
A. HClO是一元弱酸 B. HClO不稳定,见光易分解
C. HClO具有强氧化性 D. HClO中氯元素的化合价为1价
25. 下列物质中既含有氯离子又含有氯分子的是
A. 氯水 B. 液氯 C. 次氯酸 D. 氯化钠
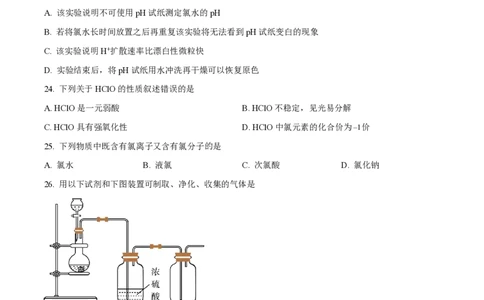
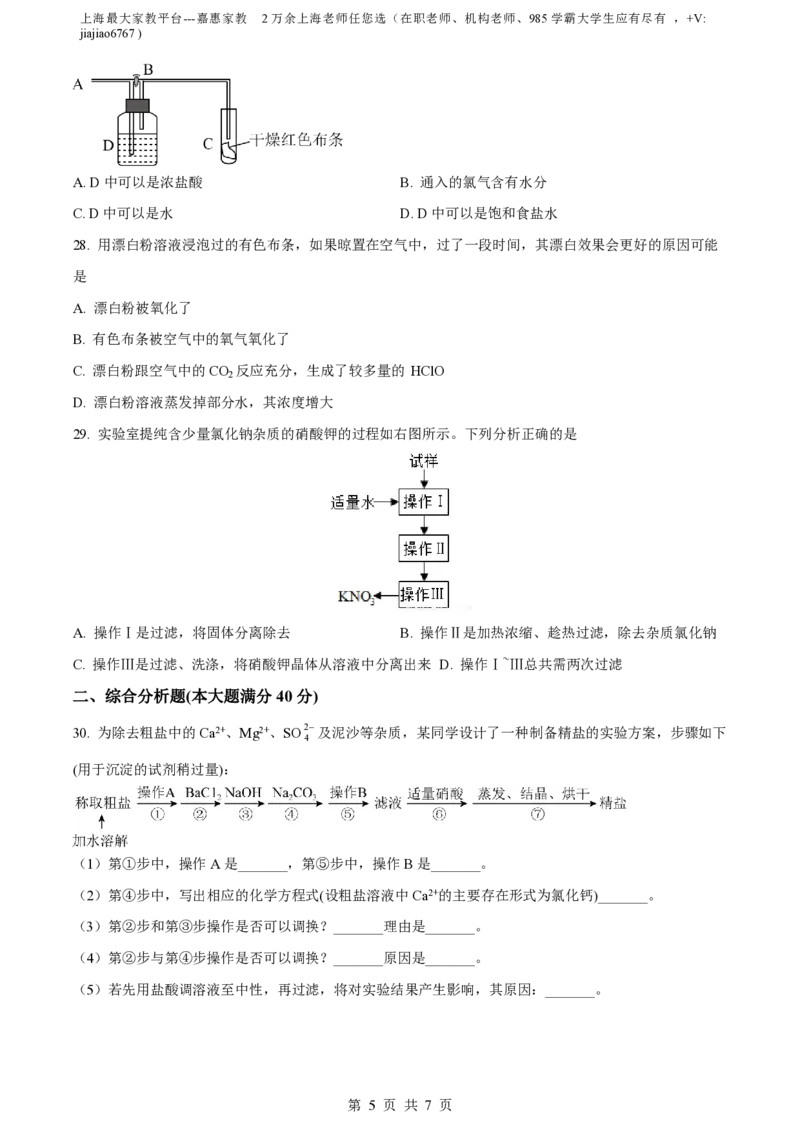
26. 用以下试剂和下图装置可制取、净化、收集的气体是
A. 锌和稀硫酸制氢气 B. 双氧水和二氧化锰制取氧气
C. 大理石和稀硫酸制二氧化碳 D. 氯酸钾和二氧化锰制氧气
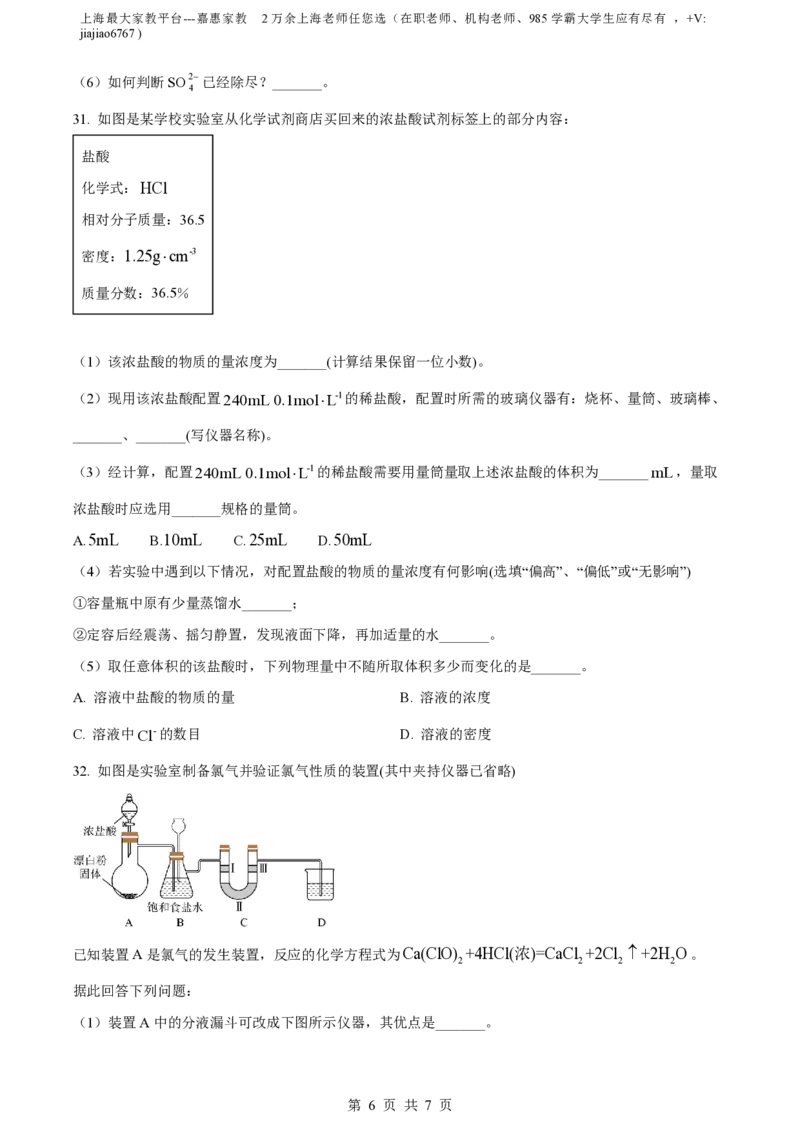
27. 如图:A处通入氯气,关闭B阀时,C处干燥红色布条无变化,打开B阀时,C处红色布条褪色。由
此作出的判断正确的是
第 4 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
A. D中可以是浓盐酸 B. 通入的氯气含有水分
C. D中可以是水 D. D中可以是饱和食盐水
28. 用漂白粉溶液浸泡过的有色布条,如果晾置在空气中,过了一段时间,其漂白效果会更好的原因可能
是
A. 漂白粉被氧化了
B. 有色布条被空气中的氧气氧化了
C. 漂白粉跟空气中的CO 反应充分,生成了较多量的 HClO
2
D. 漂白粉溶液蒸发掉部分水,其浓度增大
29. 实验室提纯含少量氯化钠杂质的硝酸钾的过程如右图所示。下列分析正确的是
A. 操作Ⅰ是过滤,将固体分离除去 B. 操作Ⅱ是加热浓缩、趁热过滤,除去杂质氯化钠
C. 操作Ⅲ是过滤、洗涤,将硝酸钾晶体从溶液中分离出来 D. 操作Ⅰ~Ⅲ总共需两次过滤
二、综合分析题(本大题满分 40分)
30. 为除去粗盐中的Ca2+、Mg2+、SO2及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下
4
(用于沉淀的试剂稍过量):
(1)第①步中,操作A是_______,第⑤步中,操作B是_______。
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为氯化钙)_______。
(3)第②步和第③步操作是否可以调换?_______理由是_______。
(4)第②步与第④步操作是否可以调换?_______原因是_______。
(5)若先用盐酸调溶液至中性,再过滤,将对实验结果产生影响,其原因:_______。
第 5 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(6)如何判断SO2已经除尽?_______。
4
31. 如图是某学校实验室从化学试剂商店买回来的浓盐酸试剂标签上的部分内容:
盐酸
化学式:HCl
相对分子质量:36.5
密度:1.25gcm-3
质量分数:36.5%
(1)该浓盐酸的物质的量浓度为_______(计算结果保留一位小数)。
(2)现用该浓盐酸配置240mL 0.1molL-1的稀盐酸,配置时所需的玻璃仪器有:烧杯、量筒、玻璃棒、
_______、_______(写仪器名称)。
(3)经计算,配置240mL 0.1molL-1的稀盐酸需要用量筒量取上述浓盐酸的体积为_______mL,量取
浓盐酸时应选用_______规格的量筒。
A.5mL B.10mL C.25mL D.50mL
(4)若实验中遇到以下情况,对配置盐酸的物质的量浓度有何影响(选填“偏高”、“偏低”或“无影响”)
①容量瓶中原有少量蒸馏水_______;
②定容后经震荡、摇匀静置,发现液面下降,再加适量的水_______。
(5)取任意体积的该盐酸时,下列物理量中不随所取体积多少而变化的是_______。
A. 溶液中盐酸的物质的量 B. 溶液的浓度
C. 溶液中Cl-的数目 D. 溶液的密度
32. 如图是实验室制备氯气并验证氯气性质的装置(其中夹持仪器已省略)
已知装置A是氯气的发生装置,反应的化学方程式为Ca(ClO) +4HCl(浓)=CaCl +2Cl +2H O。
2 2 2 2
据此回答下列问题:
(1)装置A中的分液漏斗可改成下图所示仪器,其优点是_______。
第 6 页 共 7 页上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸大学生应有尽有 ,+V:
jiajiao6767 )
(2)装置B是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置
B中的实验现象:_______。
(3)装置C中的作用是验证氯气是否具有漂白性,则装置C中I、II、III处依次应放入的物质是
_______(填序号)。
序号 I II III
a 干燥的有色布条 碱石灰 湿润的有色布条
b 湿润的有色布条 浓硫酸 干燥的有色布条
c 湿润的有色布条 无水氯化钙 干燥的有色布条
(4)装置D的作用是_______,则烧杯中的溶液是_______,写出所发生反应的化学方程式:_______。
(5)如果将20mL 10molL-1的浓盐酸与氯化钙充分反应,实际能收集到的氯气在标准状况下的体积将
_______。
A. 2.24L B. >2.24L C. 2.24L D. <2.24L
第 7 页 共 7 页