文档内容
吉安市五校联盟2028届高一第一次大联考(2025.10)
化学试卷
全卷满分100分,考试时间:75分钟
一、单选题(每题3分,共42分)
1.中国科学技术大学的钱逸泰教授等以CCl 和金属钠为原料,在700 ℃时反应制造出纳米级金刚
4
石粉末和另一种化合物。该成果发表在世界权威的《科学》杂志上,被科学家们高度评价为“稻
草变黄金”。同学们对此有下列的一些“理解”,其中说法错误的是( )
A.Na的活泼型强于金刚石
B.另一种化合物是NaCl
C.这个反应是置换反应
D.纳米级金刚石粉末可以透过半透膜
2.下列各组物质间的反应属于离子反应的是( )
A.北京冬奥会场馆使用CO 跨临界直冷制冰
2
B.《神农本草经》中记载的“石胆能化铁为铜”
C.氢气还原灼热的氧化铜
D.火药的发明与使用
3. 根据所学知识分析,下列物质分类正确的是( )
A.酸:CH COOH 、NH HSO 、 H SO 、HNO
3 4 4 2 4 3
B.碱:Ba(OH) 、NaOH、C H OH、KOH
2 2 5
C.碱性氧化物:CaO、 CuO 、Fe O 、MgO
2 3
D.酸性氧化物:CO 、SO 、CO、 SO
2 2 3
4.下列颜色变化中,与氧化还原反应无关的是( )
A.黑色的氧化铜溶于稀硫酸,溶液变蓝色
B.高温下,红棕色的氧化铁与焦炭充分反应转化为黑色固体
C.长时间使用的铜制水龙头上有铜绿[Cu (OH) CO ]产生
2 2 3
D.强光照射下,胶片中淡黄色的AgBr分解产生黑色的银单质
5.把b中三个碎纸片补充到a中,可得到一个完整的离子方程式(未配平)。b中补充到a中的反
应物是( )
A.OH- B. S2- C.SO 2- D.OH-和SO 2-
3 3
6.室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )
选项 实验操作和现象 结论
向某溶液中滴入AgNO 溶液,有白色沉
A 3 溶液中一定含有Cl-
淀产生.
向溶液X中先滴加稀硝酸,再滴加BaCl 溶液X中不一定含有
B 2
溶液,出现白色沉淀。 SO 2-
4
某钠盐溶于盐酸,产生能使澄清石灰水变
C 该钠盐一定是Na CO
浑浊的无色无味气体 2 3
向CuSO 溶液中加入铁粉,有红色固体析 Fe2+的 氧化性强于
D 4
出 Cu2+的氧化性
7. 按照物质的树状分类和交叉分类,硫酸应属于( )
①酸 ②能导电的纯净物 ③含氧酸 ④混合物
⑤化合物 ⑥二元酸 ⑦强电解质A.①②③④⑦ B.①③⑤⑥⑦
C.①②③⑤⑥⑦ D.②③⑤⑥⑦
8.下列反应的离子方程式书写错误的是( )
A.三氯化铁溶液与氢氧化钠溶液反应:Fe3++3OH-=Fe(OH) ↓
3
B.铁粉与稀硫酸反应:Fe+2H+=Fe2++H ↑
2
C.向BaCl 溶液中通入CO :Ba2++H O+CO =BaCO ↓+2H+
2 2 2 2 3
D.氢氧化铜与盐酸反应:Cu(OH) +2H+=2H O+Cu2+
2 2
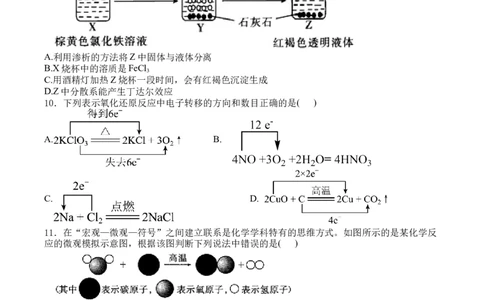
9.某同学在实验室进行了如图所示的实验,Y中发生的反应为
3CaCO +2FeCl +3H O==2Fe(OH) +3CO ↑+3CaCl ,下列说法中错误的是( )
3 3 2 3 2 2
A.利用渗析的方法将Z中固体与液体分离
B.X烧杯中的溶质是FeCl
3
C.用酒精灯加热Z烧杯一段时间,会有红褐色沉淀生成
D.Z中分散系能产生丁达尔效应
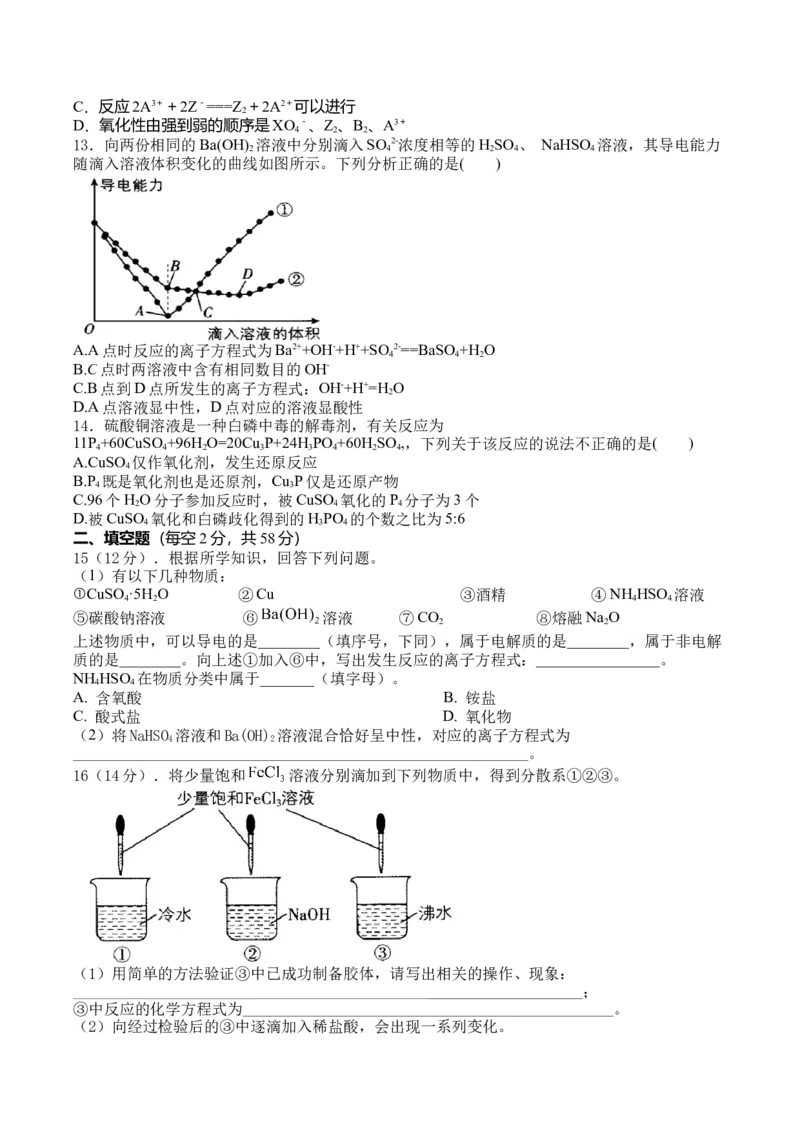
10.下列表示氧化还原反应中电子转移的方向和数目正确的是( )
A. B.
C. D.
11.在“宏观—微观—符号”之间建立联系是化学学科特有的思维方式。如图所示的是某化学反
应的微观模拟示意图,根据该图判断下列说法中错误的是( )
A.图中的反应物中有单质
B.化学反应前后氧元素的化合价没有改变
C.该反应属于置换反应
D.该反应是一个离子反应,同时也是氧化还原反应。
12.已知常温下,在溶液中发生如下反应:
①2A2++B ===2A3++2B-
2
②2B-+Z ===B +2Z-
2 2
③16H++10Z-+2XO===2X2++5Z +8H O
2 2
由此推断下列说法错误的是( )
A.还原性由强到弱的顺序是A2+、B-、Z-、X2+
B.Z元素在反应②中被还原,在反应③中被氧化C.反应2A3++2Z-===Z +2A2+可以进行
2
D.氧化性由强到弱的顺序是XO -、Z 、B 、A3+
4 2 2
13.向两份相同的Ba(OH) 溶液中分别滴入SO 2-浓度相等的H SO 、 NaHSO 溶液,其导电能力
2 4 2 4 4
随滴入溶液体积变化的曲线如图所示。下列分析正确的是( )
A.A点时反应的离子方程式为Ba2++OH-+H++SO 2-==BaSO +H O
4 4 2
B.C点时两溶液中含有相同数目的OH-
C.B点到D点所发生的离子方程式:OH-+H+=H O
2
D.A点溶液显中性,D点对应的溶液显酸性
14.硫酸铜溶液是一种白磷中毒的解毒剂,有关反应为
11P +60CuSO +96H O=20Cu P+24H PO +60H SO ,,下列关于该反应的说法不正确的是( )
4 4 2 3 3 4 2 4
A.CuSO 仅作氧化剂,发生还原反应
4
B.P 既是氧化剂也是还原剂,Cu P仅是还原产物
4 3
C.96个H O分子参加反应时,被CuSO 氧化的P 分子为3个
2 4 4
D.被CuSO 氧化和白磷歧化得到的H PO 的个数之比为5:6
4 3 4
二、填空题(每空2分,共58分)
15(12分).根据所学知识,回答下列问题。
(1)有以下几种物质:
①CuSO ·5H O ②Cu ③酒精 ④NH HSO 溶液
4 2 4 4
⑤碳酸钠溶液 ⑥ 溶液 ⑦CO ⑧熔融Na O
2 2
上述物质中,可以导电的是________(填序号,下同),属于电解质的是________,属于非电解
质的是________。向上述①加入⑥中,写出发生反应的离子方程式:________________。
NH HSO 在物质分类中属于_______(填字母)。
4 4
A. 含氧酸 B. 铵盐
C. 酸式盐 D. 氧化物
(2)将NaHSO 溶液和Ba(OH) 溶液混合恰好呈中性,对应的离子方程式为
4 2
___________________________________________________________。
16(14分).将少量饱和 溶液分别滴加到下列物质中,得到分散系①②③。
(1)用简单的方法验证③中已成功制备胶体,请写出相关的操作、现象:
__________________________________________________________________;
③中反应的化学方程式为________________________________________________。
(2)向经过检验后的③中逐滴加入稀盐酸,会出现一系列变化。先出现和②中相同的现象,因为_____________________________________。
随后发生变化得到和①相同的溶液,此反应的化学方程式为
________________________________________________________________________。
(3)下列关于分散系②和③的描述,说法正确的是________(填序号)。
A.两者颜色相同 B.两者稳定性相同
C.两者分散质粒子大小相同 D.两者的分散质都不能透过半透膜
(4)Fe(OH) 胶体可以与污水中的砷酸(H A O )反应生成砷酸铁( )沉淀,从而达到净水
3 3 S 4
的目的,该反应的化学方程式是
______________________________________________________________________。
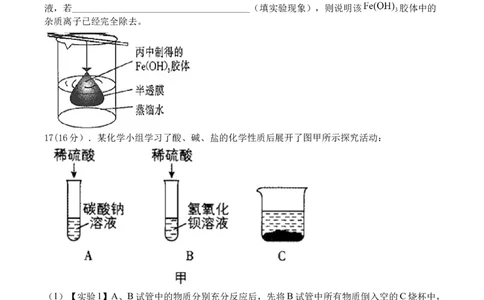
(5)可用如图所示的装置除去 胶体中的杂质离子来提纯 胶体,实验过程中需
不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入 溶
液,若______________________________________(填实验现象),则说明该 胶体中的
杂质离子已经完全除去。
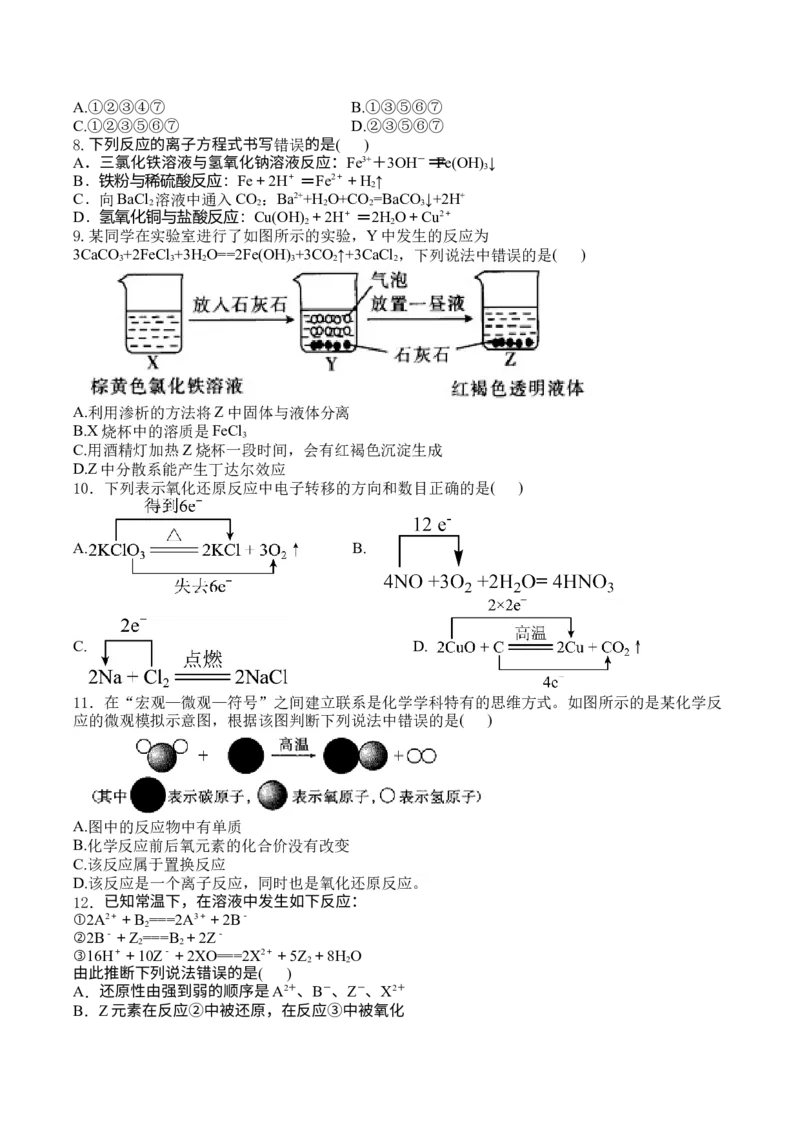
17(16分).某化学小组学习了酸、碱、盐的化学性质后展开了图甲所示探究活动:
(1)【实验1】A、B试管中的物质分别充分反应后,先将B试管中所有物质倒入空的C烧杯中,
再将A试管中所得溶液慢慢加入C烧杯中,烧杯内固体质量随加入A试管中液体质量的变化如图
乙所示。据此判断B试管中反应后所得溶液中的溶质是_________________(填化学式)。(2)【实验2】将C烧杯中沉淀过滤,向滤渣中加入过量稀硝酸,观察到的实验现象为
_________________________________________________,进而证明滤渣为混合物。写出烧杯内
固体质量增加所发生的离子方程式:________________________________、
________________________________
(3)某实验小组对某些物质进行性质探究实验后,将废液收集得到了澄清的溶液,该澄清溶液
中可能含有H+ 、Mg2+ 、Ba2+ 、NO - 、CO 2- 、SO 2-中的若干种,取该澄清溶液进行以下实验:
3 3 4
①用pH试纸检验,结果表明溶液呈强酸性。
②取出部分溶液于试管中,逐滴加入NaOH溶液,使溶液从酸性逐渐变为碱性,继续滴加NaOH
溶液,有白色沉淀生成,则可证明_______的存在。
③取部分②中碱性溶液于试管中,滴加Na CO 溶液,有白色沉淀生成,证明_______的存在,同
2 3
时可以排除_______的存在。
④综上实验分析,该澄清溶液中肯定存在的离子是________________________。
18(16分).氧化还原反应在生产、生活中有广泛的应用。
Ⅰ.古代炼铜时,所用原料主要是孔雀石[主要成分是Cu (OH) CO ]和木炭,冶炼温度为1000℃左
2 2 3
右,可能涉及的反应有
① ;② ;
③ ; ④ 。
(1)反应②中,还原剂是________(填化学式,下同),还原产物的是_______。
(2)Cu、C和CO的还原性由弱到强的顺序为________。
(3)在上述4个反应中属于氧化还原反应的是_______(填序号)。
Ⅱ.实验室可用KMnO 和浓盐酸反应制取氯气,其反应可表示为:2KMnO +16HCl
4 4 (浓)
=2KCl+2MnCl +5Cl ↑+8H O
2 2 2
(4)请将上述化学方程式改写为离子方程式:
________________________________________________________________________。
(5)上述反应每生成一个水分子转移了____________个电子。
(6)此反应中还原剂与氧化剂的个数比是_______________。
(7)实验室也可以用KClO 与浓盐酸制备氯气,请配平下面的化学方程式
3
_____KClO +_____HCl == _____KCl+_____Cl +_____H O
3 (浓) 2 2化学参考答案
一、单选题(每题3分,共42分)
1.答案:D
解析:胶体的分散质粒子直径在1~100 nm之间,粒子直径小于100 nm的纳米级金刚石粉末
可透过滤纸,不能透过半透膜。
2.答案:B
解析:CO 跨临界直冷制冰属于物理变化,A不符合题意;石胆能化铁为铜,描述的是铁与硫
2
酸铜溶液的反应,方程式是Cu2++Fe=Cu+Fe2+,属于离子反应,B符合题意:氢气还原灼热的
氧化铜,该反应不在水溶液中或熔融状态下进行,因此没有发生电离,不属于离子反应,C
不符合题意;火药的发明与使用,也不是在水溶液或熔融状态下进行,不属于离子反应,D
不符合题意。
3.答案:C
解析:A.电离产生的阳离子都是氢离子的化合物为酸, 属于盐,不是酸,故A不选;
B.电离产生的阴离子都是氢氧根离子的化合物为碱, 为非电解质,不是碱,故B不
选;
C.与酸反应只生成盐和水的氧化物为碱性氧化物,CaO、 CuO 、Fe O 、MgO都能与酸反应,
2 3
且产物都只是盐和水,属于碱性氧化物,故C选;
D.与碱反应只生成盐和水的氧化物酸性氧化物,CO与碱不反应,不是酸性氧化物,故D不选;
4.答案:A
解析:黑色的氧化铜与稀硫酸反应生成硫酸铜(蓝色)和水,没有元素化合价的改变,与氧
化还原反应无关,A符合题意;高温下,红棕色的氧化铁与焦炭充分反应转化为黑色固体铁,
铁、碳元素化合价发生改变,与氧化还原反应有关,B不符合题意:铜转化为铜绿的过程中
铜元素化合价升高,与氧化还原反应有关,C不符合题意;AgBr分解产生Ag的过程中银元素
化合价降低,与氧化还原反应有关,D不符合题意
5.答案:A
解析:根据电子守恒、电荷守恒、质量守恒可知, 是反应物,A项正确。
6.答案:B
解析:向某溶液中滴入 溶液,有白色沉淀产生,该白色沉淀可能是氯化银,也可能是
硫酸银等,溶液中不一定含有 ,A错误。向溶液X中先滴加稀硝酸,再滴加 溶液,
出现白色沉淀,原溶液中可能含有银离子,不一定含有 ,B正确。某钠盐溶于盐酸,产
生能使澄清石灰水变浑浊的无色无味气体,该气体是二氧化碳,则该钠盐可能是碳酸钠或碳
酸氢钠,C错误;;向 溶液中加入铁粉,有红色固体析出,发生的反应是
, 是氧化产物, 是氧化剂,氧化剂的氧化性强于氧化产物,
的氧化性弱于 的氧化性,D错误。
7.答案:B
解析:①硫酸的水溶液中电离生成的阳离子都是氢离子,从结构分类属于酸,故①正确;
②纯净的硫酸中没有能够自由移动的离子,不能导电,故②错误;
③硫酸由氢元素、硫元素、氧元素三种元素组成,属于含氧酸,故③正确;
④、⑤硫酸由氢元素、硫元素、氧元素三种元素组成的纯净物,属于化合物,故④错误、⑤
正确;
1mol硫酸可电离出2mol氢离子,属于二元酸,故⑥正确;
⑦硫酸在水溶液中能够完全电离,属于强电解质,故⑦正确;
故选:B。
8.答案:C解析:C项中向BaCl 溶液中通入 是弱酸,HCl是强酸,弱酸不能制强酸,故不发
2
生反应,C选项错误.
9.答案:A
解析:Z中是沉淀和胶体应该使用过滤的方法进行分离,A项错误
10.答案:B
解析:A.该反应中Cl元素化合价降低得电子,氧元素化合价升高失电子,转移电子数为12,
则电子转移的方向和数目为 ,选项A错误
B.反应中电子转移的方向和数目均正确,选项B正确;
C.反应中Na共失去 , 共得到 ,电子转移数目正确,但电子转移方向有误,选项C
错误;
D.;CuO与C反应,铜得电子,C失电子,则电子转移的方向和数目为
,选项D错误;
答案选C。
11.答案:D
解析:图示反应为 ,图中的反应物有C单质,A正确;反应前H O中的O
2
元素和反应后CO中中O元素的化合价均为-2价,故反应前后氧元素的化合价没有变化,B正
确;该反应中单质与化合物反应,产生新的单质和新的化合物,因此该反应属于置换反应,C
正确。该反应的H元素和C元素化合价发生改变,所以是氧化还原反应;由于高温下H O是气
2
体分子,C是单质,所以反应物不会电离,该反应不是离子反应,D错误。
12.答案:C
解析:由③可知氧化性:XO >Z ,还原性:Z-> X2+;由①可知氧化性:B >A3+,还原性:A2+>
2 2
B-;由②可知氧化性:Z > B ,还原性:B->Z-。即氧化性顺序为 XO >Z >B >A3+,还原性顺
2 2 2 2
序为A2+>B->Z->X2+,因此2A3++2Z-===Z +2A2+不能进行,选项C错误。
2
13.答案:C
解析: 溶液和 溶液的反应分别为
,
、
,由题图可知,曲线在A点溶液导
电能力接近0,说明A点溶液中几乎没有自由移动的离子,曲线①应该为滴加 溶液的变
化曲线,曲线②为滴加 溶液的变化曲线,由题图可知,A点时 和 恰好
反应,反应的离子方程式为Ba2++2OH-+2H++SO 2-==BaSO +H O,A错误;曲线①C点表示稀硫酸
4 4 2过量,溶质为硫酸,曲线②C点表示硫酸氢钠与溶液中的OH继续反应,结合上述分析可知
溶质为NaOH、 ,两溶液中含有的 数目不同,B错误;曲线②中B点是NaOH溶液,
从B点到D点是NaOH与NaHSO 的反应,离子方程式为H++OH-=H O,故C项正确。由题图知,曲
4 2
线①A点硫酸和氢氧化钡恰好完全反应,溶液中只含水,溶液显中性;曲线②中D点后溶液
导电能力逐渐增大,则D点 与沉淀 时生成的NaOH恰好完全反应,溶质为
,溶液都呈中性,D错误。
14.答案:D
解析: 中Cu元素化合价降低,其他元素化合价不变, 仅作氧化剂,发生还原反
应,A正确。 中部分P元素化合价升高,部分P元素化合价降低,则 既是氧化剂也是还
原剂,CuP中的Cu和P分别为+1价和-3价,即分别由 中Cu和 中P还原而来,则
仅是还原产物,B正确。1个 分子被氧化时,失去20个电子;96个 分子参加反
应时, 得到60个电子,则被 氧化的 分子数目为 ,C正确。 被氧化为
的过程中,每生成1个 分子转移5个电子,则被 氧化得到的 的个
数为 ,白磷歧化得到的 分子的个数为24-12=12,其质量之比为1:1,D错误。
二、填空题(每空2分,共58分)
15(每空2分,共12分).
(1)②④⑤⑥⑧; ①⑧; ③⑦;Cu2++SO 2-+Ba2++2OH-=BaSO ↓+Cu(OH) ↓ ; BC
4 4 2
(2)
解析:(1)①CuSO ·5H O是固体不能导电,属于盐,属于电解质;②Cu能导电,是单质,
4 2
不属于电解质,也不属于非电解质;③酒精是有机物,不能导电,属于非电解质;④NH HSO
4 4
溶液能导电,是混合物,不属于电解质,也不属于非电解质;⑤碳酸钠溶液能导电,是混合
物,不属于电解质,也不属于非电解质;⑥ 溶液能导电,是混合物,不属于电解质,
也不属于非电解质;⑦ 不能导电,属于非电解质;⑧熔融Na O能导电,属于电解质。因
2
此可以导电的是②④⑤⑥⑧,属于电解质的是①⑧,属于非电解质的是③⑦。向 溶液
加入CuSO ·5H O固体,CuSO ·5H O会溶解并电离Cu2+、SO 2-,该反应的离子方程式Cu2++SO 2-
4 2 4 2 4 4
+Ba2++2OH-=BaSO ↓+Cu(OH) ↓。NH HSO 因为阳离子是NH +,所以属于铵盐,又因为阴离子是
4 2 4 4 4
HSO -,所以属于酸式盐。
4
(2)NaHSO =Na++H++SO 2- ,Ba(OH) =Ba2++2OH-,NaHSO 溶液和Ba(OH) 溶液混合恰好呈中性,因
4 4 2 4 2
此NaHSO 与Ba(OH) 的个数比为2:1,反应的离子方程式为:2H++SO 2-+Ba2++2OH-
4 2 4
=BaSO ↓+2H O
4 2
16 (每空2分,共14分).
(1)用一束光照射,有光亮的“通路”;
(2)Fe(OH) 胶体遇到稀盐酸会发生聚沉,因而形成红褐色沉淀;
3
(3)AD(4)Fe(OH) H AsO FeAsO 3H O
3 3 4 4 2
(5)不出现白色沉淀
解析:(1)分散系③为胶体;光束通过胶体时,光线能够发生散射作用而产生丁达尔效应,
光束通入其他分散系时不能产生丁达尔效应,则可利用丁达尔效应来验证胶体,具体操作:
使用一束光线照射分散系,然后观察是否产生一条光亮的“通路”。向沸水中滴加饱和氯化
铁溶液后,继续加热煮沸至液体变为红褐色可得到氢氧化铁胶体,化学方程式为
。
(2)稀盐酸中有 和 ,由于 胶体的胶粒带正电荷,遇到带负电的阴离子会发生
聚沉,因而形成红褐色沉淀。氢氧化铁能与盐酸发生反应生成氯化铁和水,沉淀溶解,此反
应的化学方程式为 。
(3)氢氧化钠和氯化铁反应生成氢氧化铁红褐色沉淀,则分散系②是悬浊液;分散系③是氢
氧化铁胶体。两者均为红褐色,颜色相同,A正确:悬浊液与胶体稳定性不同,悬浊液不稳
定,胶体介稳定,B错误;胶体和悬浊液的分散质粒子直径大小不同,C错误;胶体和沉淀的
分散质不能透过半透膜,D正确。
(4) 胶体可以与污水中的砷酸反应生成砷酸铁(FeAsO )沉淀,同时生成水,该
4
反应为酸碱中和反应,由 化学式可知砷酸是三元酸,与 按个数比1:1进行反
应,该反应的化学方程式是 。
(5) 与Cl反应生成AgCl沉淀。向其中加入 溶液,若不出现白色沉淀,则说明
该 胶体中的杂质离子已经完全除去。
17(每空2分,共16分)
(1) ;
(2)沉淀部分溶解,有气泡产生;Ba2++SO 2-=BaSO ↓ 、 Ba2++CO 2-=BaCO ↓
4 4 3 3
(3)② ③ ; ④
解析:
(1)向C烧杯中加入A试管中液体后固体质量逐渐增加,说明有沉淀生成,碳酸钠、硫酸钠
与氢氧化钡反应都可以直接生成沉淀,所以B试管中氢氧化钡过量,(2)已知结论为滤渣为
混合物,则滤渣为 与 的混合物,碳酸钡可溶于稀硝酸,硫酸钡不溶于稀硝酸,
因此加入稀硝酸后滤渣部分溶解,并有气泡产生。烧杯内固体质量增加所发生的离子方程式:
Ba2++SO 2-=BaSO ↓ 、 Ba2++CO 2-=BaCO ↓
4 4 3 3
(3)①用pH试纸检验,结果表明溶液呈强酸性,则溶液中含有大量 能与 反应,
所以可以排除 的存在。②取出部分溶液于试管中,逐滴加入NaOH溶液,使溶液从酸性
逐渐变为碱性,继续滴加NaOH溶液,有白色沉淀生成,说明 与 反应生成
白色沉淀,则可证明 的存在。③取部分②中碱性溶液于试管中,滴加 溶液,有
白色沉淀生成,说明 与 反应生成 白色沉淀,则可证明 的存在,由于
能与 反应生成 沉淀,因此可以排除 的存在。④综上实验分析,该澄清溶液中不存在的离子有 ,肯定存在的离子有 ,由于溶液呈电中
性,所以溶液中还存在 。
18(每空2分,第7小问算一空,共16分).
(1)C;Cu
(2) Cu