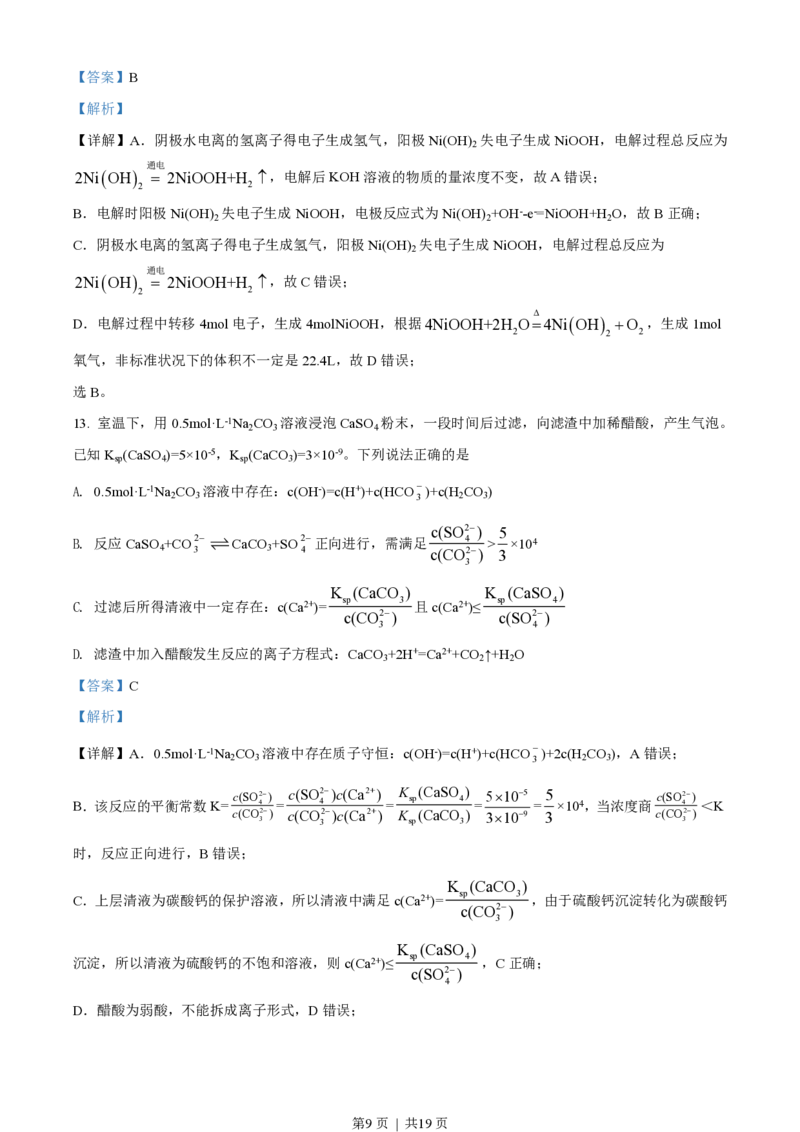文档内容
江苏省 2021 年普通高中学业水平选择性考试
化学
注意事项:
1.本试卷满分为 100分,考试时间为 75分钟。考试结束后,请将本试卷和答题卡一并交回。
2.答题前,请务必将自己的姓名、准考证号用 0.5 毫米黑色墨水的签字笔填写在试卷及答题卡
的规定位置。
3.请认真核对监考员在答题卡上所粘贴的条形码上的姓名、准考证号与本人是否相符。
4.作答选择题,必须用 2B 铅笔将答题卡上对应选项的方框涂满、涂黑;如需改动,请用橡皮
擦干净后,再选涂其他答案。作答非选择题,必须用 0.5毫米黑色墨水的签字笔在答题卡上的
指定位置作答,在其他位置作答一律无效。
5.如需作图,必须用 2B铅笔绘写清楚,线条符号等须加黑加粗。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 C1-35.5 Mn-55 Fe-56
Zn-65
一、单项选择题:共 14题,每题 3分,共 42分。每题只有一个选项最符合题意。
1. 黑火药是中国古代四大发明之一,其爆炸反应为2KNO +S+3C=K S+N ↑+3CO ↑。下列说法正确的是
3 2 2 2
A. 黑火药中含有两种单质 B. 爆炸时吸收热量
C. 反应中S作还原剂 D. 反应为置换反应
【答案】A
【解析】
【详解】A.黑火药中含有S、C两种单质,A正确;
B.爆炸反应为放热反应,B错误;
C.该反应中S元素化合价降低,作氧化剂,C错误;
D.该反应不符合“单质+化合物=另一种单质+另一种化合物”的形式,不是置换反应,D错误;
综上所述答案为A。
2. 反应Cl +2NaOH=NaClO+NaCl+H O可用于制备含氯消毒剂。下列说法正确的是
2 2
A. Cl 是极性分子
2
B. NaOH的电子式为
C. NaClO既含离子键又含共价键
D. Cl-与Na+具有相同的电子层结构
【答案】C
第1页 | 共19页【解析】
【详解】A.氯气分子结构对称,正负电荷中心重合,为非极性分子,A错误;
B.NaOH为离子化合物,电子式为 ,B错误;
C.NaClO含有钠离子和次氯酸根形成的离子键,含有O原子和Cl原子形成的共价键,C正确;
D.Cl-有3层电子,Na+有2层电子,D错误;
综上所述答案为C。
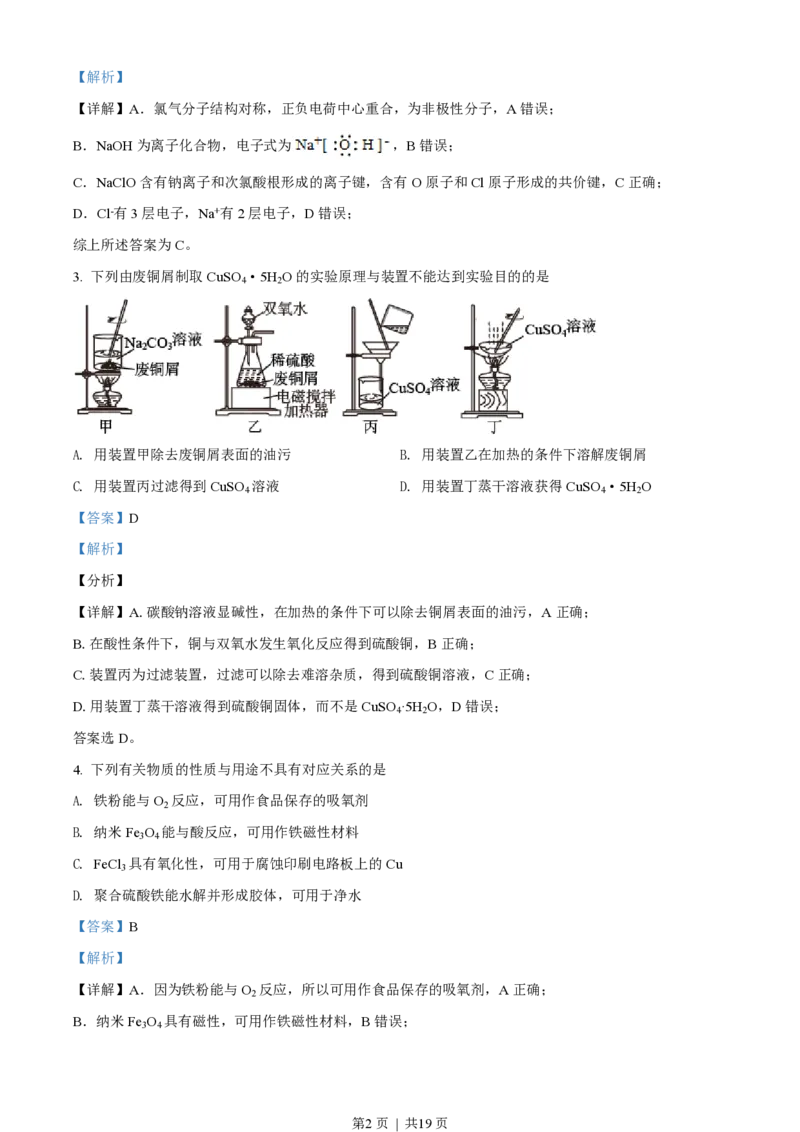
3. 下列由废铜屑制取CuSO ·5H O的实验原理与装置不能达到实验目的的是
4 2
A. 用装置甲除去废铜屑表面的油污 B. 用装置乙在加热的条件下溶解废铜屑
C. 用装置丙过滤得到CuSO 溶液 D. 用装置丁蒸干溶液获得CuSO ·5H O
4 4 2
【答案】D
【解析】
【分析】
【详解】A.碳酸钠溶液显碱性,在加热的条件下可以除去铜屑表面的油污,A正确;
B.在酸性条件下,铜与双氧水发生氧化反应得到硫酸铜,B正确;
C.装置丙为过滤装置,过滤可以除去难溶杂质,得到硫酸铜溶液,C正确;
D.用装置丁蒸干溶液得到硫酸铜固体,而不是CuSO ·5H O,D错误;
4 2
答案选D。
4. 下列有关物质的性质与用途不具有对应关系的是
A. 铁粉能与O 反应,可用作食品保存的吸氧剂
2
B. 纳米Fe O 能与酸反应,可用作铁磁性材料
3 4
C. FeCl 具有氧化性,可用于腐蚀印刷电路板上的Cu
3
D. 聚合硫酸铁能水解并形成胶体,可用于净水
【答案】B
【解析】
【详解】A.因为铁粉能与O 反应,所以可用作食品保存的吸氧剂,A正确;
2
B.纳米Fe O 具有磁性,可用作铁磁性材料,B错误;
3 4
第2页 | 共19页C.FeCl 与Cu反应生成FeCl 和CuCl ,主要利用其氧化性,C正确;
3 2 2
D.聚合硫酸铁能水解并形成胶体,具有吸附性,可用于净水,D正确;
故选B。
5. 前4周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量最多的元素,Y的周期序数与族
序数相等,基态时Z原子3p原子轨道上有5个电子,W与Z处于同个主族。下列说法正确的是
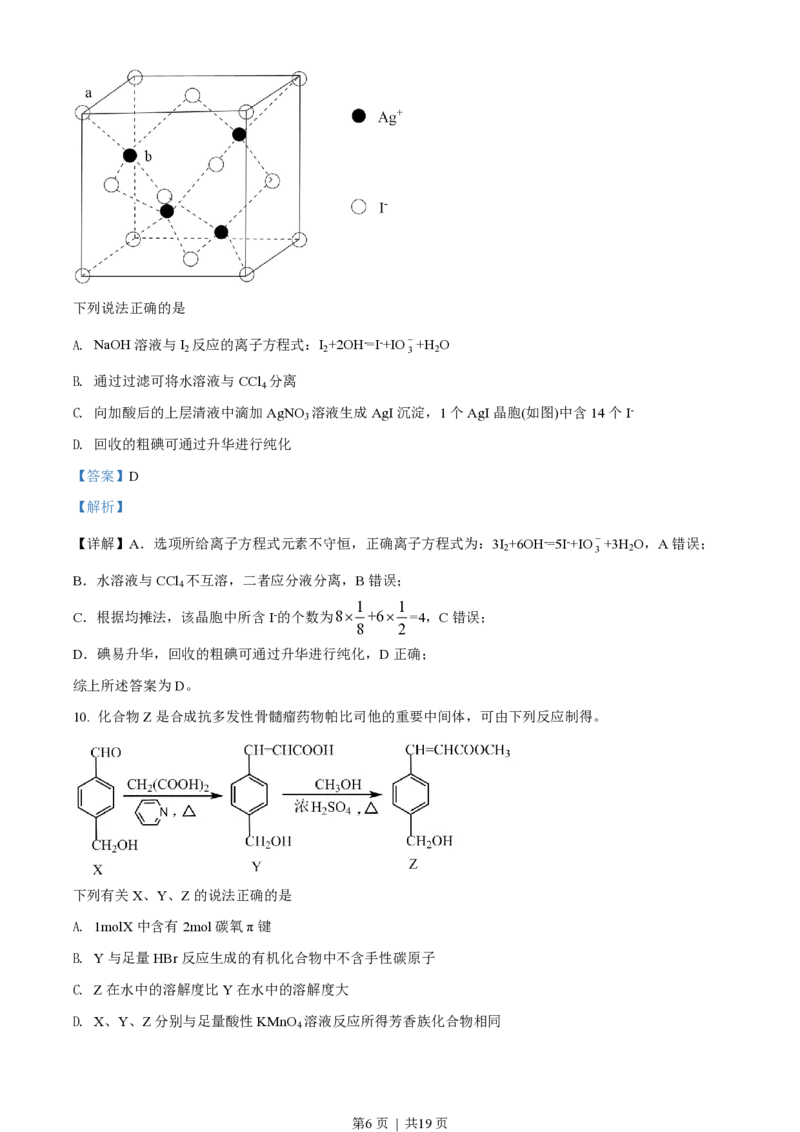
A. 原子半径:r(X) w
a2 2 3 K (H CO )
a1 2 3
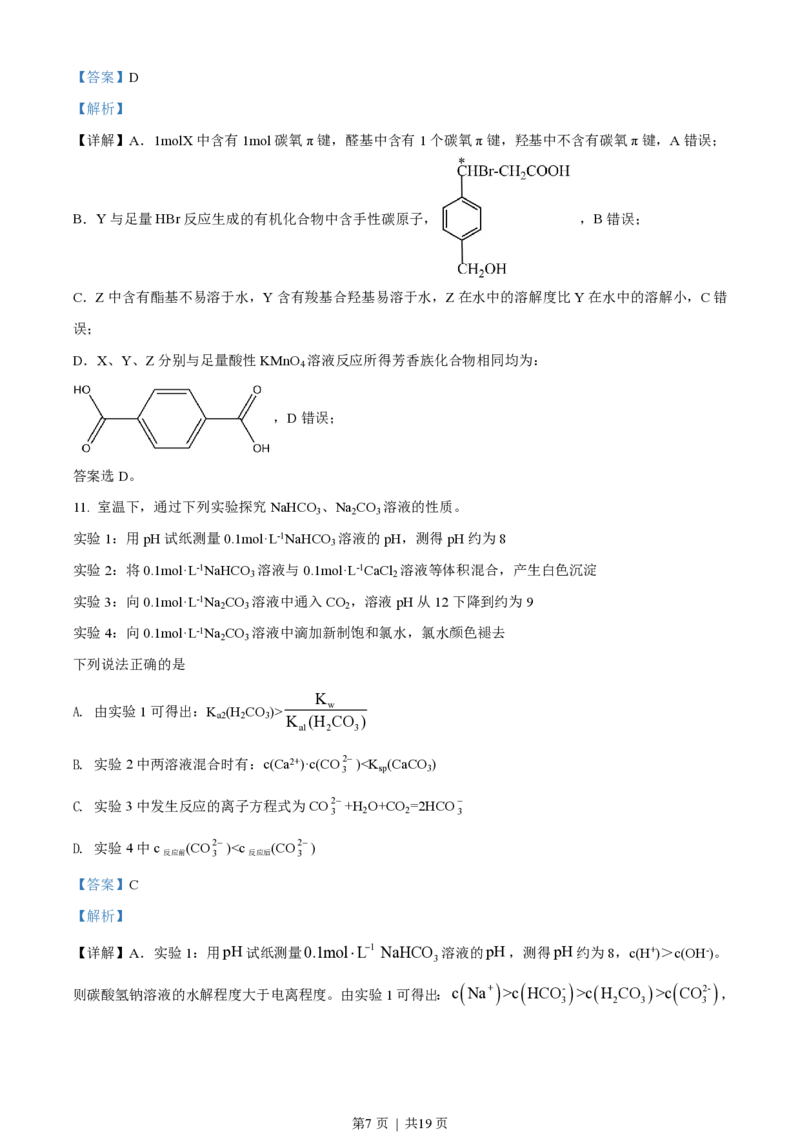
B. 实验2中两溶液混合时有:c(Ca2+)·c(CO2-)c HCO- >cH CO >c CO2- ,
3 2 3 3
第7页 | 共19页H+·HCO- H+·CO2- H+·CO2- K
K =H+·OH- , K = 3 , K = 3 , K (H CO )= 3 < w =
w a1 H CO a2 HCO- a2 2 3 HCO- K (H CO )
2 3 3 3 a1 2 3
OH-·H CO
2 3 ,A错误;
HCO-
3
B.实验2:将0.1mol×L-1 NaHCO 溶液与0.1mol×L-1 CaCl 溶液等体积混合,产生白色沉淀碳酸钙,则
3 2
由沉淀溶解平衡原理知,实验2中两溶液混合时有:c Ca2+ ×c CO2- >K CaCO ,B错误;
3 sp 3
C.等物质的量浓度的碳酸钠碱性大于碳酸氢钠。实验3:0.1mol×L-1 Na CO 溶液中通入一定量的CO ,
2 3 2
溶液pH从12下降到10,则实验3中发生反应的离子方程式为CO2- +H O+CO =2HCO-,C正确;
3 2 2 3
D. 由图知:Na CO 和盐酸反应是放热反应, NaHCO 和盐酸反应是吸热反应,c (CO2-)>c (CO
2 3 3 反应前 3 反应后
2-),D错误;
3
答案选C。
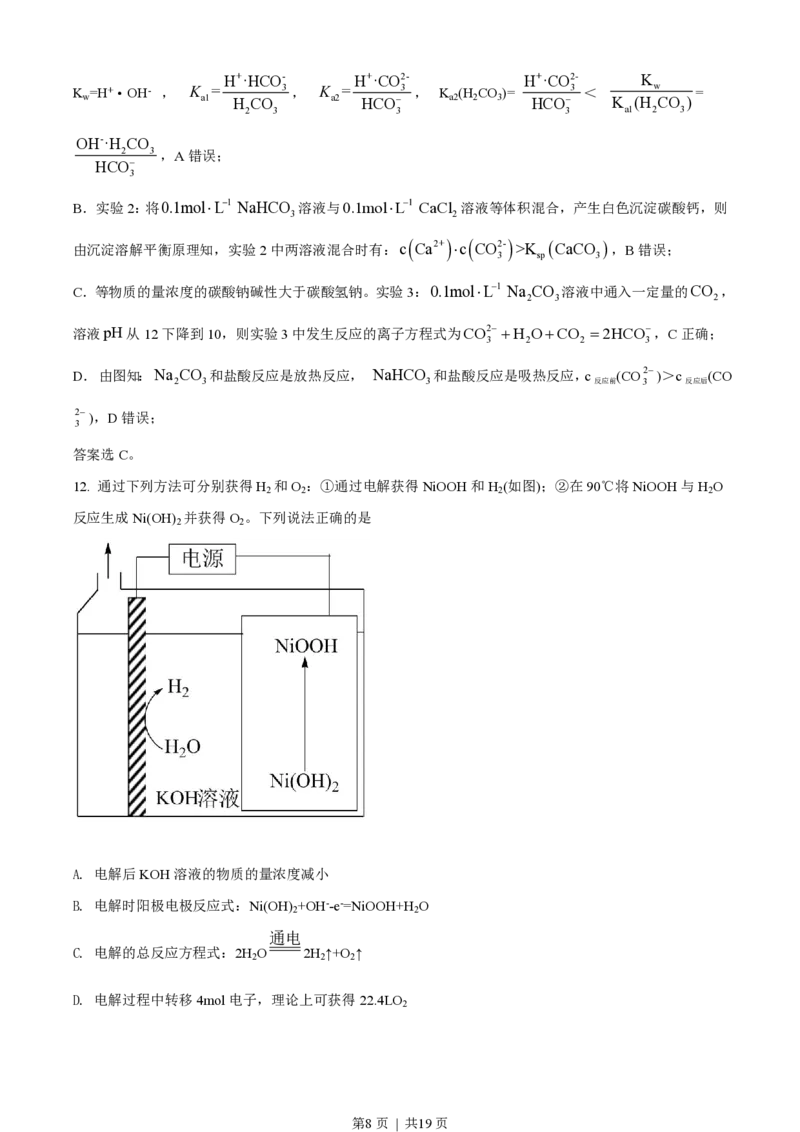
12. 通过下列方法可分别获得H 和O :①通过电解获得NiOOH和H (如图);②在90℃将NiOOH与H O
2 2 2 2
反应生成Ni(OH) 并获得O 。下列说法正确的是
2 2
A. 电解后KOH溶液的物质的量浓度减小
B. 电解时阳极电极反应式:Ni(OH) +OH--e-=NiOOH+H O
2 2
通电
C. 电解的总反应方程式:2H O 2H ↑+O ↑
2 2 2
D. 电解过程中转移4mol电子,理论上可获得22.4LO
2
第8页 | 共19页【答案】B
【解析】
【详解】A.阴极水电离的氢离子得电子生成氢气,阳极Ni(OH) 失电子生成NiOOH,电解过程总反应为
2
通电
2NiOH = 2NiOOH+H ,电解后KOH溶液的物质的量浓度不变,故A错误;
2 2
B.电解时阳极Ni(OH) 失电子生成NiOOH,电极反应式为Ni(OH) +OH--e-=NiOOH+H O,故B正确;
2 2 2
C.阴极水电离的氢离子得电子生成氢气,阳极Ni(OH) 失电子生成NiOOH,电解过程总反应为
2
通电
2NiOH = 2NiOOH+H ,故C错误;
2 2
D
D.电解过程中转移4mol电子,生成4molNiOOH,根据4NiOOH+2H O=4NiOH +O ,生成1mol
2 2 2
氧气,非标准状况下的体积不一定是22.4L,故D错误;
选B。
13. 室温下,用0.5mol·L-1Na CO 溶液浸泡CaSO 粉末,一段时间后过滤,向滤渣中加稀醋酸,产生气泡。
2 3 4
已知K (CaSO )=5×10-5,K (CaCO )=3×10-9。下列说法正确的是
sp 4 sp 3
A. 0.5mol·L-1Na CO 溶液中存在:c(OH-)=c(H+)+c(HCO-)+c(H CO )
2 3 3 2 3
c(SO2-) 5
B. 反应CaSO
4
+CO
3
2- CaCO
3
+SO2
4
-正向进行,需满足
c(CO
4
2-)
>
3
×104
3
K (CaCO ) K (CaSO )
sp 3 sp 4
C. 过滤后所得清液中一定存在:c(Ca2+)= 且c(Ca2+)≤
c(CO2-) c(SO2-)
3 4
D. 滤渣中加入醋酸发生反应的离子方程式:CaCO +2H+=Ca2++CO ↑+H O
3 2 2
【答案】C
【解析】
【详解】A.0.5mol·L-1Na CO 溶液中存在质子守恒:c(OH-)=c(H+)+c(HCO-)+2c(H CO ),A错误;
2 3 3 2 3
B.该反应的平衡常数K=
c(SO2
4
-)
=
c(SO2
4
-)c(Ca2+)
=
K
sp
(CaSO
4
)
=
5´10-5
=
5
×104,当浓度商
c(SO2
4
-)
<K
c(CO2-) c(CO2-)c(Ca2+) K (CaCO ) 3´10-9 3 c(CO2-)
3 3 sp 3 3
时,反应正向进行,B错误;
K (CaCO )
sp 3
C.上层清液为碳酸钙的保护溶液,所以清液中满足c(Ca2+)= ,由于硫酸钙沉淀转化为碳酸钙
c(CO2-)
3
K (CaSO )
sp 4
沉淀,所以清液为硫酸钙的不饱和溶液,则c(Ca2+)≤ ,C正确;
c(SO2-)
4
D.醋酸为弱酸,不能拆成离子形式,D错误;
第9页 | 共19页综上所述答案为C。
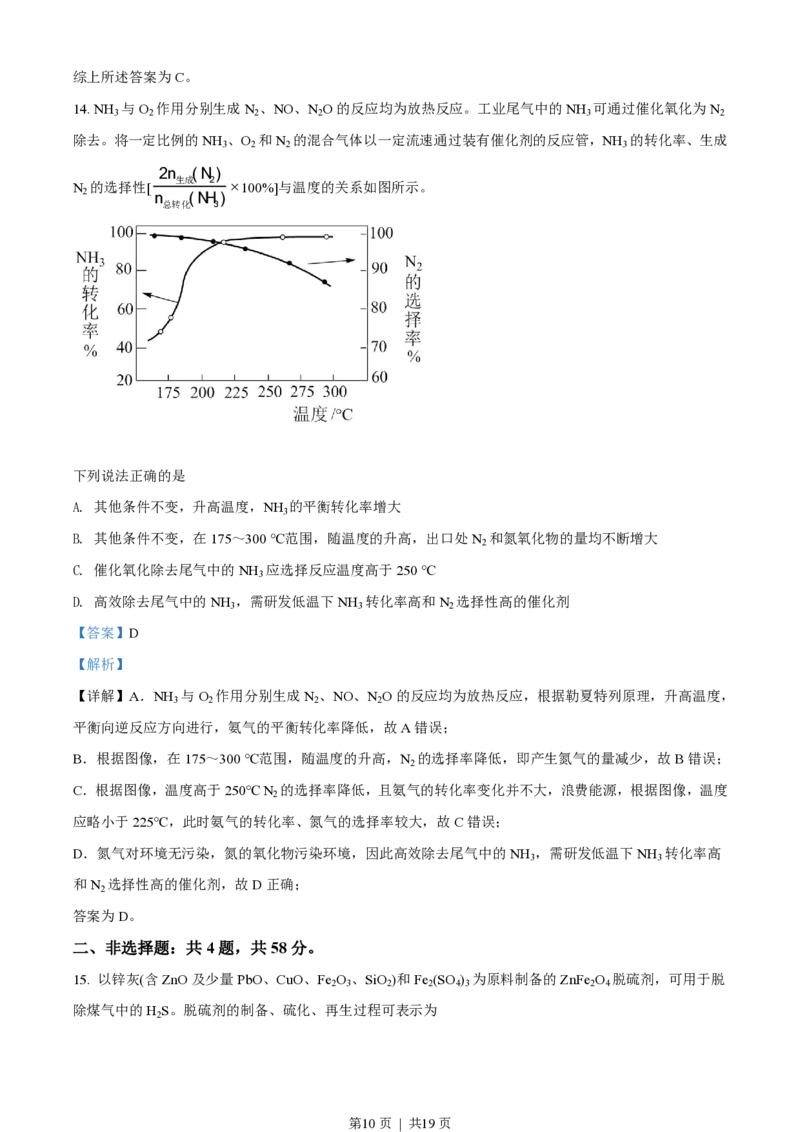
14. NH 与O 作用分别生成N 、NO、N O的反应均为放热反应。工业尾气中的NH 可通过催化氧化为N
3 2 2 2 3 2
除去。将一定比例的NH 、O 和N 的混合气体以一定流速通过装有催化剂的反应管,NH 的转化率、生成
3 2 2 3
2n (N)
N 的选择性[ 生成 2 ´100%]与温度的关系如图所示。
2 n (NH)
总转化 3
下列说法正确的是
A. 其他条件不变,升高温度,NH 的平衡转化率增大
3
B. 其他条件不变,在175~300 ℃范围,随温度的升高,出口处N 和氮氧化物的量均不断增大
2
C. 催化氧化除去尾气中的NH 应选择反应温度高于250 ℃
3
D. 高效除去尾气中的NH ,需研发低温下NH 转化率高和N 选择性高的催化剂
3 3 2
【答案】D
【解析】
【详解】A.NH 与O 作用分别生成N 、NO、N O的反应均为放热反应,根据勒夏特列原理,升高温度,
3 2 2 2
平衡向逆反应方向进行,氨气的平衡转化率降低,故A错误;
B.根据图像,在175~300 ℃范围,随温度的升高,N 的选择率降低,即产生氮气的量减少,故B错误;
2
C.根据图像,温度高于250℃ N 的选择率降低,且氨气的转化率变化并不大,浪费能源,根据图像,温度
2
应略小于225℃,此时氨气的转化率、氮气的选择率较大,故C错误;
D.氮气对环境无污染,氮的氧化物污染环境,因此高效除去尾气中的NH ,需研发低温下NH 转化率高
3 3
和N 选择性高的催化剂,故D正确;
2
答案为D。
二、非选择题:共 4题,共 58分。
15. 以锌灰(含ZnO及少量PbO、CuO、Fe O 、SiO )和Fe (SO ) 为原料制备的ZnFe O 脱硫剂,可用于脱
2 3 2 2 4 3 2 4
除煤气中的H S。脱硫剂的制备、硫化、再生过程可表示为
2
第10页 | 共19页(1)“除杂”包括加足量锌粉、过滤加H O 氧化等步骤。除Pb2+和Cu2+外,与锌粉反应的离子还有___(填化
2 2
学式)。
(2)“调配比”前,需测定ZnSO 溶液的浓度。准确量取2.50mL除去Fe3+的ZnSO 溶液于100mL容量瓶中,
4 4
加水稀释至刻度;准确量取20.00mL稀释后的溶液于锥形瓶中,滴加氨水调节溶液pH=10,用
0.0150mol·L-1EDTA(Na H Y)溶液滴定至终点(滴定反应为Zn2++Y4-=ZnY2-),平行滴定3次,平均消耗EDTA
2 2
溶液25.00mL。计算ZnSO 溶液的物质的量浓度___(写出计算过程)。
4
(3)400℃时,将一定比例H 、CO、CO 和H S的混合气体以一定流速通过装有ZnFe O 脱硫剂的硫化反
2 2 2 2 4
应器。
①硫化过程中ZnFe O 与H 、H S反应生成ZnS和FeS,其化学方程式为___。
2 4 2 2
②硫化一段时间后,出口处检测到COS。研究表明ZnS参与了H S与CO 生成COS的反应,反应前后ZnS
2 2
的质量不变,该反应过程可描述为___。
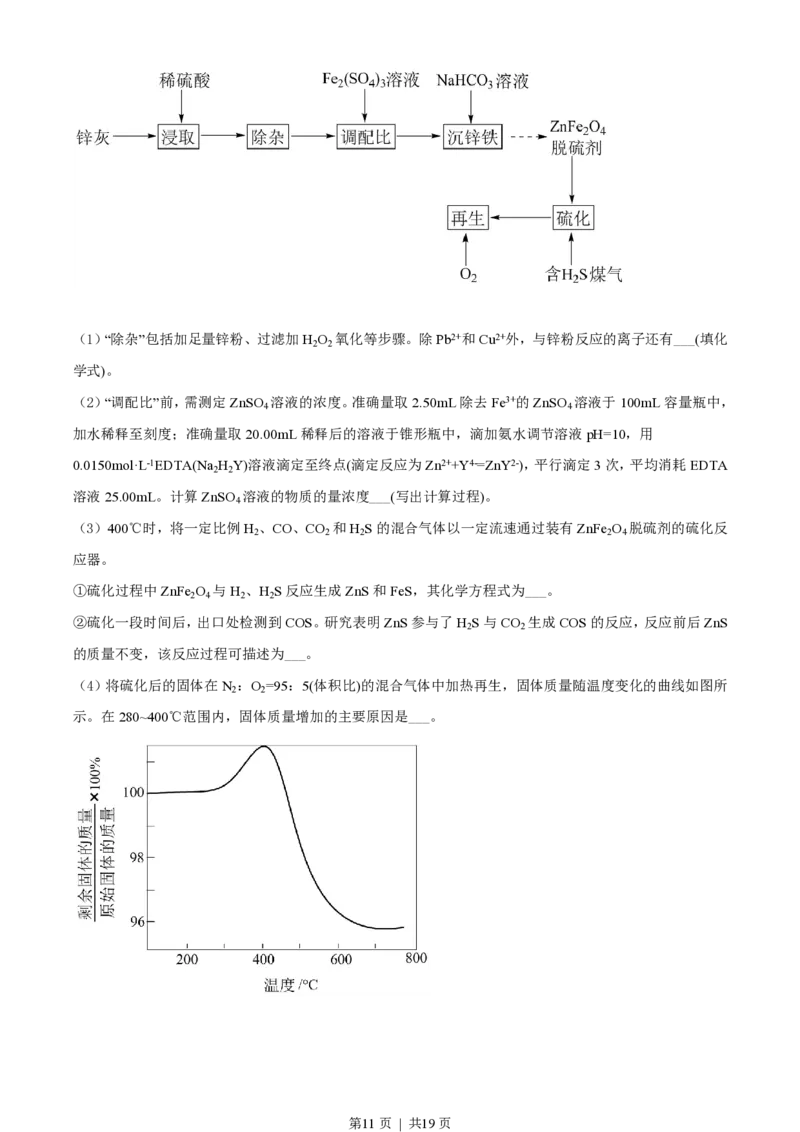
(4)将硫化后的固体在N :O =95:5(体积比)的混合气体中加热再生,固体质量随温度变化的曲线如图所
2 2
示。在280~400℃范围内,固体质量增加的主要原因是___。
第11页 | 共19页【答案】(1)Fe3+、H+
(2)0.7500mol·L-1
400℃
( 3 ) ①. ZnFe O +3H S+H ZnS+2FeS+4H O ②. ZnS+CO =ZnO+COS ;
2 4 2 2 2 2
ZnO+H S=ZnS+H O
2 2
(4)ZnS和FeS部分被氧化为硫酸盐
【解析】
【分析】锌灰含 ZnO 及少量 PbO、CuO、Fe O 、SiO ,加入稀硫酸浸取,SiO 和硫酸不反应,过滤出
2 3 2 2
SiO ,所得溶液中含有硫酸锌、硫酸铅、硫酸铜、硫酸铁、硫酸,加足量锌粉,硫酸铜、硫酸铁、硫酸都能
2
与锌反应,加H O 氧化,再加入硫酸铁调节锌、铁的配比,加入碳酸氢钠沉锌铁,制得脱硫剂ZnFe O 。
2 2 2 4
【小问1详解】
“除杂”加足量锌粉,硫酸铜、硫酸铁、硫酸都能与锌反应,除Pb2+和Cu2+外,与锌粉反应的离子还有Fe3+、
H+。
【小问2详解】
根 据 Zn2++Y4-=ZnY2- , 可 知 20.00mL 稀 释 后 的 溶 液 中 含 ZnSO 的 物 质 的 量 为
4
3.75´10-4mol
=0.75mol/L
0.025L×0.015mol·L-1=3.75×10-4mol;ZnSO 溶液的物质的量浓度为 20 ;
4 2.5´10-3´
100
【小问3详解】
①硫化过程中ZnFe O 与H 、H S反应生成ZnS和FeS,铁元素化合价由+3降低为+2、氢气中H元素化合
2 4 2 2
400℃
价由0升高为+1,根据得失电子守恒,其化学方程式为ZnFe O +3H S+H ZnS+2FeS+4H O;
2 4 2 2 2
②硫化一段时间后,出口处检测到COS。研究表明ZnS参与了H S与CO 生成COS的反应,反应前后ZnS
2 2
的质量不变,ZnS为催化剂,该反应过程可描述为ZnS+CO =ZnO+COS;ZnO+H S=ZnS+H O;
2 2 2
【小问4详解】
在280~400℃范围内,ZnS和FeS吸收氧气,ZnS和FeS部分被氧化为硫酸盐,固体质量增加。
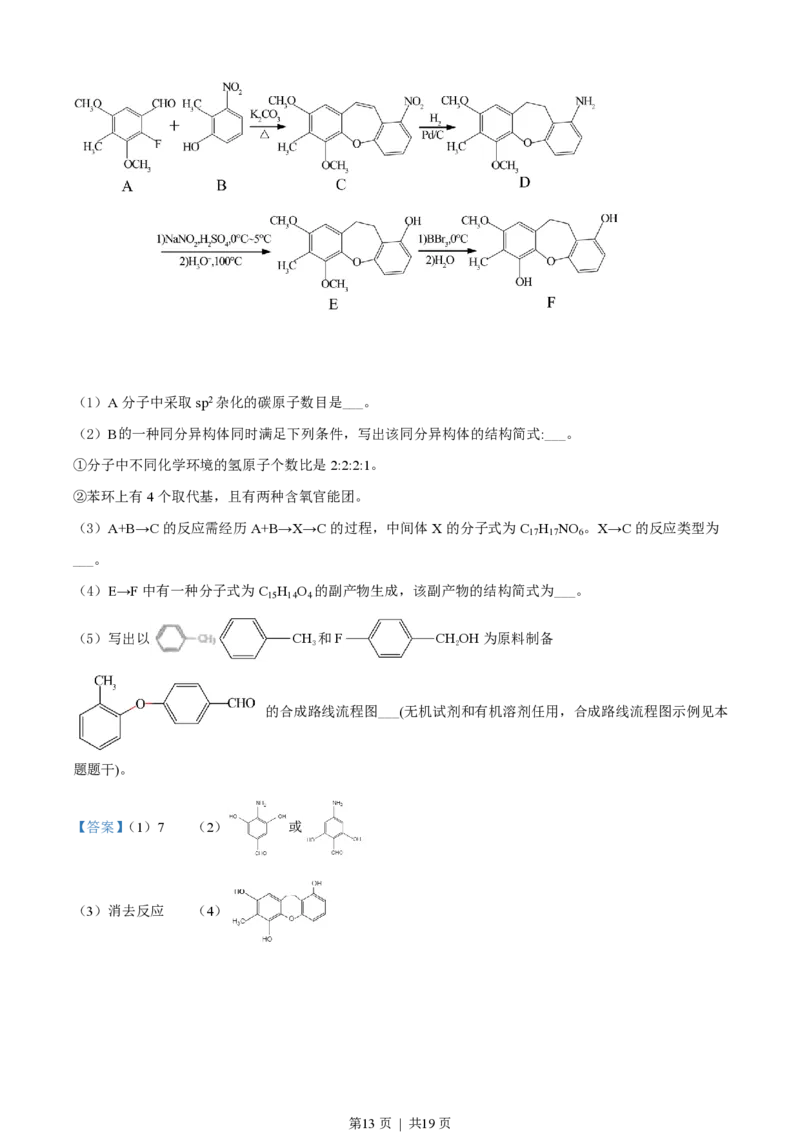
16. F是一种天然产物,具有抗肿瘤等活性,其人工合成路线如图:
第12页 | 共19页(1)A分子中采取sp2杂化的碳原子数目是___。
(2)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:___。
①分子中不同化学环境的氢原子个数比是2:2:2:1。
②苯环上有4个取代基,且有两种含氧官能团。
(3)A+B→C的反应需经历A+B→X→C的过程,中间体X的分子式为C H NO 。X→C的反应类型为
17 17 6
___。
(4)E→F中有一种分子式为C H O 的副产物生成,该副产物的结构简式为___。
15 14 4
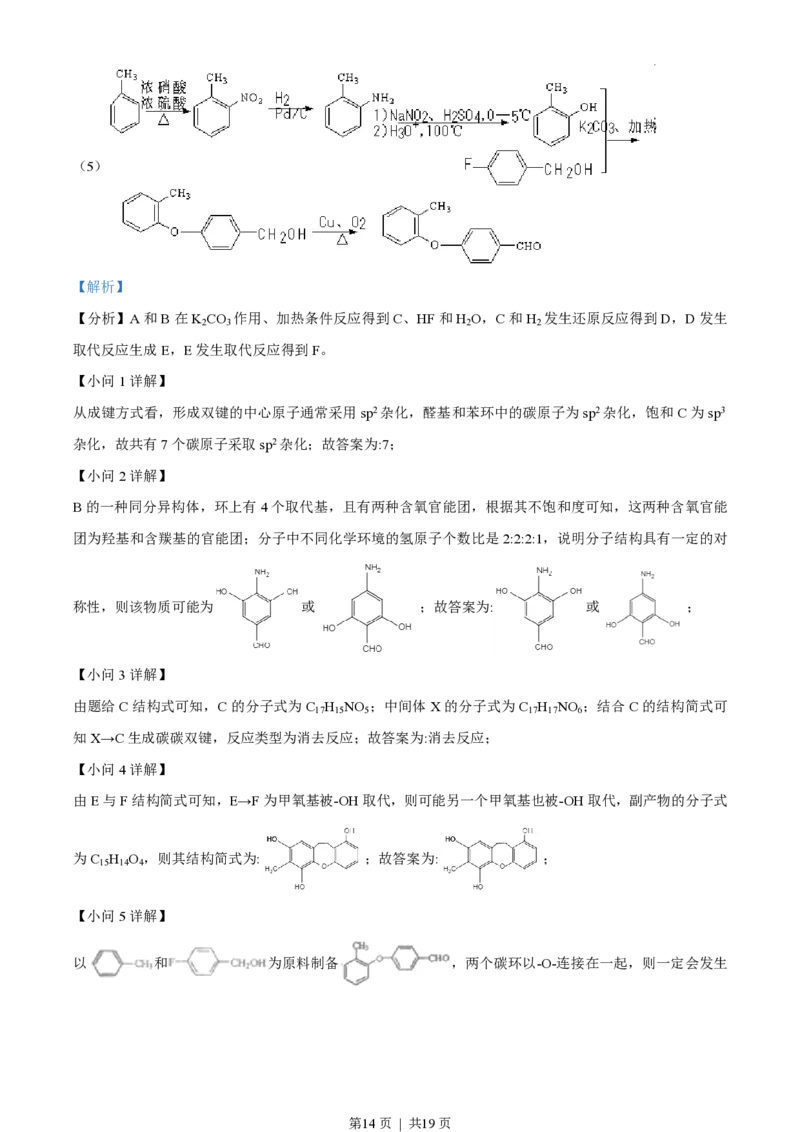
(5)写出以 CH 和F CHOH为原料制备
3 2
的合成路线流程图___(无机试剂和有机溶剂任用,合成路线流程图示例见本
题题干)。
【答案】(1)7 (2) 或
(3)消去反应 (4)
第13页 | 共19页(5)
【解析】
【分析】A和B在K CO 作用、加热条件反应得到C、HF和H O,C和H 发生还原反应得到D,D发生
2 3 2 2
取代反应生成E,E发生取代反应得到F。
【小问1详解】
从成键方式看,形成双键的中心原子通常采用sp2杂化,醛基和苯环中的碳原子为sp2杂化,饱和C为sp3
杂化,故共有7个碳原子采取sp2杂化;故答案为:7;
【小问2详解】
B的一种同分异构体,环上有4个取代基,且有两种含氧官能团,根据其不饱和度可知,这两种含氧官能
团为羟基和含羰基的官能团;分子中不同化学环境的氢原子个数比是2:2:2:1,说明分子结构具有一定的对
称性,则该物质可能为 或 ;故答案为: 或 ;
【小问3详解】
由题给C结构式可知,C的分子式为C H NO ;中间体X的分子式为C H NO ;结合C的结构简式可
17 15 5 17 17 6
知X→C生成碳碳双键,反应类型为消去反应;故答案为:消去反应;
【小问4详解】
由E与F结构简式可知,E→F为甲氧基被-OH取代,则可能另一个甲氧基也被-OH取代,副产物的分子式
为C H O ,则其结构简式为: ;故答案为: ;
15 14 4
【小问5详解】
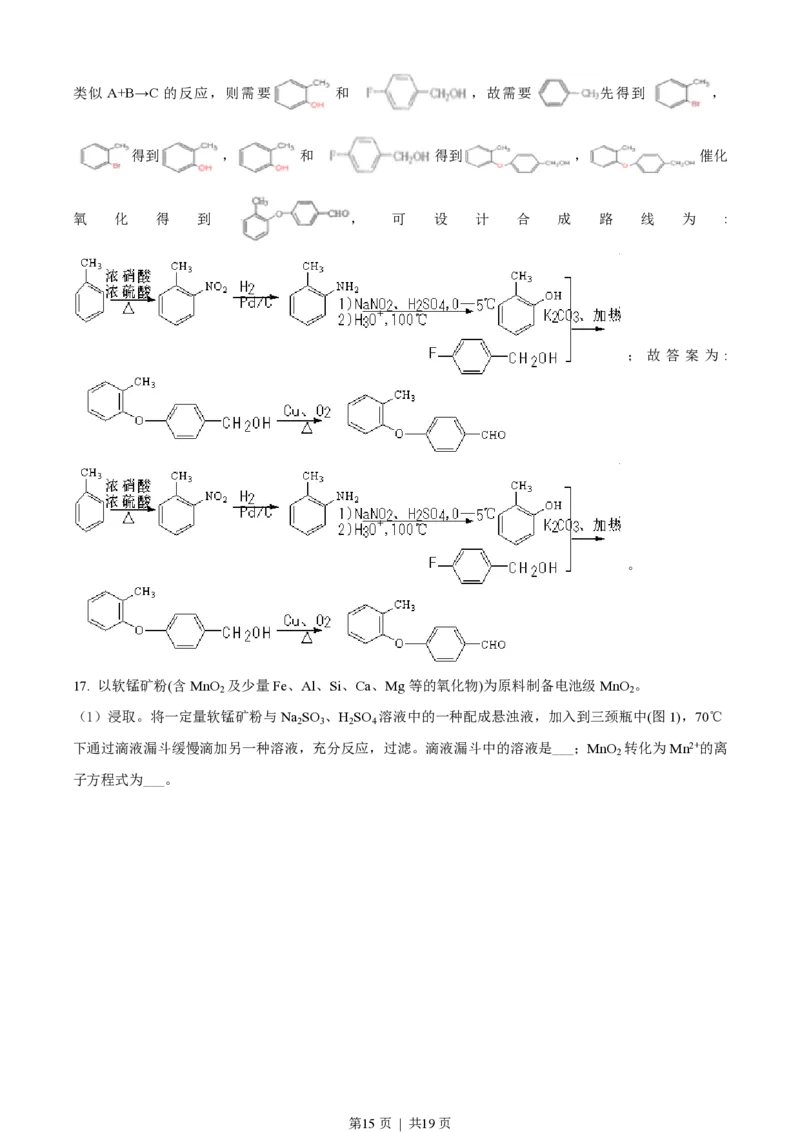
以 和 为原料制备 ,两个碳环以-O-连接在一起,则一定会发生
第14页 | 共19页类似 A+B→C 的反应,则需要 和 ,故需要 先得到 ,
得到 , 和 得到 , 催化
氧 化 得 到 , 可 设 计 合 成 路 线 为 :
; 故 答 案 为 :
。
17. 以软锰矿粉(含MnO 及少量Fe、Al、Si、Ca、Mg等的氧化物)为原料制备电池级MnO 。
2 2
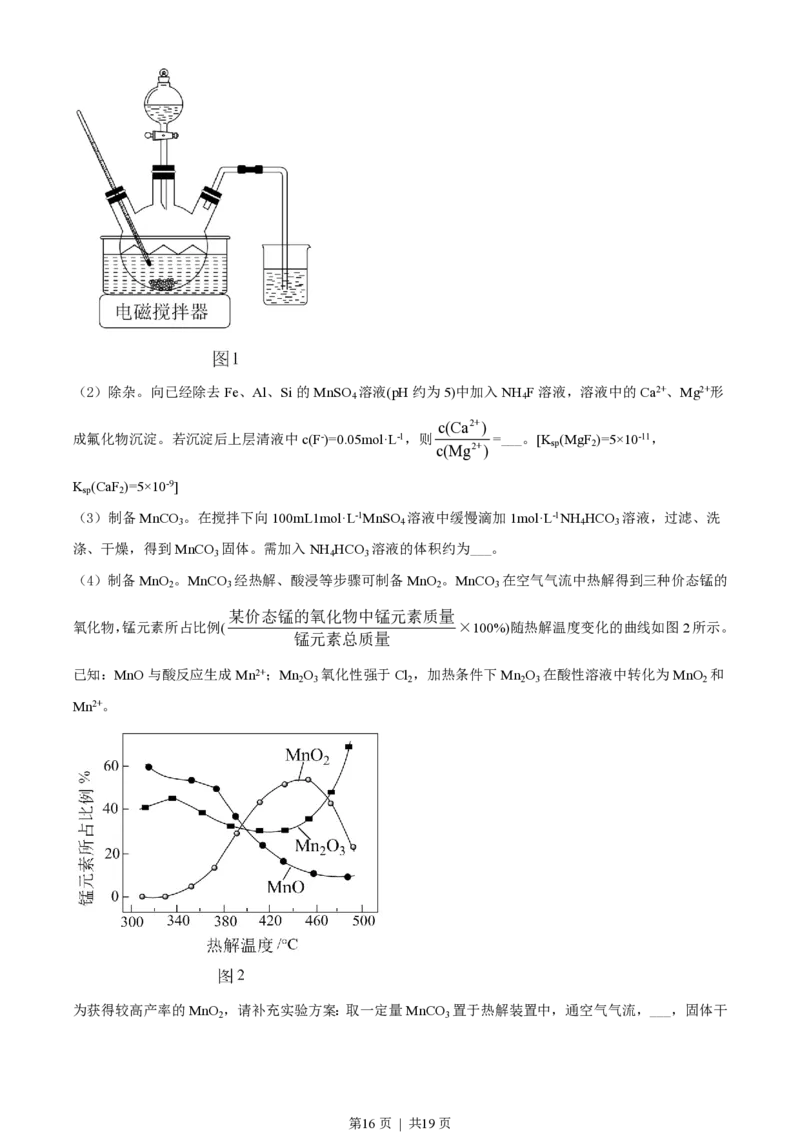
(1)浸取。将一定量软锰矿粉与Na SO 、H SO 溶液中的一种配成悬浊液,加入到三颈瓶中(图1),70℃
2 3 2 4
下通过滴液漏斗缓慢滴加另一种溶液,充分反应,过滤。滴液漏斗中的溶液是___;MnO 转化为Mn2+的离
2
子方程式为___。
第15页 | 共19页(2)除杂。向已经除去Fe、Al、Si的MnSO 溶液(pH约为5)中加入NH F溶液,溶液中的Ca2+、Mg2+形
4 4
c(Ca2+)
成氟化物沉淀。若沉淀后上层清液中c(F-)=0.05mol·L-1,则 =___。[K (MgF )=5×10-11,
c(Mg2+) sp 2
K (CaF )=5×10-9]
sp 2
(3)制备MnCO 。在搅拌下向100mL1mol·L-1MnSO 溶液中缓慢滴加1mol·L-1NH HCO 溶液,过滤、洗
3 4 4 3
涤、干燥,得到MnCO 固体。需加入NH HCO 溶液的体积约为___。
3 4 3
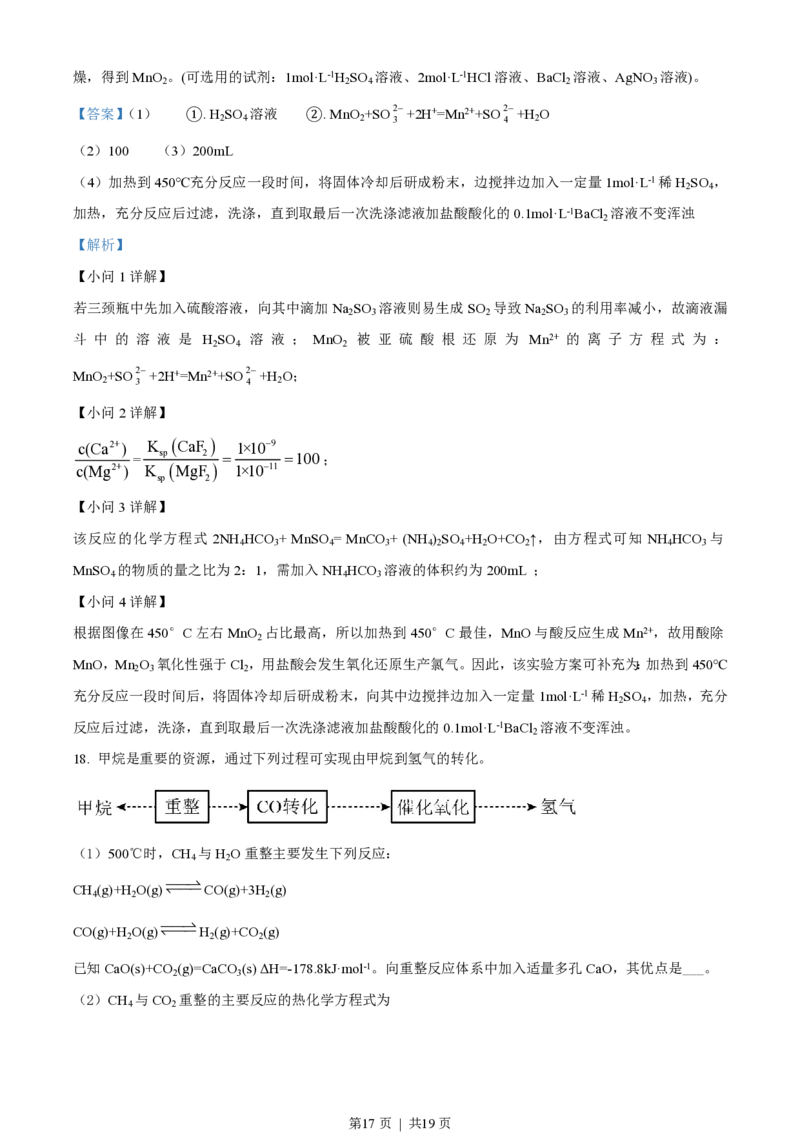
(4)制备MnO 。MnCO 经热解、酸浸等步骤可制备MnO 。MnCO 在空气气流中热解得到三种价态锰的
2 3 2 3
某价态锰的氧化物中锰元素质量
氧化物,锰元素所占比例( ×100%)随热解温度变化的曲线如图2所示。
锰元素总质量
已知:MnO与酸反应生成Mn2+;Mn O 氧化性强于Cl ,加热条件下Mn O 在酸性溶液中转化为MnO 和
2 3 2 2 3 2
Mn2+。
为获得较高产率的MnO ,请补充实验方案:取一定量MnCO 置于热解装置中,通空气气流,___,固体干
2 3
第16页 | 共19页燥,得到MnO 。(可选用的试剂:1mol·L-1H SO 溶液、2mol·L-1HCl溶液、BaCl 溶液、AgNO 溶液)。
2 2 4 2 3
【答案】(1) ①. H SO 溶液 ②. MnO +SO2-+2H+=Mn2++SO2-+H O
2 4 2 3 4 2
(2)100 (3)200mL
(4)加热到450℃充分反应一段时间,将固体冷却后研成粉末,边搅拌边加入一定量1mol·L-1稀H SO ,
2 4
加热,充分反应后过滤,洗涤,直到取最后一次洗涤滤液加盐酸酸化的0.1mol·L-1BaCl 溶液不变浑浊
2
【解析】
【小问1详解】
若三颈瓶中先加入硫酸溶液,向其中滴加Na SO 溶液则易生成SO 导致Na SO 的利用率减小,故滴液漏
2 3 2 2 3
斗 中 的 溶 液 是 H SO 溶 液 ; MnO 被 亚 硫 酸 根 还 原 为 Mn2+ 的 离 子 方 程 式 为 :
2 4 2
MnO +SO2-+2H+=Mn2++SO2-+H O;
2 3 4 2
【小问2详解】
c(Ca2+) K CaF 1×10-9
= sp 2 = =100;
c(Mg2+) K MgF 1×10-11
sp 2
【小问3详解】
该反应的化学方程式 2NH HCO + MnSO = MnCO + (NH ) SO +H O+CO ↑,由方程式可知 NH HCO 与
4 3 4 3 4 2 4 2 2 4 3
MnSO 的物质的量之比为2:1,需加入NH HCO 溶液的体积约为200mL ;
4 4 3
【小问4详解】
根据图像在450°C左右MnO 占比最高,所以加热到450°C最佳,MnO与酸反应生成Mn2+,故用酸除
2
MnO,Mn O 氧化性强于Cl ,用盐酸会发生氧化还原生产氯气。因此,该实验方案可补充为:加热到450℃
2 3 2
充分反应一段时间后,将固体冷却后研成粉末,向其中边搅拌边加入一定量1mol·L-1稀H SO ,加热,充分
2 4
反应后过滤,洗涤,直到取最后一次洗涤滤液加盐酸酸化的0.1mol·L-1BaCl 溶液不变浑浊。
2
18. 甲烷是重要的资源,通过下列过程可实现由甲烷到氢气的转化。
(1)500℃时,CH 与H O重整主要发生下列反应:
4 2
CH 4 (g)+H 2 O(g)‡ ˆˆ ˆ † ˆCO(g)+3H 2 (g)
CO(g)+H 2 O(g)‡ ˆˆ ˆ † ˆH 2 (g)+CO 2 (g)
已知CaO(s)+CO (g)=CaCO (s) ΔH=-178.8kJ·mol-1。向重整反应体系中加入适量多孔CaO,其优点是___。
2 3
(2)CH 与CO 重整的主要反应的热化学方程式为
4 2
第17页 | 共19页反应I:CH (g)+CO (g)=2CO(g)+2H (g) ΔH=246.5kJ·mol-1
4 2 2
反应II:H (g)+CO (g)=CO(g)+H O(g) ΔH=41.2kJ·mol-1
2 2 2
反应III:2CO(g)=CO (g)+C(s) ΔH=-172.5kJ·mol-1
2
①在CH 与CO 重整体系中通入适量H O(g),可减少C(s)的生成,反应
4 2 2
3CH (g)+CO (g)+2H O(g)=4CO(g)+8H (g)的ΔH=___。
4 2 2 2
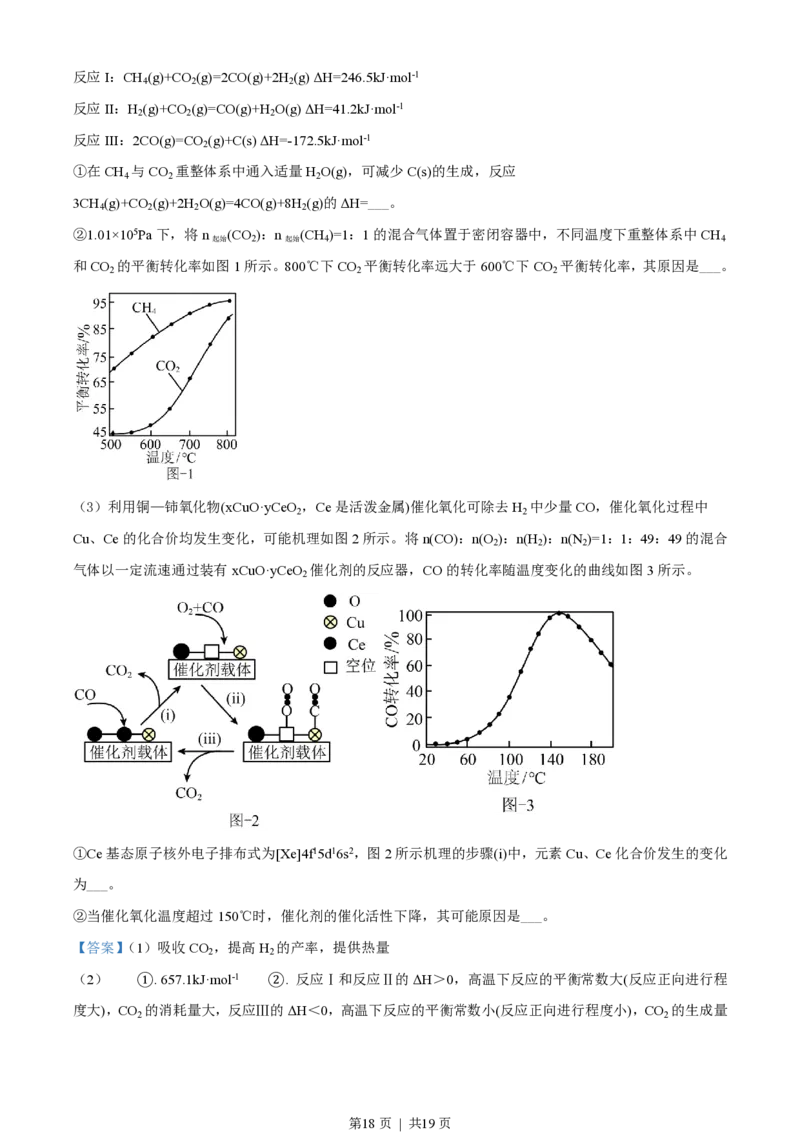
②1.01×105Pa下,将n (CO ):n (CH )=1:1的混合气体置于密闭容器中,不同温度下重整体系中CH
起始 2 起始 4 4
和CO 的平衡转化率如图1所示。800℃下CO 平衡转化率远大于600℃下CO 平衡转化率,其原因是___。
2 2 2
(3)利用铜—铈氧化物(xCuO·yCeO ,Ce是活泼金属)催化氧化可除去H 中少量CO,催化氧化过程中
2 2
Cu、Ce的化合价均发生变化,可能机理如图2所示。将n(CO):n(O ):n(H ):n(N )=1:1:49:49的混合
2 2 2
气体以一定流速通过装有xCuO·yCeO 催化剂的反应器,CO的转化率随温度变化的曲线如图3所示。
2
①Ce基态原子核外电子排布式为[Xe]4f15d16s2,图2所示机理的步骤(i)中,元素Cu、Ce化合价发生的变化
为___。
②当催化氧化温度超过150℃时,催化剂的催化活性下降,其可能原因是___。
【答案】(1)吸收CO ,提高H 的产率,提供热量
2 2
(2) ①. 657.1kJ·mol-1 ②. 反应Ⅰ和反应Ⅱ的ΔH>0,高温下反应的平衡常数大(反应正向进行程
度大),CO 的消耗量大,反应Ⅲ的ΔH<0,高温下反应的平衡常数小(反应正向进行程度小),CO 的生成量
2 2
第18页 | 共19页小
(3) ①. 铜的化合价由+2变为+1价,铈的化合价由+4价变为+3价 ②. 高温下,Cu(+2价)或Cu(+1
价)被H 还原为金属Cu
2
【解析】
【小问1详解】
已知CaO(s)+CO (g)=CaCO (s) ΔH=-178.8kJ·mol-1,因此向重整反应体系中加入适量多孔CaO的优点是
2 3
吸收CO ,使平衡正向移动,提高H 的产率,同时提供热量。
2 2
【小问2详解】
①反应I:CH (g)+CO (g)=2CO(g)+2H (g) ΔH=246.5kJ·mol-1
4 2 2
反应II:H (g)+CO (g)=CO(g)+H O(g) ΔH=41.2kJ·mol-1
2 2 2
依据盖斯定律可知I×3-II×2即得到反应3CH (g)+CO (g)+2H O(g)=4CO(g)+8H (g)的ΔH=657.1kJ·mol-1。
4 2 2 2
②由于反应Ⅰ和反应Ⅱ的ΔH>0,高温下反应的平衡常数大(反应正向进行程度大),CO 的消耗量大,反应
2
Ⅲ的ΔH<0,高温下反应的平衡常数小(反应正向进行程度小),CO 的生成量小,所以800℃下CO 平衡转
2 2
化率远大于600℃下CO 平衡转化率。
2
【小问3详解】
①图2所示机理的步骤(i)中CO结合氧元素转化为二氧化碳,根据Cu、Ce两种元素的核外电子排布式可判
断元素Cu、Ce化合价发生的变化为铜的化合价由+2变为+1价,铈的化合价由+4价变为+3价。
②由于高温下,Cu(+2价)或Cu(+1价)被H 还原为金属Cu,所以当催化氧化温度超过150℃时,催化剂的
2
催化活性下降。
第19页 | 共19页