文档内容
湖南省 2022 年普通高中学业水平选择性考试
化学
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在本试卷和答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在
本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 K 39 Fe 56 Se 79 Ba
137
一、选择题:本题共 10小题,每小题 3分,共 30 分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 化学促进了科技进步和社会发展,下列叙述中没有涉及化学变化的是
A. 《神农本草经》中记载的“石胆能化铁为铜”
B. 利用“侯氏联合制碱法”制备纯碱
C. 科学家成功将CO 转化为淀粉或葡萄糖
2
D. 北京冬奥会场馆使用CO 跨临界直冷制冰
2
2. 下列说法错误的是
A. 氢键,离子键和共价键都属于化学键
B. 化学家门捷列夫编制了第一张元素周期表
C. 药剂师和营养师必须具备化学相关专业知识
D. 石灰石是制造玻璃和水泥的主要原料之一
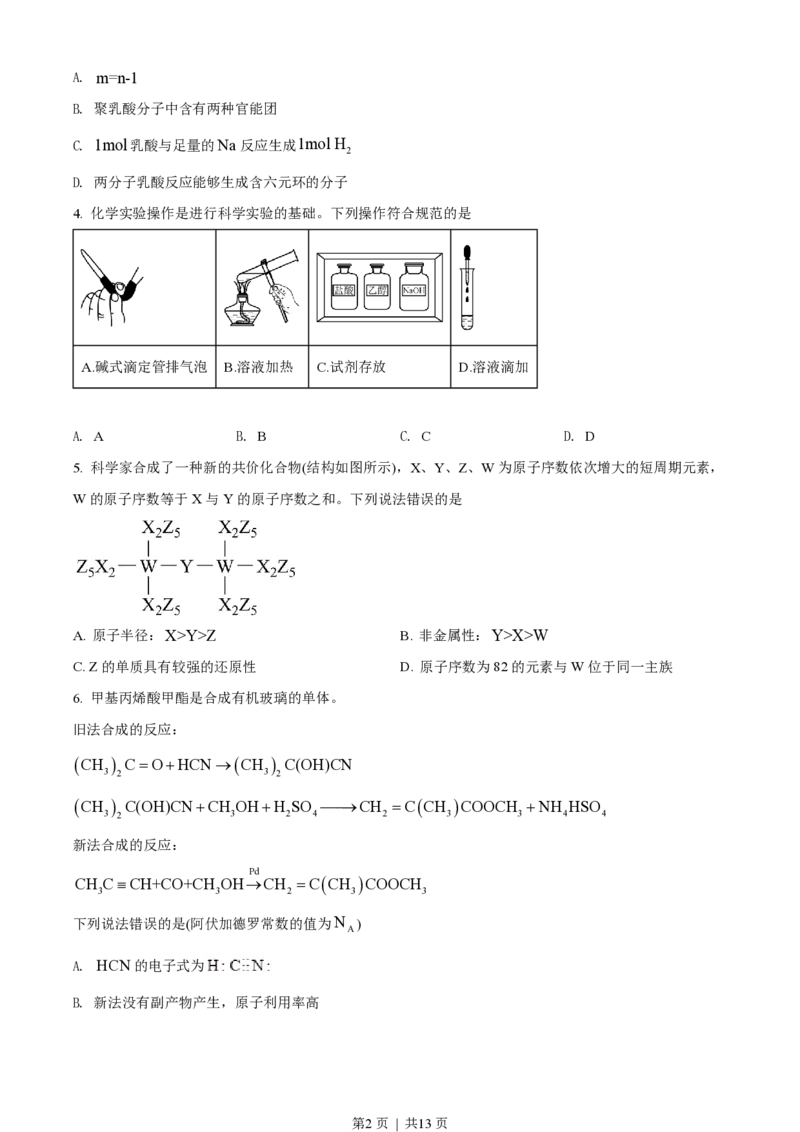
3. 聚乳酸是一种新型的生物可降解高分子材料,其合成路线如下:
下列说法错误的是
第1页 | 共13页A. m=n-1
B. 聚乳酸分子中含有两种官能团
C. 1mol乳酸与足量的Na 反应生成1mol H
2
D. 两分子乳酸反应能够生成含六元环的分子
4. 化学实验操作是进行科学实验的基础。下列操作符合规范的是
A.碱式滴定管排气泡 B.溶液加热 C.试剂存放 D.溶液滴加
A. A B. B C. C D. D
5. 科学家合成了一种新的共价化合物(结构如图所示),X、Y、Z、W为原子序数依次增大的短周期元素,
W的原子序数等于X与Y的原子序数之和。下列说法错误的是
A. 原子半径:X>Y>Z B. 非金属性:Y>X>W
C. Z的单质具有较强的还原性 D. 原子序数为82的元素与W位于同一主族
6. 甲基丙烯酸甲酯是合成有机玻璃的单体。
旧法合成的反应:
CH C=O+HCN®CH C(OH)CN
3 2 3 2
CH C(OH)CN+CH OH+H SO ¾¾®CH =CCH COOCH +NH HSO
3 2 3 2 4 2 3 3 4 4
新法合成的反应:
Pd
CH CºCH+CO+CH OH®CH =CCH COOCH
3 3 2 3 3
下列说法错误的是(阿伏加德罗常数的值为N )
A
A. HCN的电子式为
B. 新法没有副产物产生,原子利用率高
第2页 | 共13页C. 1L0.05mol×L-1的NH HSO 溶液中NH+的微粒数小于0.05N
4 4 4 A
D. Pd的作用是降低反应的活化能,使活化分子数目增多,百分数不变
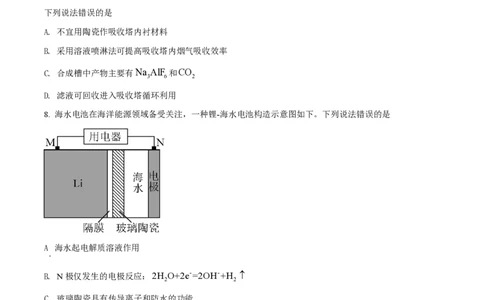
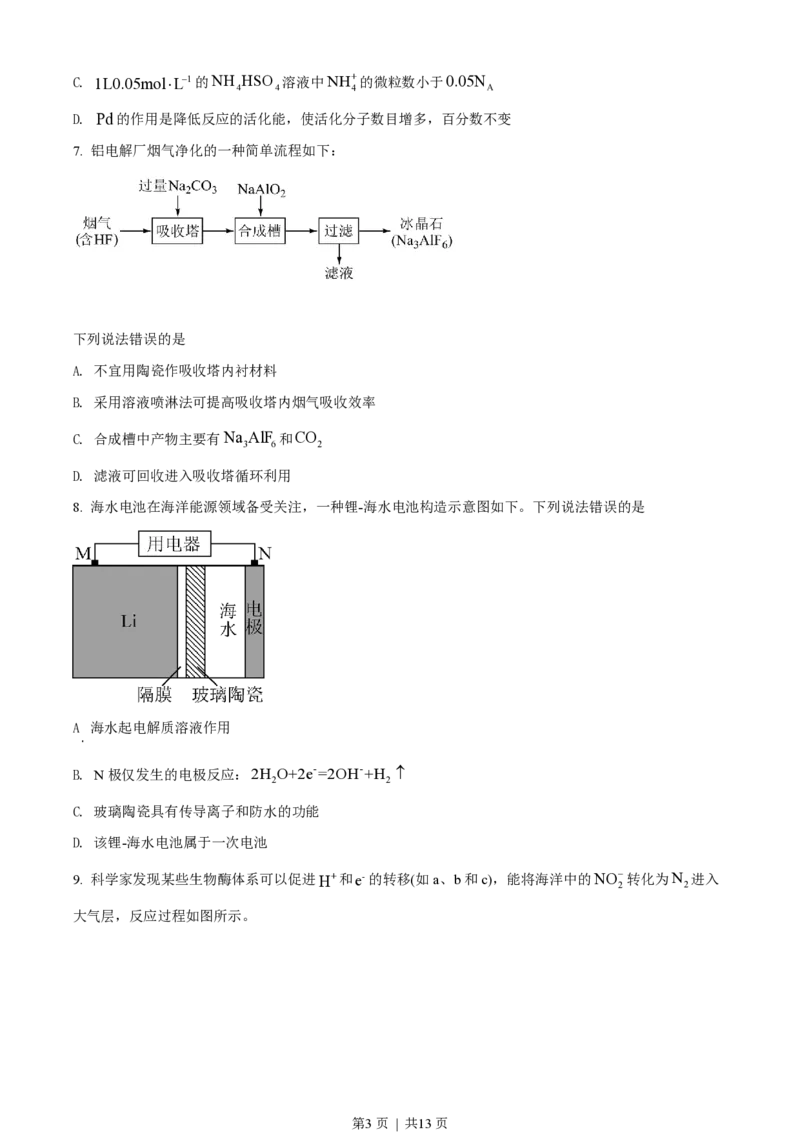
7. 铝电解厂烟气净化的一种简单流程如下:
下列说法错误的是
A. 不宜用陶瓷作吸收塔内衬材料
B. 采用溶液喷淋法可提高吸收塔内烟气吸收效率
C. 合成槽中产物主要有Na AlF 和CO
3 6 2
D. 滤液可回收进入吸收塔循环利用
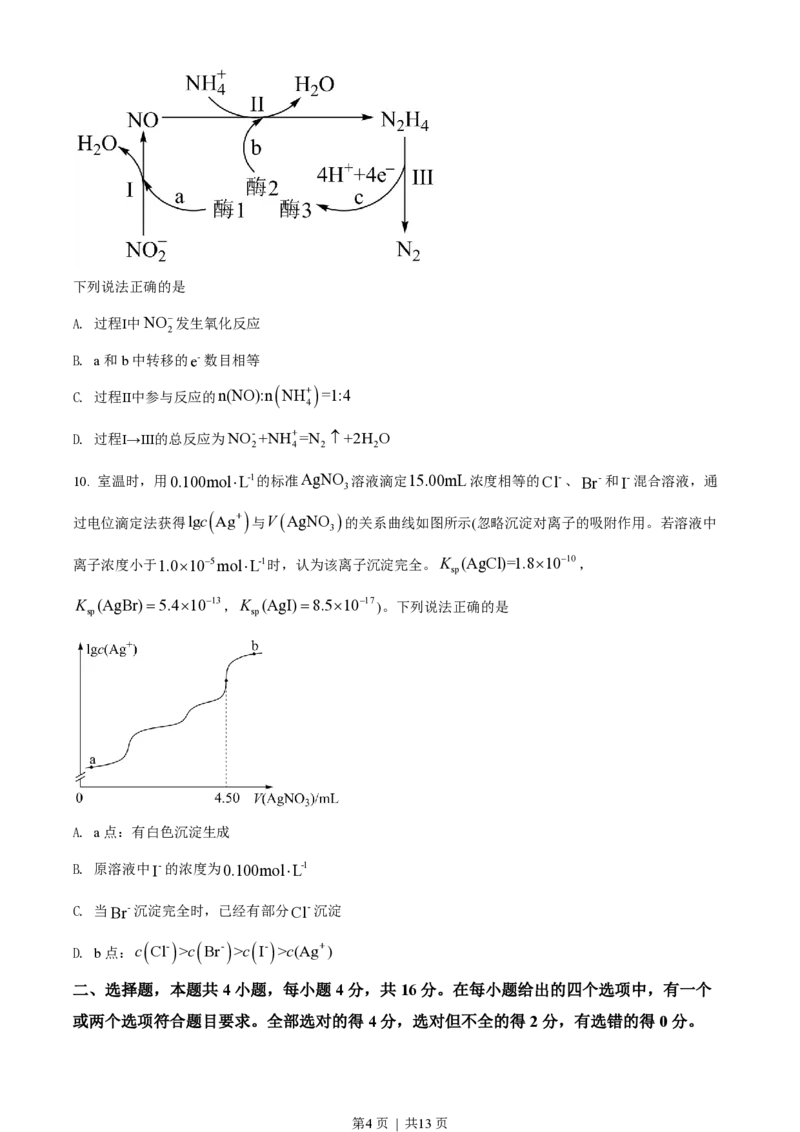
8. 海水电池在海洋能源领域备受关注,一种锂-海水电池构造示意图如下。下列说法错误的是
A 海水起电解质溶液作用
.
B. N极仅发生的电极反应:2H O+2e-=2OH-+H
2 2
C. 玻璃陶瓷具有传导离子和防水的功能
D. 该锂-海水电池属于一次电池
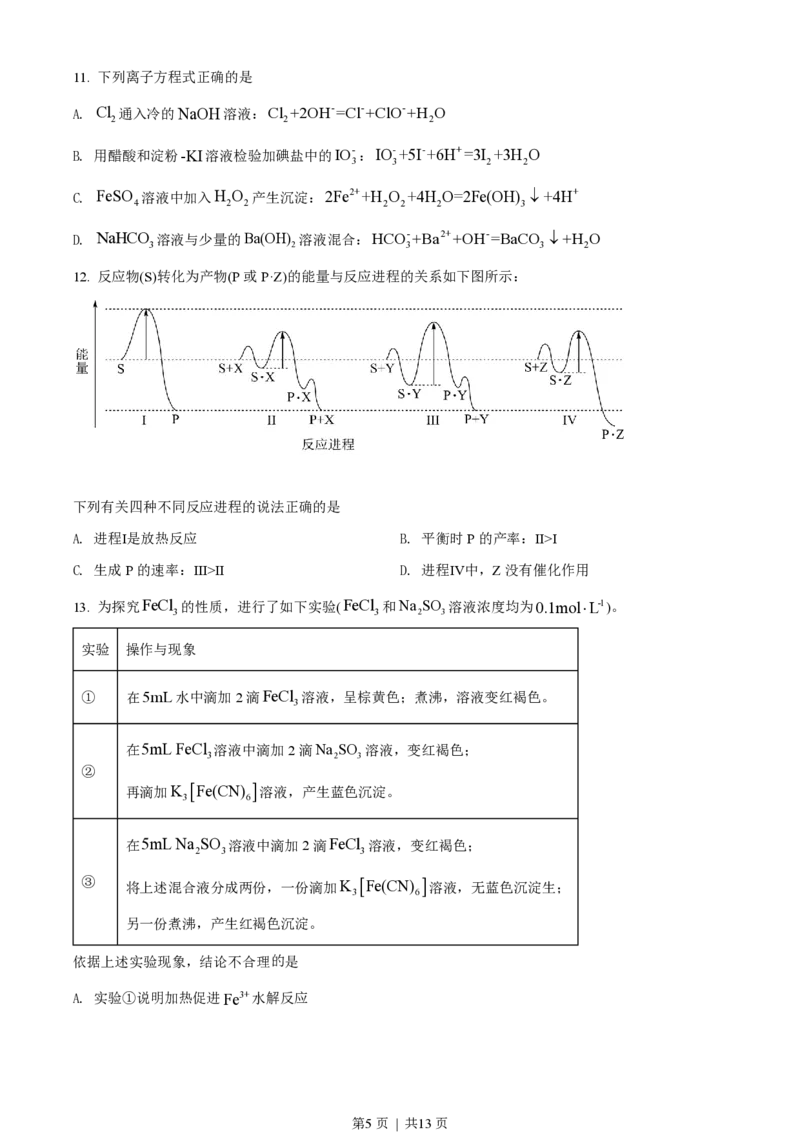
9. 科学家发现某些生物酶体系可以促进H+和e-的转移(如a、b和c),能将海洋中的NO-转化为N 进入
2 2
大气层,反应过程如图所示。
第3页 | 共13页下列说法正确的是
A. 过程Ⅰ中NO-发生氧化反应
2
B. a和b中转移的e-数目相等
C. 过程Ⅱ中参与反应的n(NO):n
NH+
=1:4
4
D. 过程Ⅰ→Ⅲ的总反应为NO-+NH+=N +2H O
2 4 2 2
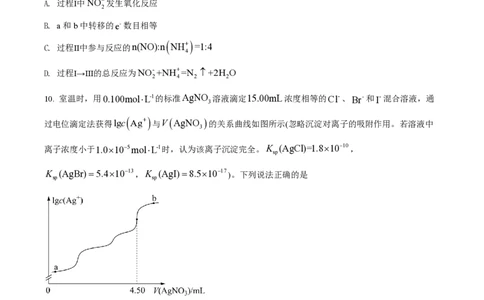
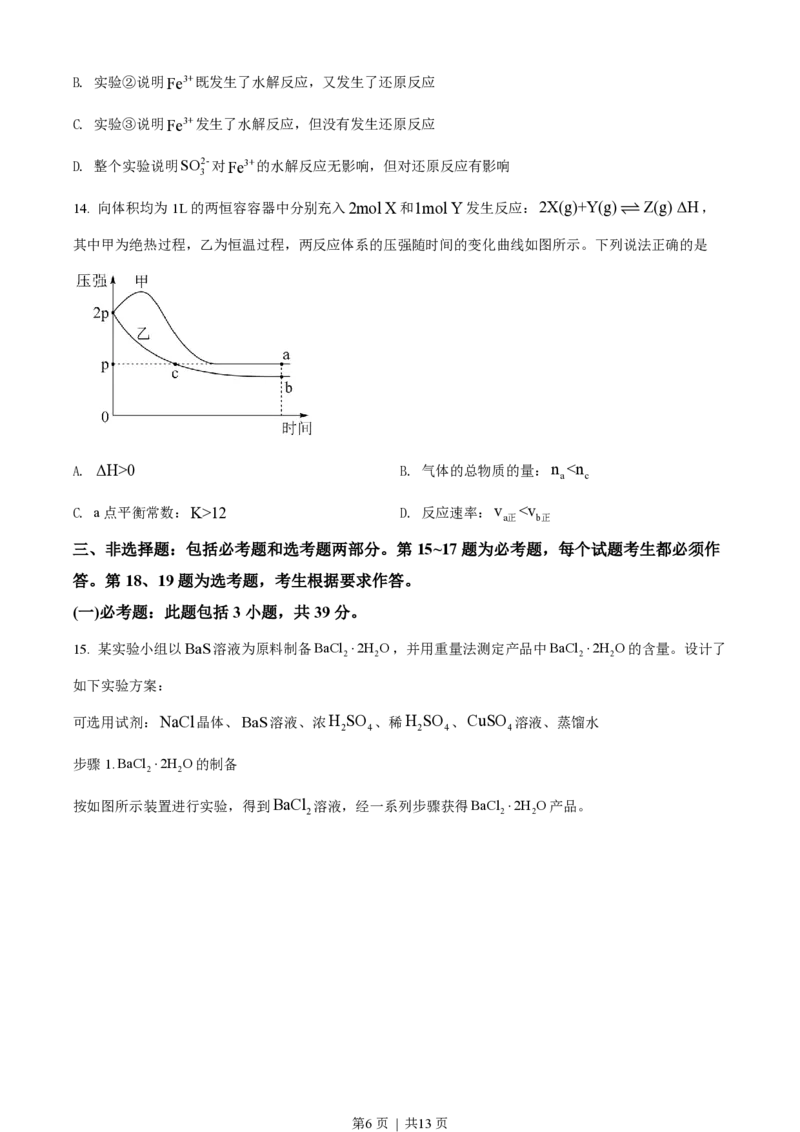
10. 室温时,用0.100mol×L-1的标准AgNO 溶液滴定15.00mL浓度相等的Cl-、Br-和I-混合溶液,通
3
过电位滴定法获得lgc Ag+ 与VAgNO 的关系曲线如图所示(忽略沉淀对离子的吸附作用。若溶液中
3
离子浓度小于1.0´10-5mol×L-1时,认为该离子沉淀完全。K (AgCl)=1.8´10-10,
sp
K (AgBr)=5.4´10-13,K (AgI)=8.5´10-17 )。下列说法正确的是
sp sp
A. a点:有白色沉淀生成
B. 原溶液中I-的浓度为0.100mol×L-1
C. 当Br-沉淀完全时,已经有部分Cl-沉淀
D. b点:c Cl- >c Br- >c I- >c(Ag+)
二、选择题,本题共 4小题,每小题 4分,共 16 分。在每小题给出的四个选项中,有一个
或两个选项符合题目要求。全部选对的得 4分,选对但不全的得 2分,有选错的得 0分。
第4页 | 共13页11. 下列离子方程式正确的是
A. Cl 通入冷的NaOH溶液:Cl +2OH-=Cl-+ClO-+H O
2 2 2
B. 用醋酸和淀粉-KI溶液检验加碘盐中的IO- :IO-+5I-+6H+=3I +3H O
3 3 2 2
C. FeSO 溶液中加入H O 产生沉淀:2Fe2++H O +4H O=2Fe(OH) ¯+4H+
4 2 2 2 2 2 3
D. NaHCO 溶液与少量的Ba(OH) 溶液混合:HCO-+Ba2++OH-=BaCO ¯+H O
3 2 3 3 2
12. 反应物(S)转化为产物(P或P·Z)的能量与反应进程的关系如下图所示:
下列有关四种不同反应进程的说法正确的是
A. 进程Ⅰ是放热反应 B. 平衡时P的产率:Ⅱ>Ⅰ
C. 生成P的速率:Ⅲ>Ⅱ D. 进程Ⅳ中,Z没有催化作用
13. 为探究FeCl 的性质,进行了如下实验(FeCl 和Na SO 溶液浓度均为0.1mol×L-1)。
3 3 2 3
实验 操作与现象
① 在5mL水中滴加2滴FeCl 溶液,呈棕黄色;煮沸,溶液变红褐色。
3
在5mL FeCl 溶液中滴加2滴Na SO 溶液,变红褐色;
3 2 3
②
再滴加K Fe(CN) 溶液,产生蓝色沉淀。
3 6
在5mL Na SO 溶液中滴加2滴FeCl 溶液,变红褐色;
2 3 3
③ 将上述混合液分成两份,一份滴加K Fe(CN) 溶液,无蓝色沉淀生;
3 6
另一份煮沸,产生红褐色沉淀。
依据上述实验现象,结论不合理的是
A. 实验①说明加热促进Fe3+水解反应
第5页 | 共13页B. 实验②说明Fe3+既发生了水解反应,又发生了还原反应
C. 实验③说明Fe3+发生了水解反应,但没有发生还原反应
D. 整个实验说明SO2-对Fe3+的水解反应无影响,但对还原反应有影响
3
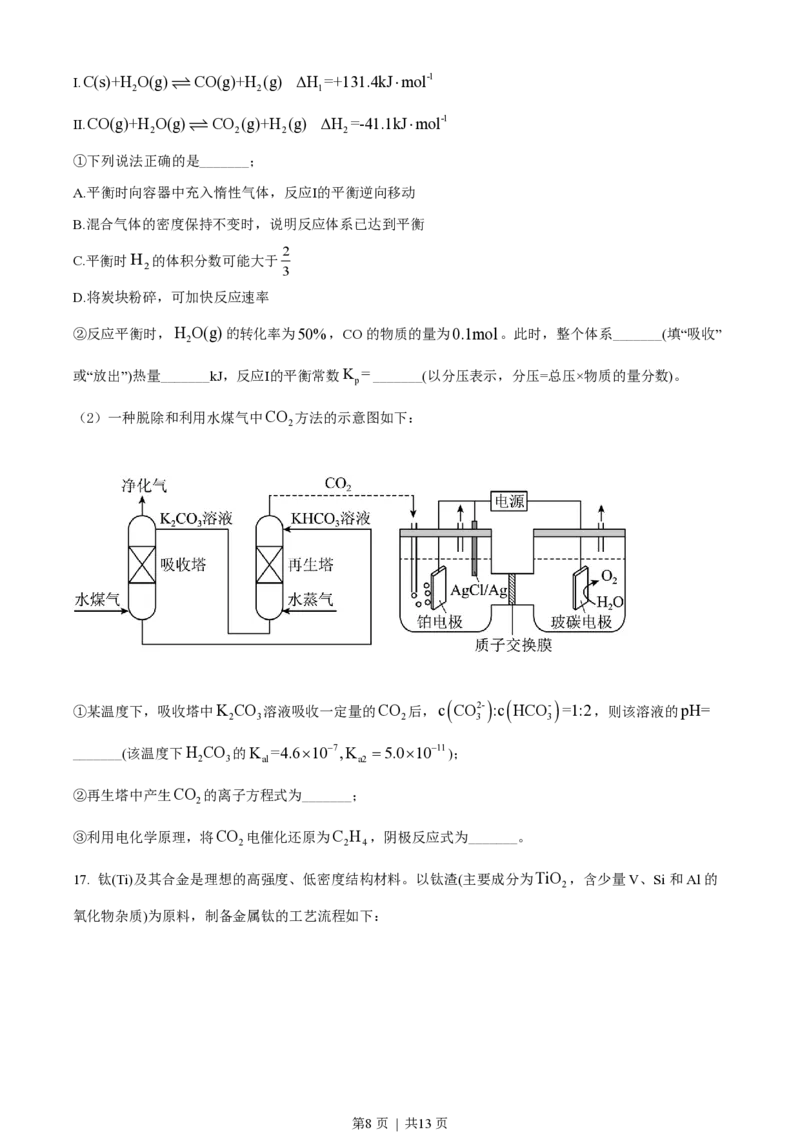
14. 向体积均为1L的两恒容容器中分别充入2mol X和1mol Y发生反应:2X(g)+Y(g) ƒ Z(g) ΔH,
其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
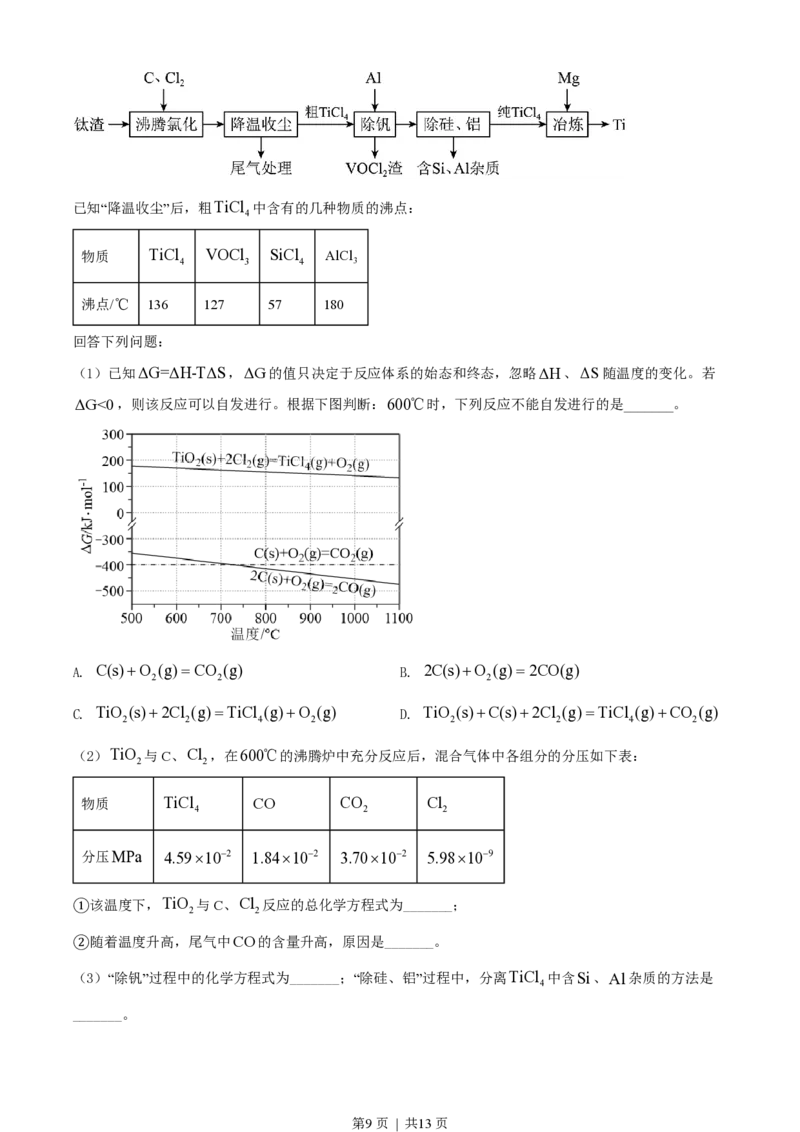
A. ΔH>0 B. 气体的总物质的量:n 12 D. 反应速率:v ”“<”或“=”),原因是_______。
3 3
(2)富马酸亚铁FeC H O 是一种补铁剂。富马酸分子的结构模型如图所示:
4 2 4
①富马酸分子中s键与π键的数目比为_______;
②富马酸亚铁中各元素的电负性由大到小的顺序为_______。
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H ,将N3-转化为
2
NH-,反应过程如图所示:
2
第10页 | 共13页①产物中N原子的杂化轨道类型为_______;
②与NH-互为等电子体的一种分子为_______(填化学式)。
2
(4)钾、铁、硒可以形成一种超导材料,其晶胞在xz、yz和xy平面投影分别如图所示:
①该超导材料的最简化学式为_______;
②Fe原子的配位数为_______;
③该晶胞参数a=b=0.4nm、c=1.4nm。阿伏加德罗常数的值为N ,则该晶体的密度为_______g×cm-1
A
(列出计算式)。
[选修 5:有机化学基础]
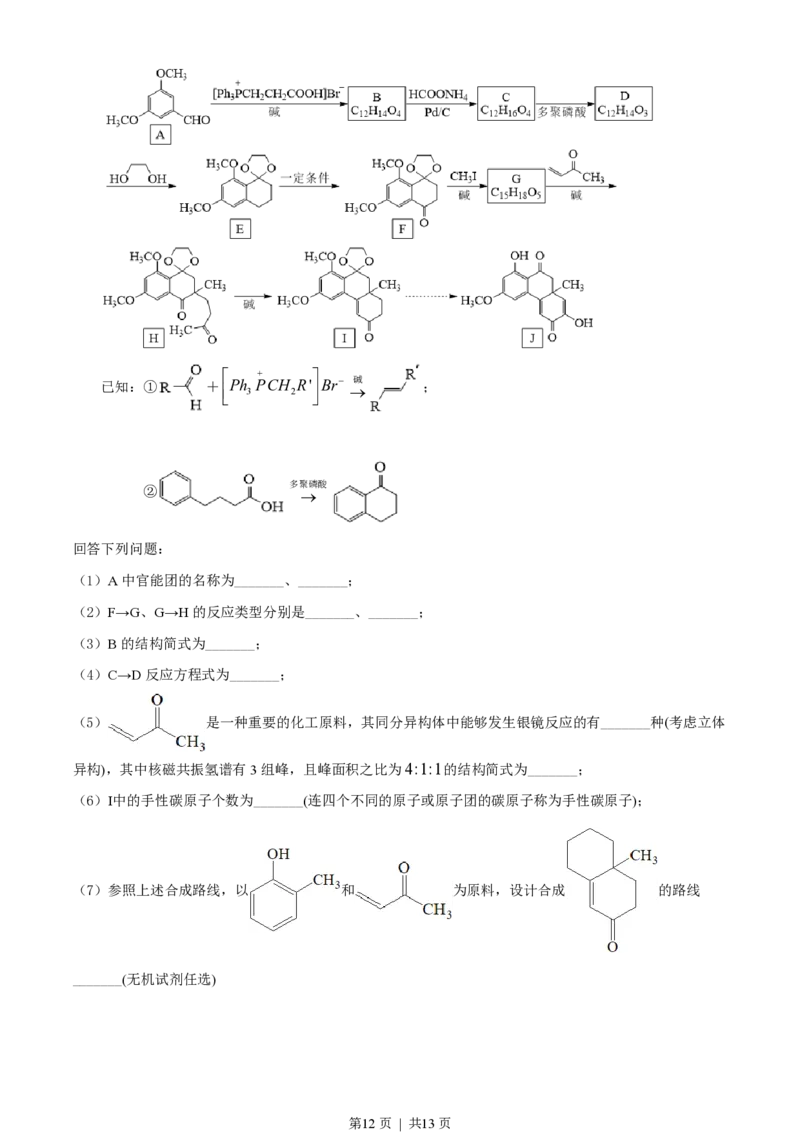
19. 物质J是一种具有生物活性的化合物。该化合物的合成路线如下:
第11页 | 共13页é + ù
已知:① + Ph PCH R' Br- 碱 ;
ê 3 2 ú ®
ë û
多聚磷酸
②
®
回答下列问题:
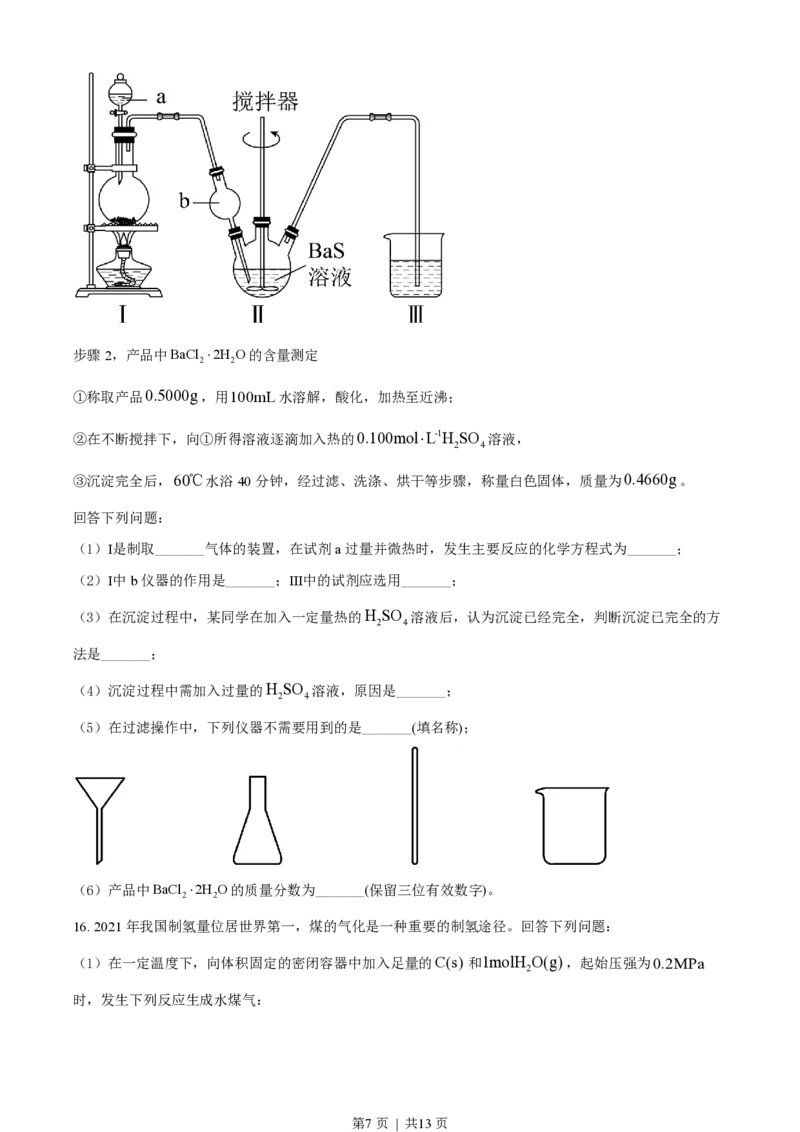
(1)A中官能团的名称为_______、_______;
(2)F→G、G→H的反应类型分别是_______、_______;
(3)B的结构简式为_______;
(4)C→D反应方程式为_______;
(5) 是一种重要的化工原料,其同分异构体中能够发生银镜反应的有_______种(考虑立体
异构),其中核磁共振氢谱有3组峰,且峰面积之比为4:1:1的结构简式为_______;
(6)Ⅰ中的手性碳原子个数为_______(连四个不同的原子或原子团的碳原子称为手性碳原子);
(7)参照上述合成路线,以 和 为原料,设计合成 的路线
_______(无机试剂任选)
第12页 | 共13页第13页 | 共13页