文档内容
2025 年上海市等级考化学试卷(回忆版)
PC
一、碳酸丙烯酯 的合成
DH =215kJ/mol
1. 已知反应1 的 1
DH =xxkJ/mol
反应2的 2
DH =xxkJ/mol
反应3的 3
DH =?kJ/mol
的
反应4 4
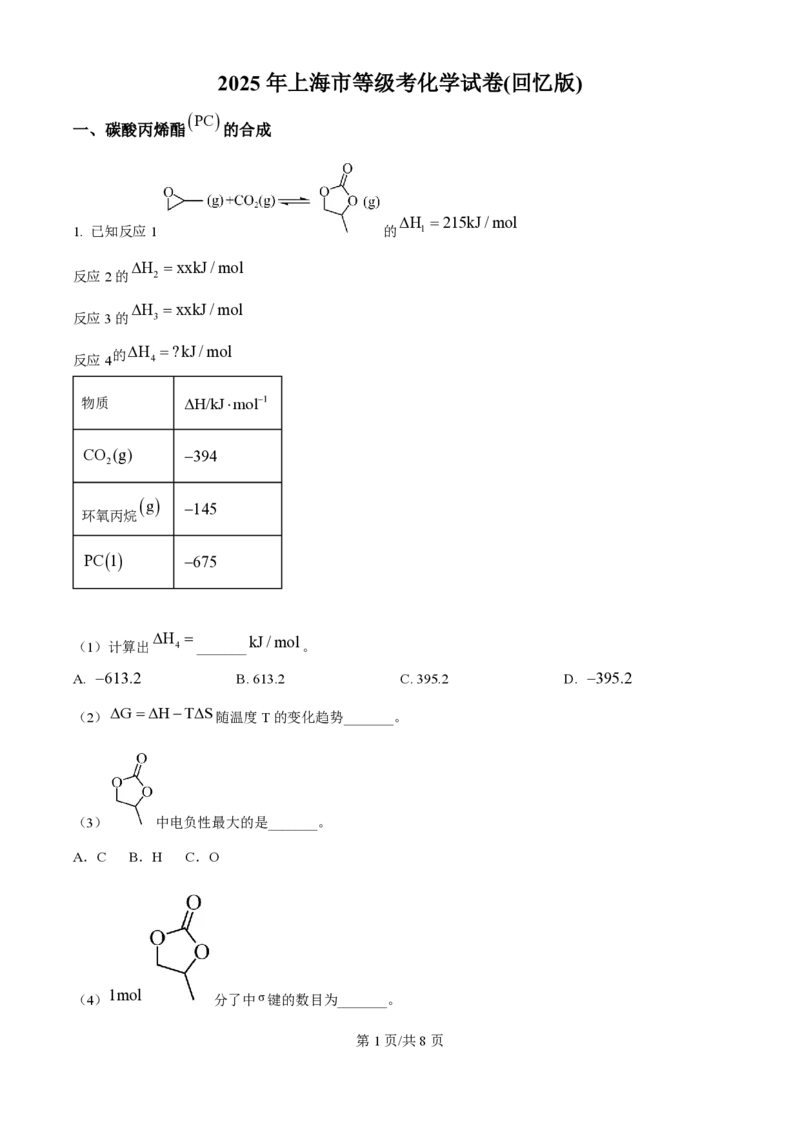
物质 DH/kJ×mol-1
CO (g) -394
2
g
-145
环氧丙烷
PC1
-675
DH = kJ/mol
(1)计算出 4 _______ 。
A. -613.2 B. 613.2 C. 395.2 D. -395.2
DG =DH-TDS
(2) 随温度T的变化趋势_______。
(3) 中电负性最大的是_______。
A.C B.H C.O
1mol
(4) 分了中σ键的数目为_______。
第1页/共8页
学科网(北京)股份有限公司A. 7 B. 12 C. 13 D. 14
已知:环氧丙烷生成 会发生副反应
´100%
选择性=转化生成A的环氧丙烷/消耗环氧丙烷
=58g/mol =1.2g/mL
M(环氧丙烷) ρ(环氧丙烷)
容器容积 25mL 的高压反应釜反应后体积缩小为 10mL ,选择性为95%,反应4h。
mol/(L×h)
(5)求环氧丙烷的化学反应速率_______(精确到小数点后2位)
(6)下列哪种操作可以使得活化分子的百分数变大_______。
A. 升高温度 B. 增大CO 浓度 C. 压缩容器 D. 充入惰性气体
2
(7)碳酸丙烯酯相同时间内随温度变化如图所示,请解释产率随温度先升后下降的原因_______。
(8)达到平衡的判据_______。
A. v正
CO
=v逆
PC
B. 体系总质量不变
2
C. 气体体积不再变化 D. 混合气体密度(可能是摩尔质量)不变
(9)制备 还有一种光气法,用 。请从绿色化学的
CO PC
角度解释,写出3点与光气-二醇法相比, 2法合成 的优势_______。
二、“重石头”元素——钨
2. (以下题目中的图片根据回忆所得信息结合文献资料重新整合所得,仅供参考)
第2页/共8页
学科网(北京)股份有限公司(1)钨作灯丝与_______性质有关(不定项)。
A. 延展性 B. 导电性 C. 高熔点 D.
(2)钨有金属光泽的原因_______ (从微观角度解释)。
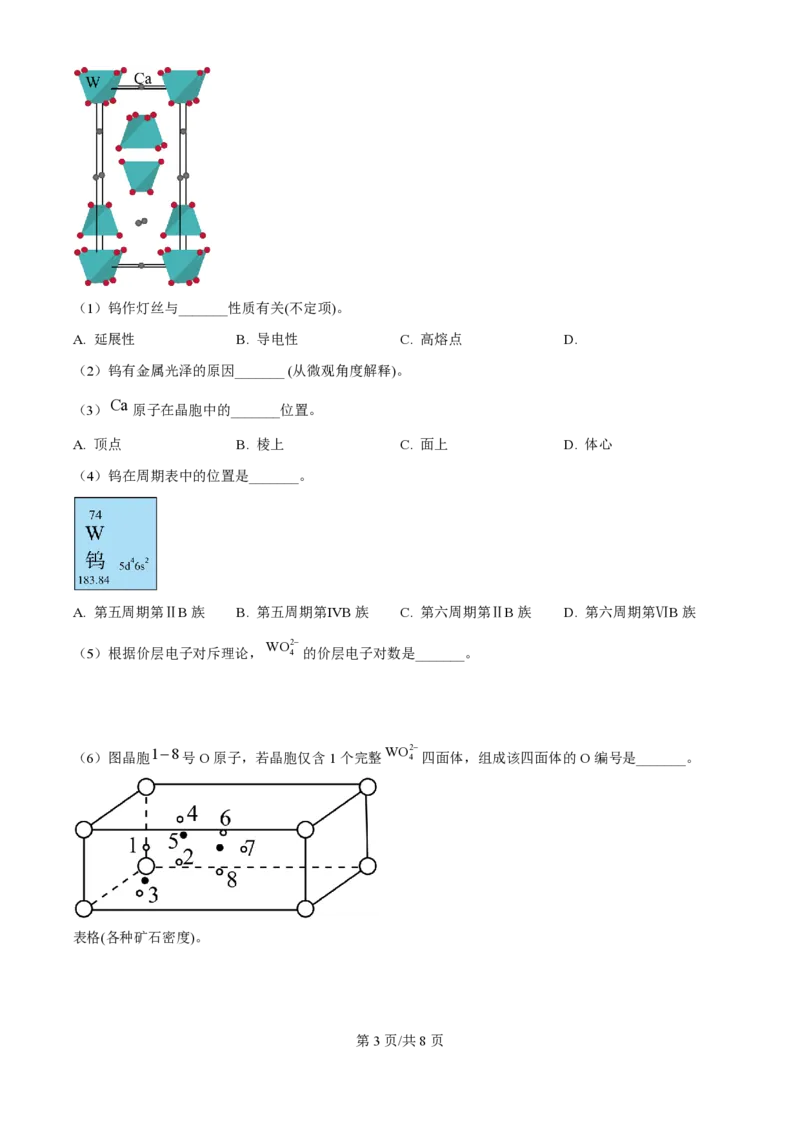
Ca
(3) 原子在晶胞中的_______位置。
A. 顶点 B. 棱上 C. 面上 D. 体心
(4)钨在周期表中的位置是_______。
A. 第五周期第ⅡB族 B. 第五周期第ⅣB族 C. 第六周期第ⅡB族 D. 第六周期第ⅥB族
WO2-
(5)根据价层电子对斥理论, 4 的价层电子对数是_______。
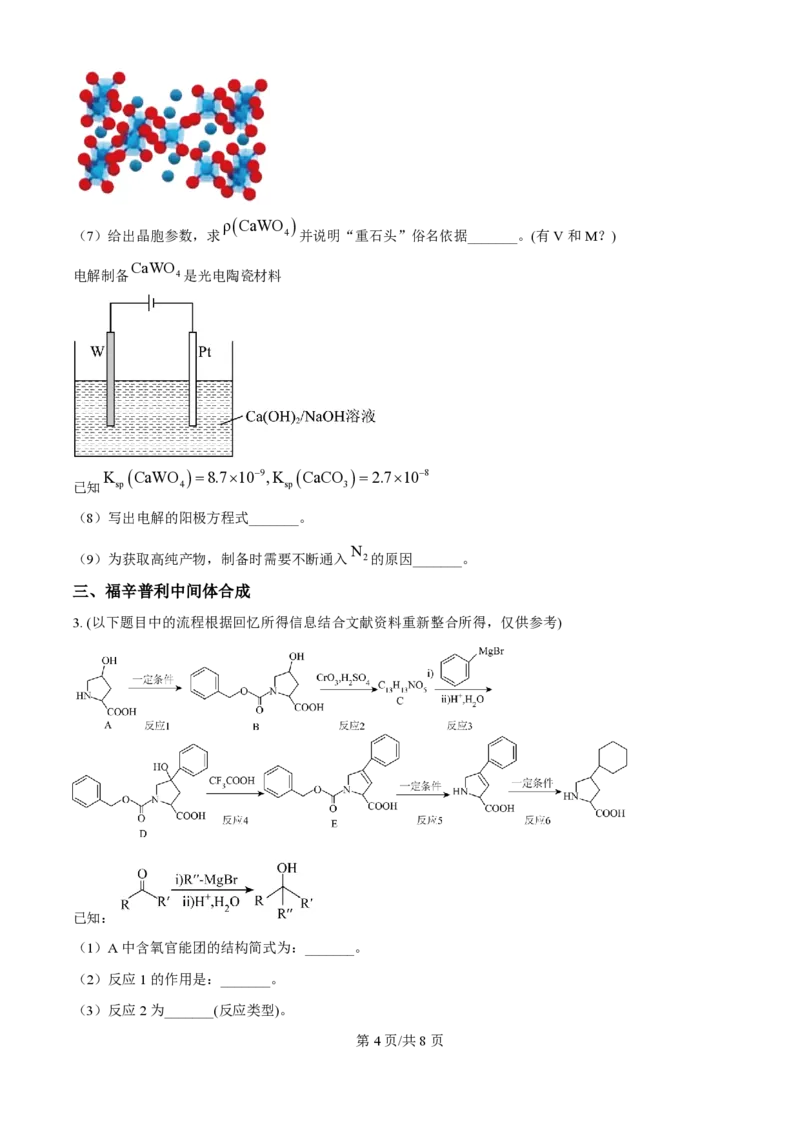
(6)图晶胞1-8号O原子,若晶胞仅含1个完整 WO2 4 - 四面体,组成该四面体的O编号是_______。
表格(各种矿石密度)。
第3页/共8页
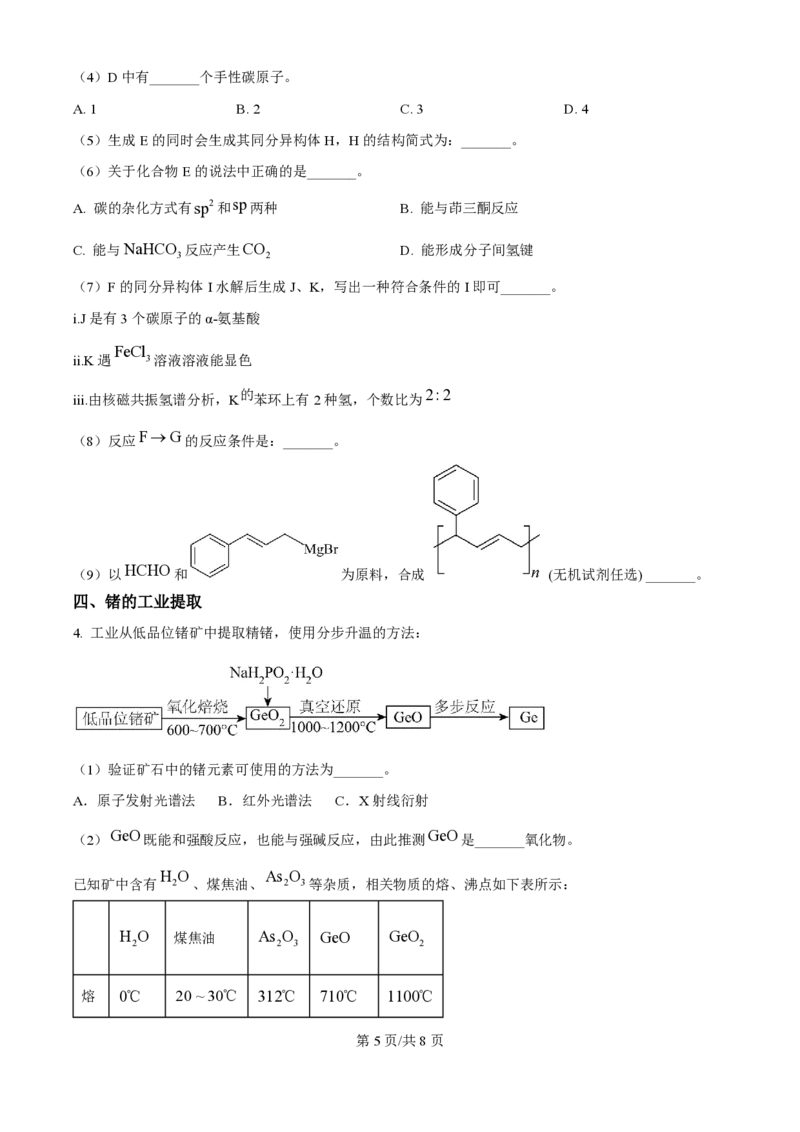
学科网(北京)股份有限公司ρCaWO
(7)给出晶胞参数,求 4 并说明“重石头”俗名依据_______。(有V和M?)
CaWO
电解制备 4是光电陶瓷材料
K CaWO =8.7´10-9,K CaCO =2.7´10-8
已知 sp 4 sp 3
(8)写出电解的阳极方程式_______。
N
(9)为获取高纯产物,制备时需要不断通入 2的原因_______。
三、福辛普利中间体合成
3. (以下题目中的流程根据回忆所得信息结合文献资料重新整合所得,仅供参考)
已知:
(1)A中含氧官能团的结构简式为:_______。
(2)反应1的作用是:_______。
(3)反应2为_______(反应类型)。
第4页/共8页
学科网(北京)股份有限公司(4)D中有_______个手性碳原子。
A. 1 B. 2 C. 3 D. 4
(5)生成E的同时会生成其同分异构体H,H的结构简式为:_______。
(6)关于化合物E的说法中正确的是_______。
A. 碳的杂化方式有sp2和sp两种 B. 能与茚三酮反应
C. 能与NaHCO 反应产生CO D. 能形成分子间氢键
3 2
(7)F的同分异构体I水解后生成J、K,写出一种符合条件的I即可_______。
i.J是有3个碳原子的α-氨基酸
FeCl
ii.K遇 3溶液溶液能显色
的 2:2
iii.由核磁共振氢谱分析,K 苯环上有2种氢,个数比为
F®G
(8)反应 的反应条件是:_______。
HCHO
(9)以 和 为原料,合成 (无机试剂任选) _______。
四、锗的工业提取
4. 工业从低品位锗矿中提取精锗,使用分步升温的方法:
(1)验证矿石中的锗元素可使用的方法为_______。
A.原子发射光谱法 B.红外光谱法 C.X射线衍射
GeO GeO
(2) 既能和强酸反应,也能与强碱反应,由此推测 是_______氧化物。
H O As O
已知矿中含有 2 、煤焦油、 2 3等杂质,相关物质的熔、沸点如下表所示:
H O 煤焦油 As O GeO GeO
2 2 3 2
熔 0℃ 20~30℃ 312℃ 710℃ 1100℃
第5页/共8页
学科网(北京)股份有限公司点 升华
沸
100℃ 70~80℃ 465℃
点
(3)使用分段升温的原因是_______。
NaH PO ×H O Ge
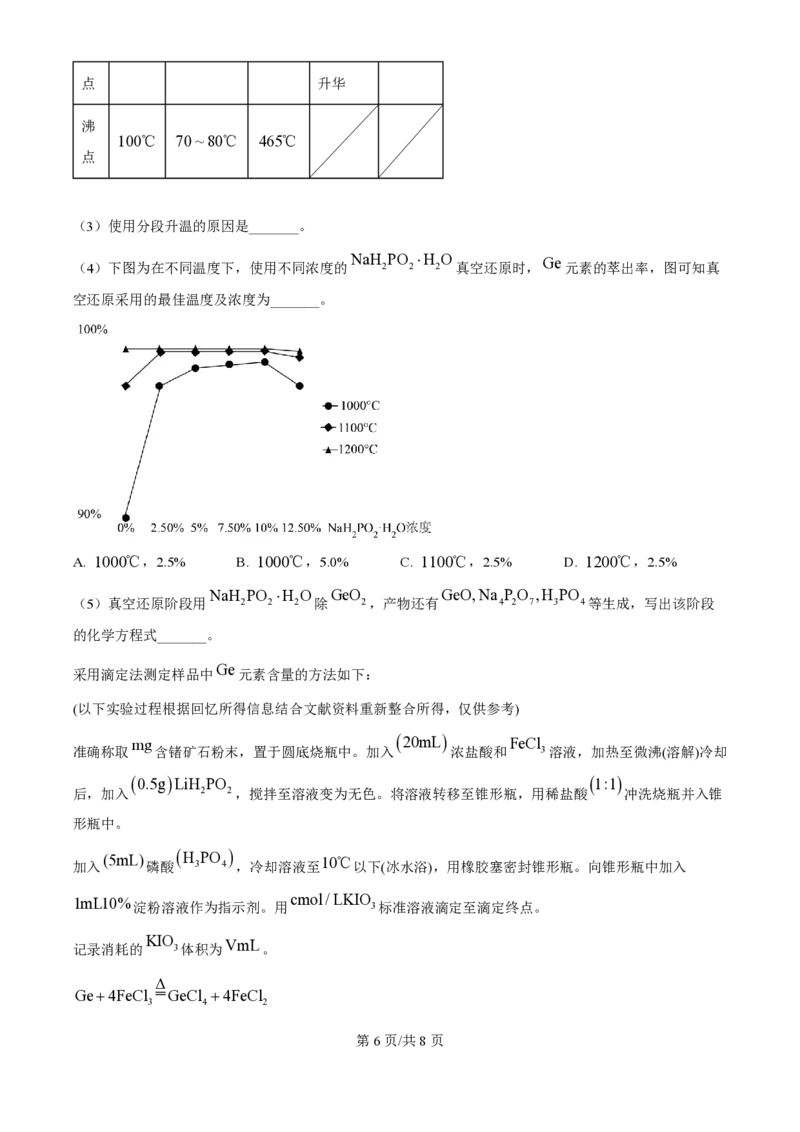
(4)下图为在不同温度下,使用不同浓度的 2 2 2 真空还原时, 元素的萃出率,图可知真
空还原采用的最佳温度及浓度为_______。
A. 1000℃,2.5% B. 1000℃,5.0% C. 1100℃,2.5% D. 1200℃,2.5%
NaH PO ×H O GeO GeO,Na PO ,H PO
(5)真空还原阶段用 2 2 2 除 2,产物还有 4 2 7 3 4等生成,写出该阶段
的化学方程式_______。
Ge
采用滴定法测定样品中 元素含量的方法如下:
(以下实验过程根据回忆所得信息结合文献资料重新整合所得,仅供参考)
mg
20mL
FeCl
准确称取 含锗矿石粉末,置于圆底烧瓶中。加入 浓盐酸和 3溶液,加热至微沸(溶解)冷却
0.5gLiH PO 1:1
后,加入 2 2,搅拌至溶液变为无色。将溶液转移至锥形瓶,用稀盐酸 冲洗烧瓶并入锥
形瓶中。
加入
(5mL)
磷酸
H
3
PO
4
,冷却溶液至
10℃
以下(冰水浴),用橡胶塞密封锥形瓶。向锥形瓶中加入
cmol/LKIO
1mL10%
淀粉溶液作为指示剂。用 3标准溶液滴定至滴定终点。
KIO VmL
记录消耗的 3体积为 。
D
Ge+4FeCl GeCl +4FeCl
3 4 2
第6页/共8页
学科网(北京)股份有限公司GeCl +LiH PO +H O=GeCl +LiH PO +2HCl
4 2 2 2 2 2 3 (还原)
3GeCl +KIO +6HCl=3GeCl +KI+3H O
2 3 4 2 (主反应)
5KI+KIO +6HCl=3I +6KCl+3H O
3 2 2 (终点反应)
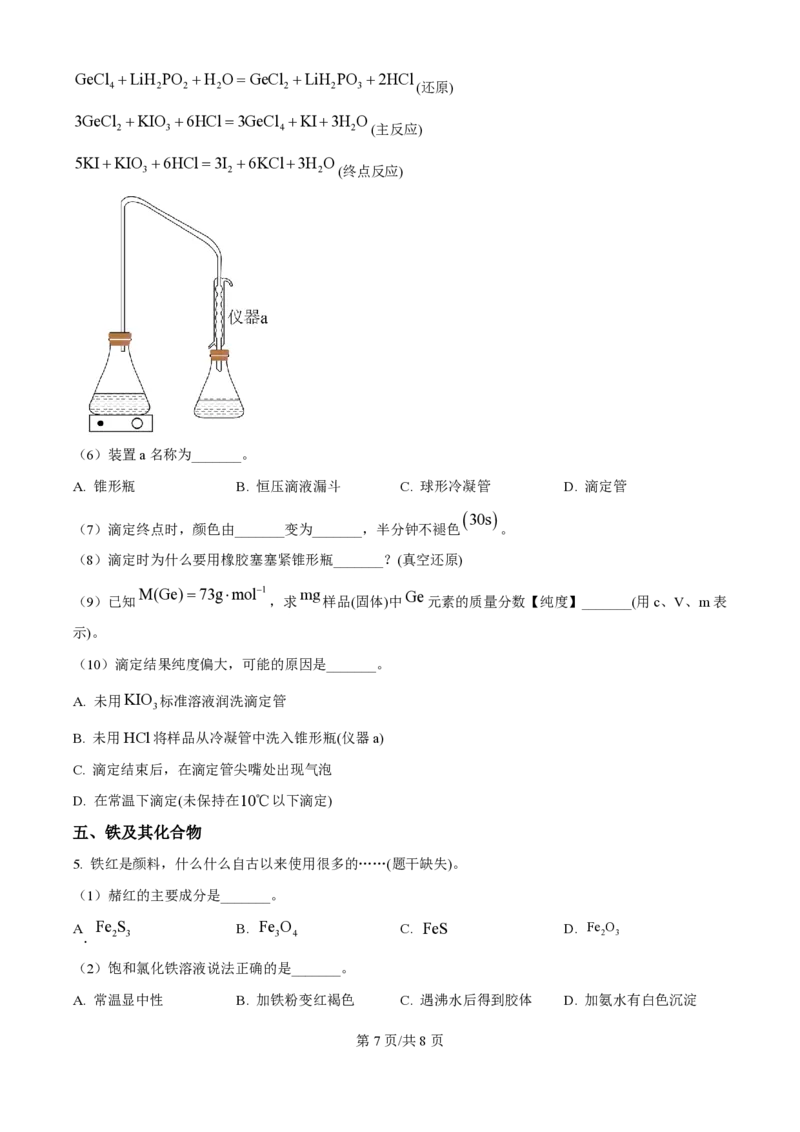
(6)装置a名称为_______。
A. 锥形瓶 B. 恒压滴液漏斗 C. 球形冷凝管 D. 滴定管
30s
(7)滴定终点时,颜色由_______变为_______,半分钟不褪色 。
(8)滴定时为什么要用橡胶塞塞紧锥形瓶_______?(真空还原)
M(Ge)=73g×mol-1 mg Ge
(9)已知 ,求 样品(固体)中 元素的质量分数【纯度】_______(用c、V、m表
示)。
(10)滴定结果纯度偏大,可能的原因是_______。
A. 未用KIO 标准溶液润洗滴定管
3
B. 未用HCl将样品从冷凝管中洗入锥形瓶(仪器a)
C. 滴定结束后,在滴定管尖嘴处出现气泡
D. 在常温下滴定(未保持在10℃以下滴定)
五、铁及其化合物
5. 铁红是颜料,什么什么自古以来使用很多的……(题干缺失)。
(1)赭红的主要成分是_______。
A Fe S B. Fe O C. FeS D. Fe O
. 2 3 3 4 2 3
(2)饱和氯化铁溶液说法正确的是_______。
A. 常温显中性 B. 加铁粉变红褐色 C. 遇沸水后得到胶体 D. 加氨水有白色沉淀
第7页/共8页
学科网(北京)股份有限公司(3)有关铁原子说法正确的是_______。(不定项)
A. 有4个不同能级的电子 B. 有5个未成对电子
C. 占据15个原子轨道 D. 有26种能量不同的电子
(4)加热试管中固体至红热,则_______。(不定项)
A. 移开酒精灯后固体保持红热 B. S只做还原剂
C. 主要产生的气体附产物为SO D. 最终得到黑色的Fe S
3 2 3
(5)éFe(SCN)H O ùCl 内界为_______,配体有_______种
ë 2 5 û 2
(6)Fe3+
(aq)
+xCl-
(aq) ƒ
FeCl
x
3-x
(aq)
(x =1,2,3,4),加水稀释至体积为原来的2倍,则n Fe3+
_______。
A.增大 B.不变 C.减小
并用浓度商Q与平衡常数K的大小关系解释原因_______。
(7)已知c
Cl-
=12mol/L,求FeCl 的分布系数_______。
3
cFeCl
3
c Fe3+ +cé(FeCl)2+ù+céFeCl +ù+cFeCl +céFeCl -ù
ë û ë 2 û 3 ë 4 û
x 1 2 3 4
97
.
K 30.2 134.9 1.02
72
第8页/共8页
学科网(北京)股份有限公司