可灌注的生物3D打印皮肤芯片模型实现药物测试与伤口愈合研究
皮肤作为人体最大的器官,覆盖全身表面,不仅承担着物理保护、体温调节、外界刺激感知和免疫防御等关键生理功能,还是机体抵御外界病原体入侵、维持内环境稳定的重要屏障,因此一直是组织工程领域的重点研究对象。近年来,随着生物医学与材料科学的交叉融合,生物3D打印成为制备皮肤替代物的极具潜力的方法,在药物测试和严重皮肤损伤的临床治疗中均具有应用前景。该技术能将细胞精准沉积在生物材料基质中,构建具有可控微环境的复杂组织结构。生物3D打印皮肤模型的一大核心挑战是构建血管系统,才能为人工皮肤内部细胞实现充足的营养供给和氧气输送,保障细胞存活与功能发挥,推动其向临床转化。

基本信息
论文题目:3D bioprinting of a perfusable skin-on-chip model suitable for drug testing and wound healing studies
DOI:10.1016/j.mtbio.2025.101974
发表期刊: Materials Today Bio (IF:10.2)
本研究开发了一种适用于药物测试和伤口愈合研究的可灌注血管化皮肤芯片模型。团队采用生物3D打印技术,以甲基丙烯酰化明胶(GelMA)分别配制8%和15%浓度的水凝胶作为真皮层和表皮层生物墨水,40%的普朗尼克F127(Pluronic F127)作为牺牲材料构建血管通道,整合新生儿包皮成纤维细胞、人表皮角质形成细胞和人脐静脉内皮细胞三种细胞类型,通过生物打印技术制备出仿生皮肤结构;同时设计定制化生物反应器实现培养基持续灌注,结合COMSOL多物理场仿真验证模型的流体流动和物质扩散特性,并通过一系列表征实验验证模型的生理仿生性、血管功能性和伤口愈合能力。该模型解决了生物3D打印皮肤模型中血管化和营养物质均匀分布的关键难题,能精准模拟皮肤的层级结构、屏障功能和血管系统,细胞存活率超90%,且可实现深层和浅表伤口的自发愈合,为体外药物测试和皮肤再生治疗研究提供了伦理且高效的仿生平台。
主要内容
研究人员对构建皮肤模型的三种生物墨水开展了系统的理化和打印性能表征,结果显示8%GelMA(G8)的溶胀率显著高于15% GelMA(G15),而G15的杨氏模量远高于G8,这一力学差异可模拟体内皮肤真皮与表皮的生理特性。通过打印方形网格并计算可打印性参数Pr,确定了G8、G15和40%Pluronic F127(P40)的最佳打印温度和压力,三者的Pr值均接近1,表现出优异的打印保真度。流变学测试表明两种GelMA水凝胶在选定打印温度下均以弹性行为为主,且溶胶-凝胶转变温度与打印温度匹配,保障了打印过程的稳定性。荧光漂白恢复实验测得的扩散系数显示,不同分子量的葡聚糖在两种GelMA中水凝胶的扩散规律一致,G15的组成差异未影响营养物质的扩散能力。此外,通过COMSOL仿真模拟了生物墨水在挤出喷嘴尖端的剪切应力,发现选定打印压力下的剪切应力处于细胞耐受范围内,可最大限度减少挤出过程对细胞的机械损伤(图1)。
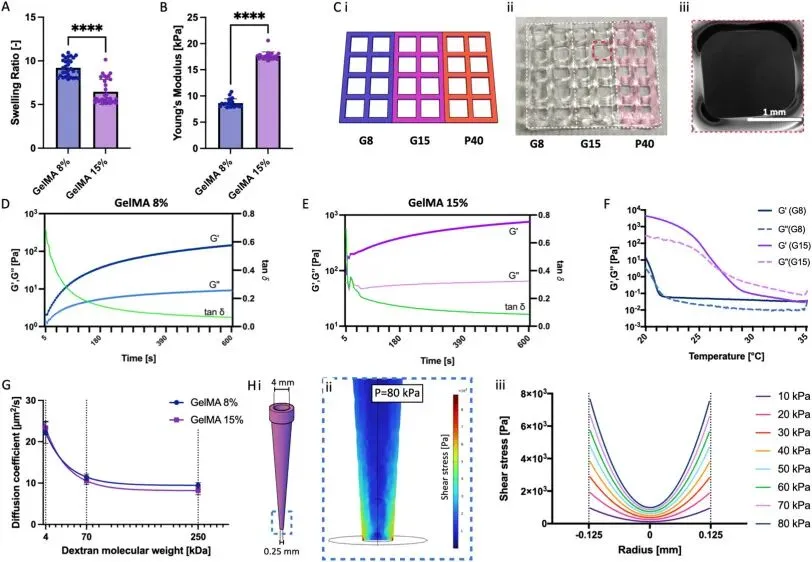
图 1 生物墨水的综合表征结果
研究人员设计了具有层级结构的3D血管化皮肤模型,真皮层为1 mm厚的G8、表皮层为0.2 mm厚的G15,直径0.5 mm的血管通道由P40打印并呈蛇形分布。利用COMSOL多物理场仿真模拟了模型内培养基的流动和稀释物质的扩散过程,结果显示目标物质在灌注开始后约10分钟即可在模型内达到浓度平台期。为验证仿真模型的准确性,制备了生物打印模型并灌注荧光标记的4kDa葡聚糖,通过检测不同时间点的荧光强度绘制出物质浓度变化曲线,实验数据与仿真模型预测的趋势高度吻合,证实了模型灌注系统的有效性。同时团队设计了由PDMS模具、上下密封层组成的定制化不锈钢生物反应器,该反应器可实现皮肤模型的密封固定和培养基的无泄漏灌注,为模型的体外培养提供了稳定的装置支持(图2)。
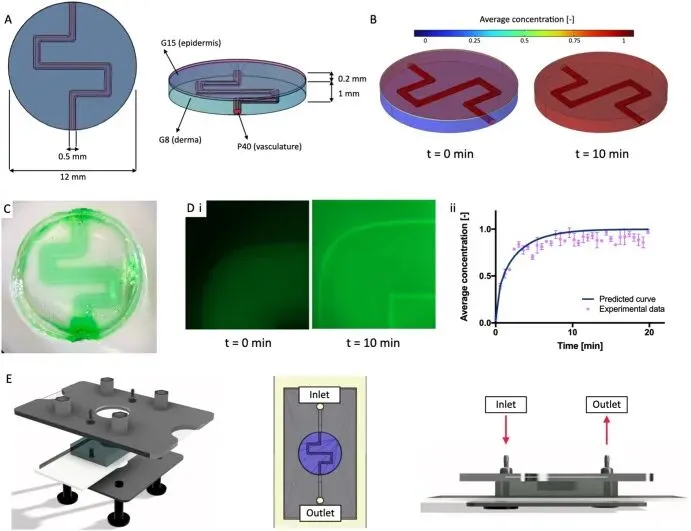
图 2 血管化皮肤模型的设计与仿真验证
活死细胞染色实验证实,真皮层内的细胞存活率在21天培养后仍高于90%,表明G8水凝胶为细胞生长提供了良好的微环境。原子力显微镜测试发现,含细胞的G8水凝胶杨氏模量较无细胞对照组显著降低,这是因为代谢活跃的细胞通过分泌酶降解基质并沉积天然细胞外基质蛋白,实现了对水凝胶基质的主动重塑,且该重塑过程未破坏模型的整体形态。免疫荧光染色和定量分析显示,成纤维细胞在培养过程中持续分泌I型、III型、IV型胶原蛋白以及弹性蛋白、纤连蛋白等真皮层关键基质蛋白,且蛋白表达量随培养时间显著增加,表明真皮层实现了良好的组织成熟(图3)。
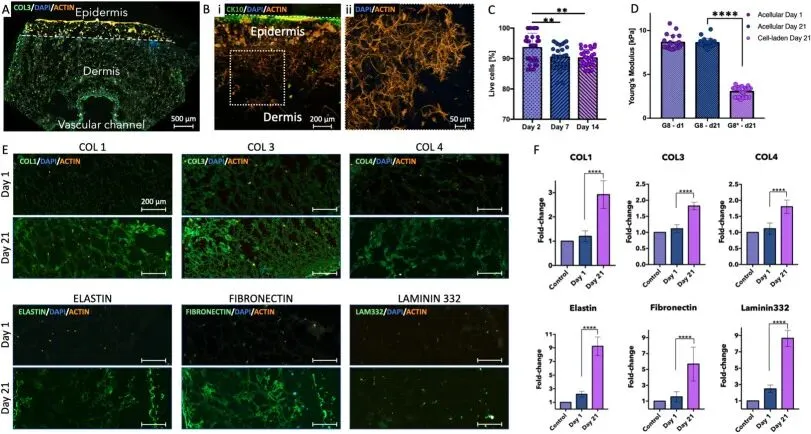
图 3 皮肤模型真皮层的生物学与力学表征
将人表皮角质形成细胞(HEK)接种于15%GelMA(G15)水凝胶构建表皮层,添加角质形成细胞生长因子(KGF)促进细胞的分层和分化。免疫荧光染色显示,表皮分化标志物CK10的表达量随培养时间显著升高,表明角质形成细胞实现了正常的分化成熟。表皮层的厚度随培养时间持续增加,21天培养后达到246.6±22.8 μm,完全填充了生物打印的G15水凝胶空间。跨上皮电阻(TEER)检测结果显示,表皮层的TEER值随培养时间显著上升,且与无角质形成细胞的对照组存在显著差异,证实角质形成细胞形成了具有紧密连接的功能性上皮屏障。苏木精-伊红(H&E)染色显示,21天成熟后的表皮层形成了多层排列的角质形成细胞结构,与天然皮肤的表皮形态高度相似。原子力显微镜测试发现,含细胞的表皮层杨氏模量随培养时间显著降低,角质形成细胞的高密度生长对水凝胶的刚度产生了显著的调控作用(图4)。
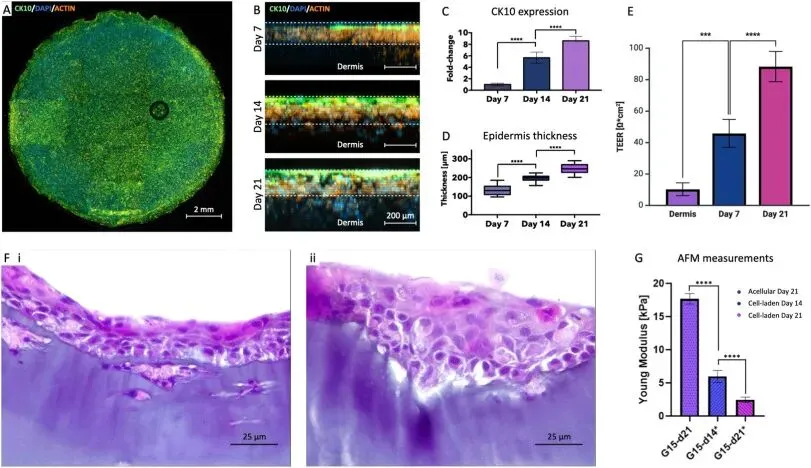
图 4 皮肤模型表皮层的形成与功能表征
免疫荧光染色显示,内皮细胞特异性标志物CD31在血管通道壁呈连续表达,细胞形成了覆盖通道壁的单层结构,并构建出完整的血管管腔。为验证内皮屏障的功能,分别对内皮化和非内皮化的血管通道灌注70 kDa荧光标记葡聚糖,检测发现内皮化的血管通道葡聚糖渗透率显著低于非内皮化对照组,表明成熟的内皮层形成了具有选择性通透的功能屏障,可有效调控营养物质的跨膜运输,同时研究证实彻底去除牺牲材料P40是保证细胞黏附和血管结构完整性的关键(图5)。
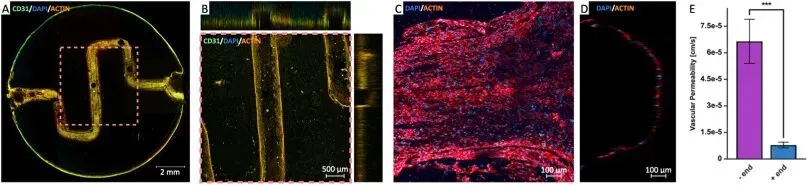
图 5 皮肤模型血管通道的内皮化与功能验证
对于全层缺损伤口,免疫荧光染色显示伤口区域的Ki67阳性细胞比例随培养时间显著升高,表明细胞发生了活跃的增殖,成纤维细胞重新填充真皮缺损区域,角质形成细胞在伤口表面分层生长,14天培养后实现了伤口的自发闭合。对于表皮浅表划伤伤口,角质形成细胞表现出协调的迁移和增殖行为,14天培养后完全覆盖了划伤区域,重新建立了表皮的连续性。Ki67表达定量分析证实,表皮和真皮层的细胞在伤口愈合过程中均处于高增殖状态,表明该3D血管化皮肤模型可精准模拟天然皮肤的深层和浅表伤口愈合过程,再现上皮再形成和真皮重塑的关键特征(图6)。
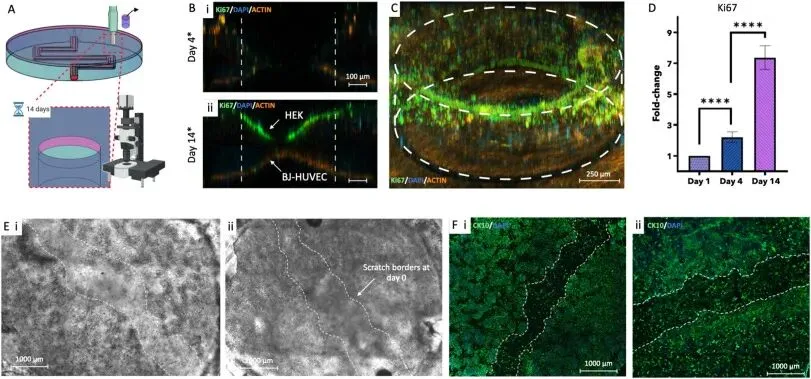
图 6 3D血管化皮肤模型的伤口愈合能力评估
总结及展望
通过生物3D打印技术实现了皮肤真皮、表皮层级结构与血管通道的精准成型,利用牺牲生物打印策略构建可灌注血管网络,解决了传统皮肤模型血管化不足、营养输送不均的问题,同时通过生物3D打印的定制化优势,实现了多种生物墨水的精准沉积和三种细胞类型的仿生分布,最终制备出高度模拟天然皮肤生理结构和功能的可灌注皮肤芯片模型,是先进体外皮肤模型研发领域的一项重要进展。该模型能够重现皮肤生理和伤口愈合过程的关键特征,使其成为化妆品和药物研究的宝贵工具,为评估产品的有效性和安全性提供了一种符合伦理且高效的研究平台。

联系我们

设备销售请联系:EFL 发发(15370087306 微信同号)

 夜雨聆风
夜雨聆风





