AIVEV文献分享丨《Nature》虚拟病理模型 CHIEF实现癌症诊断与预后一体化突破

哈佛医学院、斯坦福大学医学院等团队在Nature发表题为“A pathology foundation model for cancer diagnosis and prognosis prediction”的研究论文。该研究由 Xiyue Wang、赵俊涵等人共同完成,构建了面向数字病理的基础模型 CHIEF。值得一提的是,赵俊涵此前还参与发表了Nature Communications论文《Uncertainty-aware ensemble of foundation models differentiates glioblastoma from its mimics》,持续聚焦病理基础模型与脑肿瘤智能诊断方向。本研究通过结合 tile-level 自监督预训练与 whole-slide 弱监督预训练,从大规模多癌种病理切片中学习通用表征,实现了癌细胞检测、肿瘤来源识别、分子特征预测以及生存预后评估等多任务分析,并在多个独立外部队列中展现出优于现有方法的泛化能力。


研究背景
传统病理 AI 多围绕单一任务分别训练专用模型,例如癌细胞检测、分型判断或预后预测。这类方法虽然在特定数据集上有效,但往往依赖大规模标注数据,且容易受到制片流程、扫描设备及人群来源差异的影响,导致外部泛化能力不足。为解决这一问题,作者提出构建病理领域的“基础模型”,希望通过大规模、多癌种、多中心数据预训练,获得可迁移、可泛化的组织学表征,从而支持多种下游任务的统一分析。
本文亮点
-
提出病理基础模型 CHIEF 不再局限于某一个具体任务,而是以通用表征学习为核心,支持癌症诊断、分子预测和预后分析等多任务应用。
-
大规模、多中心、多癌种训练与验证 模型预训练覆盖 60,530 张全视野病理切片、19 个解剖部位,并在 32 个独立切片队列、24 家医院/队列 中验证,体现出较强跨中心泛化能力
-
性能与临床意义兼具 CHIEF 在癌细胞检测、IDH/MSI 状态预测及生存分析中均优于多种现有深度学习方法,显示其有望成为数字病理临床辅助分析的通用底座
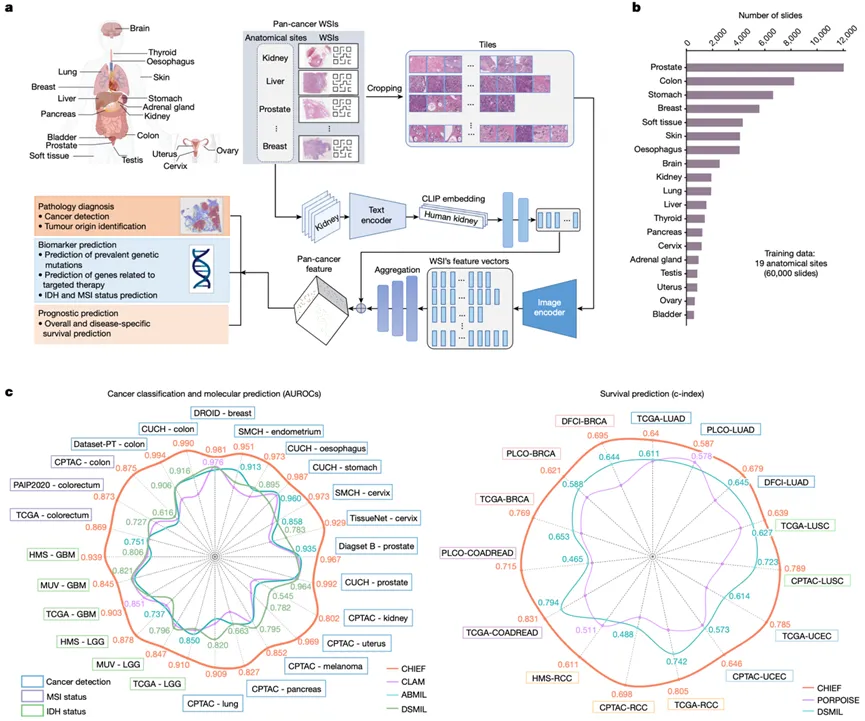
图1|CHIEF模型总体框架:从基础预训练到多任务病理分析
图注: 作者构建了病理基础模型 CHIEF。模型先基于大量病理图像 tile 进行无监督预训练,再在 whole-slide image(WSI)层面进行弱监督预训练,最终将学到的通用病理表征用于癌症检测、肿瘤来源识别、基因/分子状态预测及生存预后分析。训练集共纳入 19 个解剖部位、60,530 张切片。
图片解析: 这一图是全文最核心的总览图。它回答了三个关键问题:第一,CHIEF 是什么-它不是一个单任务分类器,而是一个通用病理基础模型。第二,CHIEF 怎么训练-先用海量 tile 学局部显微形态,再用大规模 WSI 学组织上下文与跨癌种差异。第三,CHIEF 能做什么-不仅能做传统的癌细胞检测,还能进一步预测肿瘤来源、基因突变状态和患者预后。也就是说,作者想证明的不是“某个任务做得更好”,而是“病理 AI 可以像大模型一样拥有统一底座”。
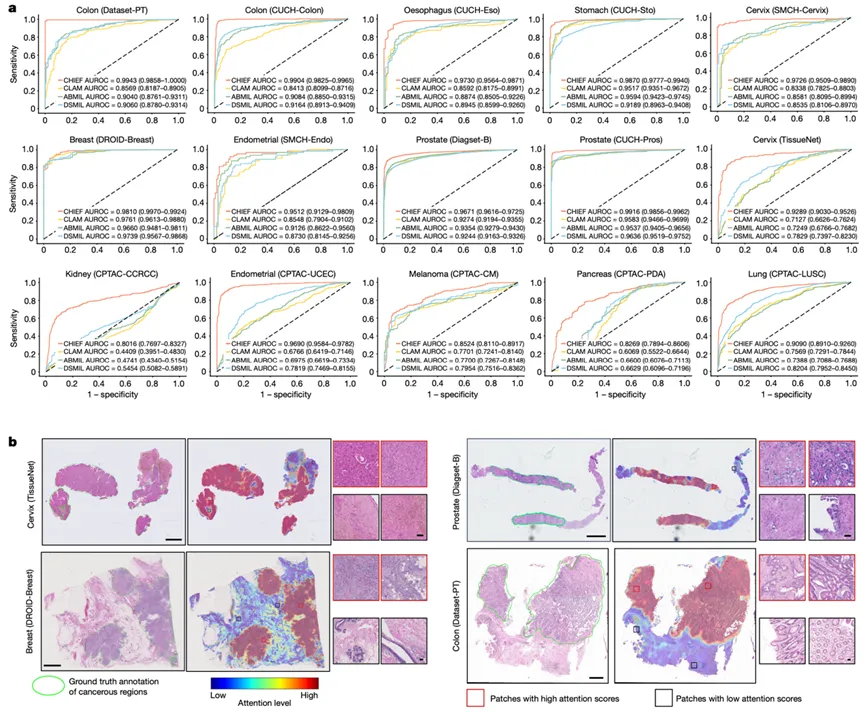
图2|CHIEF在癌细胞检测中的表现:跨癌种、跨中心依然稳定
图注: 作者在 15 个独立数据集、11 种癌症来源的 13,661 张 WSI 上验证 CHIEF 的癌细胞检测能力,并与 CLAM、ABMIL、DSMIL 等方法比较。CHIEF 在多数队列中取得最高 AUROC,且注意力热图能够较准确聚焦于病理医师标注的癌变区域。
图片解析: 这一图主要证明 CHIEF 具备强泛化的癌症识别能力。左侧一系列 ROC 曲线显示,CHIEF 在不同癌种、不同队列、不同样本来源条件下,整体上都优于现有主流弱监督方法。右侧热图则进一步告诉我们:CHIEF 不是“黑箱瞎猜”,而是把高注意力集中在真正的肿瘤区域,并捕捉到了高核浆比、核异型性、结构紊乱等典型恶性组织学特征。这说明模型学到的不是某个数据集特有的伪特征,而是更具普适性的恶性形态学信号。
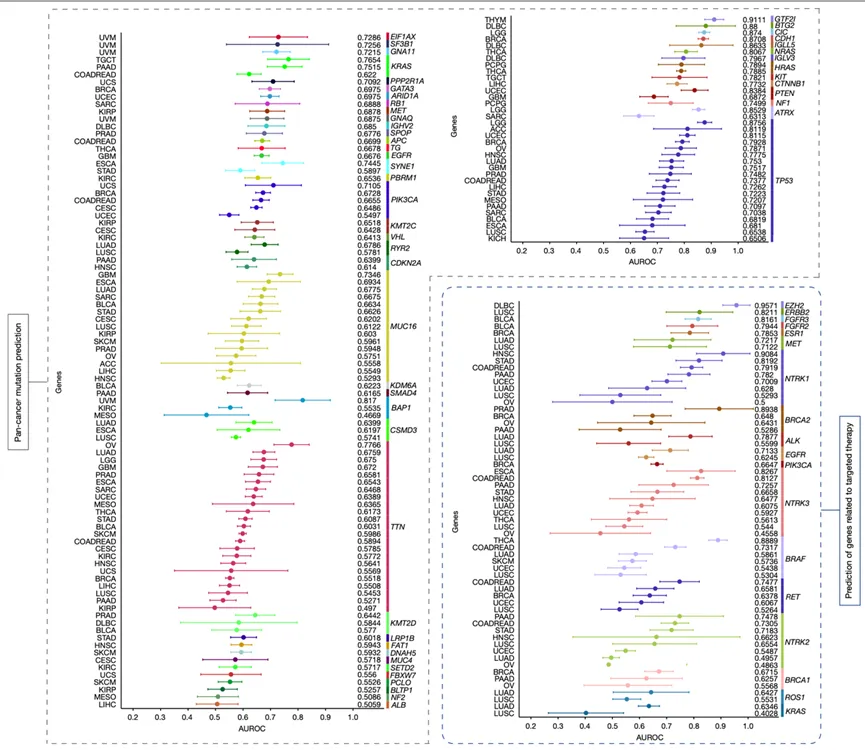
图3|CHIEF可从HE切片中预测基因突变与靶向治疗相关分子
图注: 作者系统评估了 CHIEF 对多癌种基因突变的预测能力,包括高频体细胞突变及与靶向治疗相关的基因改变。结果显示,CHIEF 可在多种癌症中较好预测 TP53、GTF2I、BAP1、EZH2、BRCA2、BRAF、FGFR3 等基因状态。
图片解析: 这一图体现了 CHIEF 的一个重要升级:它不仅能“看出是不是癌”,还能进一步从形态学中挖掘分子层面的信息。作者展示了两类任务:一类是泛癌种高频突变预测,说明某些驱动突变会在组织形态上留下可识别的线索;另一类是靶向治疗相关基因预测,更接近临床应用场景。这部分结果的意义在于,常规 HE 切片未来或许不只是形态诊断工具,还可能成为快速分子分层的入口。当然,这里更适合理解为“提供辅助线索”,而不是完全替代基因检测。
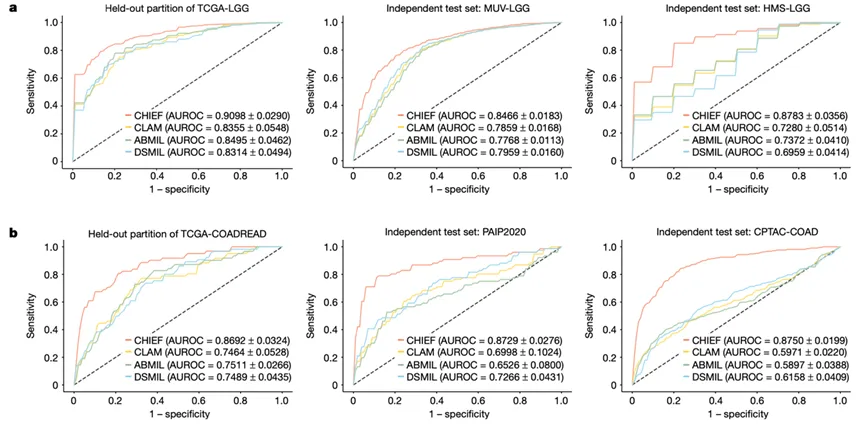
图4|CHIEF预测IDH与MSI状态:连接分子分型与治疗决策
图注:
作者分别评估了 CHIEF 对胶质瘤 IDH 状态 和结直肠癌 MSI 状态 的预测能力。结果显示,在训练集及独立外部验证集中,CHIEF 均优于对照模型,在 IDH 和 MSI 预测中取得较高 AUROC。
图片解析:
这一图的价值在于把 CHIEF 从“形态学工具”进一步推进到了临床分层工具。对于胶质瘤来说,IDH 状态已经深度参与 WHO 分类体系;对于结直肠癌来说,MSI 状态与免疫治疗获益密切相关。也就是说,这里不是简单增加一个预测任务,而是在说明:病理基础模型有机会在患者初诊阶段直接提供与分类、用药相关的分子信息。特别是 MSI 这种具有明确治疗指导意义的指标,如果未来在临床上能够稳定复现,将显著提升常规病理切片的附加价值。
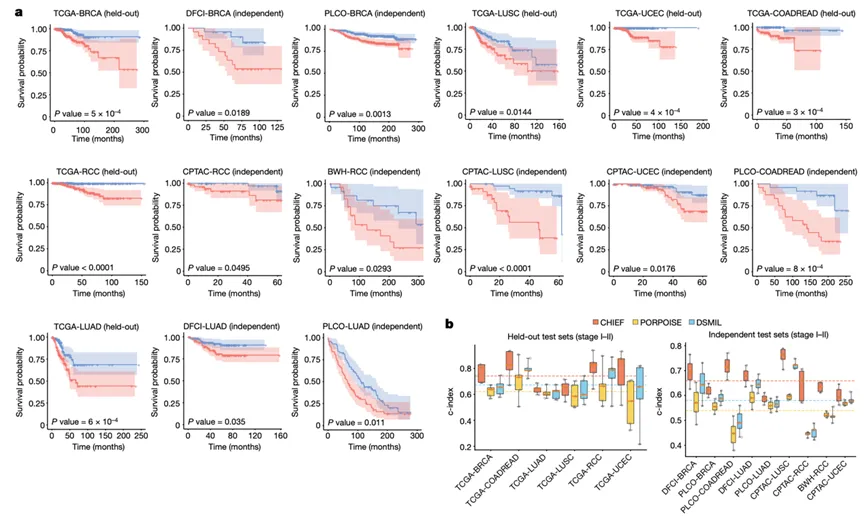
图5|CHIEF预测患者生存:病理图像也能成为预后分层工具
图注: 作者在 17 个数据集、7 类癌症的 9,404 张 WSI 中评估 CHIEF 的生存预测能力。结果显示,CHIEF 可在多队列中将患者区分为高风险与低风险组,其 c-index 整体优于 PORPOISE 和 DSMIL 等方法。
图片解析: 这一图说明 CHIEF 学到的表征不仅能用于“诊断当下”,还能在一定程度上反映“未来结局”。Kaplan–Meier 曲线显示,CHIEF 在多种癌症、多个独立队列中都能把患者分出明显不同的生存风险层级。这意味着模型提取到的显微组织信息,已经不只是病理分类特征,还包含与肿瘤侵袭性、微环境状态、疾病进展风险相关的综合信号。从应用角度看,这类结果对于术后风险评估、随访强度制定及辅助治疗决策都有潜在价值。
总结与展望
这项工作的重要意义,不仅在于提出了一个性能更高的模型,更在于它推动了数字病理研究范式的转变:从过去“一个任务训练一个模型”,走向“先学习通用病理表征,再适配多类下游任务”的基础模型路线。CHIEF 通过大规模、多中心、多癌种训练,证明了病理基础模型在诊断、分子预测和预后分析中的广泛适用性,也显示出较好的跨域泛化能力。
但从转化角度看,这项研究仍有几个值得继续推进的方向:第一,如何进一步提升模型在真实临床工作流中的可解释性与稳定性;第二,如何在更多前瞻性、多设备、多实验室场景中验证其鲁棒性;第三,如何把这类基础模型真正嵌入病理医生决策流程,而不是仅停留在离线评测阶段。总体而言,CHIEF 代表了病理 AI 从“专用工具”向“通用底座”升级的重要一步。
DOI:
10.1038/s41586-024-07894-z
文章链接:
https://www.nature.com/articles/s41586-024-07894-z
 夜雨聆风
夜雨聆风




