重磅!CDE发布药品上市后变更补充申请说明,37种情形需注册检验
2026年04月23日,CDE发布了《上市后变更补充申请事项及受理时启动注册检验情形的说明表》的通知,明确了中药、化药和生物制品哪些变更是否要开检验通知书,具体内容如下:
根据上市后药学变更工作实际,为更好地服务注册申请人,药审中心优化完善了上市后药学变更补充申请事项及受理时启动注册检验的情形,现将有关事宜通知如下:
一、依据《已上市中药药学变更研究技术指导原则(试行)》、《已上市化学药品药学变更研究技术指导原则(试行》以及《已上市生物制品药学变更研究技术指导原则(试行)》的相关要求,药审中心形成了《上市后变更补充申请事项及受理时启动注册检验情形的说明表》(见附件),现予以发布,供申请人在补充申请申报时使用。
二、《上市后变更补充申请事项及受理时启动注册检验情形的说明表》中受理时启动注册检验的情形不适用于受理前已提出前置注册检验的已上市药品补充申请。
三、由于上市后药学变更情形复杂多样,如出现不适用《上市后变更补充申请事项及受理时启动注册检验情形的说明表》中所列的特殊情形,经申请人评估无需进行注册检验的,申请人可在受理前通过沟通交流或者公文形式与药审中心进行沟通
上市后变更补充申请事项及受理时启动注册检验情形的说明表(附件)
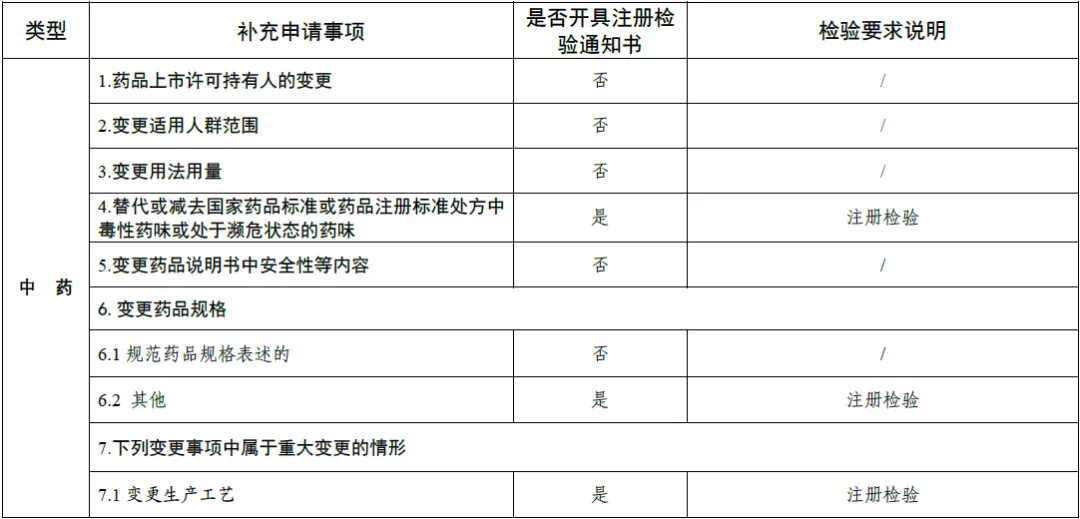
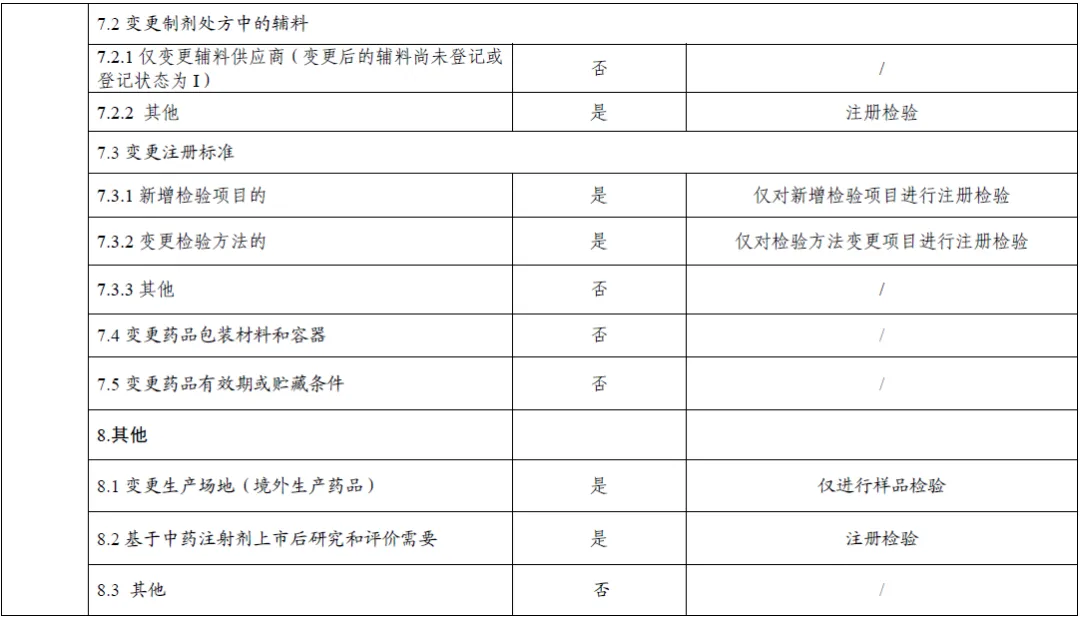
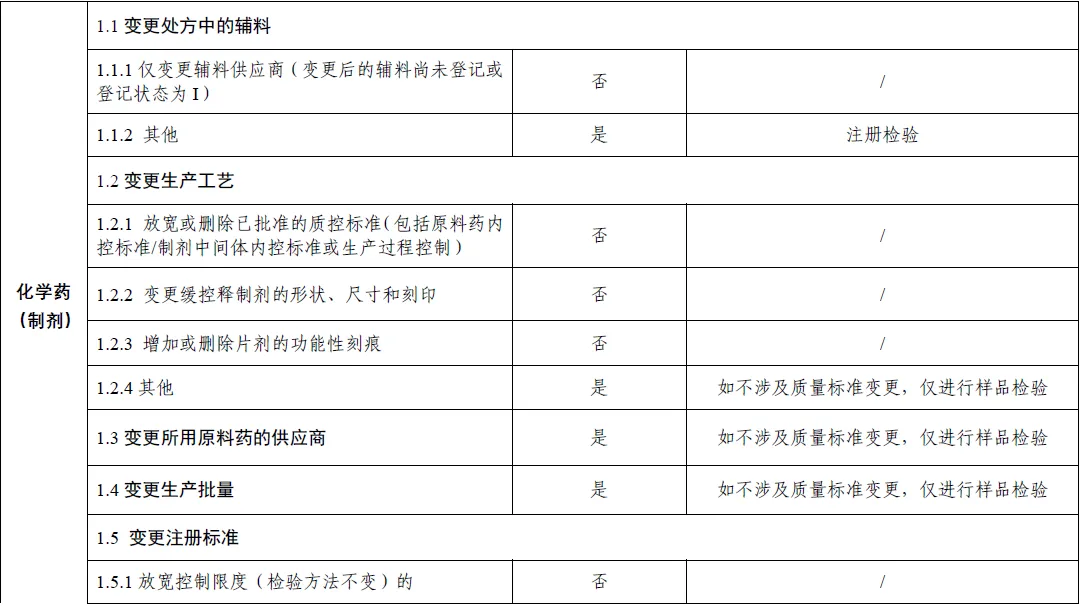
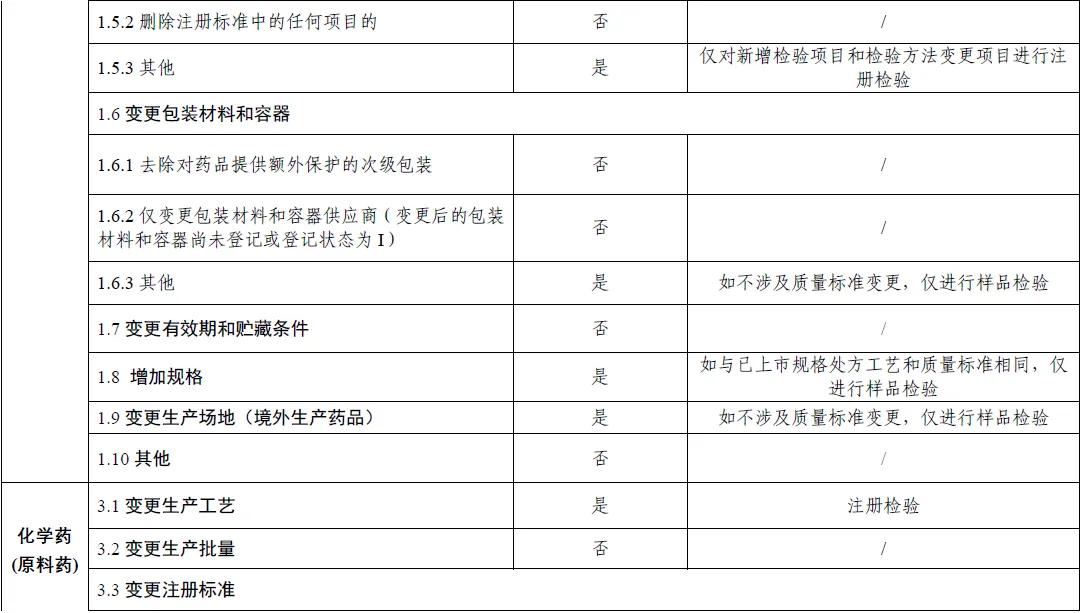
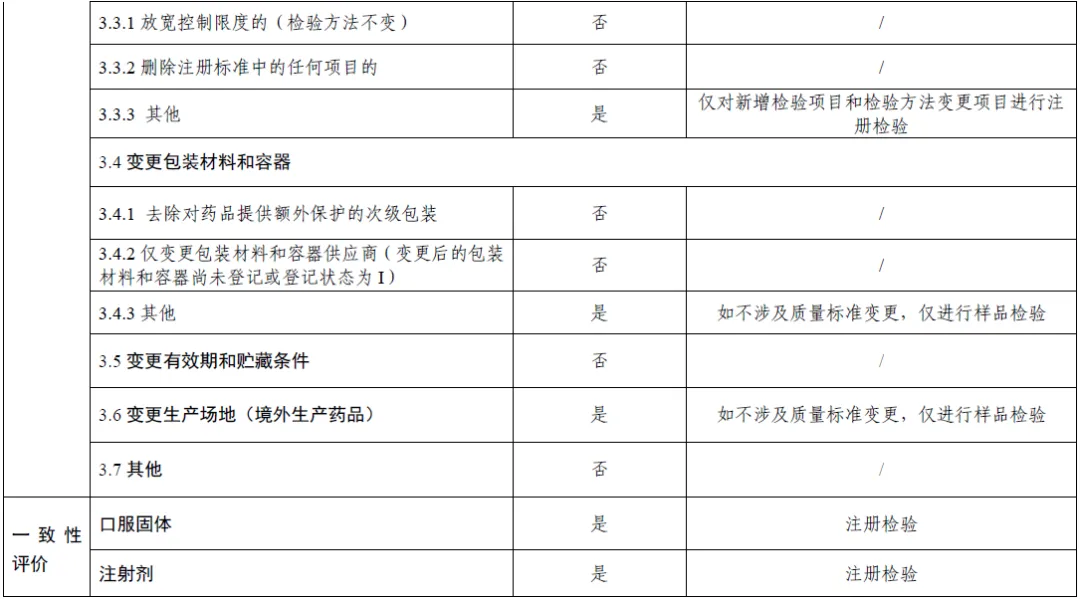
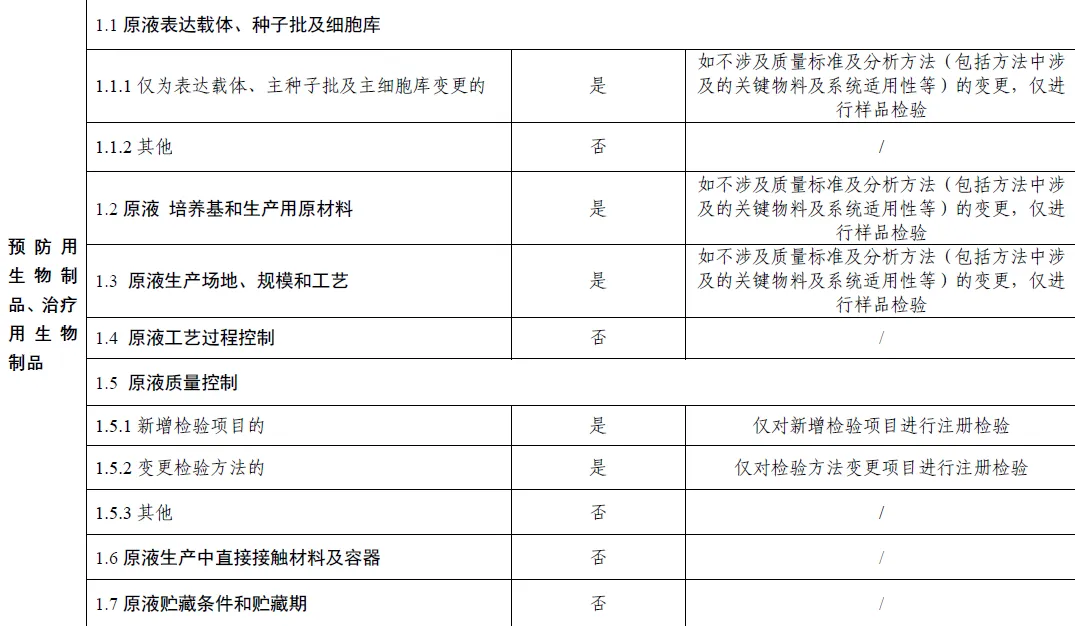
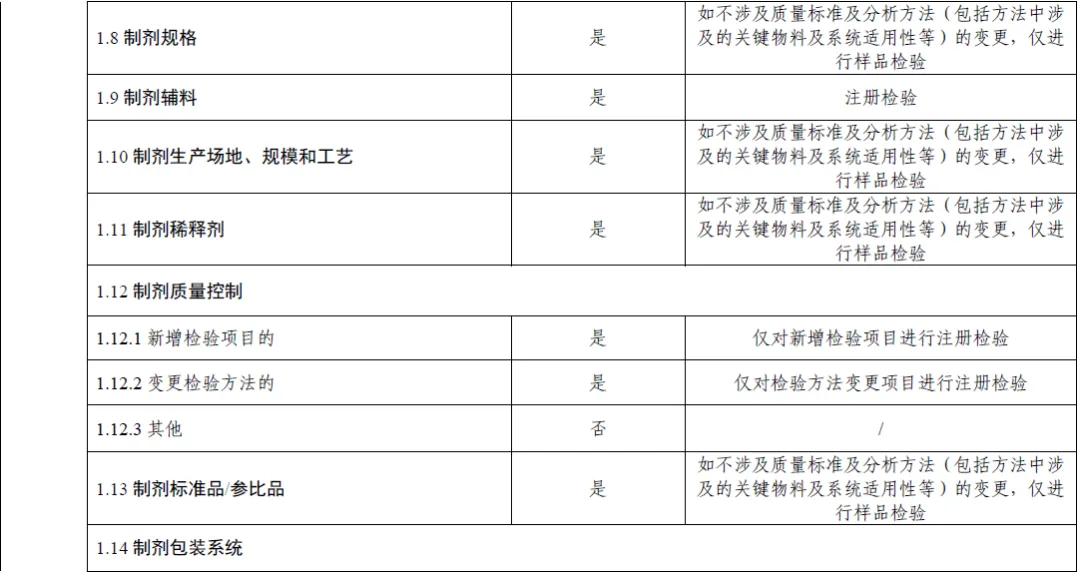
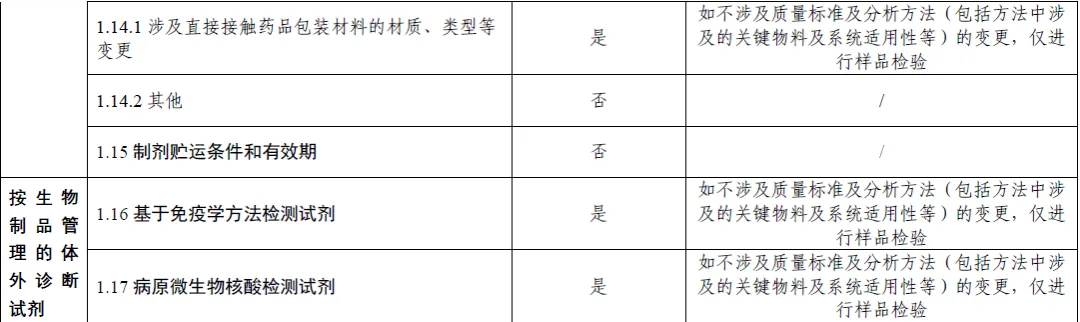
1、说明表中注册检验包括标准复核和样品检验
2、说明表中内容为原则上是否需启动注册检验的情形。由于上市后药学变更情形复杂多样,如受理时未启动注册检验,技术审评中会结合变更内容对产品质量的影响,必要时也会启动注册检验。
3、对于细化的补充申请事项,其中一项为需启动注册检验的情形,无论其他合并补充申请事项是否为启动注册检验的情形,该补充申请原则上均需要启动注册检验。
4、对于补充申请事项中既包括需开具注册检验通知书的细化项 ,又包括不需开具注册检验通知书的细化项 ,申请人未勾选相应细化项时,均按照开具注册检验通知书的情形开具注册检验通知书。

微信号:18626112796
苏州源创药物研究有限公司
 夜雨聆风
夜雨聆风




