文档内容
专练 35 原电池原理及应用(二)
授课提示:对应学生用书69页
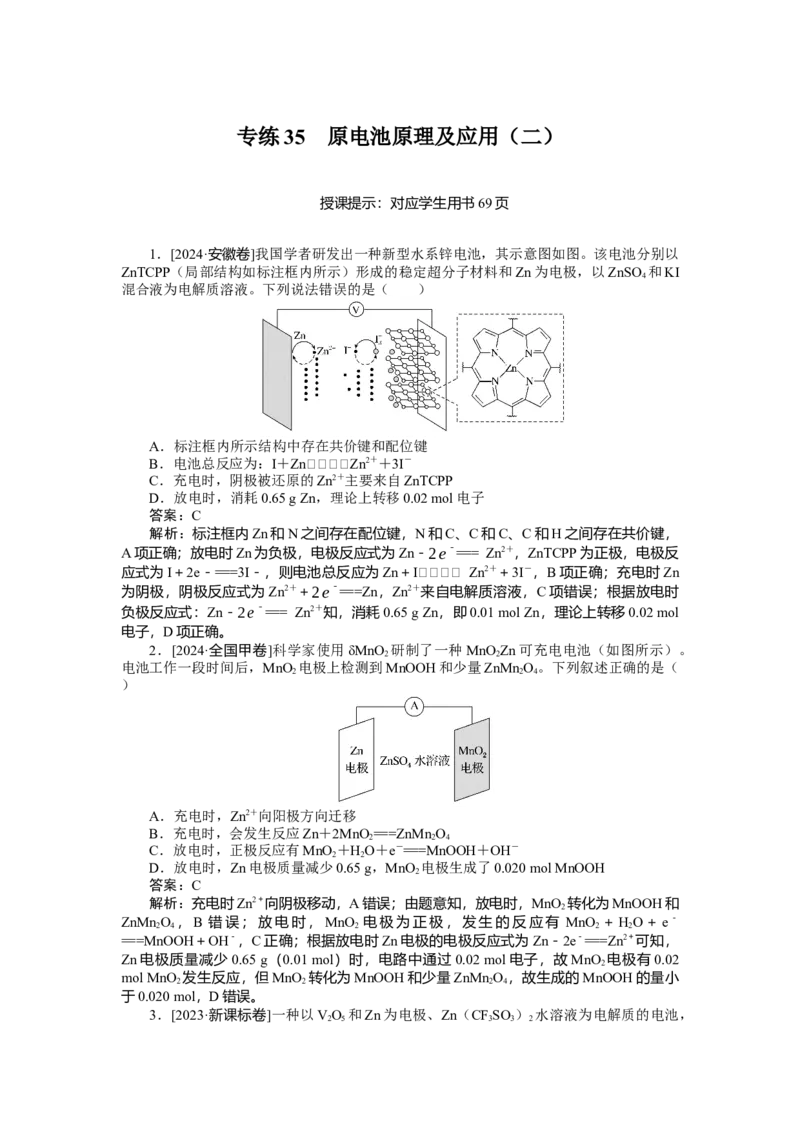
1.[2024·安徽卷]我国学者研发出一种新型水系锌电池,其示意图如图。该电池分别以
ZnTCPP(局部结构如标注框内所示)形成的稳定超分子材料和Zn为电极,以ZnSO 和KI
4
混合液为电解质溶液。下列说法错误的是( )
A.标注框内所示结构中存在共价键和配位键
B.电池总反应为:I+ZnZn2++3I-
C.充电时,阴极被还原的Zn2+主要来自ZnTCPP
D.放电时,消耗0.65 g Zn,理论上转移0.02 mol电子
答案:C
解析:标注框内Zn和N之间存在配位键,N和C、C和C、C和H之间存在共价键,
A项正确;放电时Zn为负极,电极反应式为Zn-2e-=== Zn2+,ZnTCPP为正极,电极反
应式为I+2e-===3I-,则电池总反应为Zn+I Zn2++3I-,B项正确;充电时Zn
为阴极,阴极反应式为Zn2++2e-===Zn,Zn2+来自电解质溶液,C项错误;根据放电时
负极反应式:Zn-2e-=== Zn2+知,消耗0.65 g Zn,即0.01 mol Zn,理论上转移0.02 mol
电子,D项正确。
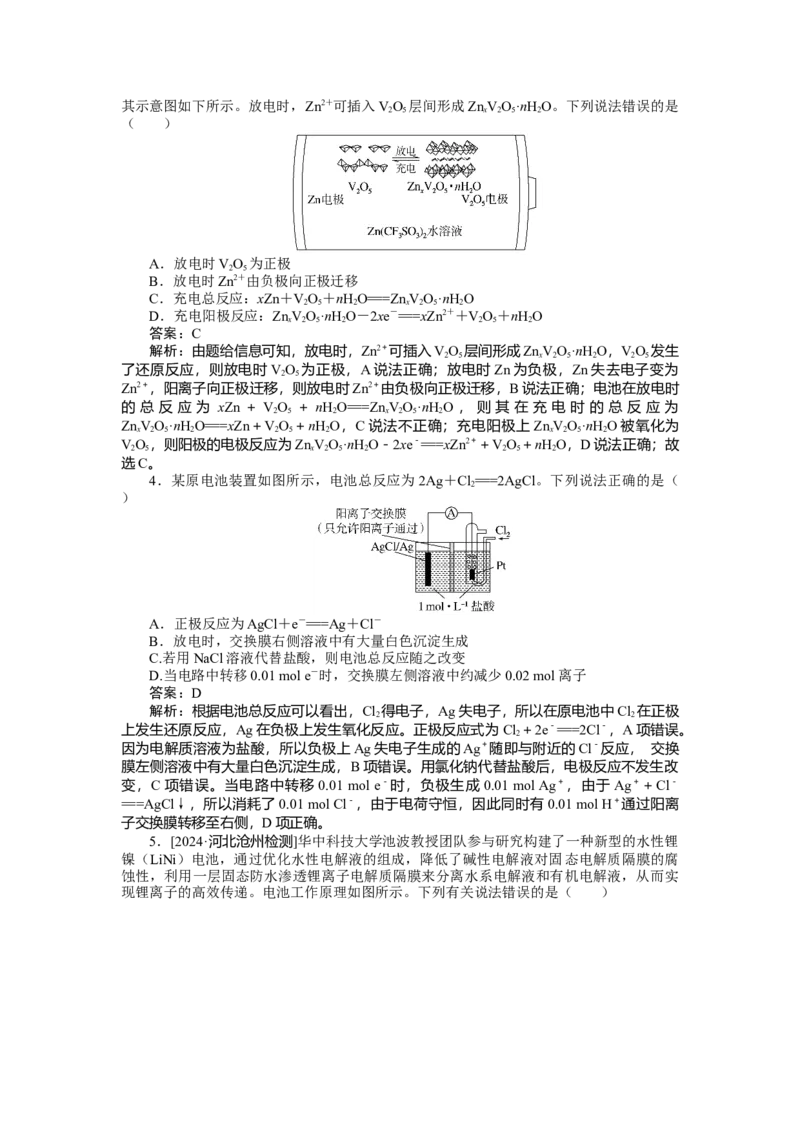
2.[2024·全国甲卷]科学家使用δMnO 研制了一种MnO Zn可充电电池(如图所示)。
2 2
电池工作一段时间后,MnO 电极上检测到MnOOH和少量ZnMn O。下列叙述正确的是(
2 2 4
)
A.充电时,Zn2+向阳极方向迁移
B.充电时,会发生反应Zn+2MnO ===ZnMn O
2 2 4
C.放电时,正极反应有MnO +HO+e-===MnOOH+OH-
2 2
D.放电时,Zn电极质量减少0.65 g,MnO 电极生成了0.020 mol MnOOH
2
答案:C
解析:充电时Zn2+向阴极移动,A错误;由题意知,放电时,MnO 转化为MnOOH和
2
ZnMn O ,B 错误;放电时,MnO 电极为正极,发生的反应有 MnO +HO+e-
2 4 2 2 2
===MnOOH+OH-,C正确;根据放电时Zn电极的电极反应式为Zn-2e-===Zn2+可知,
Zn电极质量减少0.65 g(0.01 mol)时,电路中通过0.02 mol电子,故MnO 电极有0.02
2
mol MnO 发生反应,但MnO 转化为MnOOH和少量ZnMn O ,故生成的MnOOH的量小
2 2 2 4
于0.020 mol,D错误。
3.[2023·新课标卷]一种以VO 和Zn为电极、Zn(CFSO ) 水溶液为电解质的电池,
2 5 3 3 2其示意图如下所示。放电时,Zn2+可插入VO 层间形成ZnVO·nHO。下列说法错误的是
2 5 x 2 5 2
( )
A.放电时VO 为正极
2 5
B.放电时Zn2+由负极向正极迁移
C.充电总反应:xZn+VO+nHO===ZnVO·nHO
2 5 2 x 2 5 2
D.充电阳极反应:ZnVO·nHO-2xe-===xZn2++VO+nHO
x 2 5 2 2 5 2
答案:C
解析:由题给信息可知,放电时,Zn2+可插入VO 层间形成ZnVO·nHO,VO 发生
2 5 x 2 5 2 2 5
了还原反应,则放电时 VO 为正极,A说法正确;放电时Zn为负极,Zn失去电子变为
2 5
Zn2+,阳离子向正极迁移,则放电时Zn2+由负极向正极迁移,B说法正确;电池在放电时
的 总 反 应 为 xZn + VO + nHO===ZnVO·nHO , 则 其 在 充 电 时 的 总 反 应 为
2 5 2 x 2 5 2
ZnVO·nHO===xZn+VO +nHO,C说法不正确;充电阳极上ZnVO·nHO被氧化为
x 2 5 2 2 5 2 x 2 5 2
VO ,则阳极的电极反应为ZnVO·nHO-2xe-===xZn2++VO +nHO,D说法正确;故
2 5 x 2 5 2 2 5 2
选C。
4.某原电池装置如图所示,电池总反应为2Ag+Cl===2AgCl。下列说法正确的是(
2
)
A.正极反应为AgCl+e-===Ag+Cl-
B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.若用NaCl溶液代替盐酸,则电池总反应随之改变
D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
答案:D
解析:根据电池总反应可以看出,Cl 得电子,Ag失电子,所以在原电池中Cl 在正极
2 2
上发生还原反应,Ag在负极上发生氧化反应。正极反应式为Cl +2e-===2Cl-,A项错误。
2
因为电解质溶液为盐酸,所以负极上Ag失电子生成的Ag+随即与附近的Cl-反应, 交换
膜左侧溶液中有大量白色沉淀生成,B项错误。用氯化钠代替盐酸后,电极反应不发生改
变,C项错误。当电路中转移 0.01 mol e-时,负极生成 0.01 mol Ag+,由于Ag++Cl-
===AgCl↓,所以消耗了0.01 mol Cl-,由于电荷守恒,因此同时有0.01 mol H+通过阳离
子交换膜转移至右侧,D项正确。
5.[2024·河北沧州检测]华中科技大学池波教授团队参与研究构建了一种新型的水性锂
镍(LiNi)电池,通过优化水性电解液的组成,降低了碱性电解液对固态电解质隔膜的腐
蚀性,利用一层固态防水渗透锂离子电解质隔膜来分离水系电解液和有机电解液,从而实
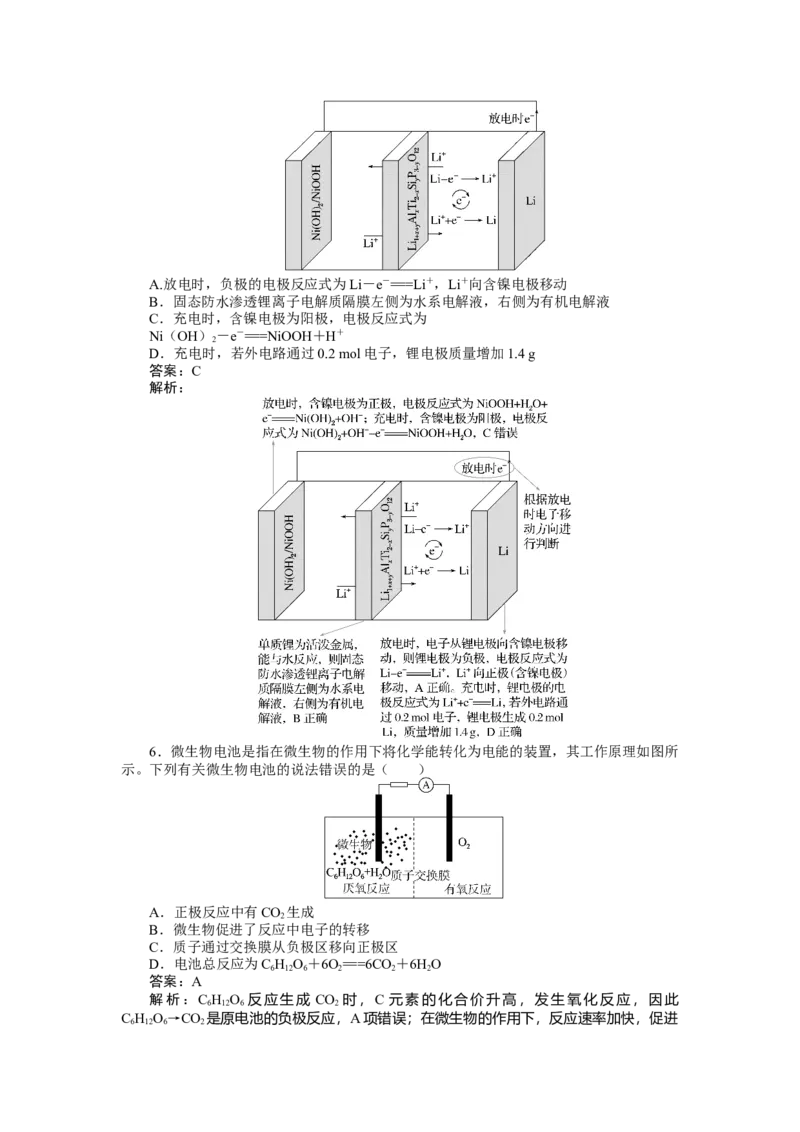
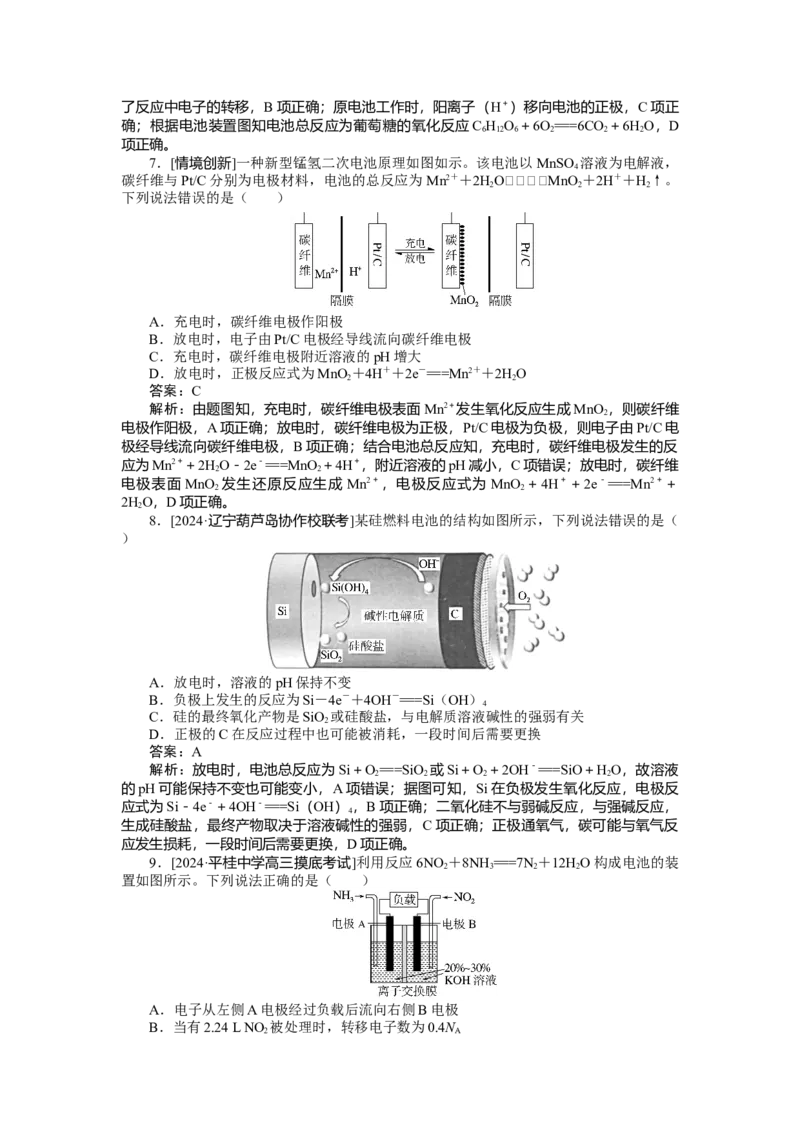
现锂离子的高效传递。电池工作原理如图所示。下列有关说法错误的是( )A.放电时,负极的电极反应式为Li-e-===Li+,Li+向含镍电极移动
B.固态防水渗透锂离子电解质隔膜左侧为水系电解液,右侧为有机电解液
C.充电时,含镍电极为阳极,电极反应式为
Ni(OH)-e-===NiOOH+H+
2
D.充电时,若外电路通过0.2 mol电子,锂电极质量增加1.4 g
答案:C
解析:
6.微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所
示。下列有关微生物电池的说法错误的是( )
A.正极反应中有CO 生成
2
B.微生物促进了反应中电子的转移
C.质子通过交换膜从负极区移向正极区
D.电池总反应为C H O+6O===6CO +6HO
6 12 6 2 2 2
答案:A
解析:C H O 反应生成 CO 时,C 元素的化合价升高,发生氧化反应,因此
6 12 6 2
C H O→CO 是原电池的负极反应,A项错误;在微生物的作用下,反应速率加快,促进
6 12 6 2了反应中电子的转移,B项正确;原电池工作时,阳离子(H+)移向电池的正极,C项正
确;根据电池装置图知电池总反应为葡萄糖的氧化反应C H O +6O===6CO +6HO,D
6 12 6 2 2 2
项正确。
7.[情境创新]一种新型锰氢二次电池原理如图如示。该电池以MnSO 溶液为电解液,
4
碳纤维与Pt/C分别为电极材料,电池的总反应为Mn2++2HOMnO +2H++H↑。
2 2 2
下列说法错误的是( )
A.充电时,碳纤维电极作阳极
B.放电时,电子由Pt/C电极经导线流向碳纤维电极
C.充电时,碳纤维电极附近溶液的pH增大
D.放电时,正极反应式为MnO +4H++2e-===Mn2++2HO
2 2
答案:C
解析:由题图知,充电时,碳纤维电极表面Mn2+发生氧化反应生成MnO ,则碳纤维
2
电极作阳极,A项正确;放电时,碳纤维电极为正极,Pt/C电极为负极,则电子由Pt/C电
极经导线流向碳纤维电极,B项正确;结合电池总反应知,充电时,碳纤维电极发生的反
应为Mn2++2HO-2e-===MnO+4H+,附近溶液的pH减小,C项错误;放电时,碳纤维
2 2
电极表面 MnO 发生还原反应生成 Mn2+,电极反应式为 MnO +4H++2e-===Mn2++
2 2
2HO,D项正确。
2
8.[2024·辽宁葫芦岛协作校联考]某硅燃料电池的结构如图所示,下列说法错误的是(
)
A.放电时,溶液的pH保持不变
B.负极上发生的反应为Si-4e-+4OH-===Si(OH)
4
C.硅的最终氧化产物是SiO 或硅酸盐,与电解质溶液碱性的强弱有关
2
D.正极的C在反应过程中也可能被消耗,一段时间后需要更换
答案:A
解析:放电时,电池总反应为Si+O===SiO 或Si+O +2OH-===SiO+HO,故溶液
2 2 2 2
的pH可能保持不变也可能变小,A项错误;据图可知,Si在负极发生氧化反应,电极反
应式为Si-4e-+4OH-===Si(OH) ,B项正确;二氧化硅不与弱碱反应,与强碱反应,
4
生成硅酸盐,最终产物取决于溶液碱性的强弱,C项正确;正极通氧气,碳可能与氧气反
应发生损耗,一段时间后需要更换,D项正确。
9.[2024·平桂中学高三摸底考试]利用反应6NO +8NH ===7N +12HO构成电池的装
2 3 2 2
置如图所示。下列说法正确的是( )
A.电子从左侧A电极经过负载后流向右侧B电极
B.当有2.24 L NO 被处理时,转移电子数为0.4N
2 AC.电极A极反应式为2NH -6e-===N +6H+
3 2
D.为使电池持续放电,离子交换膜需选用阳离子交换膜
答案:A
解析:在原电池中,负极发生氧化反应,正极发生还原反应,根据 6NO +
2
8NH ===7N +12HO可知,通入氨气的电极为负极,通入二氧化氮的为正极。电子从负极
3 2 2
流出,正极流入,则电子从左侧电极经过负载后流向右侧电极,故A正确;未说明是否为
标准状况,无法计算2.24 L NO 的物质的量,因此无法计算转移的电子数,故 B错误;电
2
极A为负极,发生氧化反应,电极反应式为2NH -6e-+6OH-===N +6HO,故C错误;
3 2 2
原电池工作时,阴离子向负极移动,为使电池持续放电,离子交换膜需选用阴离子交换膜
防止二氧化氮反应生成硝酸盐和亚硝酸盐,故D错误。